- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Электрическая цепь. Электрический ток в металлах и электролитах презентация
Содержание
- 1. Электрическая цепь. Электрический ток в металлах и электролитах
- 2. Цели: Выяснить, из каких частей состоит электрическая
- 3. План Понятие электрической цепи Условные обозначения составляющих
- 4. Электри́ческая цепь — совокупность устройств, предназначенных для протекания
- 5. Все устройства и объекты,
- 8. Электрический ток в
- 9. Электроли́т — веществовещество, расплаввещество, расплав или растворвещество, расплав
- 10. Спасибо за внимание!
Слайд 1Электрическая цепь. Электрический ток в металлах и электролитах
Выполнила учитель физики
Шаповалова Жанна
Слайд 2Цели:
Выяснить, из каких частей состоит электрическая цепь;
Объяснить назначение каждой части электрической
Познакомить с особенностями электрического тока в металлах и электролитах
Слайд 3План
Понятие электрической цепи
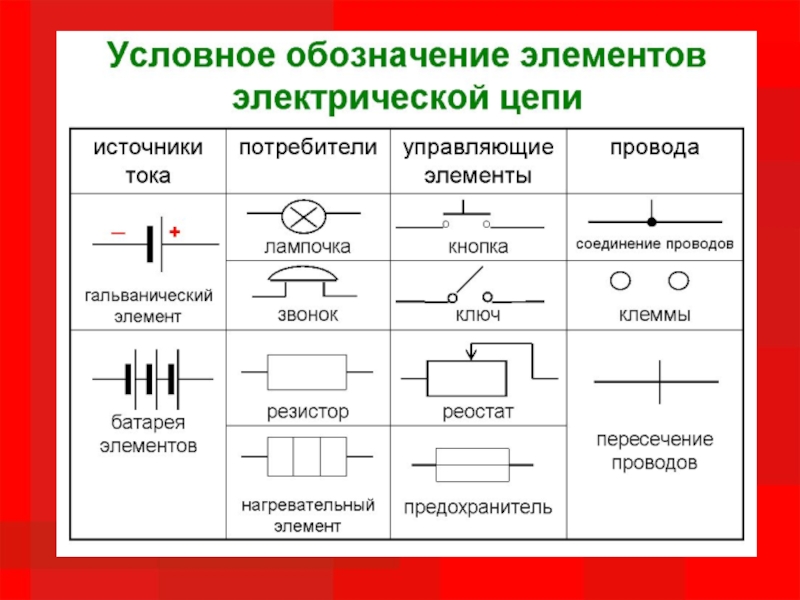
Условные обозначения составляющих электрической цепи
Электрический ток в металлах
Понятие об
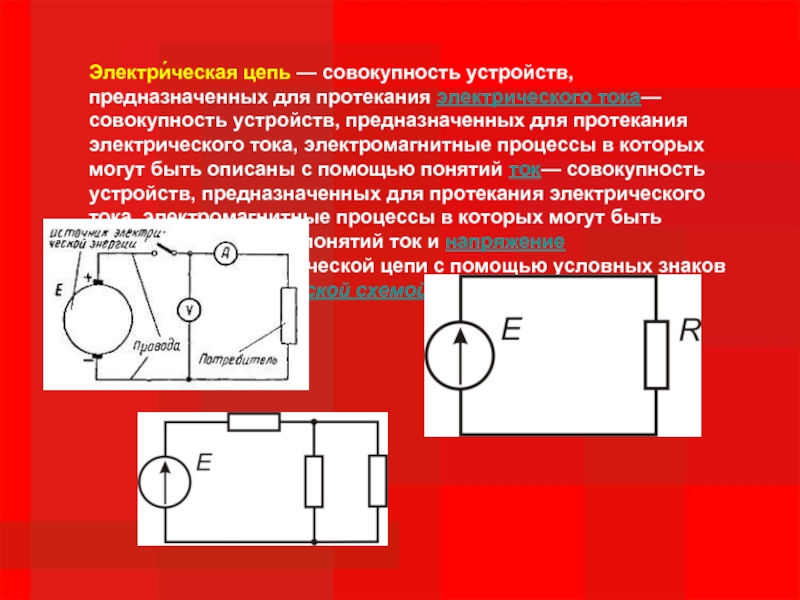
Слайд 4Электри́ческая цепь — совокупность устройств, предназначенных для протекания электрического тока— совокупность устройств,
Изображение электрической цепи с помощью условных знаков называют электрической схемой
Слайд 5 Все устройства и объекты, входящие в состав электрической
1) Источники электрической энергии (питания).
Общим свойством всех источников питания является преобразование какого-либо вида энергии в электрическую. Источники, в которых происходит преобразование неэлектрической энергии в электрическую, называются первичными источниками. Вторичные источники – это такие источники, у которых и на входе, и на выходе – электрическая энергия (например, выпрямительные устройства).
2) Потребители электрической энергии.
Общим свойством всех потребителей является преобразование электроэнергии в другие виды энергии (например, нагревательный прибор). Иногда потребители называют нагрузкой.
3) Вспомогательные элементы цепи: соединительные провода, коммутационная аппаратура, аппаратура защиты, измерительные приборы и т.д., без которых реальная цепь не работает.
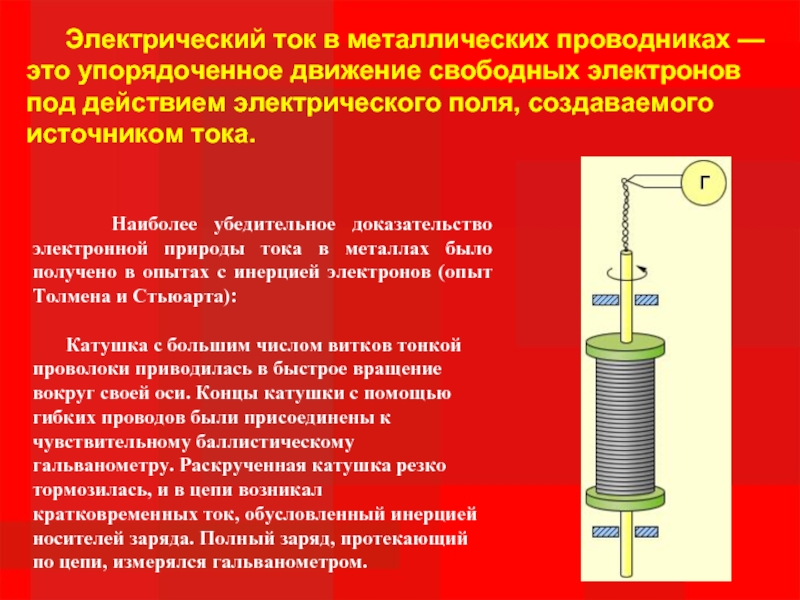
Слайд 8 Электрический ток в металлических проводниках — это
Наиболее убедительное доказательство электронной природы тока в металлах было получено в опытах с инерцией электронов (опыт Толмена и Стьюарта):
Катушка с большим числом витков тонкой проволоки приводилась в быстрое вращение вокруг своей оси. Концы катушки с помощью гибких проводов были присоединены к чувствительному баллистическому гальванометру. Раскрученная катушка резко тормозилась, и в цепи возникал кратковременных ток, обусловленный инерцией носителей заряда. Полный заряд, протекающий по цепи, измерялся гальванометром.
Слайд 9Электроли́т — веществовещество, расплаввещество, расплав или растворвещество, расплав или раствор, которое проводит
Классификация
Исходя из степени диссоциации все электролиты делятся на две группы
Сильные электролиты — электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты (HCl, HBr, HI, HNO3).
Слабые электролиты — степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду— степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот, основания p-— степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот, основания p-, d-, и f- элементов.
Между этими двумя группами четкой границы нет, одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом — слабого.