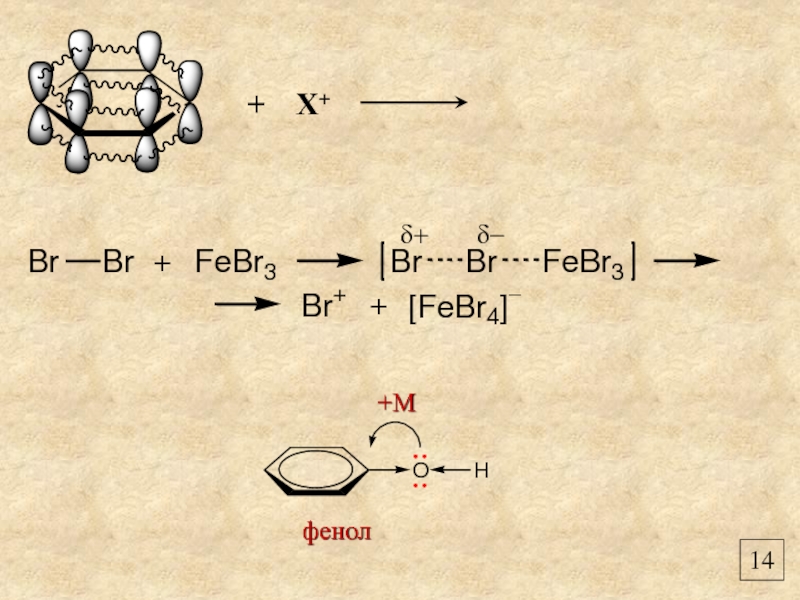- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
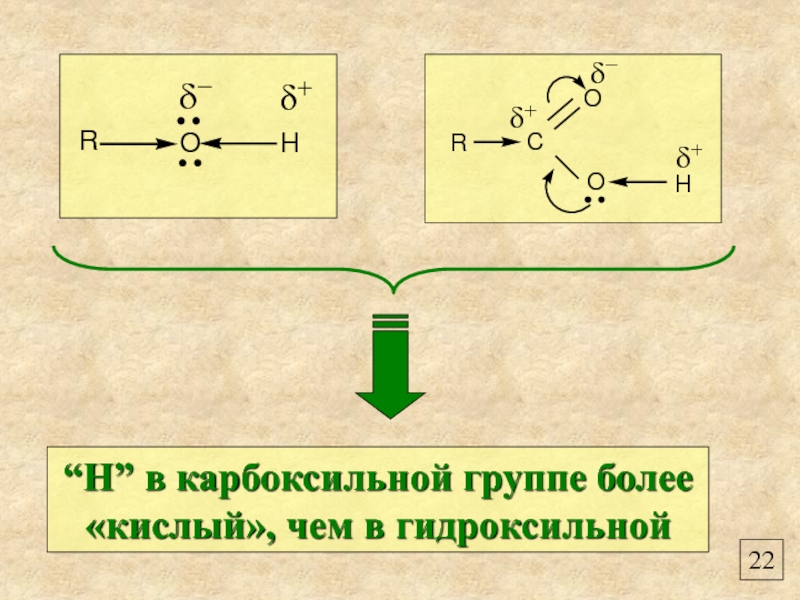
- Информатика
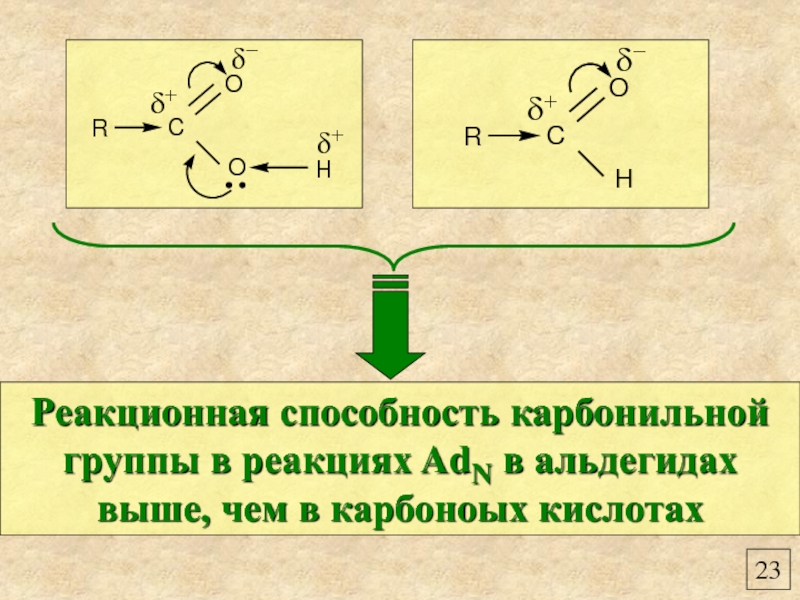
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Взаимное влияние атомов в молекулах презентация
Содержание
- 1. Взаимное влияние атомов в молекулах
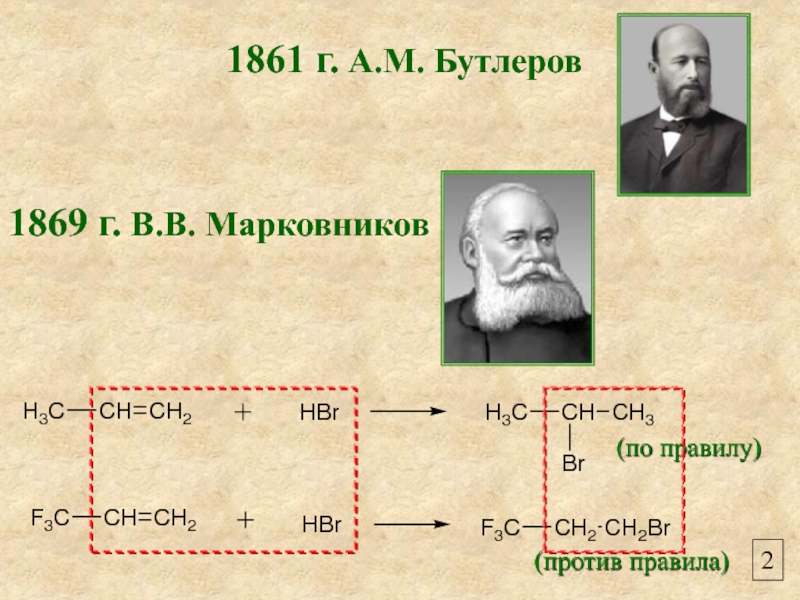
- 2. 1861 г. А.М. Бутлеров 1869 г. В.В. Марковников 2 (по правилу) (против правила)
- 3. 3 ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ЗАМЕСТИТЕЛЕЙ (ДОНОРНЫЕ, АКЦЕПТОРНЫЕ) ИЗМЕНЕНИЕ
- 4. 4 II. Эффект сопряжения (мезомерный эффект, ±
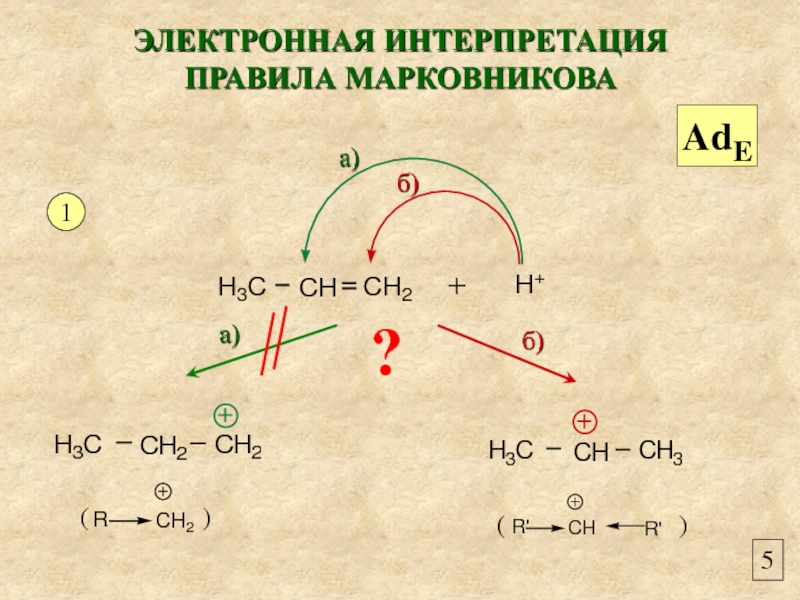
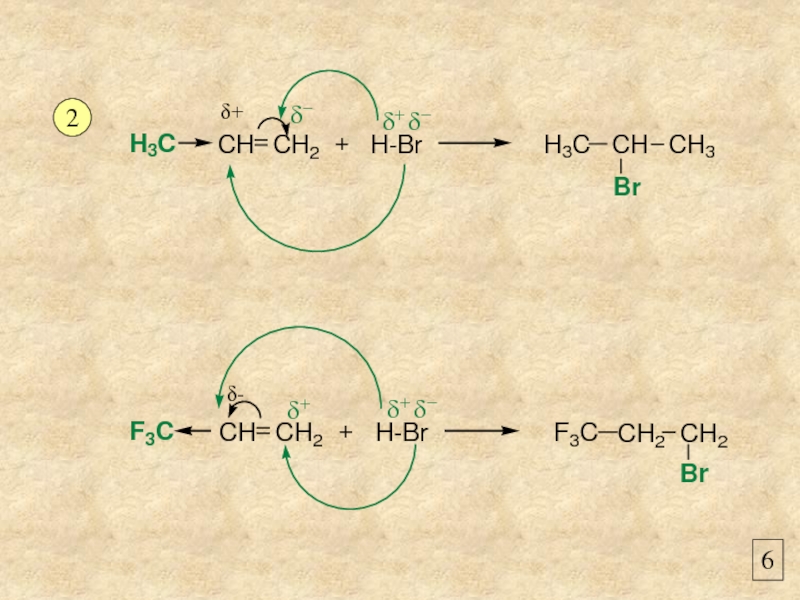
- 5. 5 ЭЛЕКТРОННАЯ ИНТЕРПРЕТАЦИЯ ПРАВИЛА МАРКОВНИКОВА 1 а) б) а) б) AdE ?
- 6. 6 2 δ+ δ-
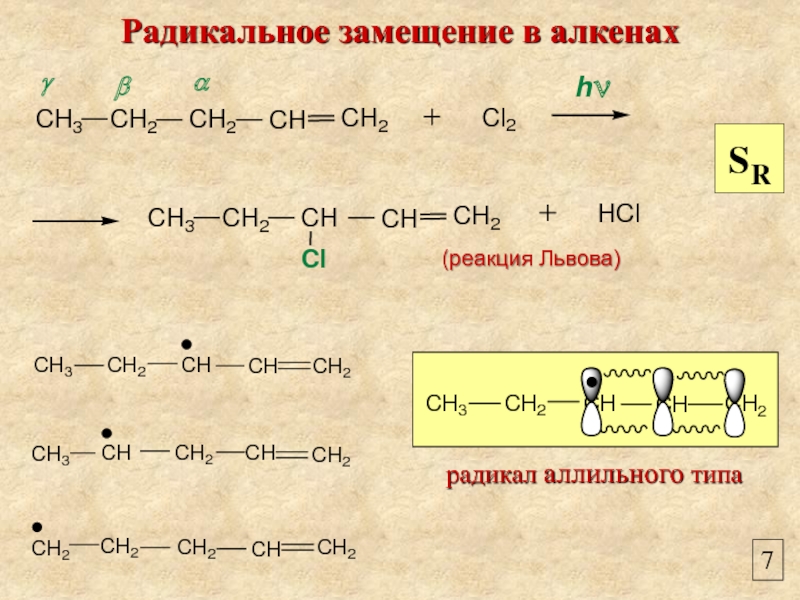
- 7. 7 радикал аллильного типа Радикальное замещение в алкенах SR (реакция Львова)
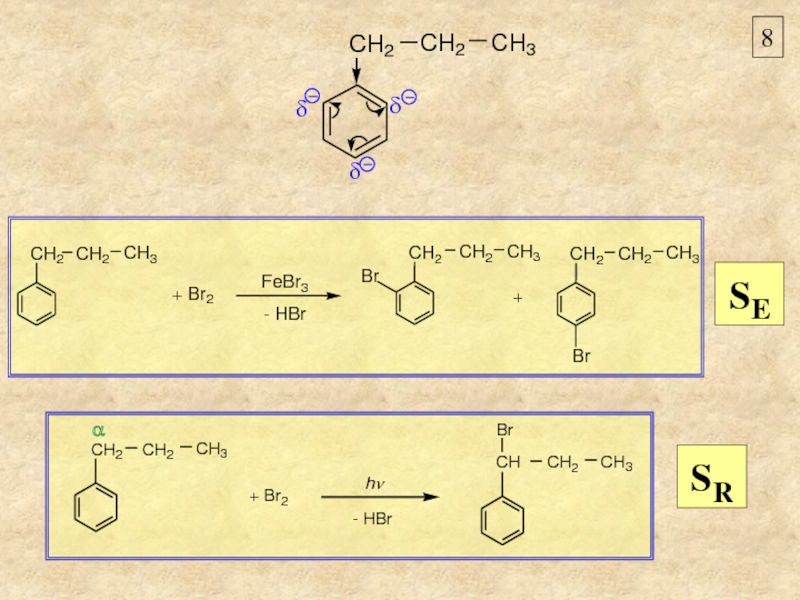
- 8. 8 SR SE
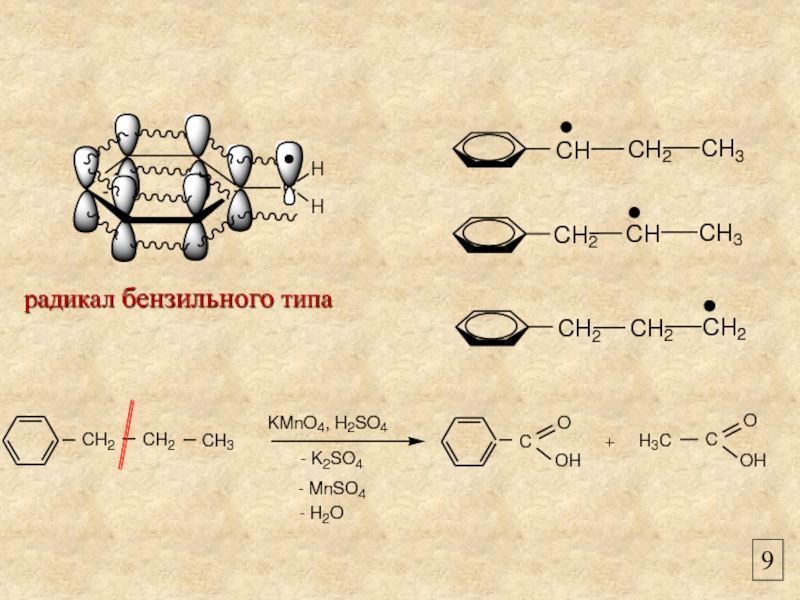
- 9. 9 радикал бензильного типа
- 10. Строение молекулы толуола.
- 11. 11 ВЗАИМНОЕ ВЛИЯНИЕ АТОМОВ В МОЛЕКУЛЕ НА
- 12. 12 Влияние природы радикалы на кислотные
- 13. 12 Влияние природы радикалы на кислотные
- 14. 12 Влияние природы радикалы на кислотные
- 15. 13 бромбензол Влияние ОН-группы на реакционную способность бензольного кольца в реакциях SE I. II.
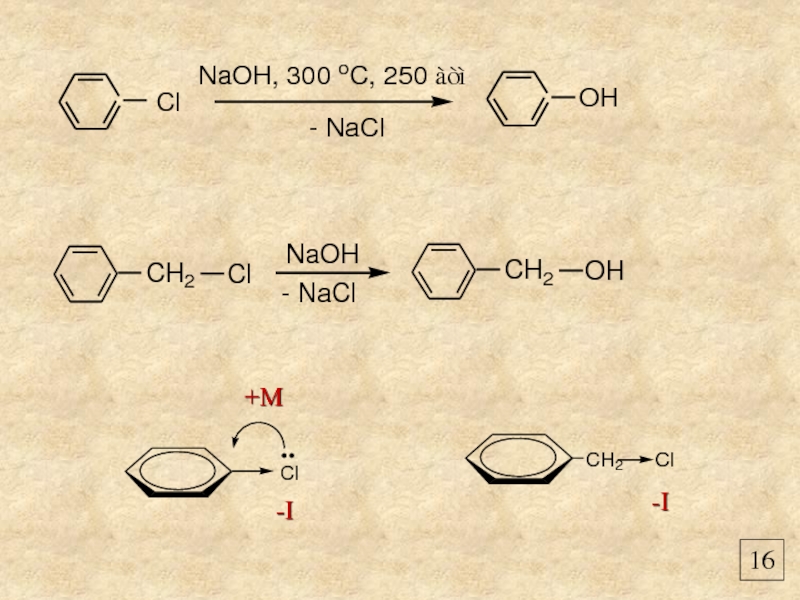
- 16. 14 +М фенол + Х+
- 17. Строение молекулы фенола. Взаимное
- 18. 16 +М -I -I
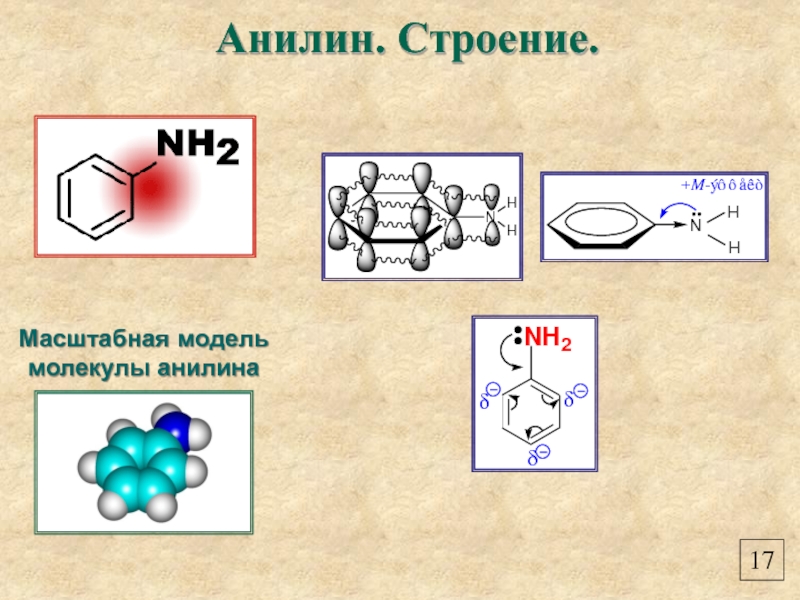
- 19. Масштабная модель молекулы анилина Анилин. Строение. 17
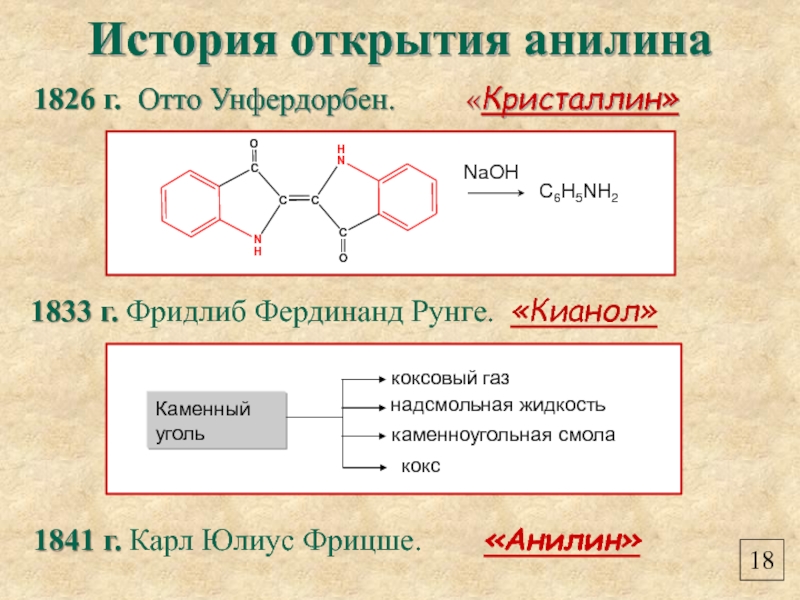
- 20. История открытия анилина 1826 г. Отто Унфердорбен.
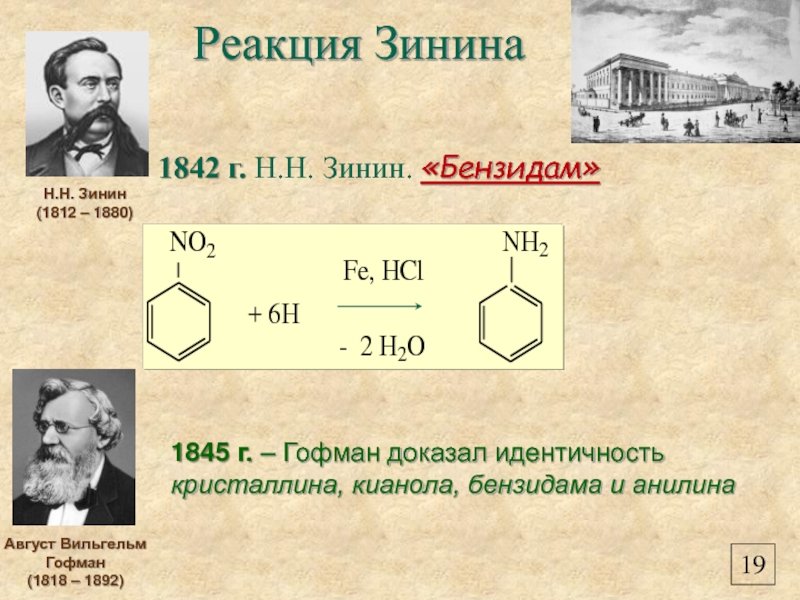
- 21. Реакция Зинина 1842 г. Н.Н. Зинин. «Бензидам»
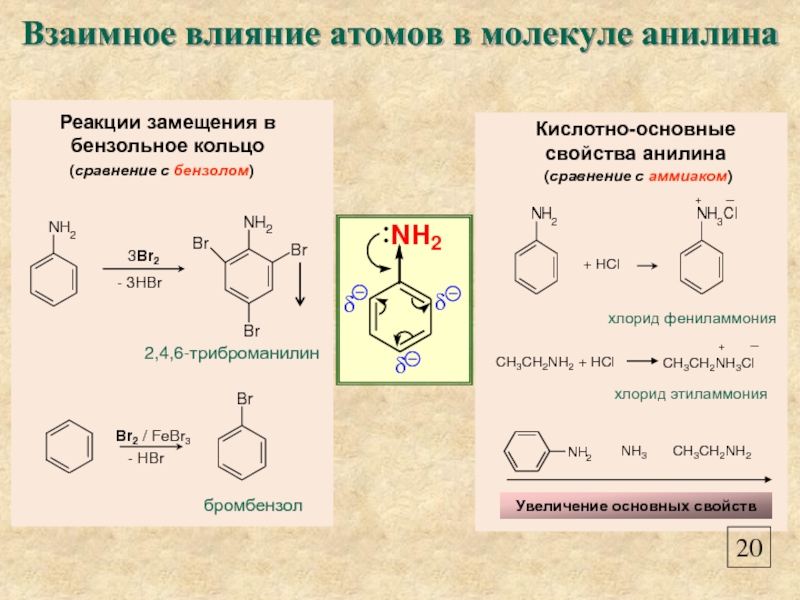
- 22. Взаимное влияние атомов в молекуле анилина 20
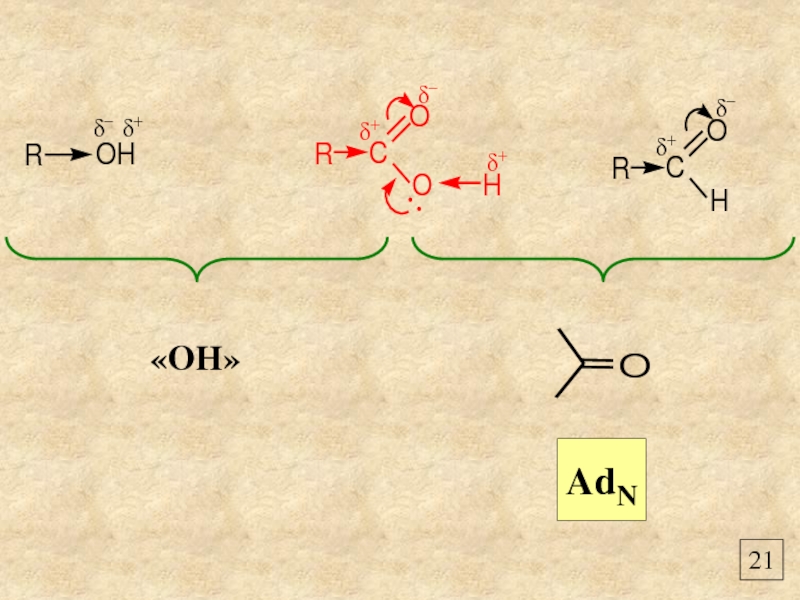
- 23. 21 AdN «OH»
- 24. 22 “Н” в карбоксильной группе более «кислый», чем в гидроксильной
- 25. 23 Реакционная способность
- 26. СПАСИБО ЗА ВНИМАНИЕ!
Слайд 33
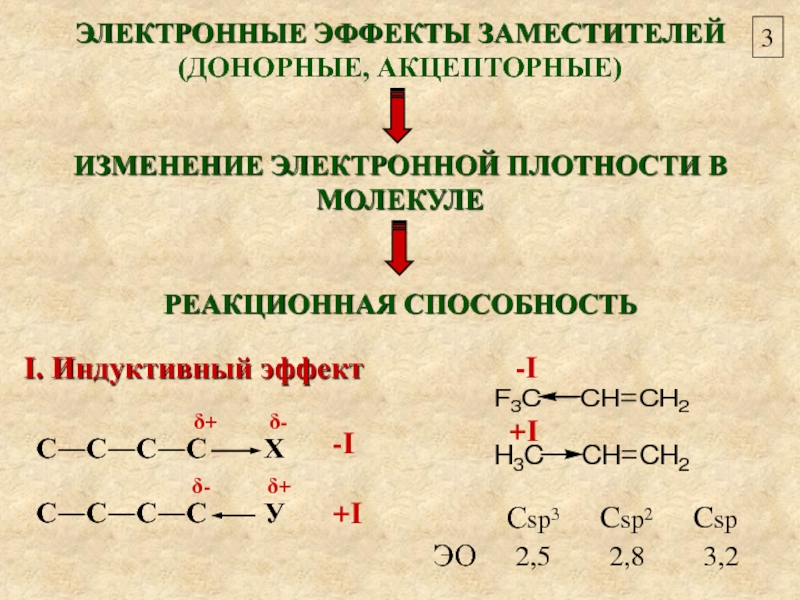
ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ЗАМЕСТИТЕЛЕЙ
(ДОНОРНЫЕ, АКЦЕПТОРНЫЕ)
ИЗМЕНЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ В МОЛЕКУЛЕ
РЕАКЦИОННАЯ СПОСОБНОСТЬ
ЭО 2,5 2,8 3,2
I. Индуктивный эффект
-I
+I
+I
-I
Слайд 44
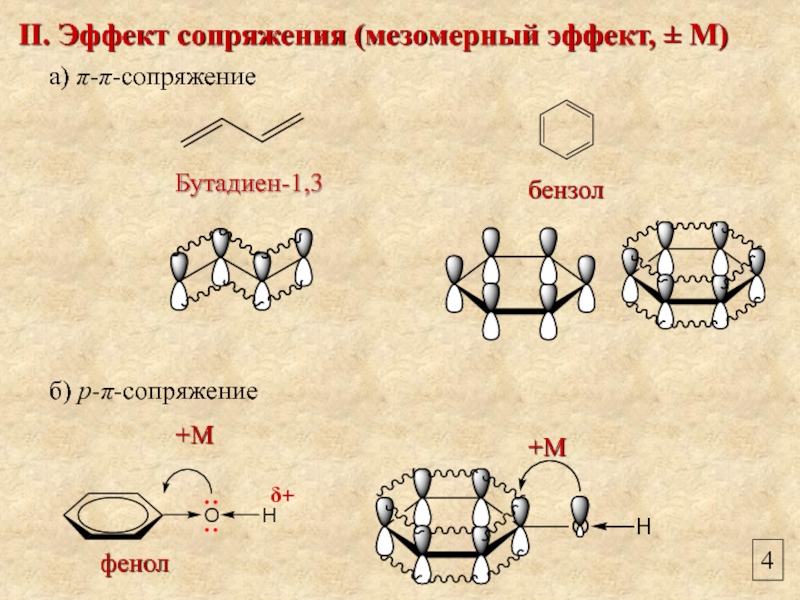
II. Эффект сопряжения (мезомерный эффект, ± М)
а) π-π-сопряжение
б) р-π-сопряжение
Бутадиен-1,3
бензол
+М
+М
фенол
δ+
Слайд 10
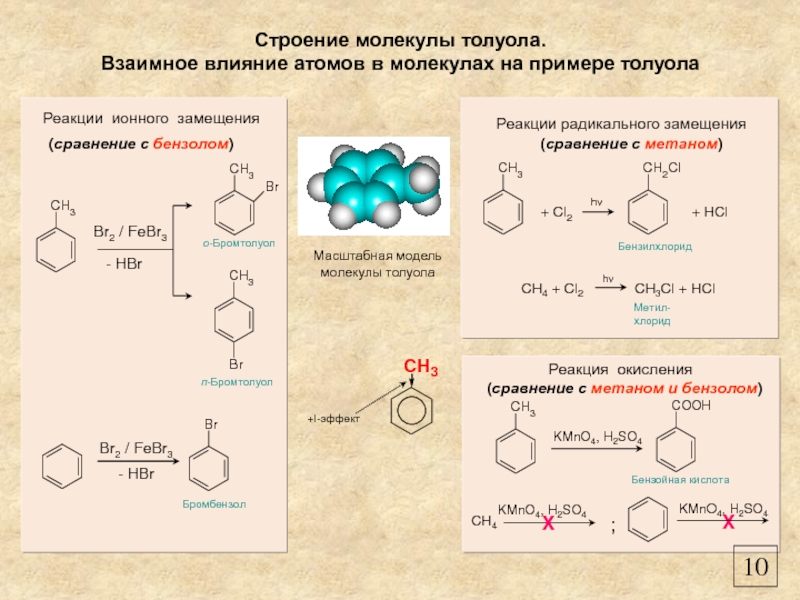
Строение молекулы толуола.
Взаимное влияние атомов в молекулах на примере толуола
Масштабная модель молекулы толуола
CH4 + Cl2
+ Cl2
CH4
CH3Cl + HCl
X
Br2 / FeBr3
- HBr
- HBr
Реакции радикального замещения
Реакции ионного замещения
+ HCl
Br2 / FeBr3
hν
hν
Реакция окисления
KMnO4, H2SO4
(сравнение с бензолом)
(сравнение с метаном)
Бромбензол
о-Бромтолуол
п-Бромтолуол
Бензилхлорид
Метил-хлорид
KMnO4, H2SO4
Бензойная кислота
(сравнение с метаном и бензолом)
KMnO4, H2SO4
X
;
+I-эффект
10
Слайд 1111
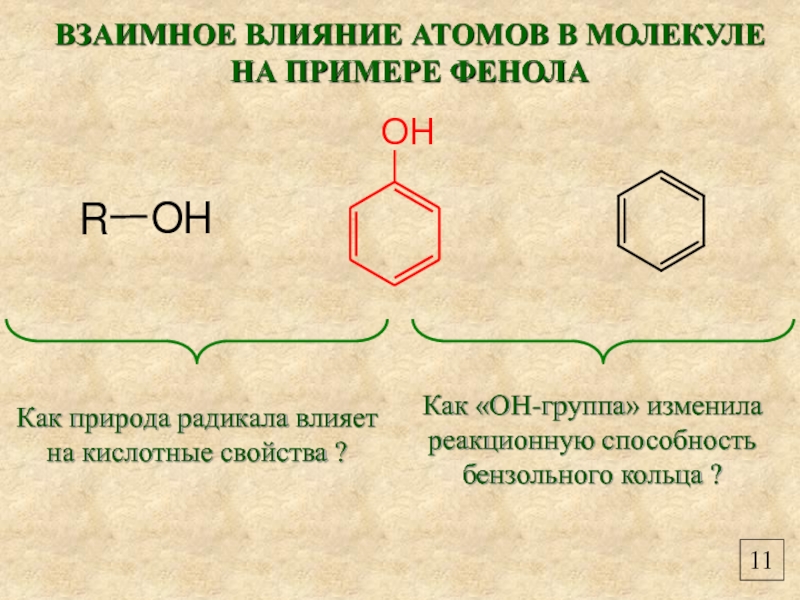
ВЗАИМНОЕ ВЛИЯНИЕ АТОМОВ В МОЛЕКУЛЕ
НА ПРИМЕРЕ ФЕНОЛА
Как природа радикала влияет на
Как «ОН-группа» изменила реакционную способность бензольного кольца ?
Слайд 1212
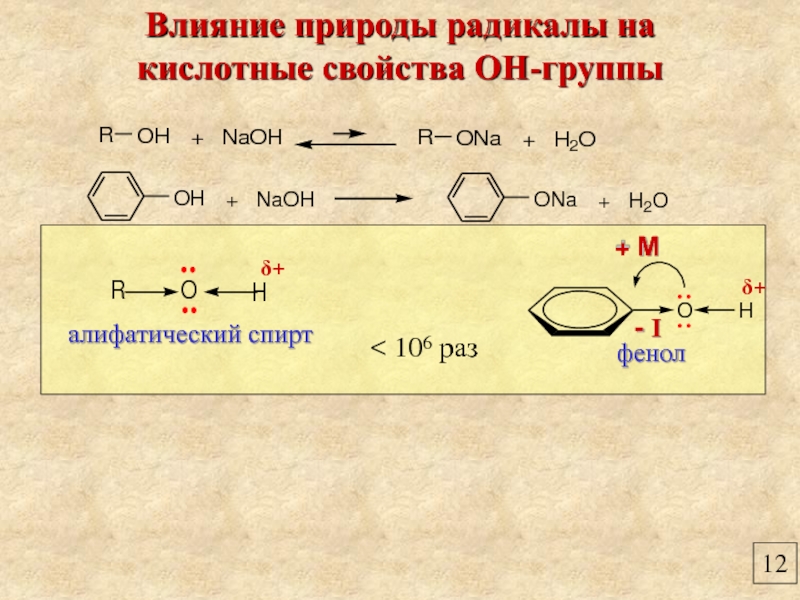
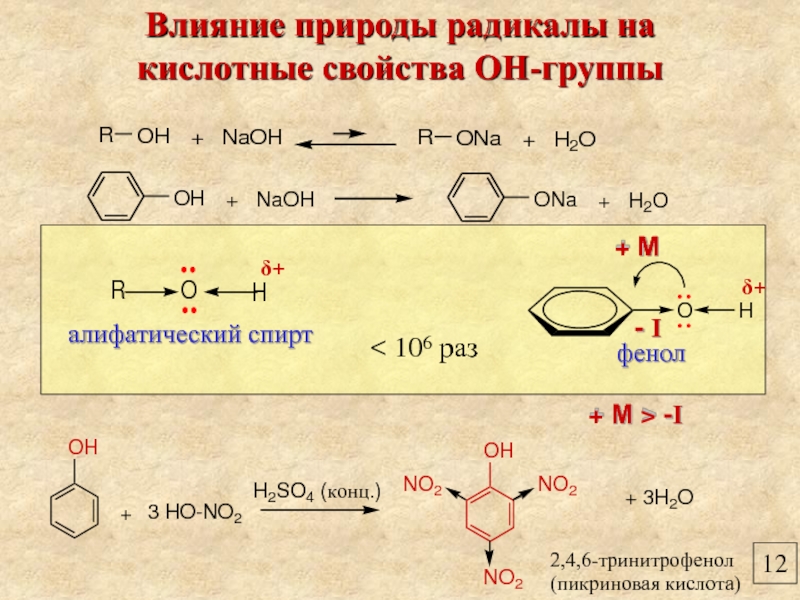
Влияние природы радикалы на
кислотные свойства ОН-группы
фенол
алифатический спирт
< 106 раз
+
- I
δ+
δ+
Слайд 1312
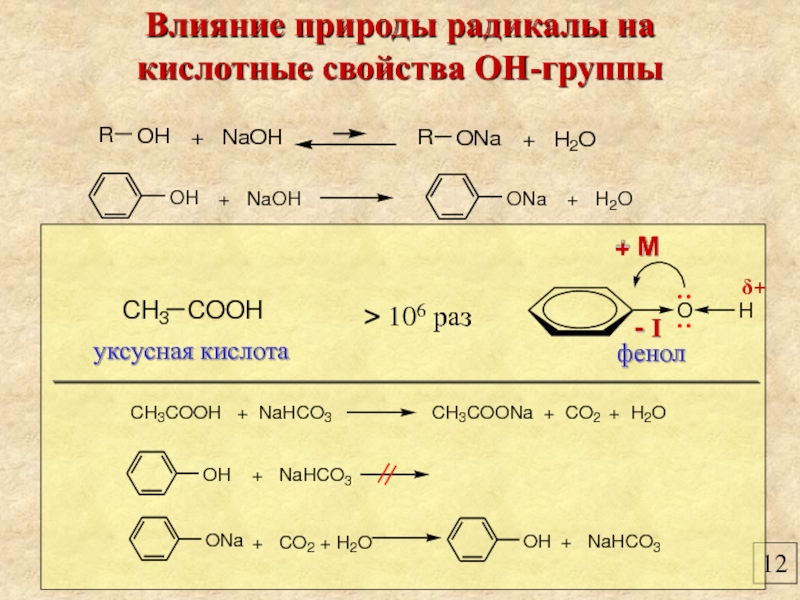
Влияние природы радикалы на
кислотные свойства ОН-группы
фенол
уксусная кислота
> 106 раз
+
- I
δ+
Слайд 1412
Влияние природы радикалы на
кислотные свойства ОН-группы
фенол
алифатический спирт
< 106 раз
+
- I
+ М > -I
δ+
δ+
Слайд 1513
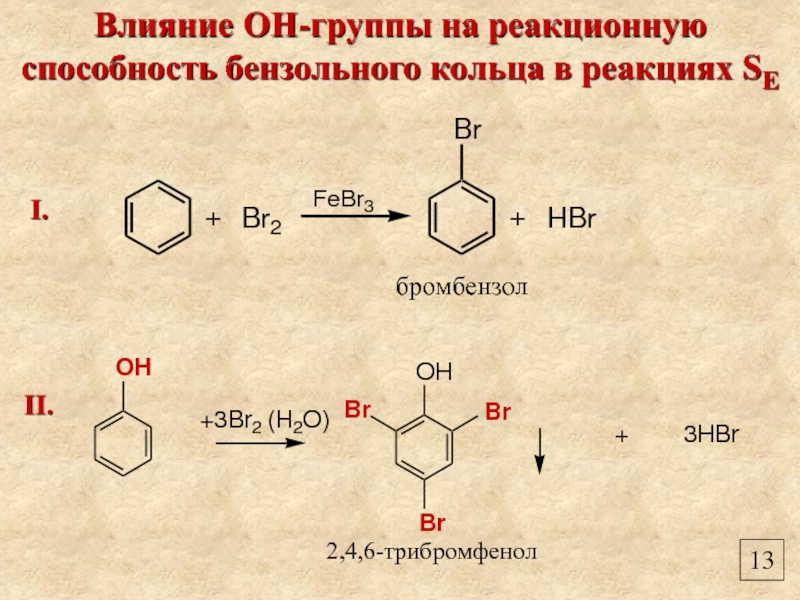
бромбензол
Влияние ОН-группы на реакционную способность бензольного кольца в реакциях SE
I.
II.
Слайд 17
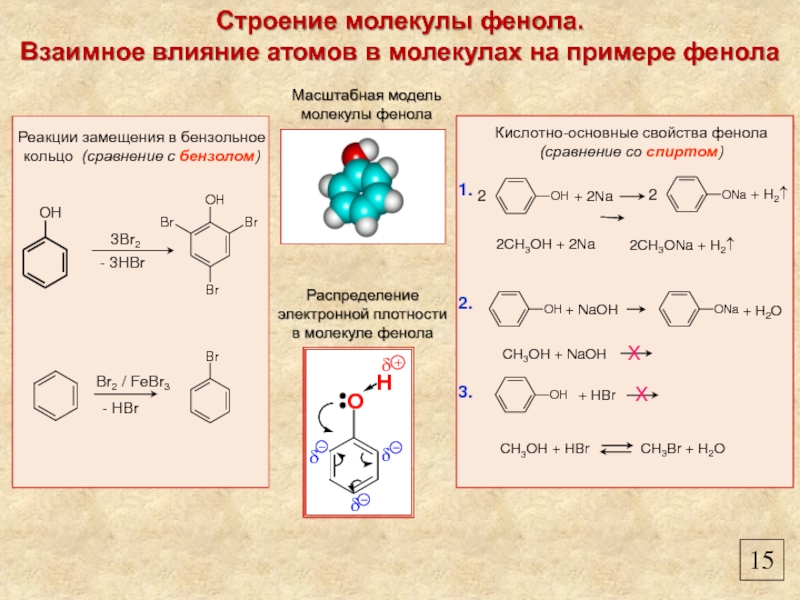
Строение молекулы фенола.
Взаимное влияние атомов в молекулах на примере фенола
Масштабная модель молекулы фенола
Распределение электронной плотности в молекуле фенола
Кислотно-основные свойства фенола (сравнение со спиртом)
Реакции замещения в бензольное кольцо (сравнение с бензолом)
1.
2.
3.
15
Слайд 20История открытия анилина
1826 г. Отто Унфердорбен. «Кристаллин»
1833
1841 г. Карл Юлиус Фрицше. «Анилин»
18
Слайд 21Реакция Зинина
1842 г. Н.Н. Зинин. «Бензидам»
Н.Н. Зинин
(1812 – 1880)
1845 г. –
кристаллина, кианола, бензидама и анилина
Август Вильгельм
Гофман
(1818 – 1892)
19