- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Соли как производные кислот и оснований презентация
Содержание
- 2. Цель
- 3. Вопросы 4. Что такое кислоты?
- 4. NO HNO NaOH HNO
- 5. CO 2 2 H
- 6. ТЕСТ 1. Определите ряд формул состоящих только
- 14. Критерии оценивая. Оценка
- 17. Cоли – это
- 18. СОЛИ Na OH H
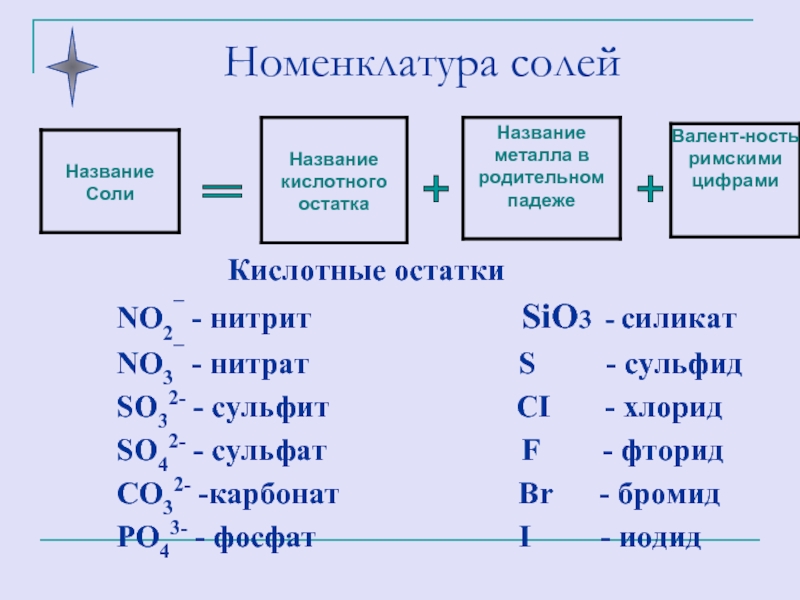
- 25. Номенклатура солей + + =
- 26. Составить формулу сульфата алюминия: Составьте формулы:
- 29. ЗАКРЕПЛЕНИЕ 1. Что такое соли?
- 30. Домашнее задание: §21, Упр.2, 3, наизусть названия солей на примере солей натрия.
Слайд 2 Цель и задачи урока.
Цель урока:
Задачи урока:
1.Дать определение солей.
2. Рассмотреть состав и название солей.
3. Продолжить обучение школьников определять степени окисления в сложных соединениях.
4. Научить, составлять формулы солей.
5. Познакомить учащихся с классификацией солей.
6. Познакомить с некоторыми свойства солей.
Слайд 3Вопросы
4. Что такое кислоты?
1. Какие классы веществ вы знаете?
2. Что
3. Что такое основания?
5. Что такое основные оксиды, кислотные оксиды, амфотерные?
Слайд 5CO
2
2
H CO
Mg(OH)
2
3
H SO
2
3
H SO
2
4
К какому классу соединений относятся вещества, дать им названия
Слайд 6ТЕСТ
1. Определите ряд формул состоящих только из:
кислотных оксидов (
основных оксидов: (II вариант)
а) Na2 O, N2O, CuO;
б) CO2, P2O5, Cl2O7;
в) MgO, BaO, K2O;
г) Li2O, CaO, CO.
Слайд 7
2. Выберите из списка веществ формулы: только кислот (I вариант), формулы только оснований (II вариант):
а) НСI, AICI3, CO2, H2SO4
б) H2SO4, HCI, HNO3, HF
в) NaOH, BaCI2, CO, Ca(OH)2
г) AI(OH)3, NaOH, KOH, Ba(OH)2
Слайд 8
3. Выберите формулу оксида серы (IV) – I вариант
Выберите формулу оксида углерода (II) –
II вариант:
а)H2S б) CO в) HNO3 г) ZnO д) SO2
Слайд 9
4. * Выберите формулу серной кислоты –
I вариант
* Выберите формулу сернистой кислоты –
II вариант
а) H2SiO3 б) H2SO4 в) H2SO3 г) H2S
Слайд 10
5. * Выберите формулу гидроксида калия –
I вариант
* Выберите формулу гидроксида кальция -
II вариант
а) Ba(OH)2, б) NaOH в) KOH г) Ca(OH)2
Слайд 11
6. * Выберите формулы растворимого в воде основания – I вариант
* Выберите формулы нерастворимого в воде основания – II вариант
а)Cu(OH)2 б) KOH в) LiOH г) AI(OH)3
Слайд 12
7. * Выберите формулы, в которых
лакмус меняет свой цвет
на красный – I вариант
* Выберите формулы, в которых лакмус меняет свой цвет на синий – II вариант
а) НСI б) H2SO4 в) NaOH г) KOH
Слайд 13 Ответы к тесту.
I вариант
1. б 1. в
2. б 2. г
3. д 3. б
4. б 4. в
5. в 5. г
6. б, в 6. а, г
7. а, б 7. в, г
Слайд 14 Критерии оценивая.
Оценка «5» - одна ошибка
Оценка «4»
Оценка «3» - три ошибки
Оценка «2» - четыре ошибки и больше.
Слайд 15
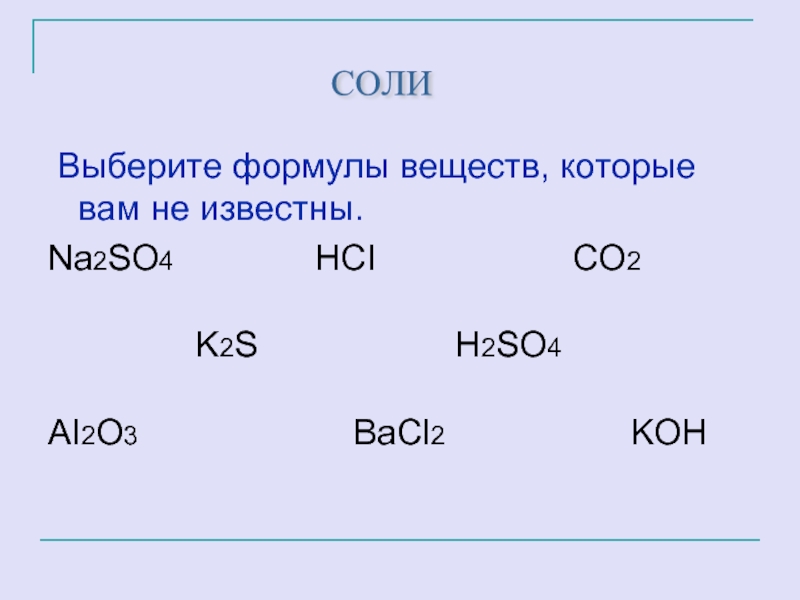
Выберите формулы веществ, которые вам не известны.
Na2SO4 HCI CO2
K2S H2SO4
AI2O3 ВаCl2 KOH
СОЛИ
Слайд 16
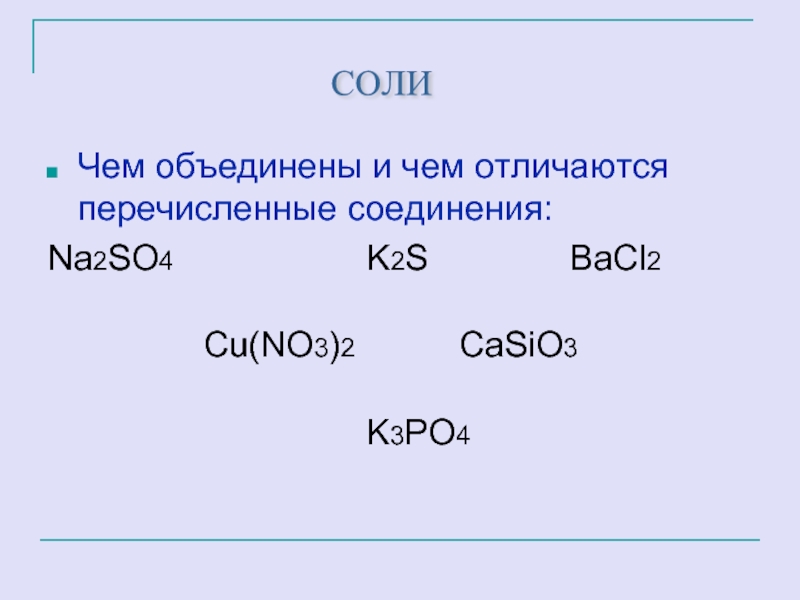
Чем объединены и чем отличаются перечисленные соединения:
Na2SO4 K2S ВаCl2
Cu(NO3)2 CaSiO3
K3PO4
СОЛИ
Слайд 19
С уверенностью можно сказать, что, по крайней мере, одно химическое соединение в довольно чистом виде имеется в каждом доме, в каждой семье. Это – поваренная соль или как ее называют химики – хлорид натрия NaCl.
Слайд 23 Соли
* Кристаллогидрат железа
FeSO4* 7H2O
* Сульфат магния –горькая английская соль
MgSO4
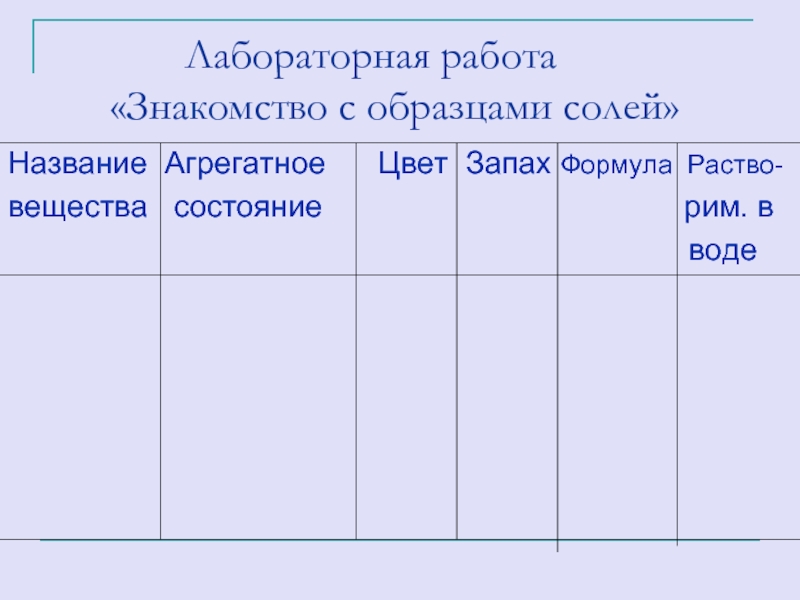
Слайд 24 Лабораторная работа
Название Агрегатное Цвет Запах Формула Раство-
вещества состояние рим. в
воде
Слайд 26Составить формулу сульфата алюминия:
Составьте формулы:
сульфата натрия,
сульфата кальция,
сульфата железа(III).
Al
2
+
SO
4
3
( )
3
2
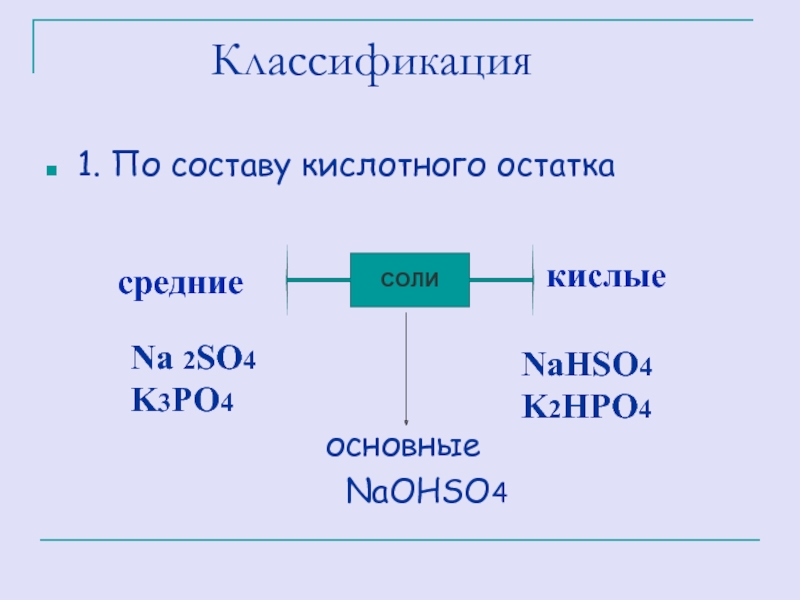
Слайд 27 Классификация
1. По составу кислотного
основные
NaOHSO4
СОЛИ
средние
кислые
Na 2SO4
K3PO4
NaHSO4
K2HPO4
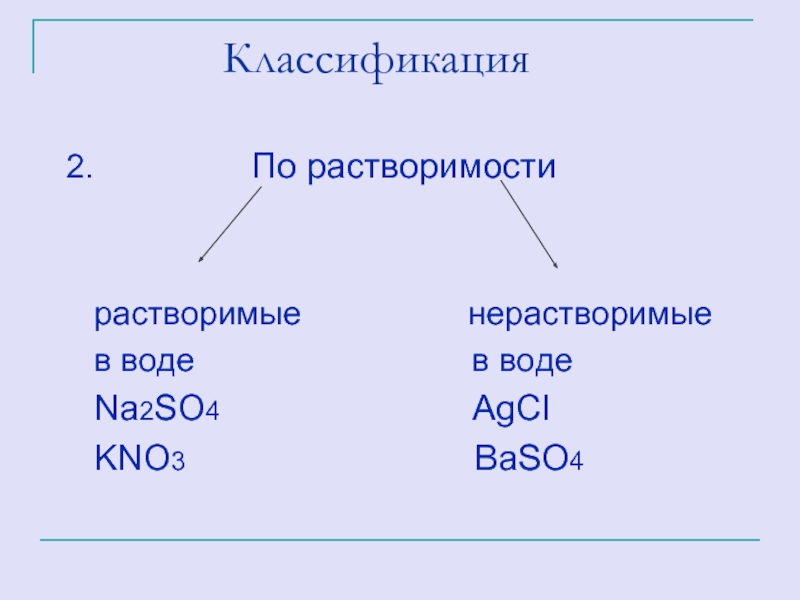
Слайд 28 Классификация
2.
растворимые нерастворимые
в воде в воде
Na2SO4 AgCI
KNO3 BaSO4
Слайд 29ЗАКРЕПЛЕНИЕ
1. Что такое соли?
2. Дать названия веществам: Ca(NO3)2, K2SO3, Li2CO3, CuSO4.
3. Составить формулы солей: нитрита магния, силиката натрия, фосфата кальция.