- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Углеводороды нефти. Алканы. Парафины презентация
Содержание
- 1. Углеводороды нефти. Алканы. Парафины
- 2. Общая формула алканов СnH2n+2
- 4. Газы СH4 метан С2H6 этан С3H8 пропан С4H10 бутан
- 5. жидкости С5H12 пентан ….. С15H32 пентадекан
- 6. Твердые вещества Начиная с С16Н34
- 7. Газообразные парафиновые углеводороды входят в состав природных
- 8. природные газы газы газоконденсатных месторождений попутные газы
- 9. Примерный состав природного газа
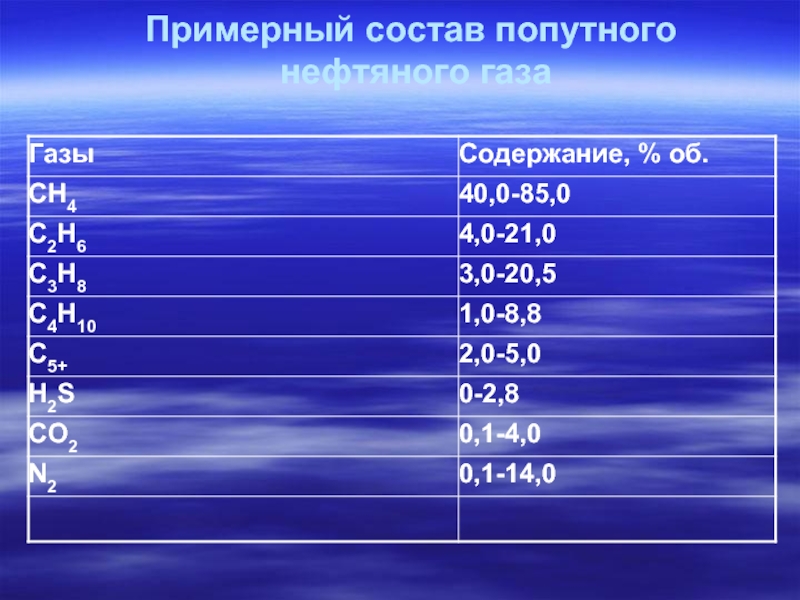
- 10. Примерный состав попутного нефтяного газа
- 11. Примерный состав газов газоконденсатных месторождений
- 12. Газообразные парафины дают комплексы с водой, они
- 13. Молекулы газов включаются в полости, образующиеся в кристаллической решетке воды.
- 14. Систематическая номенклатура алканов (ИЮПАК; JUPAC;
- 17. 2. Нумеруют атомы углерода в цепи,
- 18. Формулы и названия радикалов
- 21. 3. Перечисляют все радикалы (в порядке
- 24. 4. Дают название пронумерованной цепи, которое соответствует
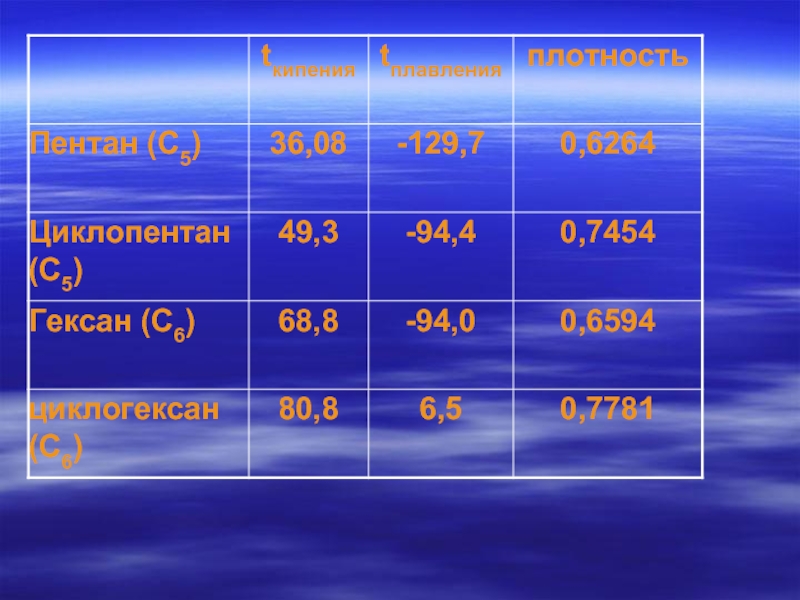
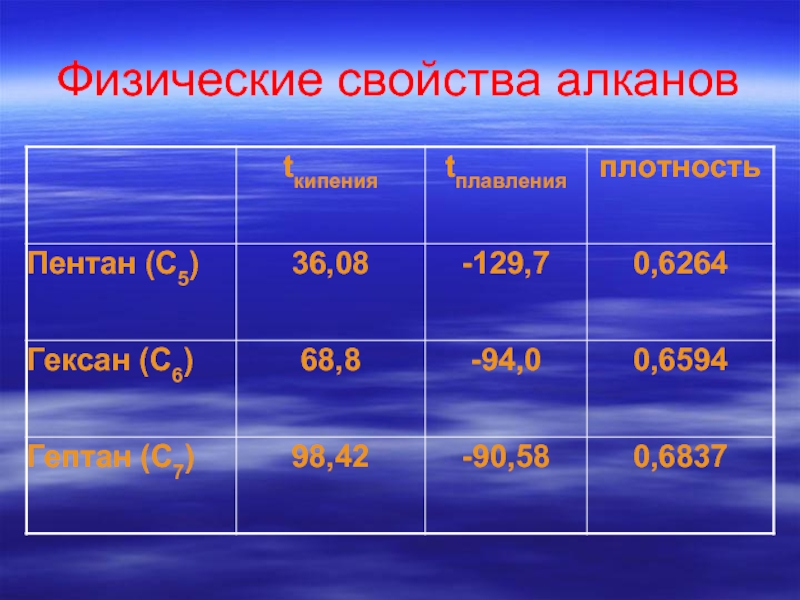
- 27. Физические свойства алканов
- 28. Вывод: Среди алканов нормального строения
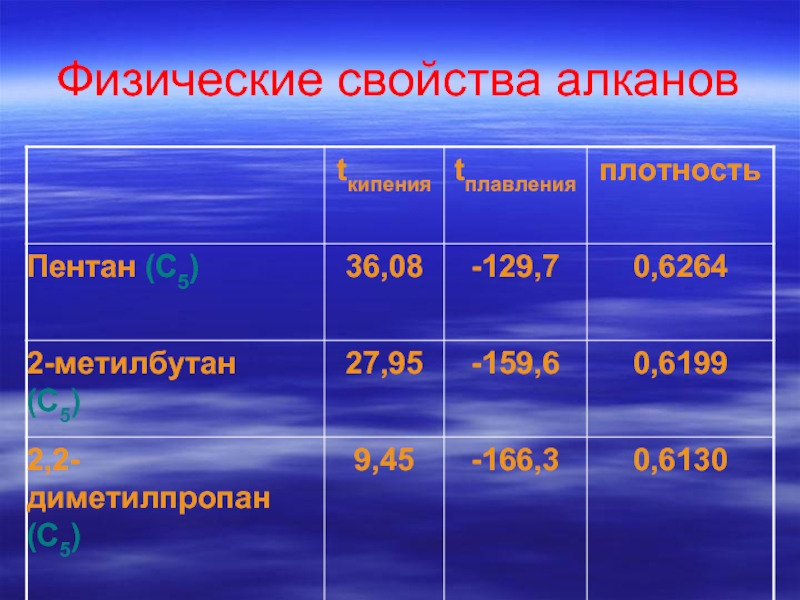
- 29. Физические свойства алканов
- 30. Вывод: Среди алканов одинакового состава, но
- 31. Углеводороды нефти Циклоалканы. Нафтены. Содержание в нефтях в среднем 25-80%
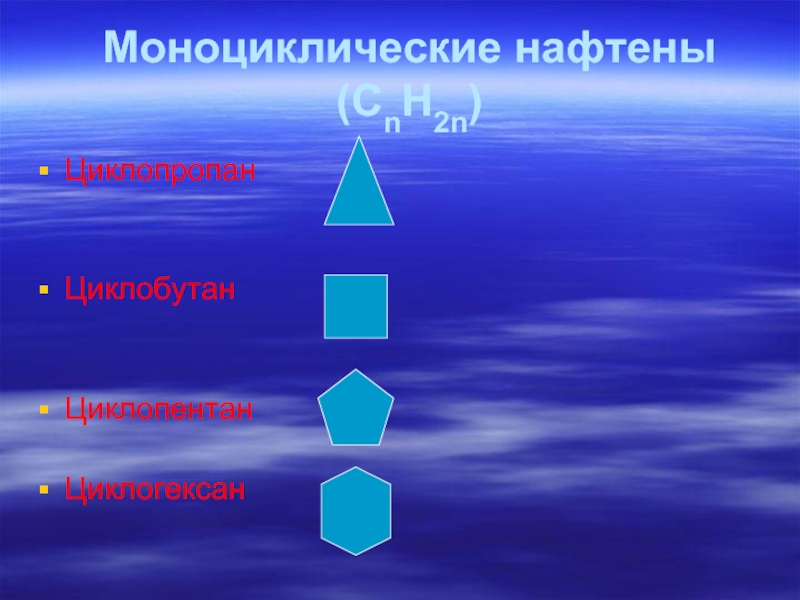
- 32. Циклопропан
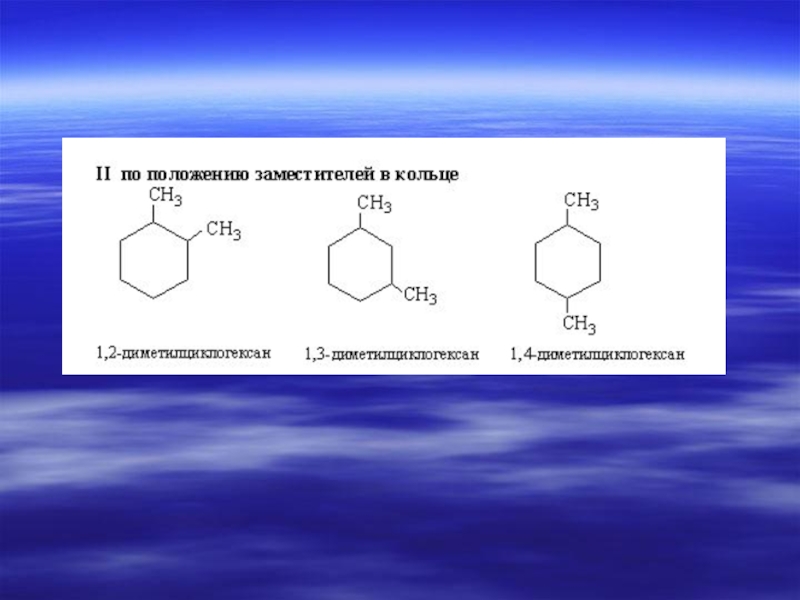
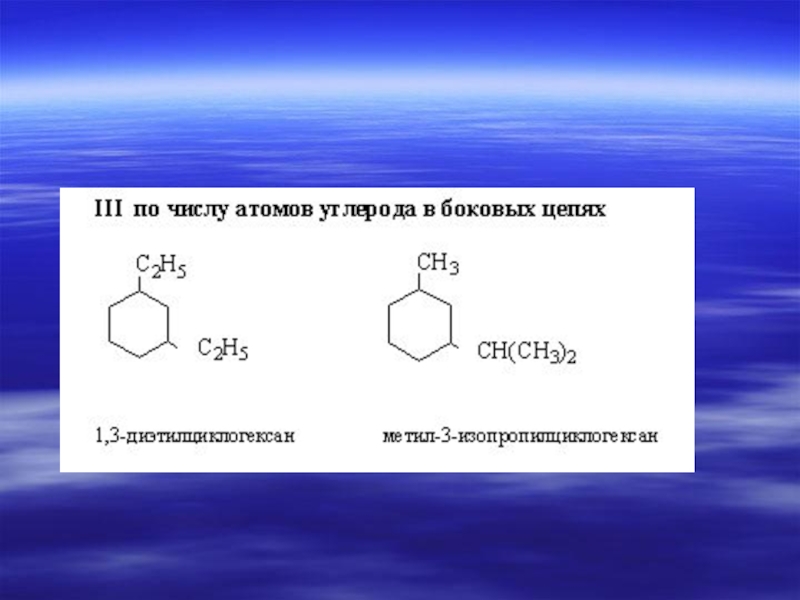
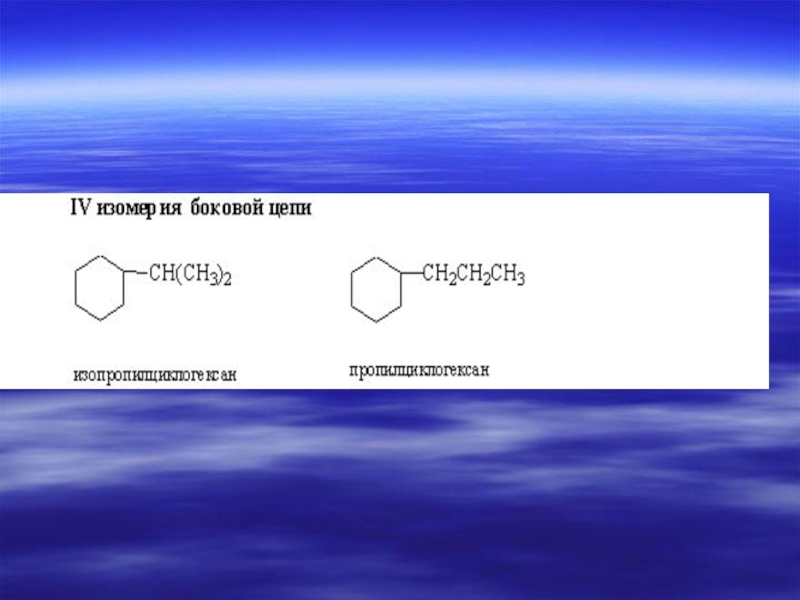
- 33. ИЗОМЕРИЯ
- 37. Бициклические нафтены СnH2n-2 Конденсированного типа
- 38. Мостикового типа
- 43. Спиро спиро [3,4] октан
- 44. Трициклические нафтены CnH2n-4 Пергидроантрацен Пергидрофенантрен адамантан
- 45. Моноциклические нафтены содержатся во фракциях выкипающих до
- 46. Физические свойства нафтенов Нафтены имеют
- 48. Введение метильной группы в молекулу нафтена резко
- 49. Химические свойства нафтенов Реакция дегидрогенизации. Реакция
- 50. Циклогексан и его гомологи в присутствии Pt,
- 51. Образование комплексов с тиомочевинной Нафтеновые углеводороды
- 52. Изомеризация Алкилпроизводные нафтенов с
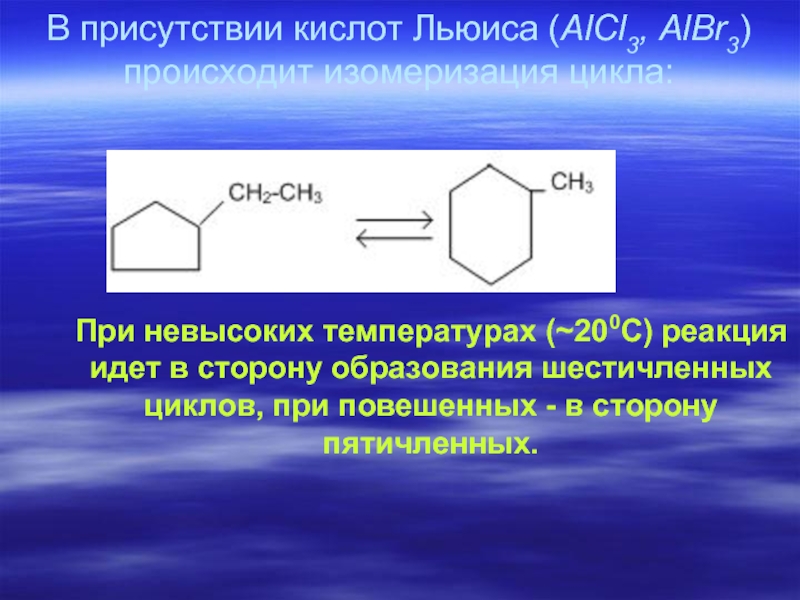
- 54. В присутствии кислот Льюиса (AlCl3, AlBr3) происходит
- 55. Реакция окисления. Устойчивость к кислороду у
- 56. Нафтены имеют более высокие октановые числа чем соответствующие им алканы
- 57. Автомобильные бензины В бензиновых фракциях содержатся моноциклические
- 58. Циклопентан содержится в очень небольших количествах (до
- 59. Углеводороды нефти Ароматические углеводороды. Арены. Содержание в нефтях в среднем 10-20%
- 60. Одноядерные арены СnH2n-6 Бензол
- 61. Толуол
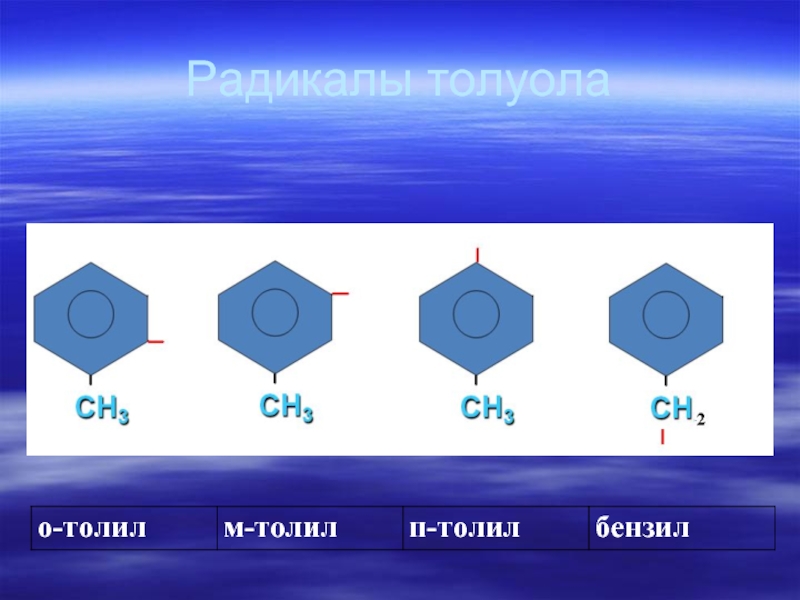
- 62. Радикалы толуола
- 63. СН3 1,2-диметилбензол Положение 1,2-орто О-диметилбензол о-ксилол СН3
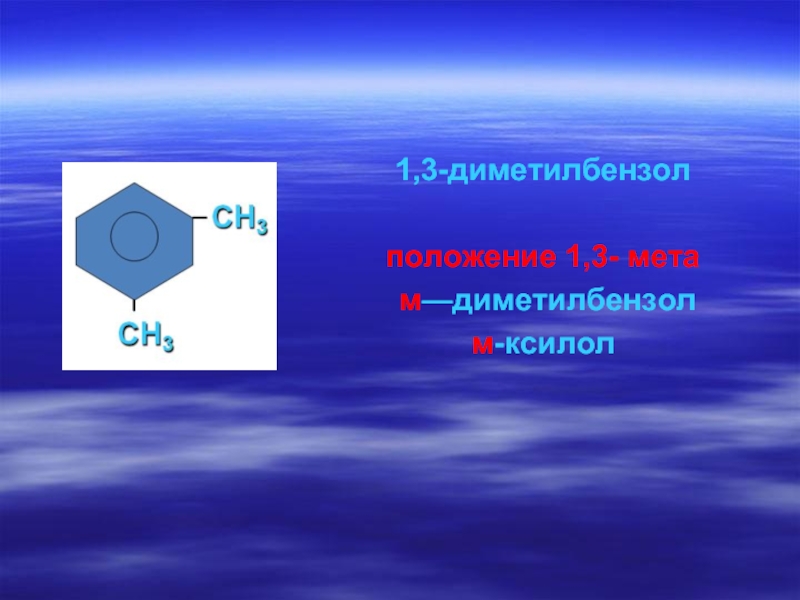
- 64. 1,3-диметилбензол положение 1,3- мета м—диметилбензол м-ксилол
- 65. 1,4-диметилбензол положение 1,4 –пара п-диметилбензол п-ксилол
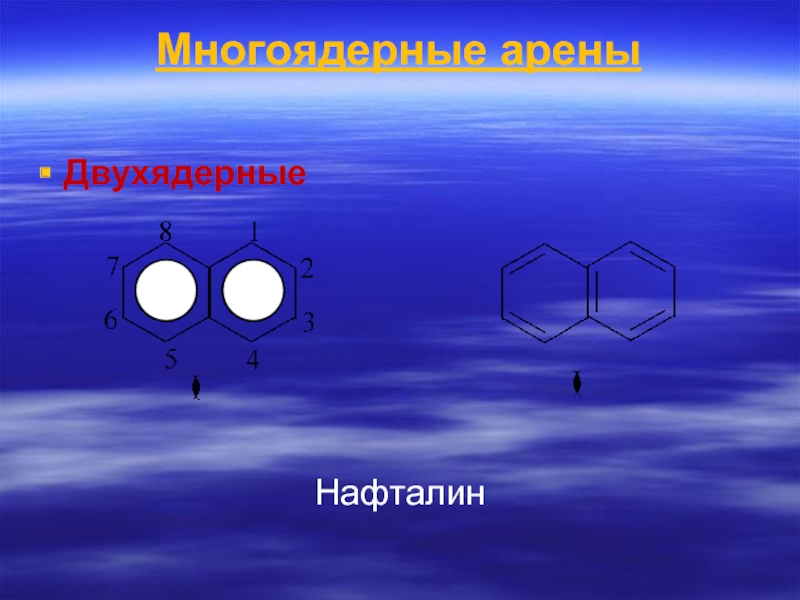
- 66. Многоядерные арены Двухядерные Нафталин
- 67. дифенилметан
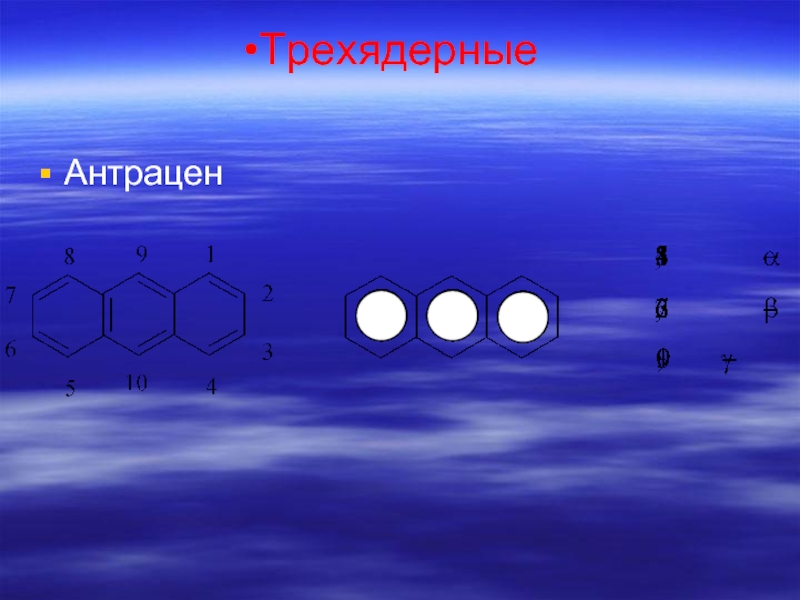
- 68. Трехядерные Антрацен
- 69. Фенантрен
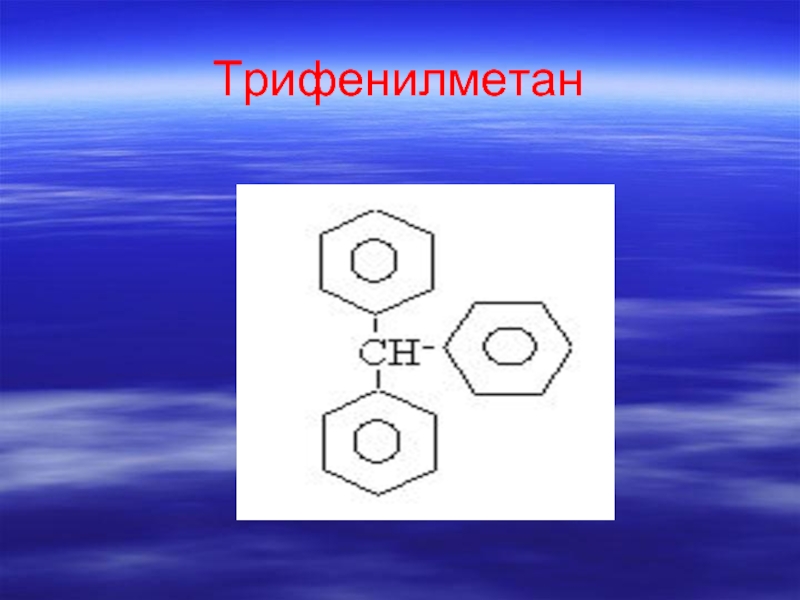
- 70. Трифенилметан
- 71. Четырехядерные ХРИЗЕН
- 72. ПИРЕН
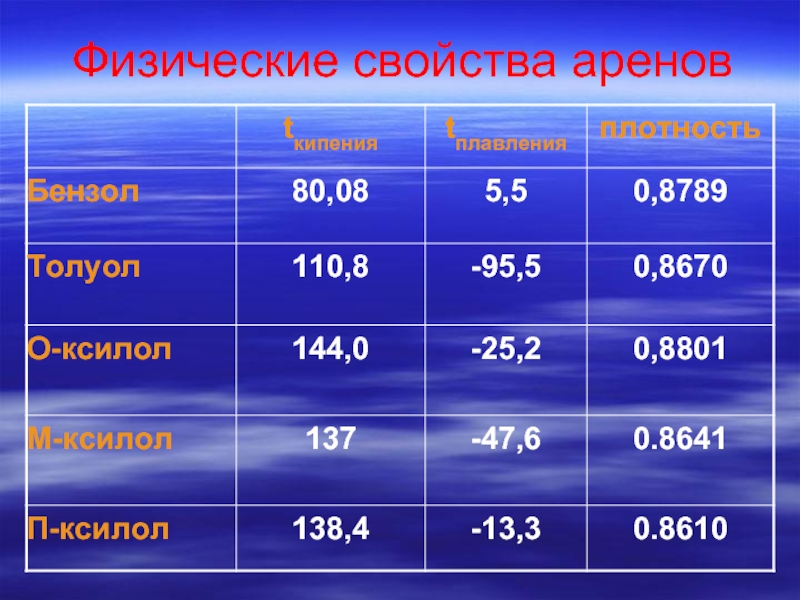
- 73. Физические свойства аренов
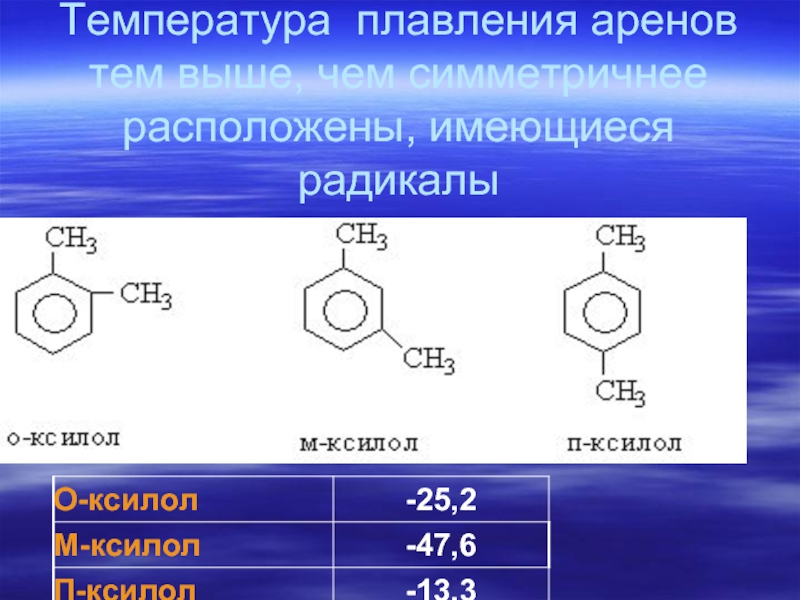
- 74. Температура плавления аренов тем выше, чем симметричнее расположены, имеющиеся радикалы
- 75. На температуру плавления в многоядерных конденсированных системах влияет взаимное расположение колец
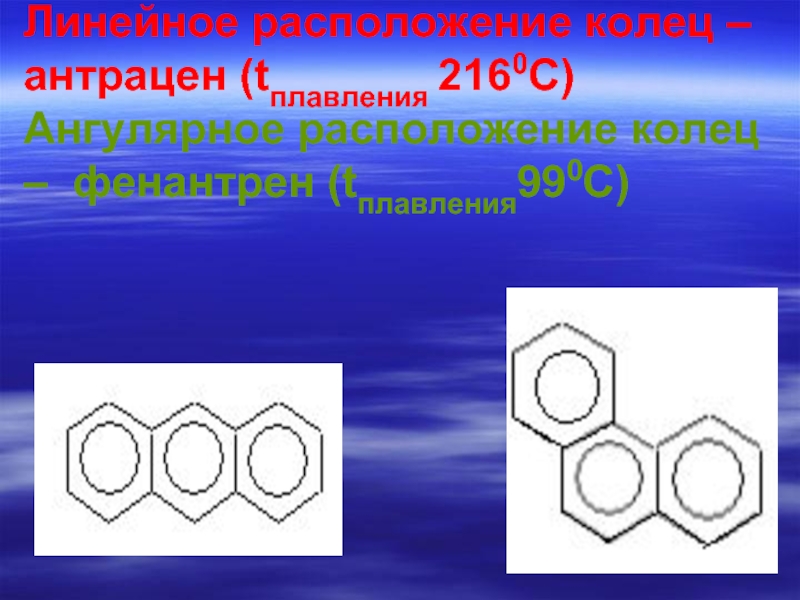
- 76. Линейное расположение колец – антрацен (tплавления 2160С) Ангулярное расположение колец – фенантрен (tплавления990С)
- 77. Окисление бензола Бензол не окисляется при нагревании
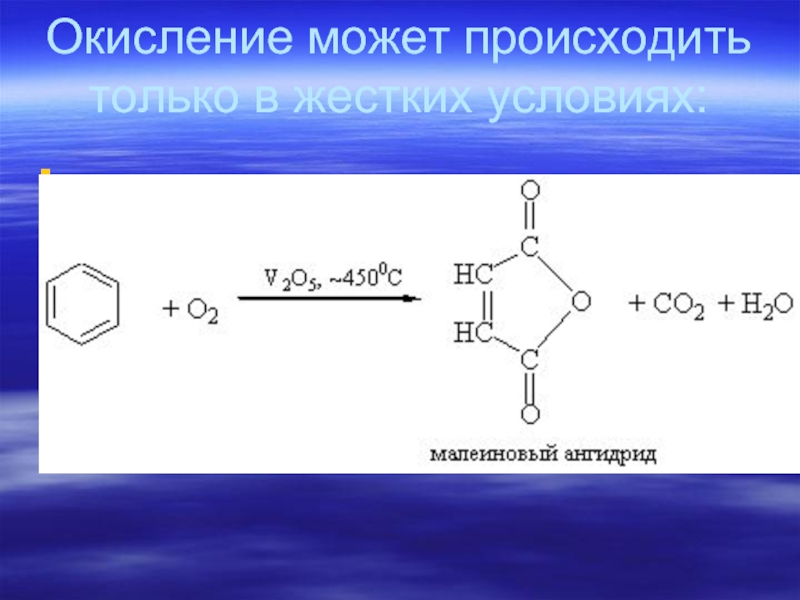
- 78. Окисление может происходить только в жестких условиях:
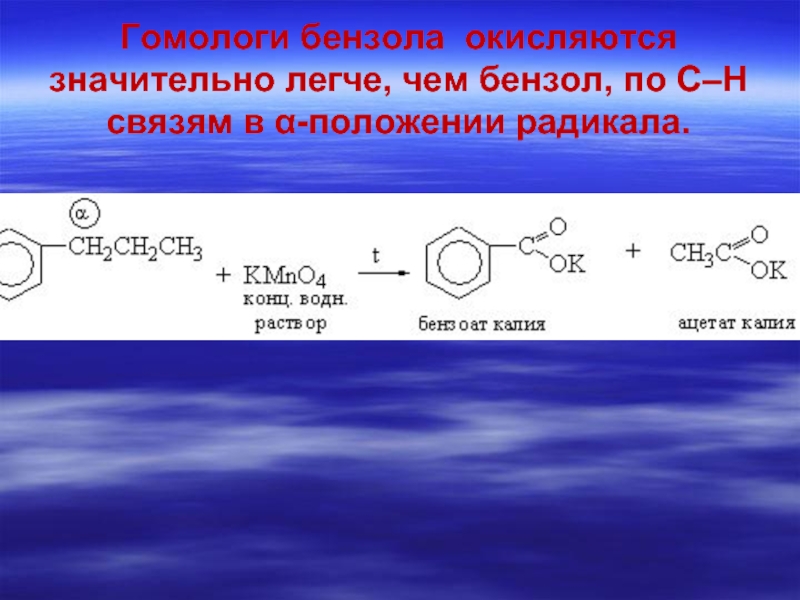
- 79. Гомологи бензола окисляются значительно легче, чем бензол, по С–Н связям в α-положении радикала.
- 80. Александр Флавианович Добрянский В зависимости от содержания
- 81. Первый класс – с плотностью 0,900
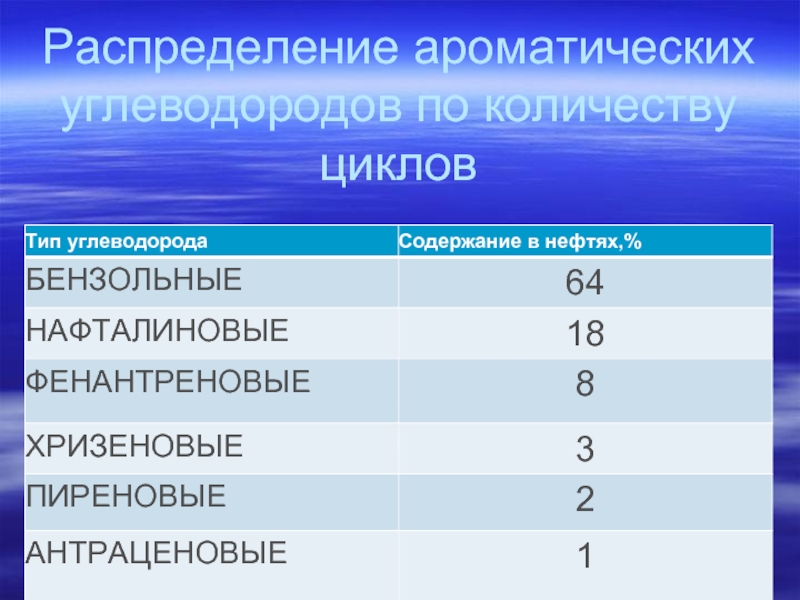
- 82. Распределение ароматических углеводородов по количеству циклов
- 83. В бензиновой фракции нефти Понка-Сити соотношение аренов С6:С7:С8:С9
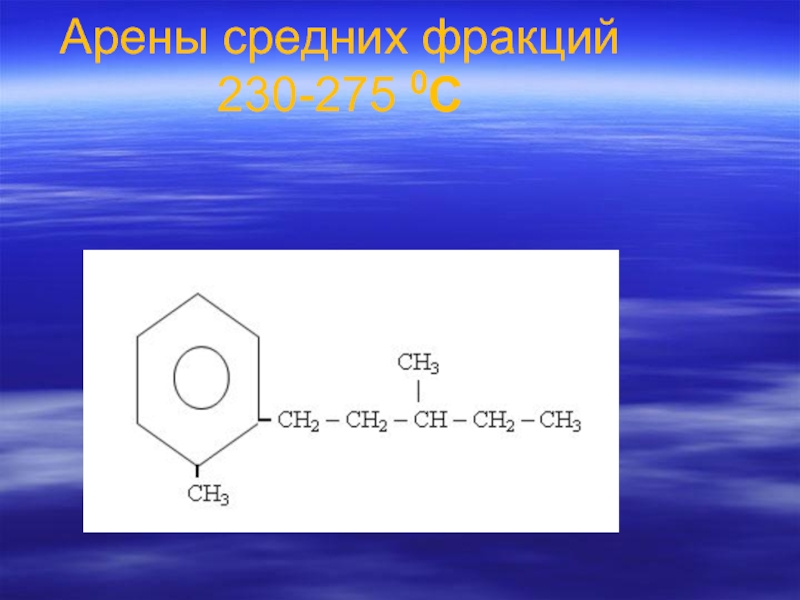
- 84. Арены средних фракций 230-275 0С
- 85. Алкильная цепь имеет изопреноидное строение
Слайд 1Углеводороды нефти
Алканы. Парафины
Содержание в нефтях в среднем 25-35%
(не считая растворенных газов)
Слайд 7Газообразные парафиновые углеводороды входят в состав природных углеводородных газов, которые в
Слайд 12Газообразные парафины дают комплексы с водой, они называются гидратами природных газов,
Слайд 14
Систематическая номенклатура алканов
(ИЮПАК; JUPAC; Международный союз теоретической и прикладной химии)
1.
Выбирают
(при одинаковой длине выбирают наиболее разветвленную)
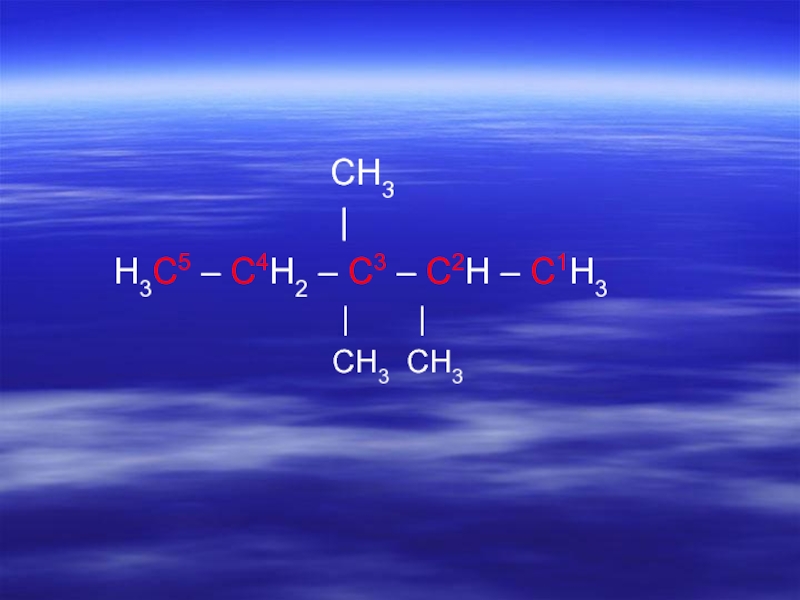
Слайд 172. Нумеруют атомы углерода в цепи, с того конца, к которому ближе
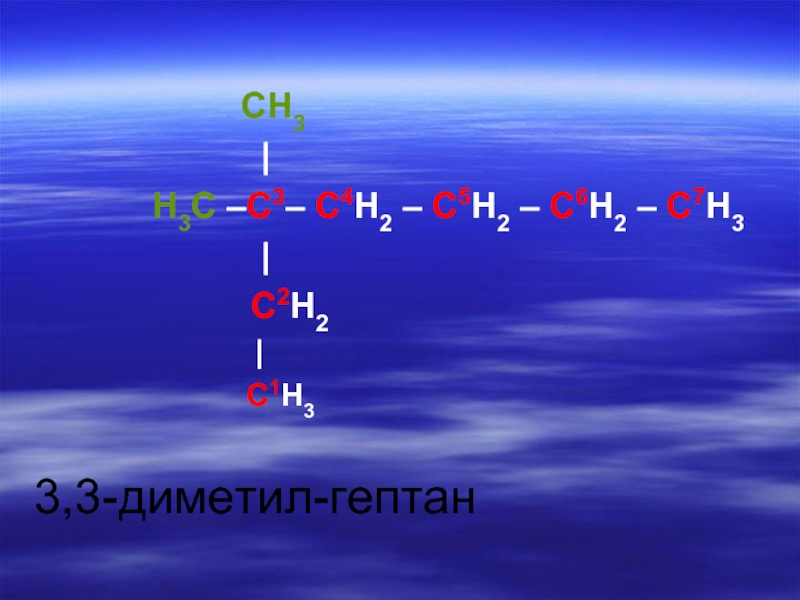
Слайд 213. Перечисляют все радикалы (в порядке возрастания сложности) перед каждым радикалом ставится
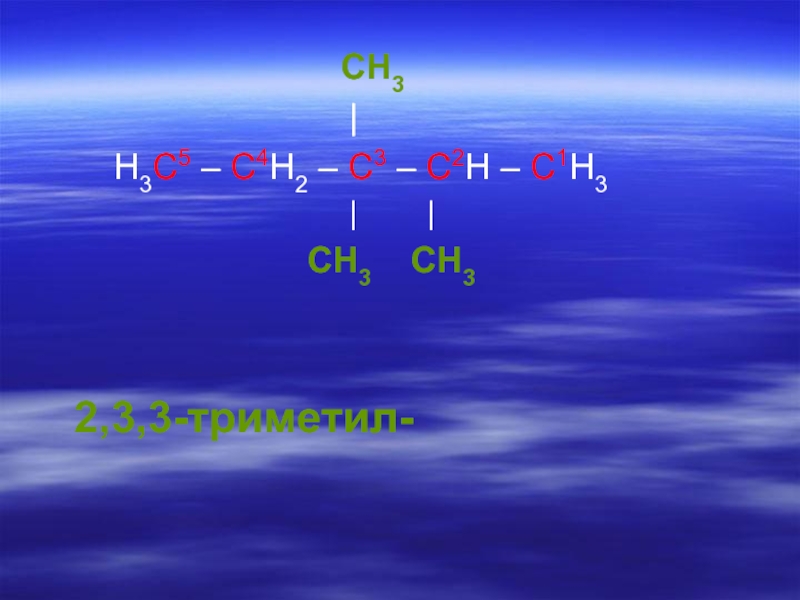
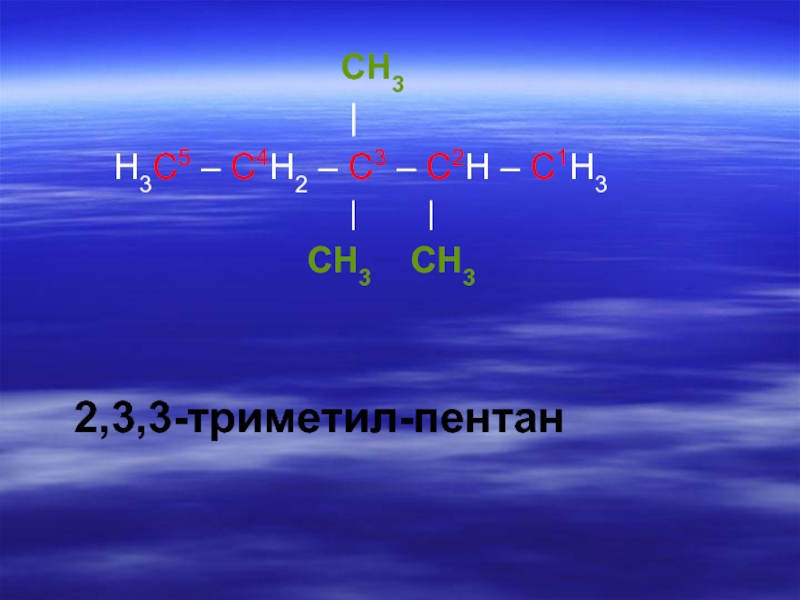
Слайд 244. Дают название пронумерованной цепи, которое соответствует названию нормального алкана, состоящего из
Слайд 28Вывод:
Среди алканов нормального строения с ростом числа атомов углерода
температура кипения
температура плавления
плотность
Слайд 30Вывод:
Среди алканов одинакового состава, но разного строения минимальными показателями:
температура кипения
температура
плотность
обладают наиболее разветвленные из них
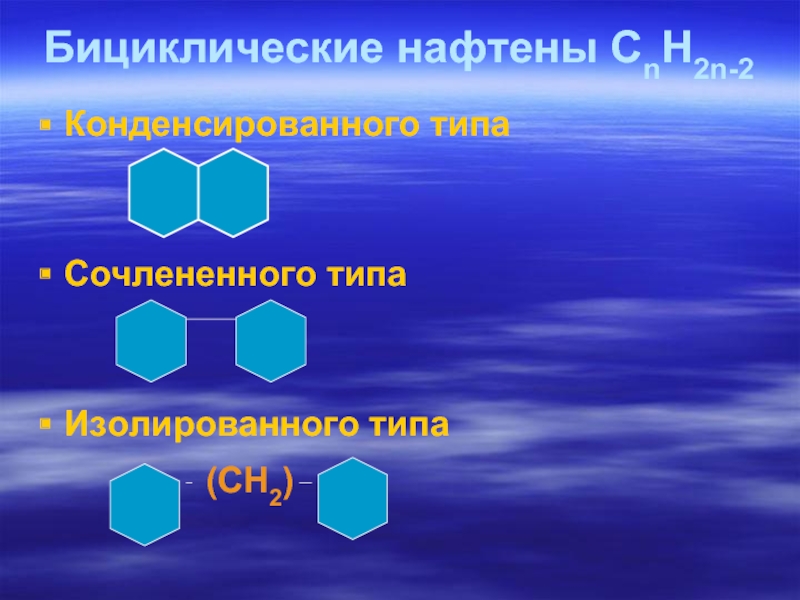
Слайд 37Бициклические нафтены СnH2n-2
Конденсированного типа
Сочлененного типа
Изолированного типа
(CH2)
Слайд 45Моноциклические нафтены содержатся во фракциях выкипающих до 3000С и содержатся они
Слайд 46Физические свойства нафтенов
Нафтены имеют более высокие температуры кипения и
Это объясняется тем, что вследствие более правильной, более жесткой структуры - молекулы нафтенов плотнее упаковываются в жидком или твердом состоянии, что увеличивает силы межмолекулярного взаимодействия.
Слайд 48Введение метильной группы в молекулу нафтена резко нарушает симметрию молекулы ,
Слайд 49Химические свойства нафтенов
Реакция дегидрогенизации.
Реакция была открыта и изучена Н. Д. Зеленским
Никола́й Дми́триевич Зели́нский (1861 (1861- 1953 (1861- 1953) — выдающийся русский и советский химик (1861- 1953) — выдающийся русский и советский химик-органик, создатель научной школы, один из основоположников органического катализа (1861- 1953) — выдающийся русский и советский химик-органик, создатель научной школы, один из основоположников органического катализа и нефтехимии (1861- 1953) — выдающийся русский и советский химик-органик, создатель научной школы, один из основоположников органического катализа и нефтехимии, академик АН СССР (1861- 1953) — выдающийся русский и советский химик-органик, создатель научной школы, один из основоположников органического катализа и нефтехимии, академик АН СССР (1929 (1861- 1953) — выдающийся русский и советский химик-органик, создатель научной школы, один из основоположников органического катализа и нефтехимии, академик АН СССР (1929), Герой Социалистического Труда (1945 (1861- 1953) — выдающийся русский и советский химик-органик, создатель научной школы, один из основоположников органического катализа и нефтехимии, академик АН СССР (1929), Герой Социалистического Труда (1945), лауреат (1861- 1953) — выдающийся русский и советский химик-органик, создатель научной школы, один из основоположников органического катализа и нефтехимии, академик АН СССР (1929), Герой Социалистического Труда (1945), лауреат Ленинской (1861- 1953) — выдающийся русский и советский химик-органик, создатель научной школы, один из основоположников органического катализа и нефтехимии, академик АН СССР (1929), Герой Социалистического Труда (1945), лауреат Ленинской и Сталинской премий.
Слайд 50Циклогексан и его гомологи в присутствии Pt, Pd при 300 0С
При анализе нафтенов эта реакция используется для отделения шестичленных циклов от пятичленных
Слайд 51Образование комплексов с тиомочевинной
Нафтеновые углеводороды образуют соединения включения (клатраты) с тиомочевиной
Молекулы тиомочевины за счет водородных связей образуют спирали внутрь, которых помещаются молекулы нафтенов.
Прочность образующихся соединений зависит от величины и строения молекул циклоалканов. С помощью тиомочевины можно разделить моно- и полициклические нафтены (последние образуют более прочные комплексы с тиомочевиной).
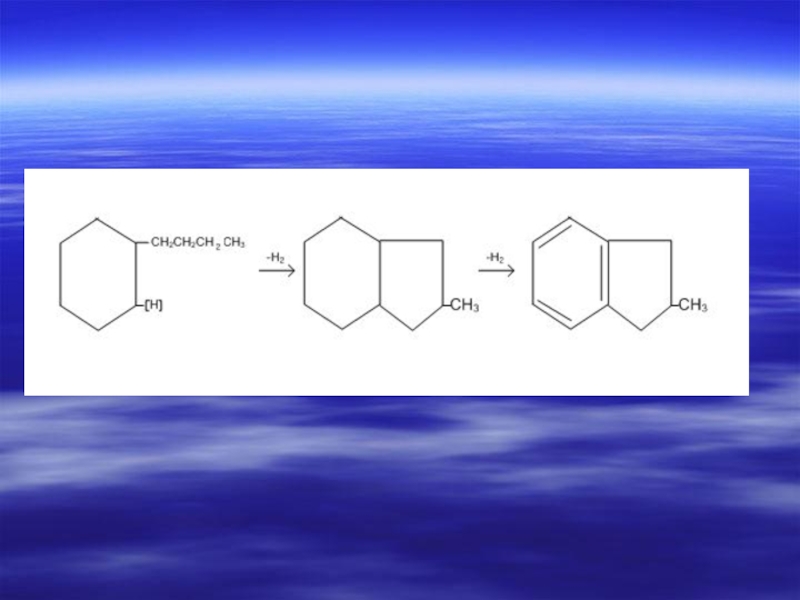
Слайд 52Изомеризация
Алкилпроизводные нафтенов с
достаточно длинной углеродной цепью
(С3 и более) над
образуют бициклические
углеводороды:
Слайд 54В присутствии кислот Льюиса (AlCl3, AlBr3) происходит изомеризация цикла:
При невысоких температурах
Слайд 55Реакция окисления.
Устойчивость к кислороду у нафтенового цикла ниже, чем у ароматического.
При
Образующиеся кислоты окисляются в оксикислоты, которые при дальнейшей конденсации дают смолы.
Пятичленный цикл более устойчив к окислению, чем шестичленный

























![Спироспиро [3,4] октан](/img/tmb/2/188135/bb3d36e535726cb3ab4327894a5fbac1-800x.jpg)