ТЭД»
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основания: классификация и свойства в свете ТЭД презентация
Содержание
- 1. Основания: классификация и свойства в свете ТЭД
- 2. Исключите «лишнее», объясните свой выбор: HCl,
- 3. Найдите соответствие между характеристиками и формулами кислот:
- 4. Определите, с какими металлами будет взаимодействовать разб.
- 5. Найдите и исправьте ошибки в следующих уравнениях:
- 6. Найдите и исправьте ошибки в следующих уравнениях:
- 7. Даны формулы веществ. Выпишите кислоты и назовите
- 8. Основания: классификация и свойства в свете ТЭД
- 9. ПЛАН 1.Состав оснований 2.Классификация оснований 3.Химические свойства
- 10. Физические свойства
- 11. Гигроскопичность NaOH
- 12. По растворимости в воде NaOH
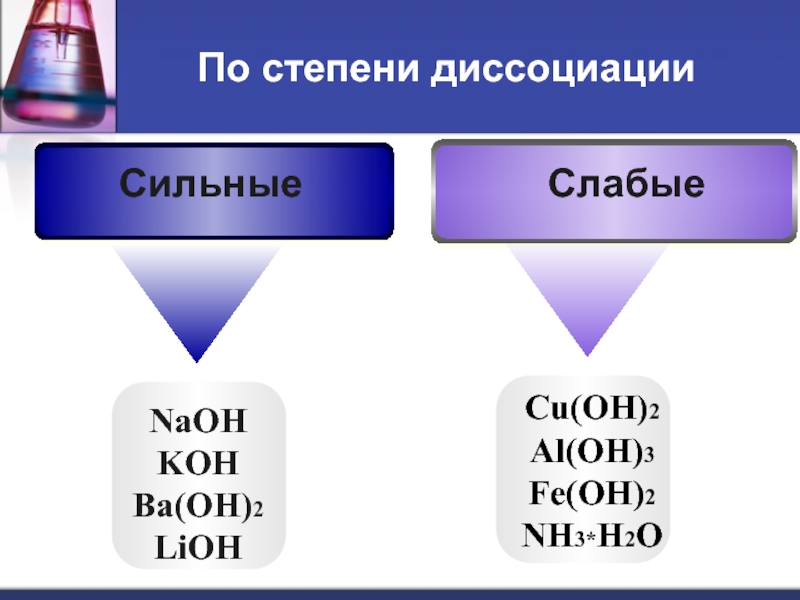
- 13. По степени диссоциации NaOH KOH
- 14. По какому признаку основания разделены на группы?
- 15. По кислотности NaOH KOH LiOH СsOH
- 16. Химические свойства оснований 1.Щелочь + индикатор
- 17. Химические свойства оснований 2. Щелочь + соль,
- 18. NaOH
- 19. KOH Ca(OH)2 Mg(OH)2
- 20. Выполни задание Выпишите формулы оснований.
Слайд 2Исключите «лишнее», объясните свой выбор:
HCl, CaO, NaOH, KOH
H2S, H2CO3, H2SO4, HNO2
+ 2+ + -
Li , Mg , Na , Cl
Li , Mg , Na , Cl
Слайд 3Найдите соответствие между характеристиками и формулами кислот:
1.Одноосновная, летучая, сильный электролит, кислородсодержащая.
2.Двухосновная,
нелетучая, сильный электролит, стабильная.
3.Двухосновная, нестабильная, слабый электролит.
А) H2SO4, Б) H2CO3, В) HCl, г) HNO3
3.Двухосновная, нестабильная, слабый электролит.
А) H2SO4, Б) H2CO3, В) HCl, г) HNO3
Слайд 4Определите, с какими металлами будет взаимодействовать разб. H2SO4:
1) Ag
2) Zn
3) Hg
4)
Cu
5) Mg
Запишите в тетради уравнение одной реакции
5) Mg
Запишите в тетради уравнение одной реакции
Слайд 5Найдите и исправьте ошибки в следующих уравнениях:
K2CO3 +HCl = 2KCl +
H2O + CO2
+ 2- + - +
2K + CO3 + 2H + 2Cl = 2K + H2O +CO2
2-
2H + CO3 = H2O + CO2
+ 2- + - +
2K + CO3 + 2H + 2Cl = 2K + H2O +CO2
2-
2H + CO3 = H2O + CO2
Слайд 6Найдите и исправьте ошибки в следующих уравнениях:
K2CO3 +2HCl = 2KCl +
H2O + CO2
+ 2- + - + -
2K +CO3 + 2H +2Cl =2K +2Сl+H2O +CO2
+ 2-
2H + CO3 = H2O + CO2
+ 2- + - + -
2K +CO3 + 2H +2Cl =2K +2Сl+H2O +CO2
+ 2-
2H + CO3 = H2O + CO2
Слайд 7Даны формулы веществ. Выпишите кислоты и назовите их:
HCl, NaOH,
Ba(OH)2 , H3PO4,
H2S, Mg(OH)2, Al(OH)3, H2SO3,
HNO2
H2S, Mg(OH)2, Al(OH)3, H2SO3,
HNO2
Слайд 9ПЛАН
1.Состав оснований
2.Классификация оснований
3.Химические свойства
а)щелочей
б)нерастворимых оснований
4.Применение оснований
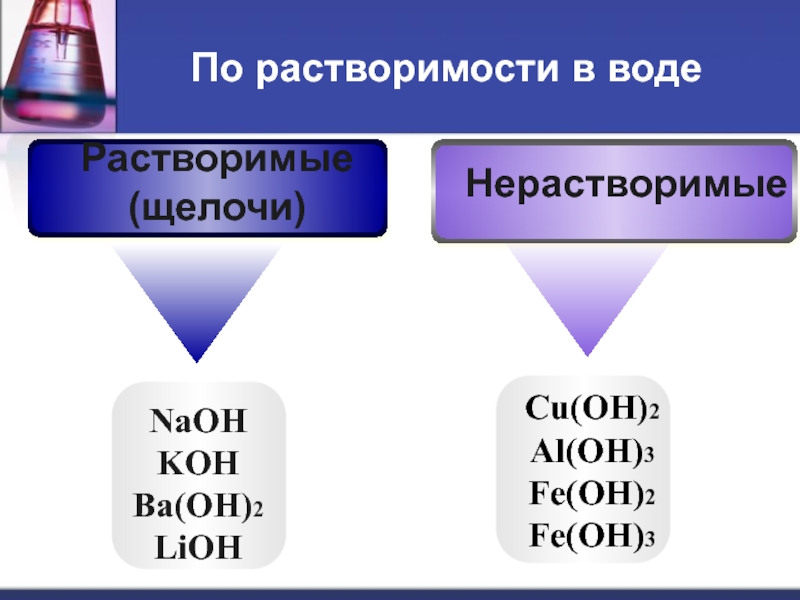
Слайд 12По растворимости в воде
NaOH
KOH
Ba(OH)2
LiOH
Cu(OH)2
Al(OH)3
Fe(OH)2
Fe(OH)3
Нерастворимые
Растворимые
(щелочи)
Слайд 14По какому признаку основания разделены на группы?
NaOH
KOH
LiOH
СsOH
Cu(OH)2
Ba(OH)2
Pb(OH)2
Fe(OH)2
Al(OH)3
Fe(OH)3
?
?
?
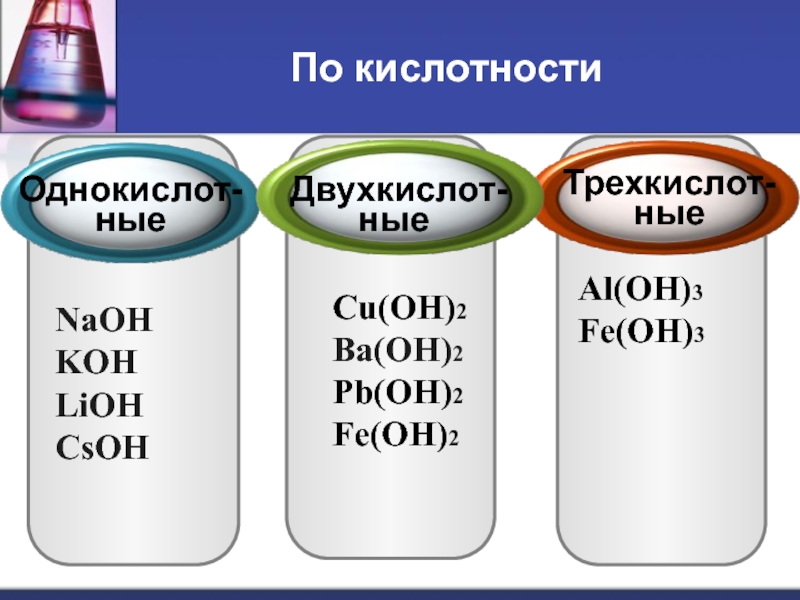
Слайд 15По кислотности
NaOH
KOH
LiOH
СsOH
Cu(OH)2
Ba(OH)2
Pb(OH)2
Fe(OH)2
Al(OH)3
Fe(OH)3
Однокислот-ные
Трехкислот-ные
Двухкислот-ные
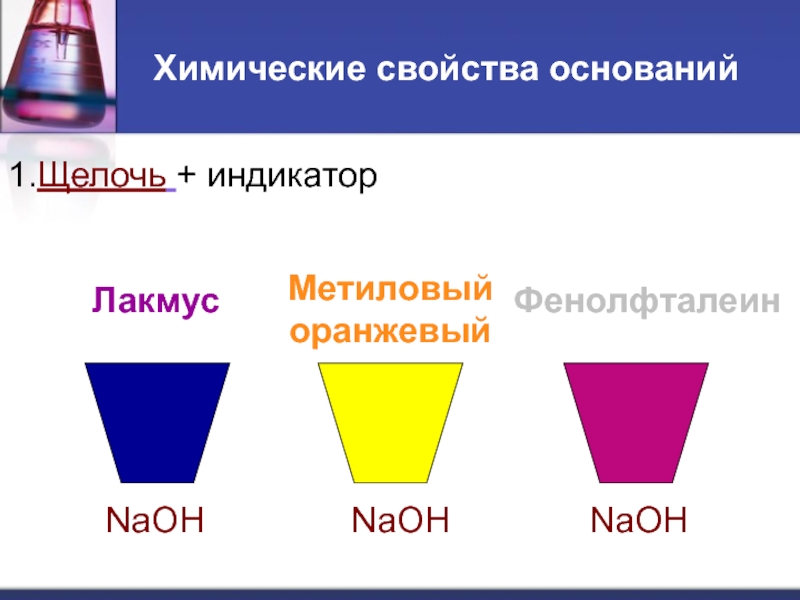
Слайд 16Химические свойства оснований
1.Щелочь + индикатор
Лакмус
Метиловый оранжевый
Фенолфталеин
NaOH
NaOH
NaOH
Слайд 17Химические свойства оснований
2. Щелочь + соль, если образуется осадок или газ
NaOH + CuSO4
3. Щелочь + кислотный или амфотерный оксид
NaOH + SO2
4.Основание + кислота
Cu(OH)2 + H2SO4
5.Нерастворимое основание разлагается при нагревании
t
Cu(OH)2 =
3. Щелочь + кислотный или амфотерный оксид
NaOH + SO2
4.Основание + кислота
Cu(OH)2 + H2SO4
5.Нерастворимое основание разлагается при нагревании
t
Cu(OH)2 =
Слайд 20Выполни задание
Выпишите формулы оснований. Охарактеризуйте одно из них по
всем признакам.
Вариант 1.
Н2OSOHBa(OH)2Na4CO2MgHCSOKOH
Вариант 2.
HClMg(OH)2SHK2SO4NaOHSiONaHSO2
Вариант 1.
Н2OSOHBa(OH)2Na4CO2MgHCSOKOH
Вариант 2.
HClMg(OH)2SHK2SO4NaOHSiONaHSO2