- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Структурно-функциональные основы протеомики. Первичная структура белка презентация
Содержание
- 1. Структурно-функциональные основы протеомики. Первичная структура белка
- 2. План лекции Свойства аминокислот Химический состав белков Первичная структура
- 3. Свойства аминокислот
- 4. Жизнь – функционирование молекулярных сетей Молекулярная сеть в клетке (Из ExPASy Biochemical Pathways; http://www.expasy.org/cgi-bin/show_thumbnails.pl?2)
- 5. Аминокислоты – структурные единицы белка Аминокислота
- 6. 20 аминокислот Glycine (G) Glutamic
- 7. задача Сколько полипептидных последовательностей с длиной полипептидной
- 8. Ионизационное равновесие в белках Методы исследования: Потенциометрическое титрование ЯМР Спектроскопия поглощения
- 9. Ионизация амино- и карбоксильных групп При рН
- 10. Полярность боковых групп АК Ala, Val, Leu,
- 11. Химический состав белков
- 12. Шкала средней гидрофобности белков 0,44-2,02
- 13. Предсказание свойств белков по аминокислотному составу Разграничение
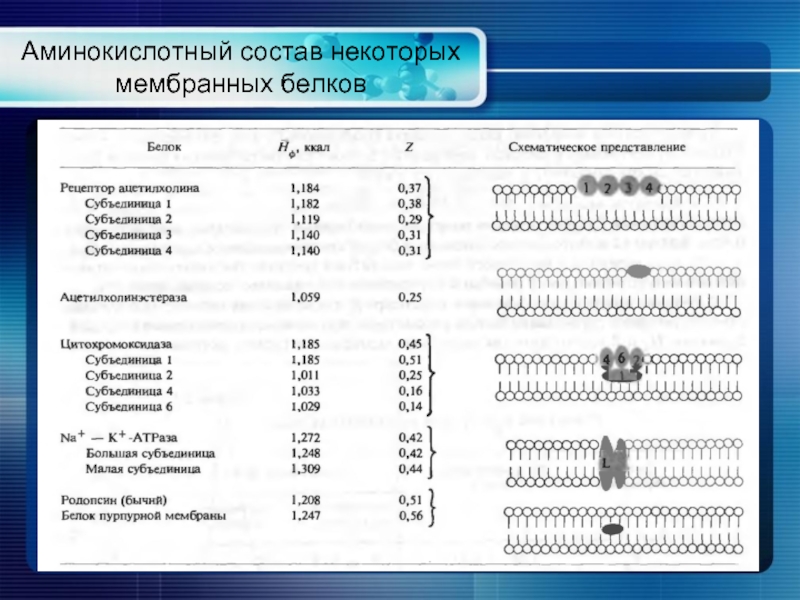
- 14. Аминокислотный состав некоторых мембранных белков
- 15. Необычные аминокислоты Трипсиноген Трипсин Lys15-Ile16 Разрыв
- 16. Металлы и простетические группы Стабилизация структуры (щелочные
- 17. Оптические свойства белков Поглощение белков в ближней УФ-области обусловлено ароматическими аминокислотами
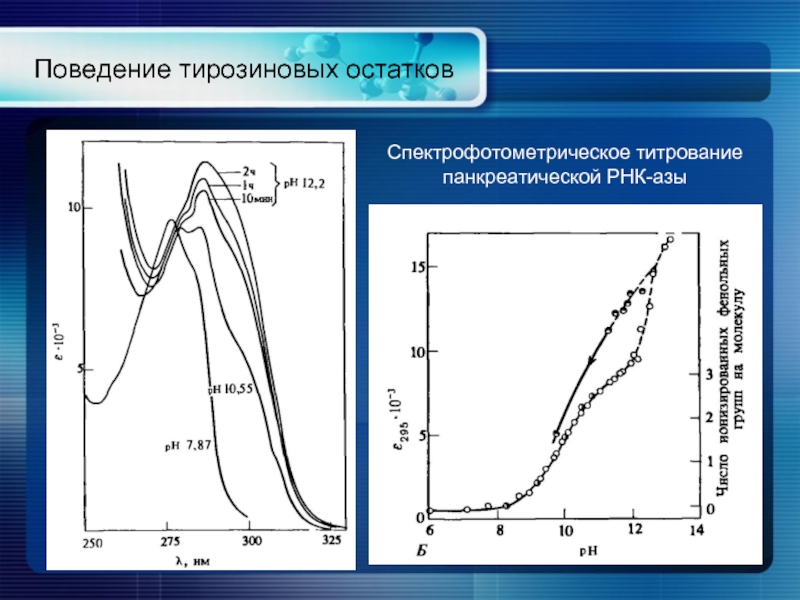
- 18. Поведение тирозиновых остатков Спектрофотометрическое титрование панкреатической РНК-азы
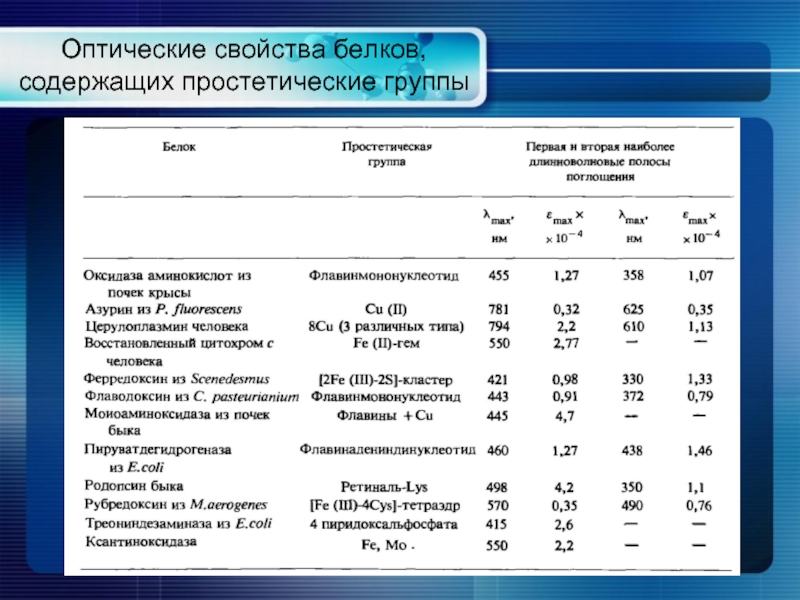
- 19. Оптические свойства белков, содержащих простетические группы
- 20. Задача Был определен аминокислотный состав
- 21. Первичная структура
- 22. Белки – линейные полимеры R1 NH3+ C
- 23. Дисульфидные и другие поперечные связи Система связей
- 24. Задача Молекулярная масса неизвестного белка, определенная с
- 25. Первичная структура и анализ вторичной и третичной
- 26. Первичная структура и предсказание вторичной и третичной структур Распределение различных типов вторичной структуры в аденилаткиназе
- 27. АК последовательность белка и анализ его функций
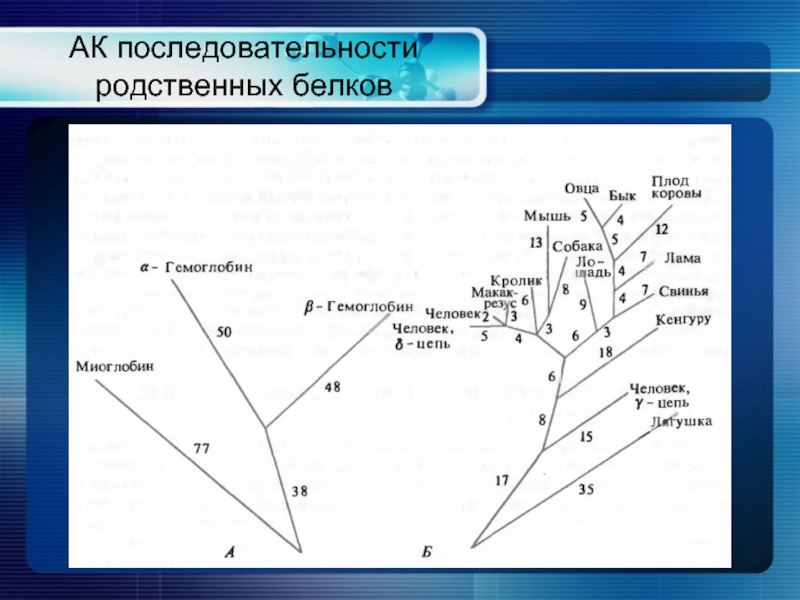
- 28. АК последовательности родственных белков
- 29. Гемоглобин Существуют сотни мутантных форм гемоглобина Серповидноклеточная
- 30. Заключение Белки – АК, металлы, простетические группы,
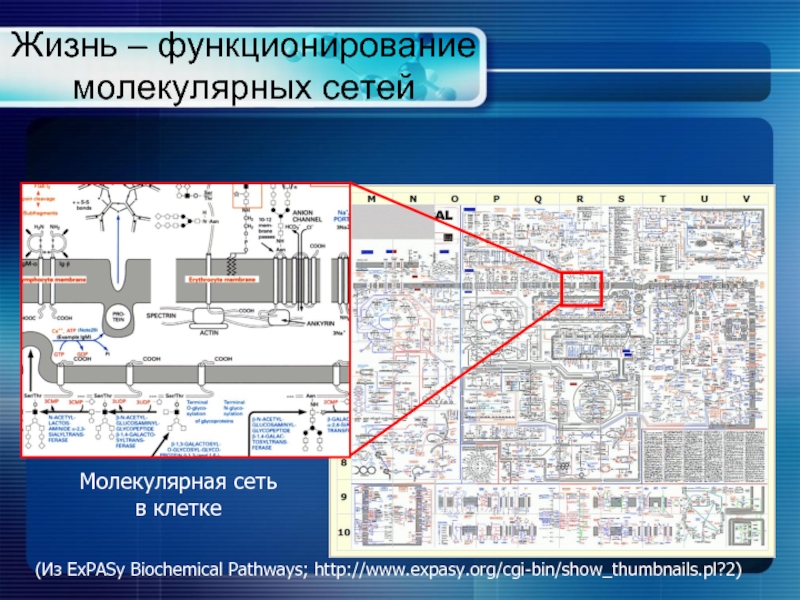
Слайд 4Жизнь – функционирование молекулярных сетей
Молекулярная сеть в клетке
(Из ExPASy Biochemical Pathways;
Слайд 5
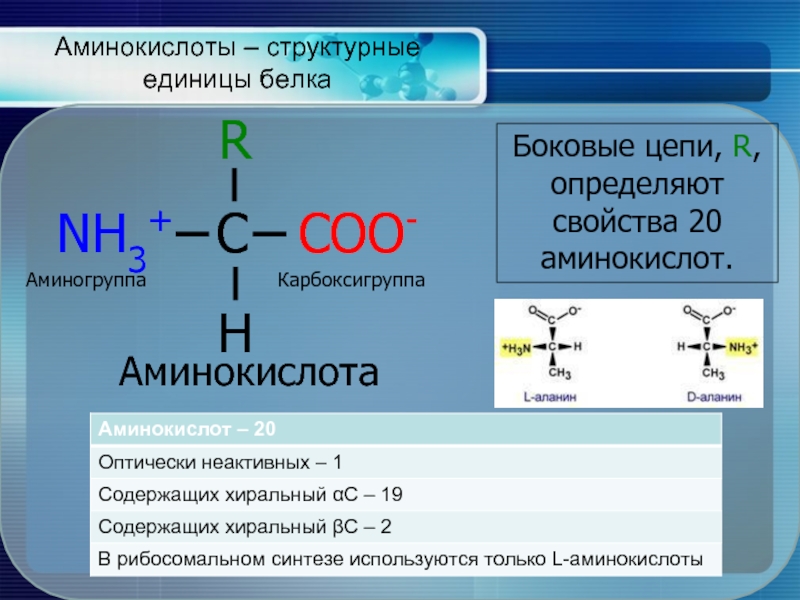
Аминокислоты – структурные единицы белка
Аминокислота
Боковые цепи, R, определяют свойства 20 аминокислот.
Аминогруппа
Карбоксигруппа
Слайд 620 аминокислот
Glycine (G)
Glutamic acid (E)
Asparatic acid (D)
Methionine (M)
Threonine (T)
Serine (S)
Glutamine (Q)
Asparagine
Tryptophan (W)
Phenylalanine (F)
Cysteine (C)
Proline (P)
Leucine (L)
Isoleucine (I)
Valine (V)
Alanine (A)
Histidine (H)
Lysine (K)
Tyrosine (Y)
Arginine (R)
White: Hydrophobic, Green: Hydrophilic, Red: Acidic, Blue: Basic
Слайд 7задача
Сколько полипептидных последовательностей с длиной полипептидной цепи 5 аминокислотных остатков можно
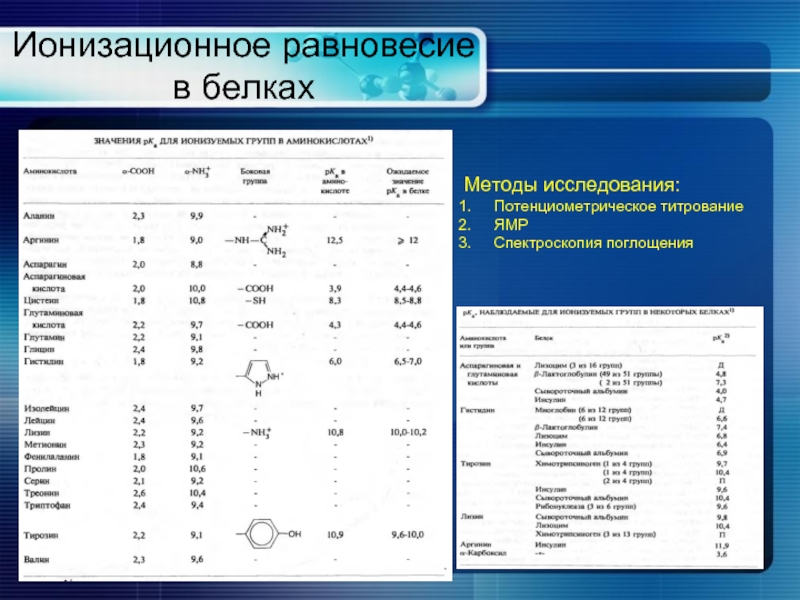
Слайд 8Ионизационное равновесие в белках
Методы исследования:
Потенциометрическое титрование
ЯМР
Спектроскопия поглощения
Слайд 9Ионизация амино- и карбоксильных групп
При рН 7.0:
α-аминогруппа протонирована (+)
α-карбоксильная группа депротонирована
Аминокислоты существуют в виде цвиттериона
Ионизация α-аминогрупп и α-карбоксильных групп аминокислот отличается от тех же групп в составе полипептидов
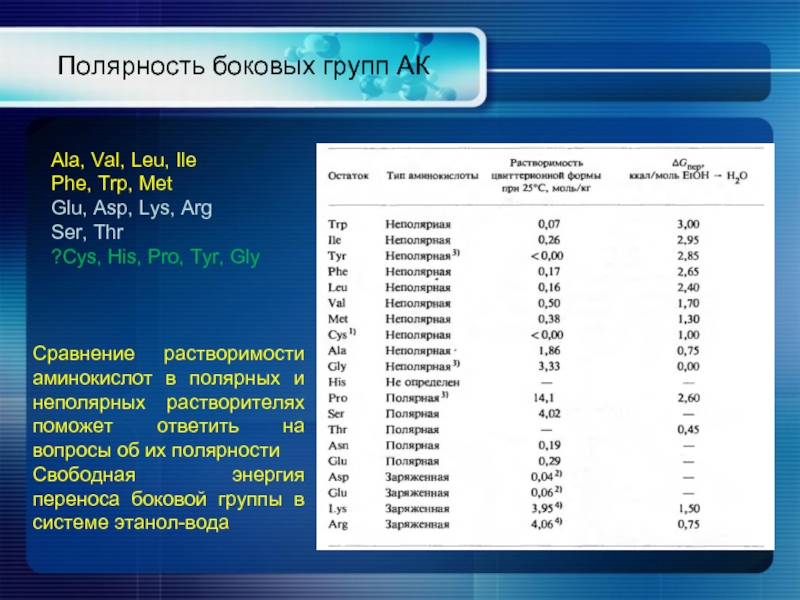
Слайд 10Полярность боковых групп АК
Ala, Val, Leu, Ile
Phe, Trp, Met
Glu, Asp, Lys,
Ser, Thr
?Cys, His, Pro, Tyr, Gly
Сравнение растворимости аминокислот в полярных и неполярных растворителях поможет ответить на вопросы об их полярности
Свободная энергия переноса боковой группы в системе этанол-вода
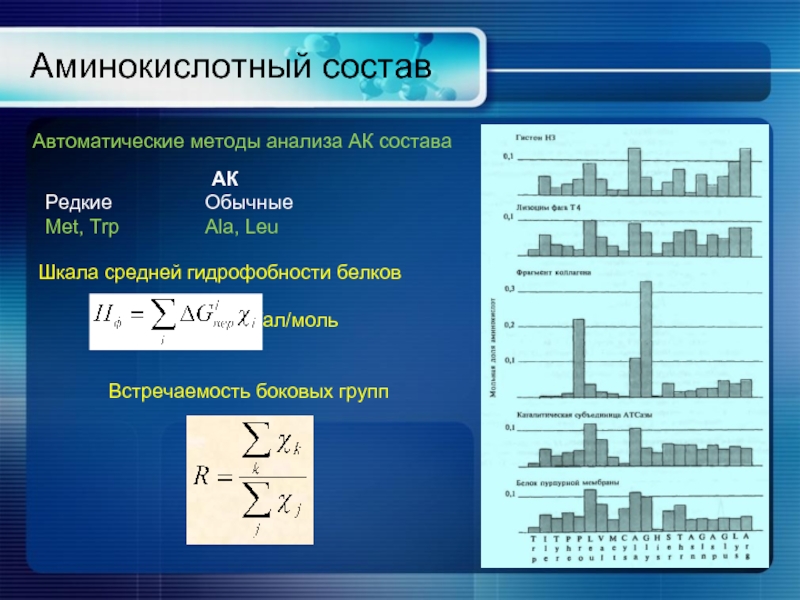
Слайд 12 Шкала средней гидрофобности белков
0,44-2,02 кКал/моль
Аминокислотный состав
Автоматические методы анализа АК состава
АК
Редкие Обычные
Met,
Встречаемость боковых групп
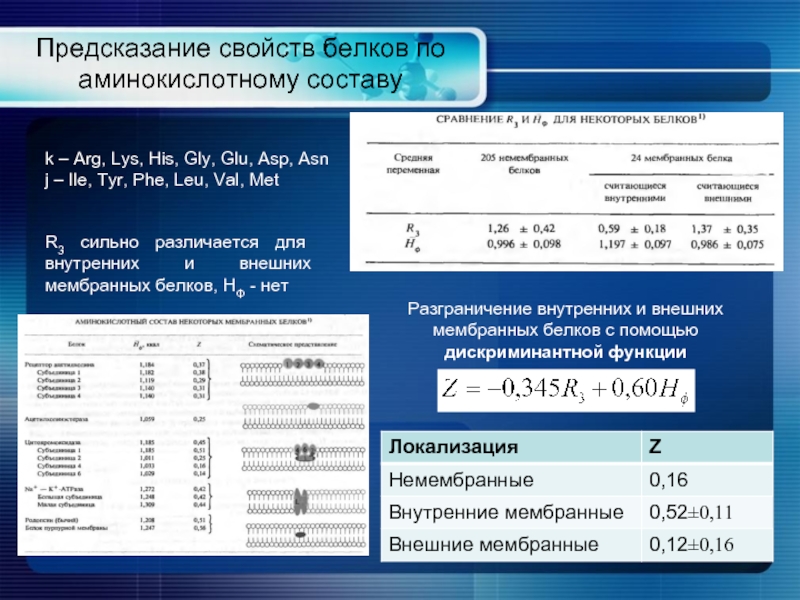
Слайд 13Предсказание свойств белков по аминокислотному составу
Разграничение внутренних и внешних мембранных белков
R3 сильно различается для внутренних и внешних мембранных белков, HΦ - нет
k – Arg, Lys, His, Gly, Glu, Asp, Asn
j – Ile, Tyr, Phe, Leu, Val, Met
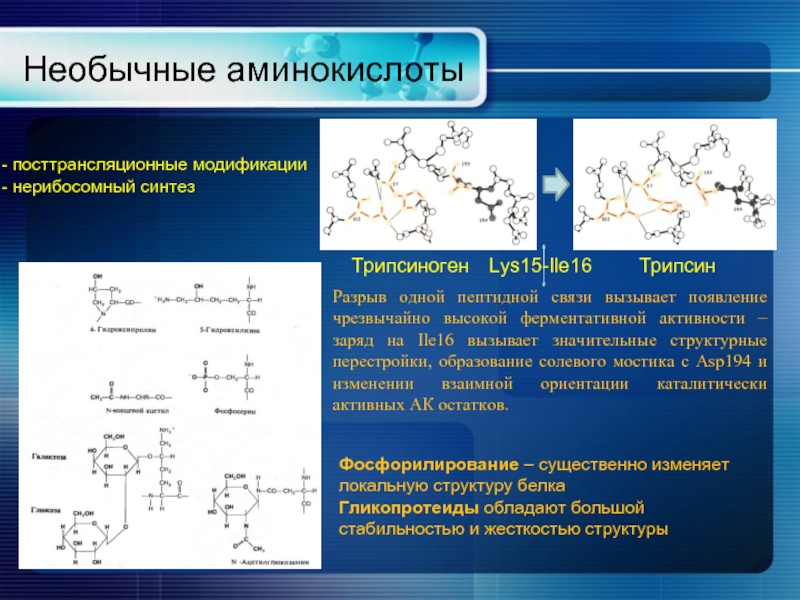
Слайд 15Необычные аминокислоты
Трипсиноген
Трипсин
Lys15-Ile16
Разрыв одной пептидной связи вызывает появление чрезвычайно высокой ферментативной активности
посттрансляционные модификации
нерибосомный синтез
Фосфорилирование – существенно изменяет локальную структуру белка
Гликопротеиды обладают большой стабильностью и жесткостью структуры
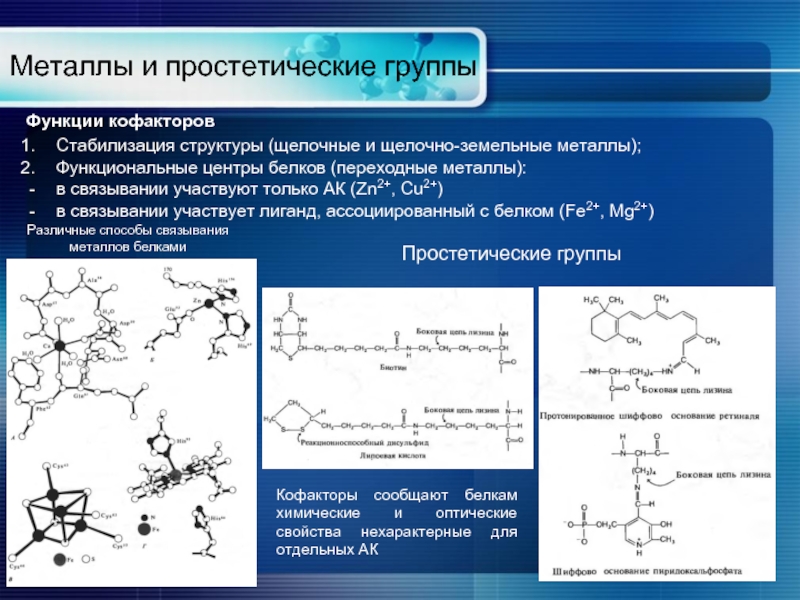
Слайд 16Металлы и простетические группы
Стабилизация структуры (щелочные и щелочно-земельные металлы);
Функциональные центры белков
в связывании участвуют только АК (Zn2+, Cu2+)
в связывании участвует лиганд, ассоциированный с белком (Fe2+, Mg2+)
Различные способы связывания металлов белками
Функции кофакторов
Простетические группы
Кофакторы сообщают белкам химические и оптические свойства нехарактерные для отдельных АК
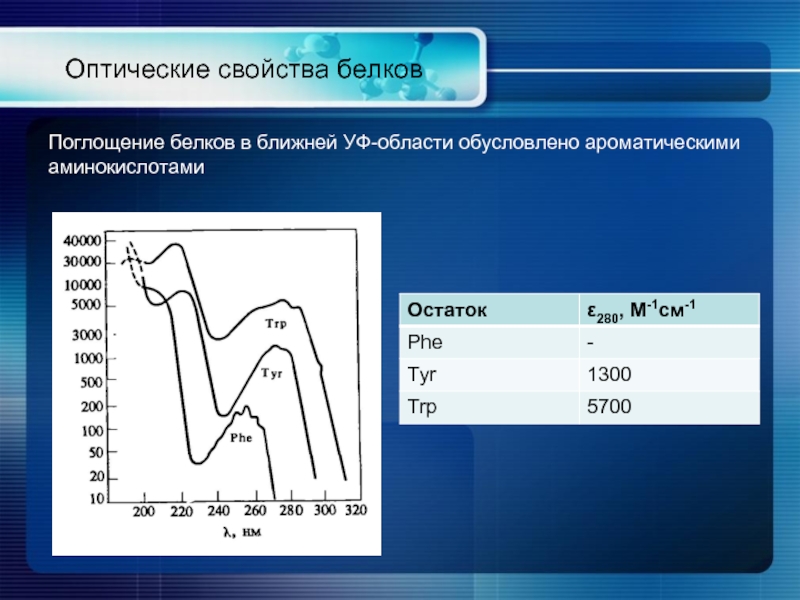
Слайд 17Оптические свойства белков
Поглощение белков в ближней УФ-области обусловлено ароматическими аминокислотами
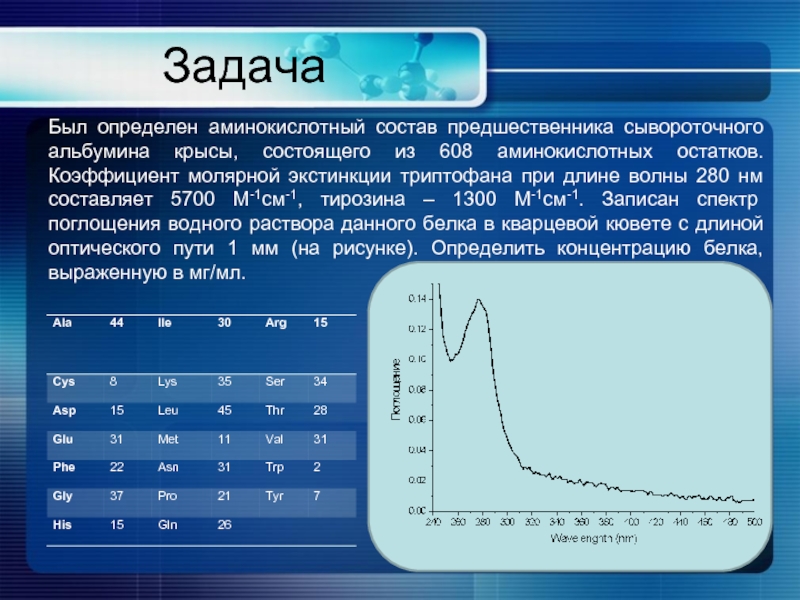
Слайд 20Задача
Был определен аминокислотный состав предшественника сывороточного альбумина крысы, состоящего из 608
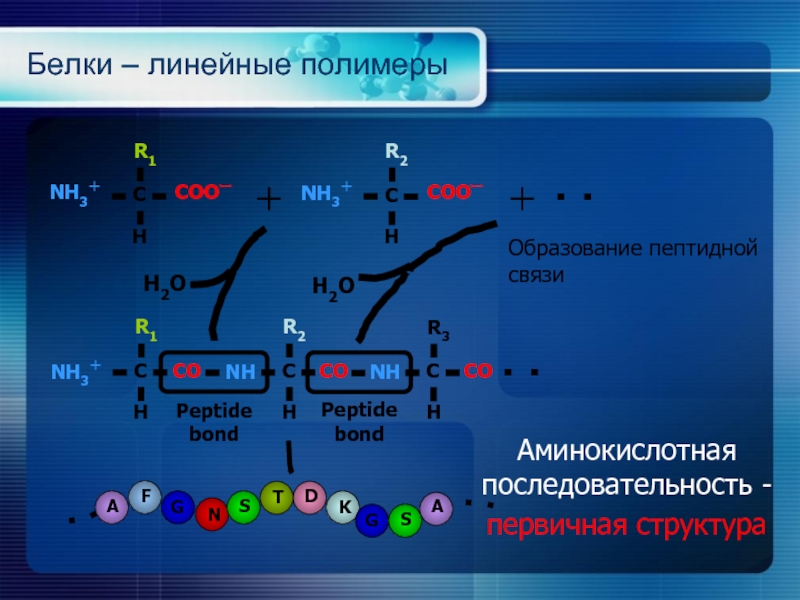
Слайд 22Белки – линейные полимеры
R1
NH3+
C
CO
H
R2
NH
C
CO
H
R3
NH
C
CO
H
R2
NH3+
C
COOー
H
+
R1
NH3+
C
COOー
H
+
H2O
H2O
Peptide bond
Peptide bond
Аминокислотная последовательность - первичная структура
A
A
F
N
G
G
S
T
S
D
K
Образование
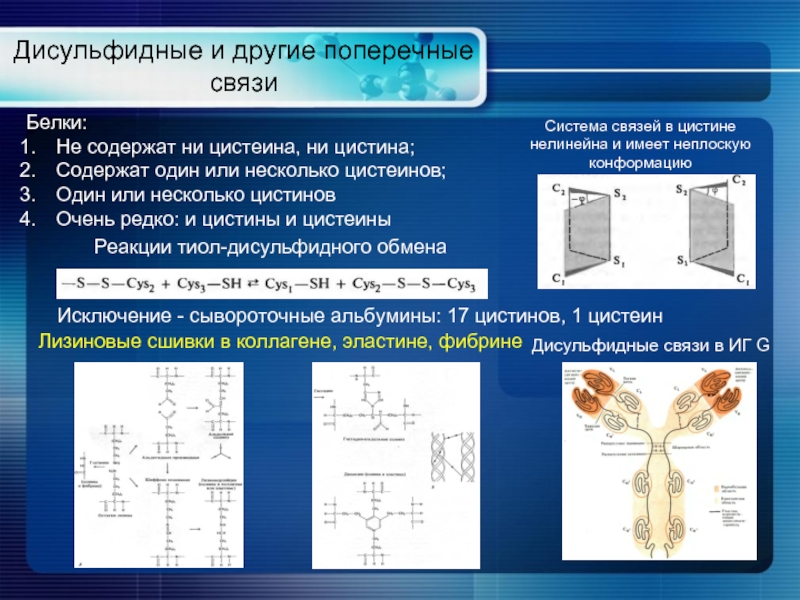
Слайд 23Дисульфидные и другие поперечные связи
Система связей в цистине нелинейна и имеет
Белки:
Не содержат ни цистеина, ни цистина;
Содержат один или несколько цистеинов;
Один или несколько цистинов
Очень редко: и цистины и цистеины
Реакции тиол-дисульфидного обмена
Исключение - сывороточные альбумины: 17 цистинов, 1 цистеин
Дисульфидные связи в ИГ G
Лизиновые сшивки в коллагене, эластине, фибрине
Слайд 24Задача
Молекулярная масса неизвестного белка, определенная с использованием метода масс-спектрометрии, составила 56
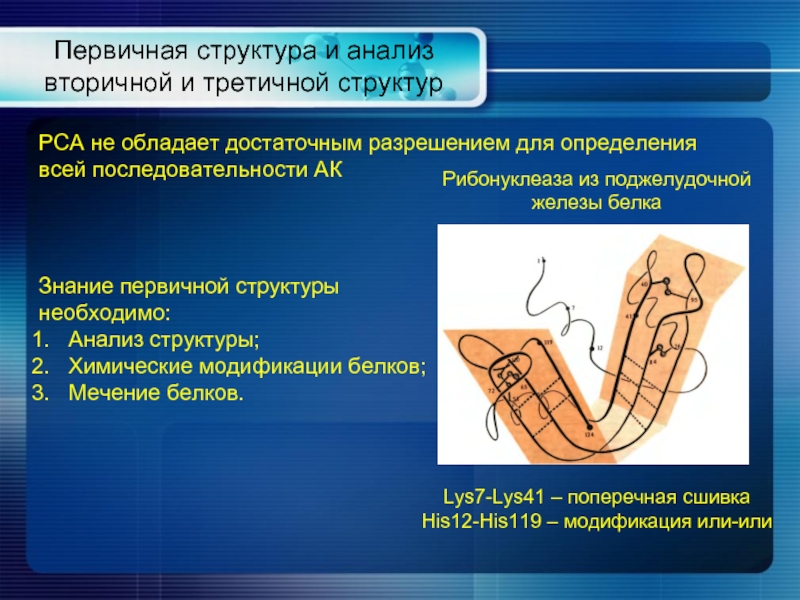
Слайд 25Первичная структура и анализ вторичной и третичной структур
РСА не обладает достаточным
Знание первичной структуры необходимо:
Анализ структуры;
Химические модификации белков;
Мечение белков.
Рибонуклеаза из поджелудочной железы белка
Lys7-Lys41 – поперечная сшивка
His12-His119 – модификация или-или
Слайд 26Первичная структура и предсказание вторичной и третичной структур
Распределение различных типов вторичной
Слайд 27АК последовательность белка и анализ его функций
Гликофорин эритроцитов человека
Гистон 2а теленка
Гликофорин
Трансмембранный
Сахара располагаются с внешней стороны клетки (О, N гликозидная связь)
Ile73-Ile95 – трансмембранная последовательность
Гистон
Первые 36 АК остатков содержат 12 положительных зарядов и ни одного отрицательного – участок важен для связывания ДНК
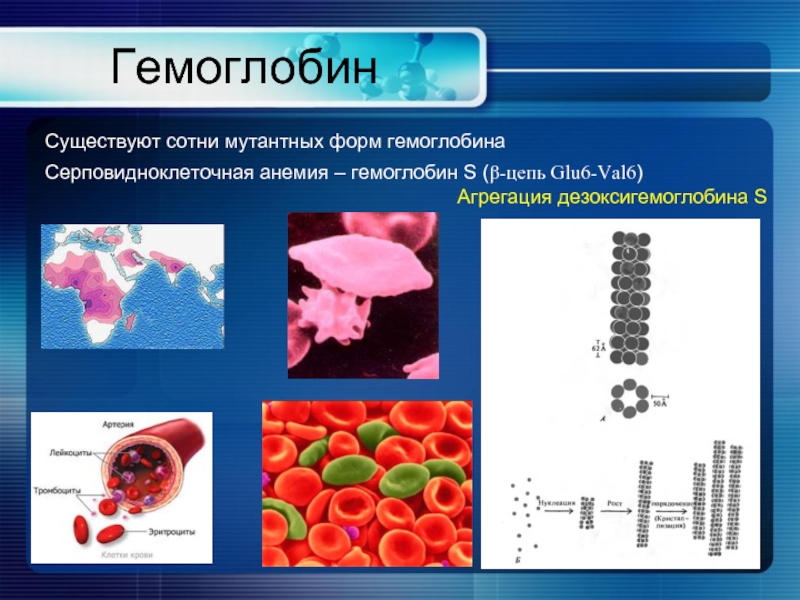
Слайд 29Гемоглобин
Существуют сотни мутантных форм гемоглобина
Серповидноклеточная анемия – гемоглобин S (β-цепь Glu6-Val6)
Агрегация
Слайд 30Заключение
Белки – АК, металлы, простетические группы, сахара.
Существует корреляция между составом, структурой
В белках с большим содержанием пролина формируются спирали полипролинового типа.
Третичные структуры организованы в плотно упакованные глобулы или несколько плотноупакованных доменов.
Четвертичные структуры делят на 2 типа – с глобулярныи и спиральным расположением субъединиц.