- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Хлор презентация
Содержание
- 1. Хлор
- 2. Саяхат жоспары: “Эксперименттік есеп” аймағы “Ақпарат” аймағы
- 3. 1. Хлордың
- 4. 7. Хлордың маңызды қосылысын ата? Ол
- 5. “Эксперимент” аймағы Cu0 + Cl20 →
- 6. Br
- 7. Хлор полимерлер алу үшін қолданылады.
- 8. Хлордың ағартқыш қасиеті бар екені 1795
- 9. Бөлмелерді дезин- фекциялау. Ауыз суды
- 10. Химия өндірісінде тұз қышқылын,
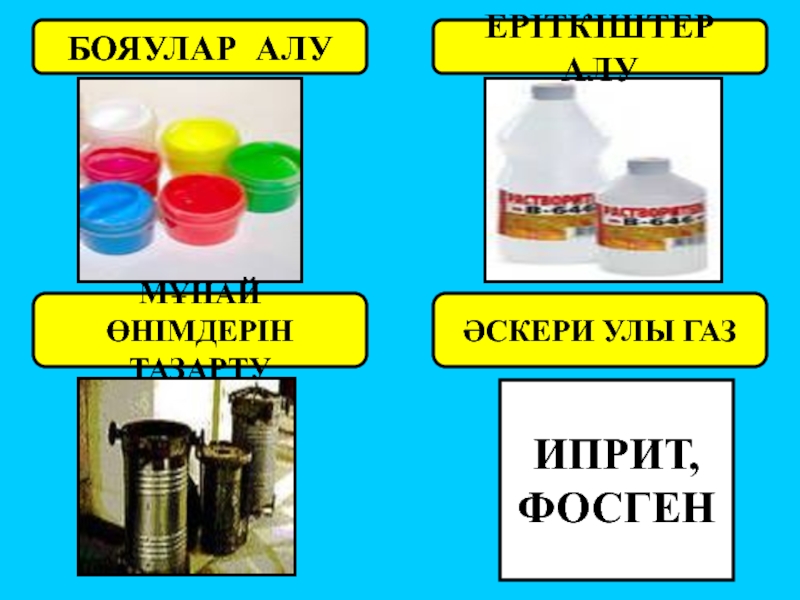
- 11. БОЯУЛАР АЛУ ЕРІТКІШТЕР АЛУ МҰНАЙ ӨНІМДЕРІН ТАЗАРТУ ӘСКЕРИ УЛЫ ГАЗ ИПРИТ, ФОСГЕН
- 12. Мыңдаған адамдардың өмірін сақтап қалған құрал
- 13. ХЛОРДЫ АЛУ 1774 ж. Швед химигі
- 14. ХЛОРДЫ АЛУ KCl+5O3+6HCl-1→KCl-1 +3Cl02↑+3H2O Cl+5 +
- 15. ХЛОРДЫ АЛУ 2KMn+7O4+16HCl-1→5Cl02↑+2Mn+5Cl 2 +2KCl-1+8H2O Mn
- 16. ХЛОРДЫ АЛУ Өнеркәсіпте хлорды концентрлі ас тұзының судағы ерітіндісін электролиздеу арқылы өндіреді.
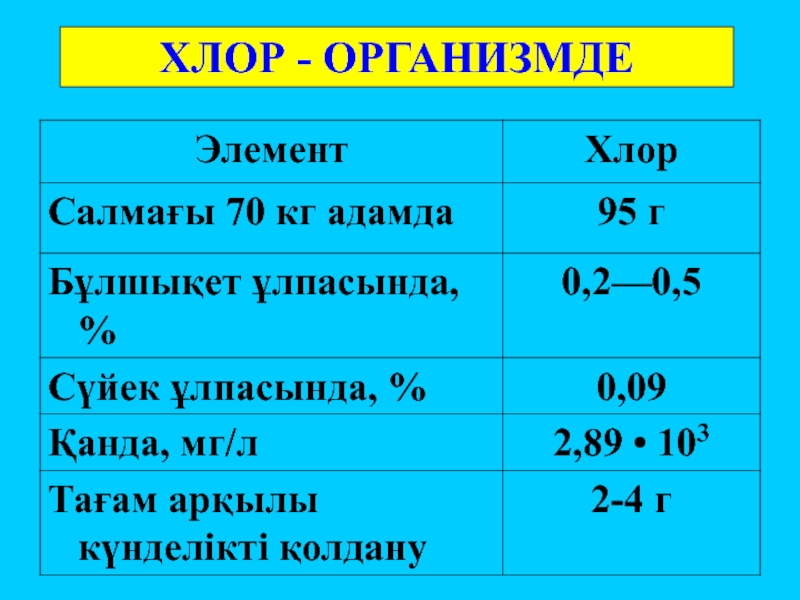
- 17. ХЛОР - ОРГАНИЗМДЕ
- 18. Хлордың организмдегі ролі: Асқазанда тұз қышқылын
- 19. Хлор ас тұзында, нанда, етте, теңіз өнімдерінде, жұмыртқада, сүтте болады.
- 20. Организмге хлор жетіспегенде пайда болады: Әлсіздік, Тәбеттің
- 21. Хлор ионы өсімдік үшін өте маңызды. Хлор
- 22. “Біліміңді тексер” аймағы Хлорды алған ғалым? Хлор
- 23. Ж.д. 4-есеп: Электрондық баланс әдісімен тапсырманы
- 24. Оқулық. 3-тапсырма. Массасы 43,5 г марганец
- 25. Хлорды өндірісте неден алады? а) тұз
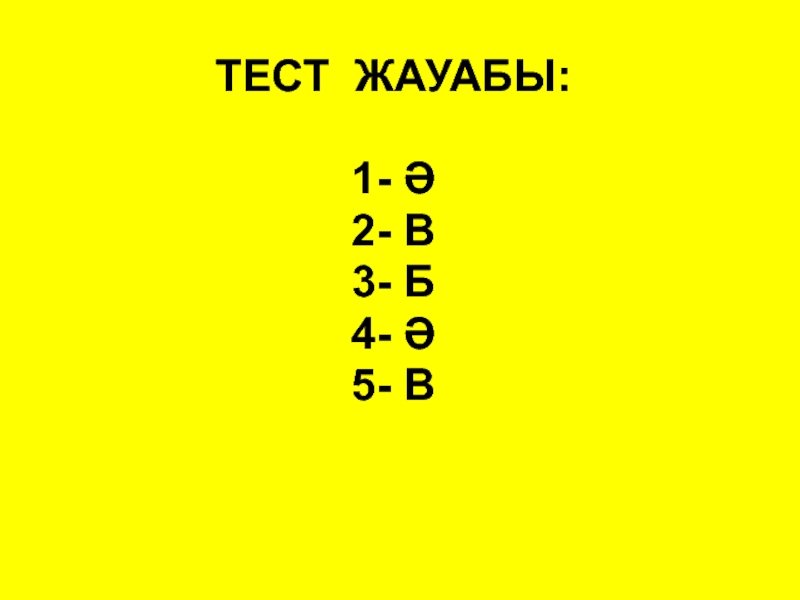
- 26. ТЕСТ ЖАУАБЫ: 1- Ә 2- В 3- Б 4- Ә 5- В
- 27. ҮЙГЕ ТАПСЫРМА: Хлордың алынуы және оның қолданылуы.
Слайд 2Саяхат жоспары:
“Эксперименттік есеп” аймағы
“Ақпарат” аймағы
“Лабораториялық тәжірибе” аймағы
“Қолданыстағы хлор” аймағы
“Биология” аймағы
“Біліміңді тексер”
Слайд 3
1. Хлордың латынша атауы қандай?
2. Хлорды периодтық жүйедегі орны бойынша сипатта.
3.
4. Хлор қандай қосылыстар түрінде кездеседі?
5. “Тас тұз” деген не?
6. Хлордың физикалық қасиеті қандай?
“Ақпарат” аймағы
Слайд 47. Хлордың маңызды қосылысын ата? Ол не үшін қолданылады?
8.
9. Хлор қандай заттармен әрекеттеседі?
10. Хлорды қайда сақтайды?
11. Хлормен жұмыс жасауда қандай қауіпсіздік ережесін сақтау керек?
12. Хлор сумен әрекеттескенде қандай заттар түзіледі?
“Ақпарат” аймағы
Слайд 5“Эксперимент” аймағы
Cu0 + Cl20 → Cu +2Cl2-1
Cu0 – 2e = Cu2+
Cl2 + 2e = 2Cl-1 2 т-ш
Cu + Cl2 =CuCl2
Fe0 + Cl20 → Fe +3Cl3-1
Fe0 –3e = Fe3+ 2 т-з-ш
Cl2 + 2e = 2Cl-1 3 т-ш
2Fe + 3Cl2 =2FeCl3
P0 + Cl20 → P+3Cl3-1
P0 –3e = P3+ 2 т-з-ш
Cl2 + 2e = 2Cl-1 3 т-ш
2P + 3Cl2 =2PCl3
H20 + Cl20 → H+Cl -
H20 –2e = 2H+ 2 т-з-ш
Cl2 + 2e = 2Cl-1 2 т-ш
H2+ Cl2 = 2HCl
Слайд 7Хлор полимерлер алу
үшін қолданылады.
Поливинилхлорид
деп аталатын полимерден
пластикалы терезе
жақтаулары,
пластмасса бұйымдары,
пенопластар, ойыншықтар,
құрылыс материалдары,
жасанды тері,
су өткізбейтін плащтар мен
аяқ киімдер,
кабель сымдарын
оқшаулағыштар жасайды.
ПОЛИМЕР АЛУ
Слайд 8Хлордың ағартқыш қасиеті
бар екені 1795 жылы-ақ
белгілі болған. Бірақ затты
ағартатын хлор емес,
реакция кезінде түзілетін
хлорлылау
қышқылы ыдырағанда бөлінетін
оттек атомы ағартады.
Cl2 + H2O → HCl + HClO → 2HCl + O
Мата, қағаз, картондарды ағартудың
бұл тәсілі бірнеше ғасырдан
бері қолданып келеді.
МАТА МЕН
ҚАҒАЗДЫ АҒАРТУ
Слайд 9Бөлмелерді
дезин-
фекциялау.
Ауыз суды
залалсыздандыру.
Сұйық хлорды ең алғаш
Нью-Йорк қаласының
жүйесін тазалау үшін
1895 жылы қолданған.
100 л суға 200 мг хлор қажет.
Слайд 10
Химия өндірісінде тұз
қышқылын, хлор әгін,
бертолле тұзын, йод, бром,
дәрі-дәрмектер алуда;
Металлургияда металл бетін
оксидтерден тазартуда;
Хлордың фреон деп
аталатын қосылысы
тоңазытқышта
салқындатқыш зат ретінде;
Тағам өндірісінде Е925 тағамдық
қоспасы пайдаланылады.
Br 35
79,904
Бром
I 53
126,904
Йод
Слайд 12Мыңдаған адамдардың өмірін сақтап
қалған құрал
Бірінші дүниежүзілік соғыста 1915 жылы Германия
1915 жылдың көктемінде Белгияның Ипр қаласы маңында ағылшындар мен неміс әскері қарама-қарсы келді. 22 сәуір күні таң ертеңгісін ағылшын әскері неміс окоптары жағынан сарғыш-жасыл түсті бұлт келе жатқанын байқайды. Бұл хлор газы болатын. Хлор газынан 15000 жауынгер уланып, оның 5000-ы қайтыс болады. Ағылшындар мұндай соғысқа мүлде дайын емес еді. Себебі, олар соғыс ережесі бойынша улы заттарды қолдануға болмайтын ережені екі жақ та сақтайды деген сенімде болған еді.
Бірақ, неміс штабы бұл ережеге бағынған жоқ. Бір айдан соң немістер орыс әскеріне қарсы газды шабуыл жасады. Түнде шығарылған 150 т улы хлордан 9000 адам қайтыс болды.
Газды шабуылдан қорғану үшін тез арада қорғаныс құралын табу қажет болды. 1915 жылы орыс ғалымы Н.Д.Зелинский газтұтқыш
ойлап тапты. Бұл аппаратта улағыш газды сорып алатын белсенді көміртегі салынған.
Слайд 13ХЛОРДЫ АЛУ
1774 ж. Швед химигі Карл Шееле.
MnO2 +4HCl →MnCl2 +Cl2↑
Mn +4 + 2 e Mn +2 1(тотықсыздану)(т-ш)
2Cl – 2e Cl 02 1 (тотығу) (т-з-ш)
Слайд 16ХЛОРДЫ АЛУ
Өнеркәсіпте хлорды
концентрлі ас тұзының
судағы ерітіндісін
электролиздеу арқылы өндіреді.
Слайд 18Хлордың организмдегі ролі:
Асқазанда тұз қышқылын өндіреді.
Қан, лимфа, ұлпалардың жұмысын реттеуге қатысады.
Зат
Дененің иілгіштігін;;
Тәбеттің болуы;
Бауыр жұмысын жақсартады;
Организмнен көмірқышқыл газын шығаруға септігін тигізеді;
Эритроциттердің құрамын қалыптастырады;
Организмнен шлак пен токсиндерді шығарады.
Слайд 20Организмге хлор жетіспегенде пайда болады:
Әлсіздік,
Тәбеттің жоқтығы;
Ұйқышылдық;
Ұмытшақтық,
Бұлшықеттің әлсіздігі,
Ауыздың құрғауы,
Дәм сезбеу.
Ауыр жағдайда шаш
Егер организмде хлор артып кетсе:
Көз жасаурайды,
Құрғақ жөтел,
Кеуденің ауыруы,
Бас ауруы,
Температураның көтерілуі,
Өкпенің ісуі..
Слайд 21 Хлор ионы өсімдік үшін өте маңызды. Хлор өсімдіктің энергия алмасуында маңызды
Слайд 22“Біліміңді тексер” аймағы
Хлорды алған ғалым?
Хлор қандай заттардан алынады?
Хлорды қайда қолданады?
Организдегі ролі
Хлор қандай тағамда кездеседі?
Хлордың қандай зияны бар?
Слайд 24Оқулық. 3-тапсырма.
Массасы 43,5 г марганец (ІY) оксидін концентрлі тұз қышқылымен
Слайд 25Хлорды өндірісте неден алады?
а) тұз қышқылы
б) ас содасы в) калий
2. Хлор атомының Cl2O7
қосылысындағы тотығу дәрежесі
А) +1 ә) + 3 б) +5 в) +7
3. Ересек адам денесіндегі хлор мөлшері?
А) 4-6 г ә) 40г б) 95 г в) 150 г
4. Хлордың неше энергетикалық деңгейі бар?
А) 2 ә) 3 б) 4 в) 5
5. Ең белсенді тотықтырғыш?
А) F ә) Br б) I в) Cl