акцептори і переносники електронів
3. Мультиферментні комплекси дихального ланцюга
4. Запасання енергії у протонному градієнті
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Дихальний ланцюг мітохондрій презентация
Содержание
- 1. Дихальний ланцюг мітохондрій
- 2. Стадія 1: окислення жирних кислот, глюкози
- 3. Біохімічна анатомія мітохондрії Кристи збільшують площу
- 4. Загальна схема потоку електронів і протонів через
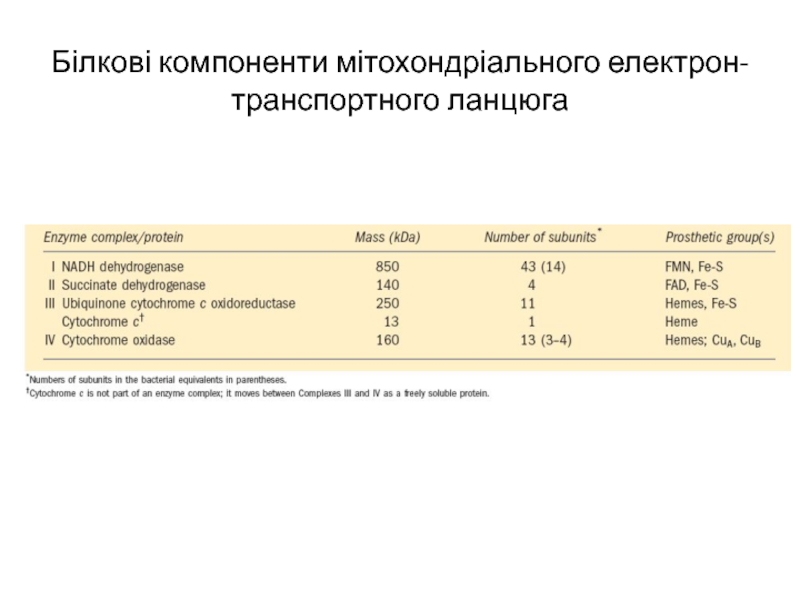
- 5. Білкові компоненти мітохондріального електрон-транспортного ланцюга
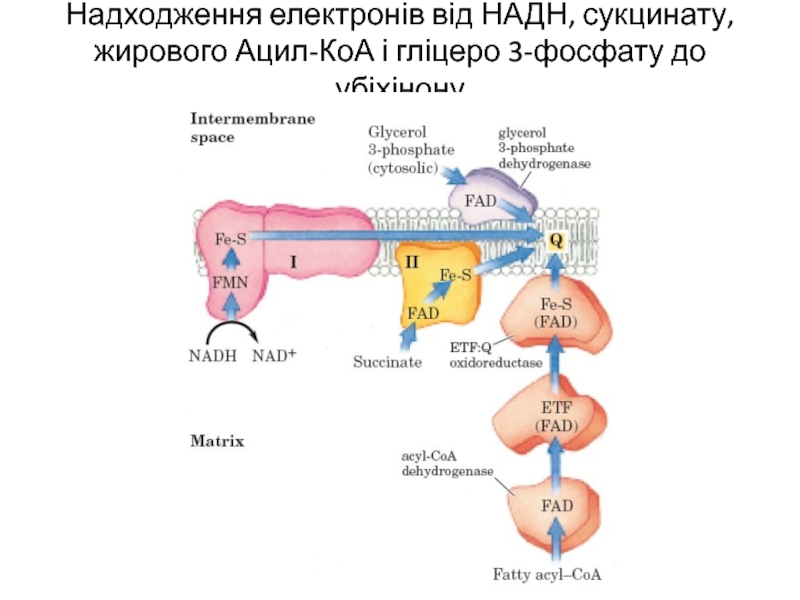
- 6. Надходження електронів від НАДН, сукцинату, жирового Ацил-КоА і гліцеро 3-фосфату до убіхінону
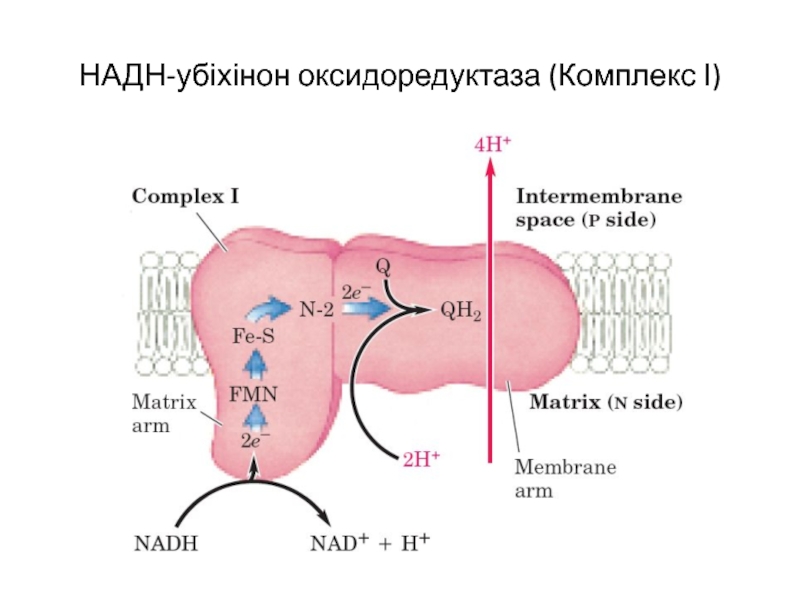
- 7. НАДН-убіхінон оксидоредуктаза (Комплекс І)
- 8. Деякі важливі реакції, що каталізуються НАД(Ф)Н-дегідрогеназами
- 9. Надходження електронів від НАДН, сукцинату, жирового Ацил-КоА і гліцеро 3-фосфату до убіхінону
- 10. Структура комплексу II (сукцинатдегідрогеназа) Дві трансмембранні C
- 11. Надходження електронів від НАДН, сукцинату, жирового Ацил-КоА і гліцеро 3-фосфату до убіхінону
- 12. Убіхінон (Q, чи коензим Q) Повне відновлення
- 13. Комплекс цитохром bc1 (комплекс ІІІ) (а) Структура
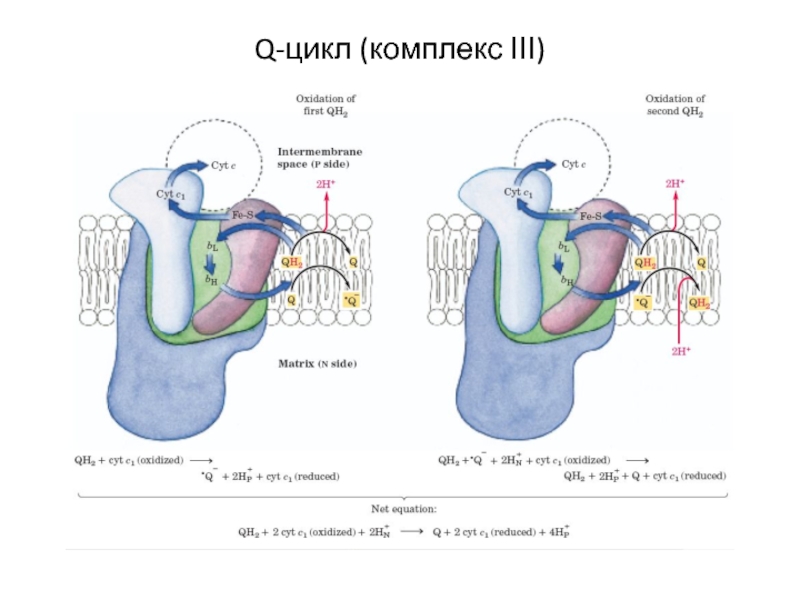
- 14. Q-цикл (комплекс ІІІ)
- 15. Простетичні групи цитохромів Кожна група містить
- 16. Субодиниці цитохромоксидази (комплекс IV) (а) Осердя комплексу:
- 17. Шлях електронів через комплекс IV Цитохром
- 18. Окисно-відновний потенціал (В) компонентів дихального ланцюга у
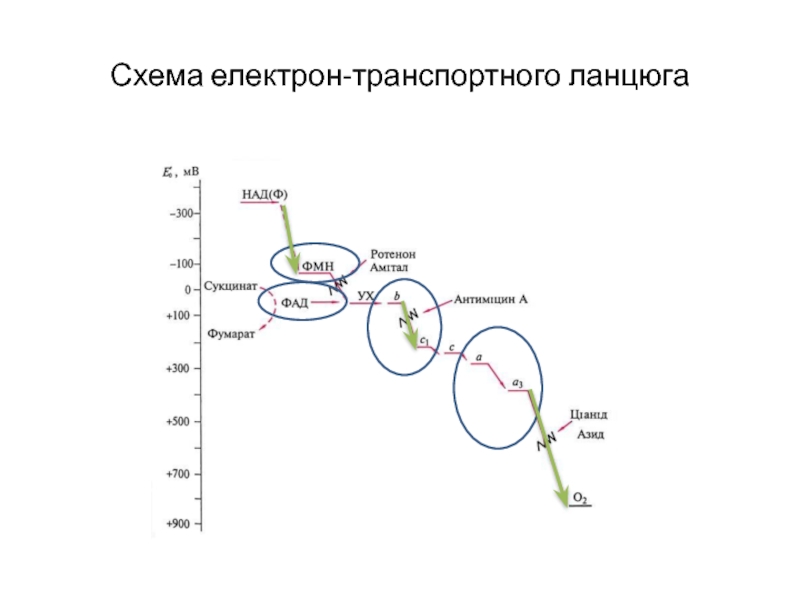
- 19. Схема електрон-транспортного ланцюга
- 20. Дихальний ланцюг ФП1 – флавопротеїд, Q –
- 21. Протонорушійна сила Внутрішня мітохондріальна мембрана розділяє
- 22. Sir Peter D. Mitchell (1920 – 1992)
- 23. Додаткова література Ленинджер А. Биохимия. Москва:
Слайд 1
Тема: Дихальний ланцюг мітохондрій
План
1. Реакції перенесення електронів у мітохондріях
2. Універсальні
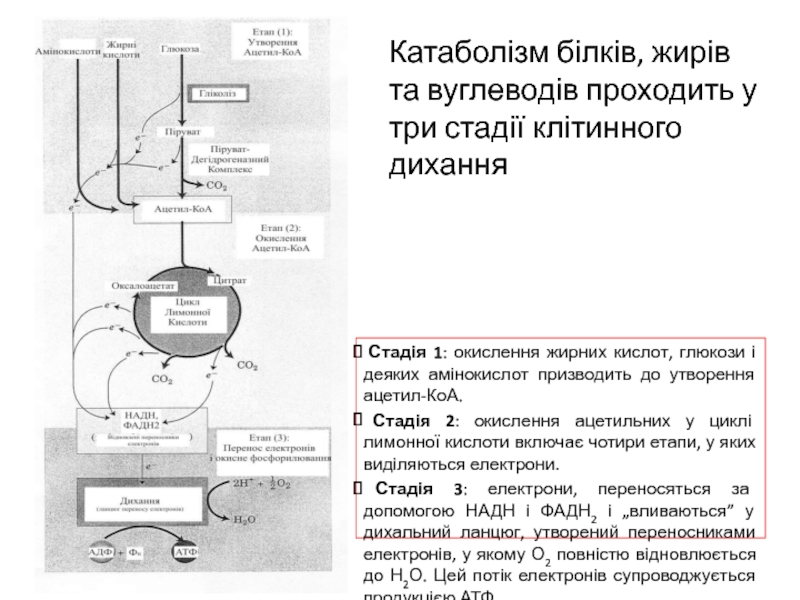
Слайд 2 Стадія 1: окислення жирних кислот, глюкози і деяких амінокислот призводить
до утворення ацетил-КоА.
Стадія 2: окислення ацетильних у циклі лимонної кислоти включає чотири етапи, у яких виділяються електрони.
Стадія 3: електрони, переносяться за допомогою НАДН і ФАДН2 і „вливаються” у дихальний ланцюг, утворений переносниками електронів, у якому О2 повністю відновлюється до Н2О. Цей потік електронів супроводжується продукцією АТФ.
Стадія 2: окислення ацетильних у циклі лимонної кислоти включає чотири етапи, у яких виділяються електрони.
Стадія 3: електрони, переносяться за допомогою НАДН і ФАДН2 і „вливаються” у дихальний ланцюг, утворений переносниками електронів, у якому О2 повністю відновлюється до Н2О. Цей потік електронів супроводжується продукцією АТФ.
Катаболізм білків, жирів та вуглеводів проходить у три стадії клітинного дихання
Слайд 3Біохімічна анатомія мітохондрії
Кристи збільшують площу поверхні внутрішньої мембрани, яка містить
у печінці понад 10000 (печінка) чи 30000 (серце) дихальних ланцюгів і молекул ATP-синтази.
Мітохондріальний запас коензимів та проміжних продуктів функціонально відокремлений від відповідного цитозольного пулу.
Мітохондрії безхребетних, рослин і мікробних еукаріотів за своєю будовою подібні до наведеної на рисунку, проте варіюють за розмірами, формою та ступенем складчастості внутрішньої мембрани.
Мітохондріальний запас коензимів та проміжних продуктів функціонально відокремлений від відповідного цитозольного пулу.
Мітохондрії безхребетних, рослин і мікробних еукаріотів за своєю будовою подібні до наведеної на рисунку, проте варіюють за розмірами, формою та ступенем складчастості внутрішньої мембрани.
Слайд 4Загальна схема потоку електронів і протонів через чотири комплекси дихального ланцюга
Електрони
переносяться на Q через комплекси І і ІІ. QH2 - мобільний переносник е- та Н+. Він доставляє електрони до комплексу ІІІ, який передає їх на цитохром с. Комплекс IV переносить е- від відновленого цитохрому с на О2. Електронний потік через комплекси І, ІІІ і IV супроводжується потоком протонів з матриксу у міжмембранний простір.
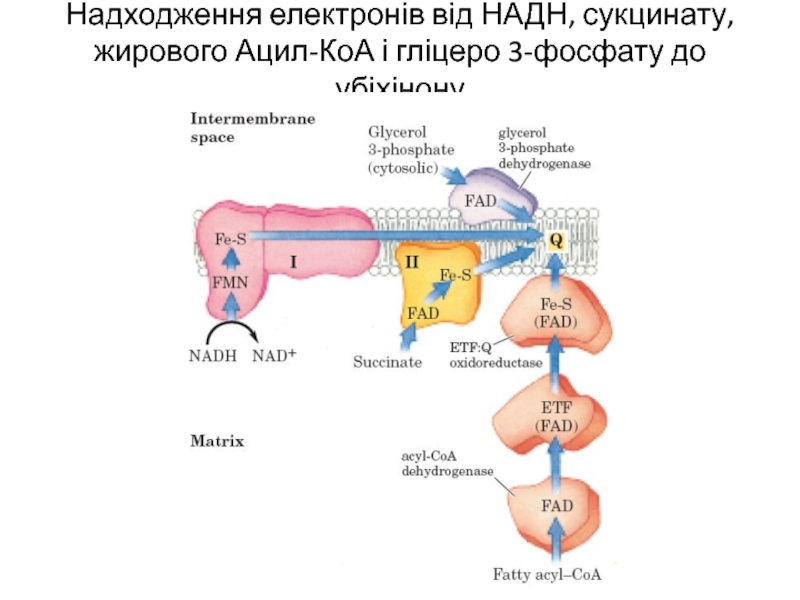
Слайд 6Надходження електронів від НАДН, сукцинату, жирового Ацил-КоА і гліцеро 3-фосфату до
убіхінону
Слайд 9Надходження електронів від НАДН, сукцинату, жирового Ацил-КоА і гліцеро 3-фосфату до
убіхінону
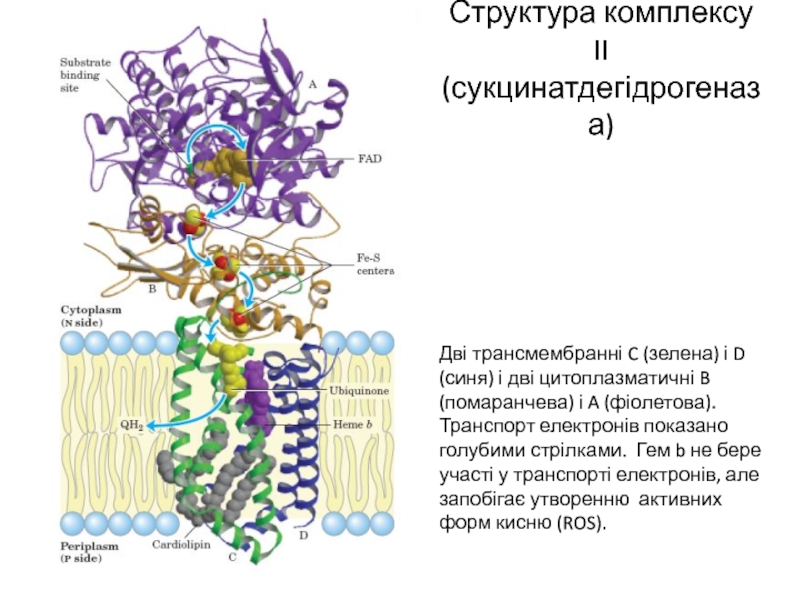
Слайд 10Структура комплексу II (сукцинатдегідрогеназа)
Дві трансмембранні C (зелена) і D (синя) і
дві цитоплазматичні B (помаранчева) і A (фіолетова). Транспорт електронів показано голубими стрілками. Гем b не бере участі у транспорті електронів, але запобігає утворенню активних форм кисню (ROS).
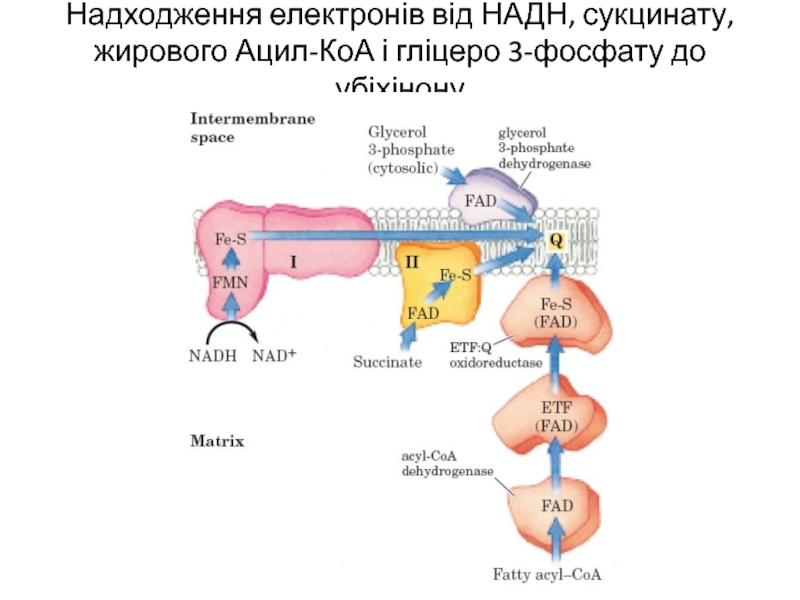
Слайд 11Надходження електронів від НАДН, сукцинату, жирового Ацил-КоА і гліцеро 3-фосфату до
убіхінону
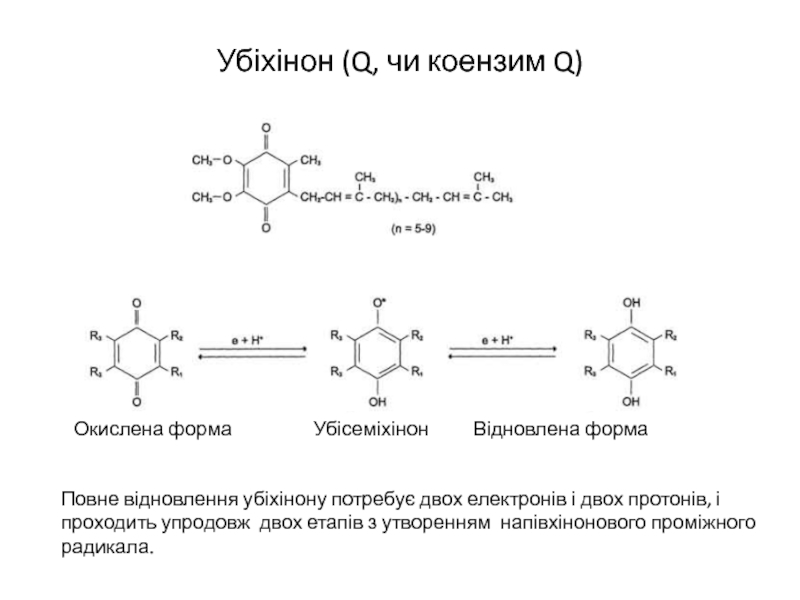
Слайд 12Убіхінон (Q, чи коензим Q)
Повне відновлення убіхінону потребує двох електронів і
двох протонів, і проходить упродовж двох етапів з утворенням напівхінонового проміжного радикала.
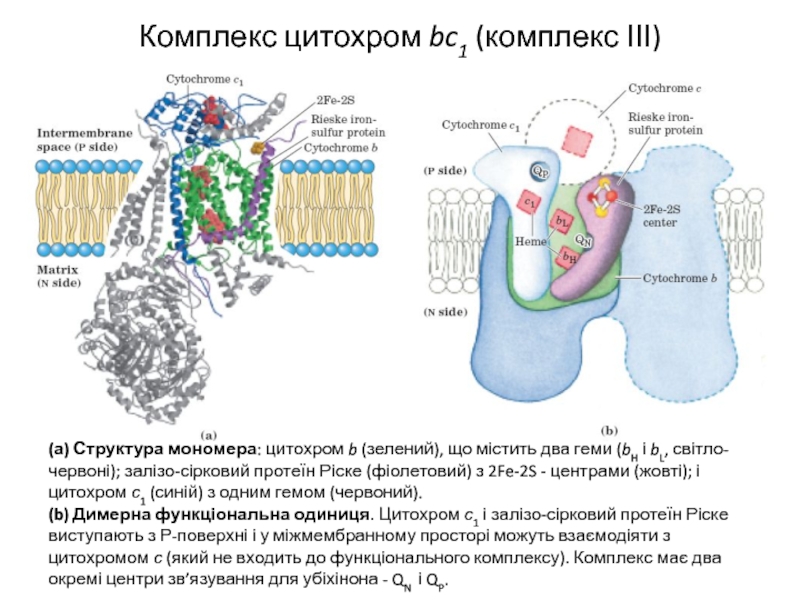
Слайд 13Комплекс цитохром bc1 (комплекс ІІІ)
(а) Структура мономера: цитохром b (зелений), що
містить два геми (bH і bL, світло-червоні); залізо-сірковий протеїн Ріске (фіолетовий) з 2Fe-2S - центрами (жовті); і цитохром с1 (синій) з одним гемом (червоний).
(b) Димерна функціональна одиниця. Цитохром с1 і залізо-сірковий протеїн Ріске виступають з Р-поверхні і у міжмембранному просторі можуть взаємодіяти з цитохромом с (який не входить до функціонального комплексу). Комплекс має два окремі центри зв’язування для убіхінона - QN і QP.
(b) Димерна функціональна одиниця. Цитохром с1 і залізо-сірковий протеїн Ріске виступають з Р-поверхні і у міжмембранному просторі можуть взаємодіяти з цитохромом с (який не входить до функціонального комплексу). Комплекс має два окремі центри зв’язування для убіхінона - QN і QP.
Слайд 15Простетичні групи цитохромів
Кожна група містить азотовмісний порфірин.
Чотири атоми
азоту зв’язані координаційними зв’язками з центральним атомом заліза – Fe2+ чи Fe3+.
Гем с ковалентно зв’язаний з протеїном цитохрому с через тіоефірні зв’язки двох залишків Cys.
Гем с ковалентно зв’язаний з протеїном цитохрому с через тіоефірні зв’язки двох залишків Cys.
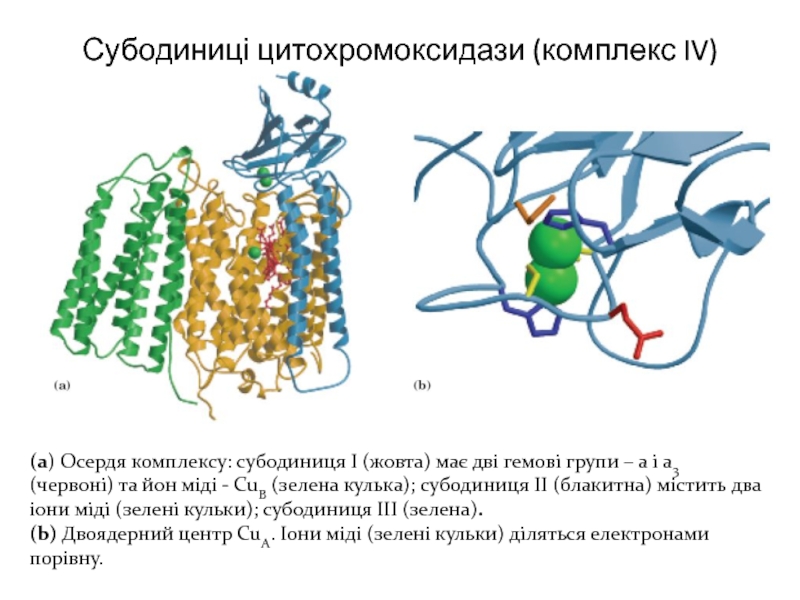
Слайд 16Субодиниці цитохромоксидази (комплекс IV)
(а) Осердя комплексу: субодиниця І (жовта) має дві
гемові групи – а і а3 (червоні) та йон міді - CuB (зелена кулька); субодиниця ІІ (блакитна) містить два іони міді (зелені кульки); субодиниця ІІІ (зелена).
(b) Двоядерний центр CuА. Іони міді (зелені кульки) діляться електронами порівну.
(b) Двоядерний центр CuА. Іони міді (зелені кульки) діляться електронами порівну.
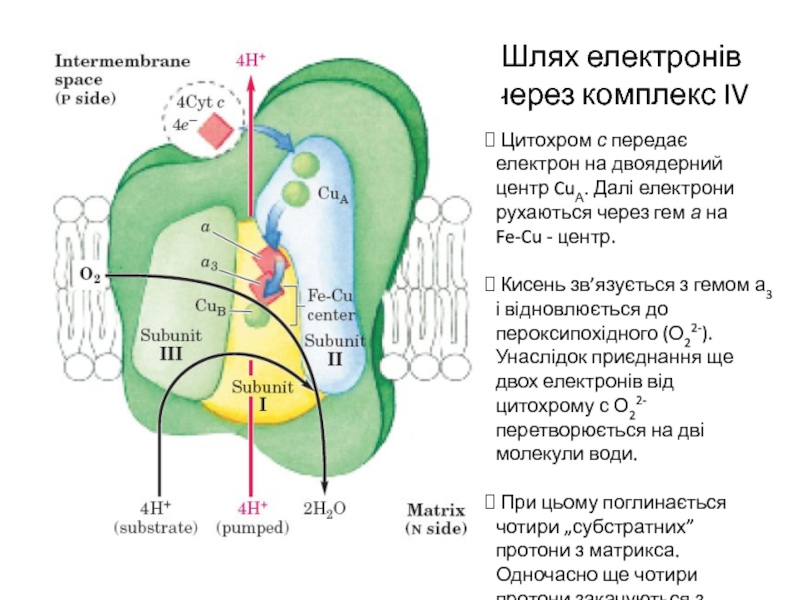
Слайд 17Шлях електронів через комплекс IV
Цитохром с передає електрон на двоядерний
центр CuА. Далі електрони рухаються через гем а на Fe-Cu - центр.
Кисень зв’язується з гемом а3 і відновлюється до пероксипохідного (О22-). Унаслідок приєднання ще двох електронів від цитохрому с О22- перетворюється на дві молекули води.
При цьому поглинається чотири „субстратних” протони з матрикса. Одночасно ще чотири протони закачуються з матрикса.
Кисень зв’язується з гемом а3 і відновлюється до пероксипохідного (О22-). Унаслідок приєднання ще двох електронів від цитохрому с О22- перетворюється на дві молекули води.
При цьому поглинається чотири „субстратних” протони з матрикса. Одночасно ще чотири протони закачуються з матрикса.
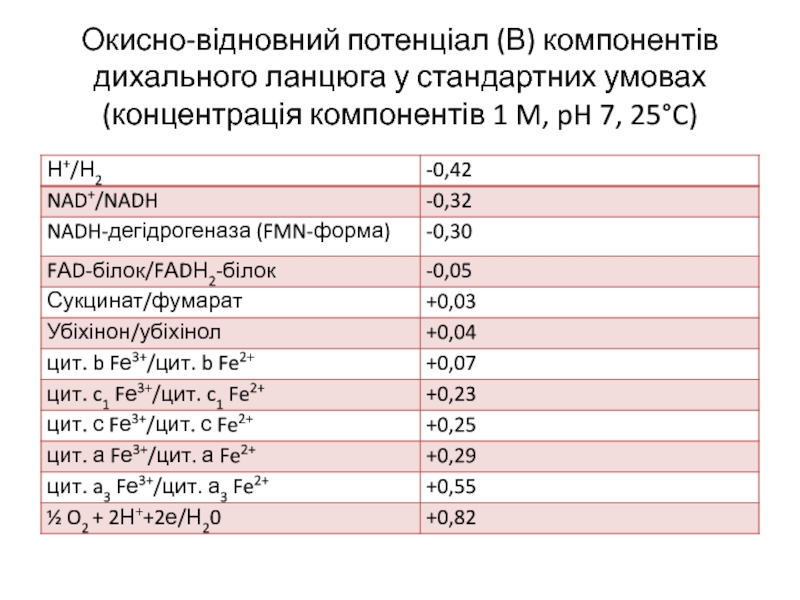
Слайд 18Окисно-відновний потенціал (В) компонентів дихального ланцюга у стандартних умовах (концентрація компонентів
1 M, pH 7, 25°C)
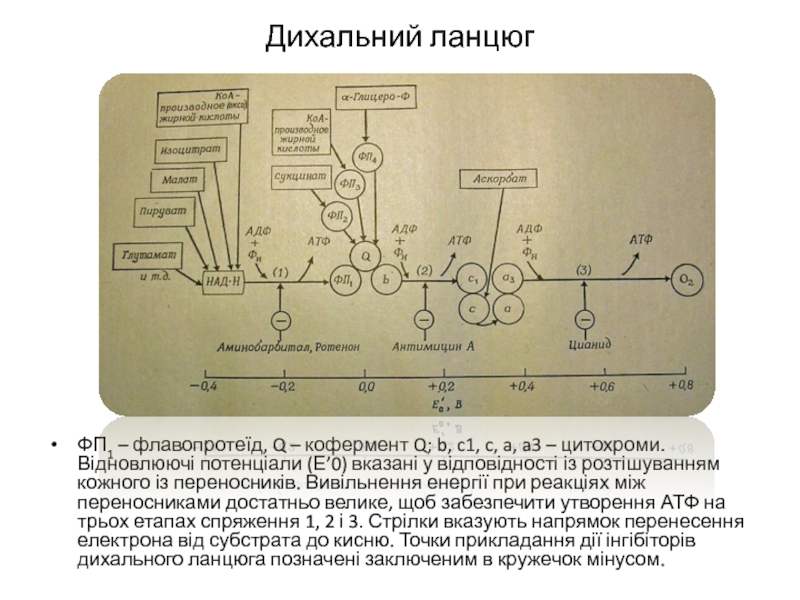
Слайд 20Дихальний ланцюг
ФП1 – флавопротеїд, Q – кофермент Q; b, c1, c,
a, a3 – цитохроми. Відновлюючі потенціали (Е’0) вказані у відповідності із розтішуванням кожного із переносників. Вивільнення енергії при реакціях між переносниками достатньо велике, щоб забезпечити утворення АТФ на трьох етапах спряження 1, 2 і 3. Стрілки вказують напрямок перенесення електрона від субстрата до кисню. Точки прикладання дії інгібіторів дихального ланцюга позначені заключеним в кружечок мінусом.
Слайд 21Протонорушійна сила
Внутрішня мітохондріальна мембрана розділяє два компартменти з різною [H+], наслідком
чого є різниці у хімічній концентрації (ΔрН) і розподілі зарядів (Δψ) по обидві сторони мембрани. У результаті виникає протонорушійна сила (ΔG), яку можна обчислити.
Слайд 22Sir Peter D. Mitchell (1920 – 1992)
Nobel prize in chemistry (1978)
"for his contribution to the understanding of biological energy transfer through the formulation of the chemiosmotic theory."
Слайд 23Додаткова література
Ленинджер А. Биохимия. Москва: Наука, 1985
Скулачев В.П. Биоэнергетика: Мембранные преобразователи
энергии. - М.: Высш. шк., 1989. – 271 с.
Рэкер Э. Биоэнергетические механизмы: Новые взгляды. - М.: Мир, 1979. – 216 с.
Mitchell, P. (1966). "Chemiosmotic Coupling in Oxidative and Photosynthetic Phosphorylation". Biological Reviews 41 (3): 445–502.
Рэкер Э. Биоэнергетические механизмы: Новые взгляды. - М.: Мир, 1979. – 216 с.
Mitchell, P. (1966). "Chemiosmotic Coupling in Oxidative and Photosynthetic Phosphorylation". Biological Reviews 41 (3): 445–502.





![Протонорушійна сила Внутрішня мітохондріальна мембрана розділяє два компартменти з різною [H+], наслідком чого є різниці](/img/tmb/5/413200/29b5520b960fb3f51276c3aa158b08ec-800x.jpg)







