- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Современный взгляд на механизмы канцерогенеза презентация
Содержание
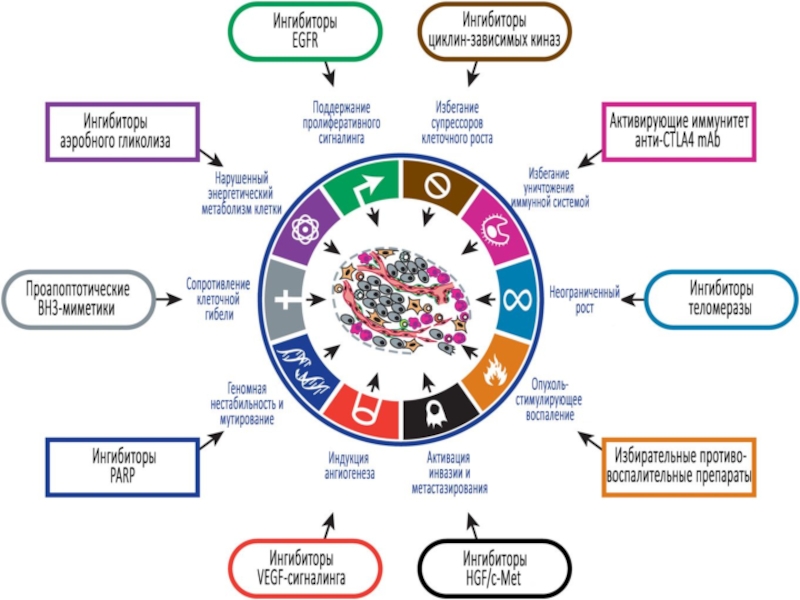
- 1. Современный взгляд на механизмы канцерогенеза
- 2. Поддержание пролиферативного сигнала Избегание супрессии клеточного роста
- 3. Геномная нестабильность В результате воздействия: Экзогенных факторов
- 6. Стимулирующее опухоль воспаление Хроническое воспаление (бактериальное, аутоиммунное,
- 8. Иммунное ускользание Большая часть микроскопических опухолей уничтожаются
- 9. Поддержание пролиферативного сигнала Фундаментальный признак опухолевого роста.
- 10. Механизмы поддержания пролиферативного сигнала Аутокринная стимуляция Паракринная
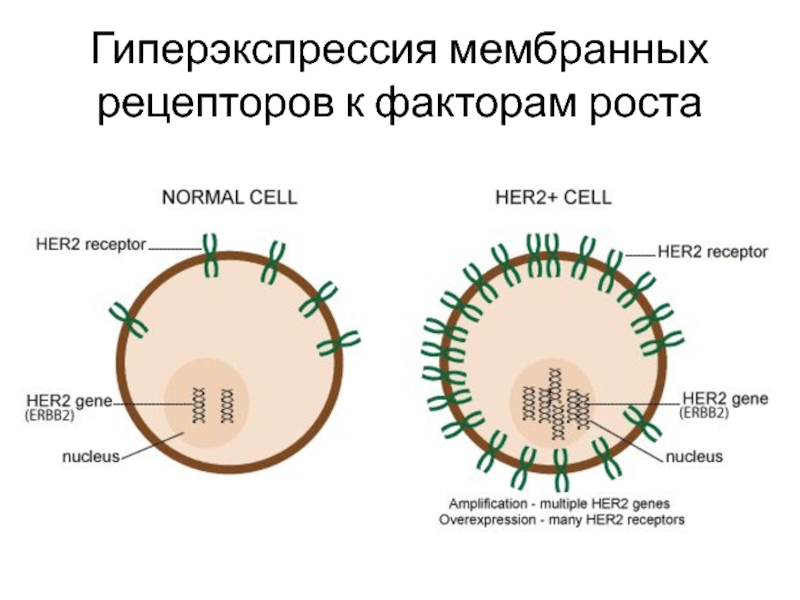
- 11. Гиперэкспрессия мембранных рецепторов к факторам роста
- 12. Механизмы поддержания пролиферативного сигнала Аутокринная стимуляция Паракринная
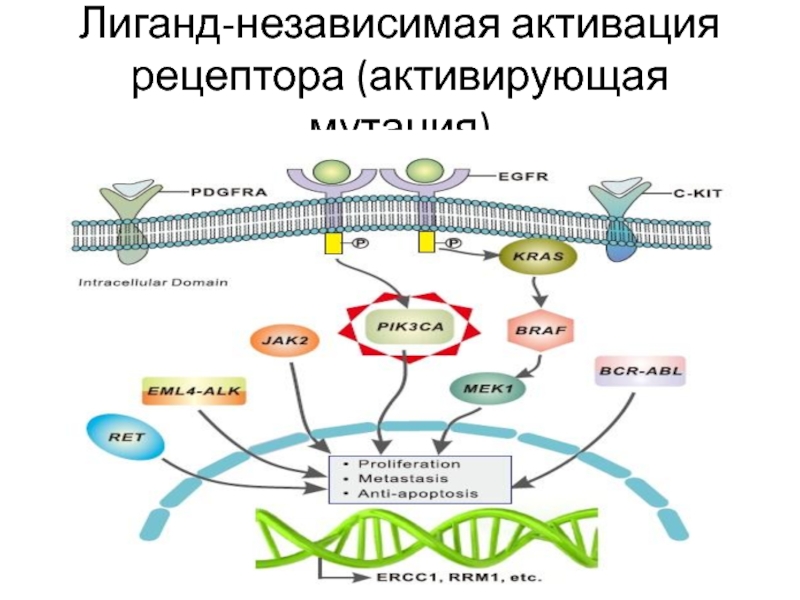
- 13. Лиганд-независимая активация рецептора (активирующая мутация)
- 14. Механизмы поддержания пролиферативного сигнала Аутокринная стимуляция Паракринная
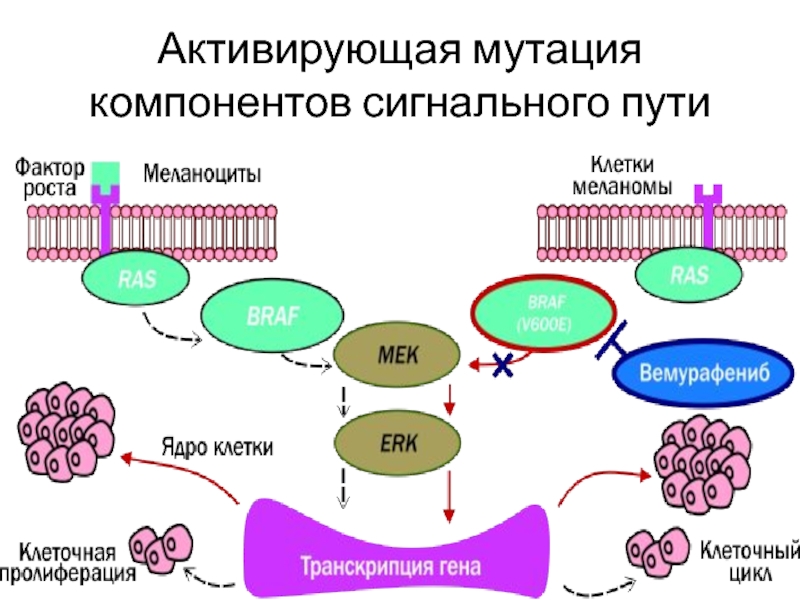
- 15. Активирующая мутация компонентов сигнального пути
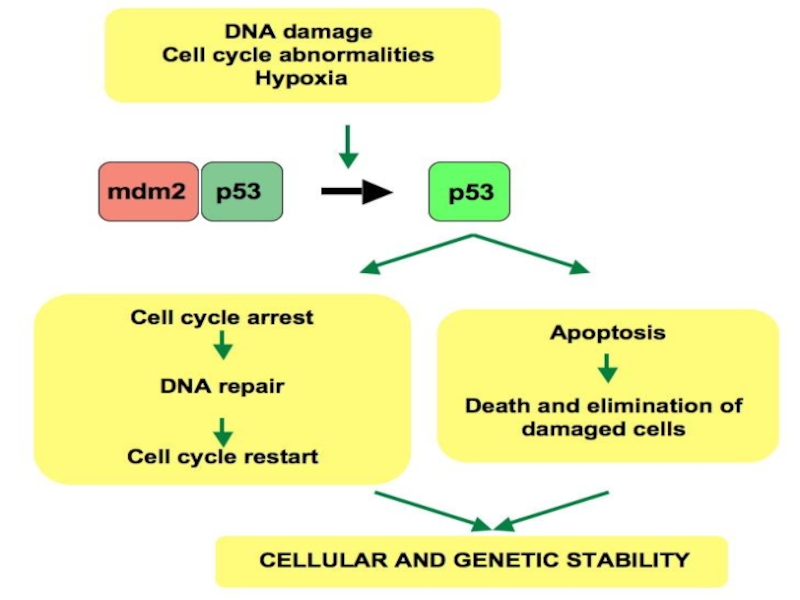
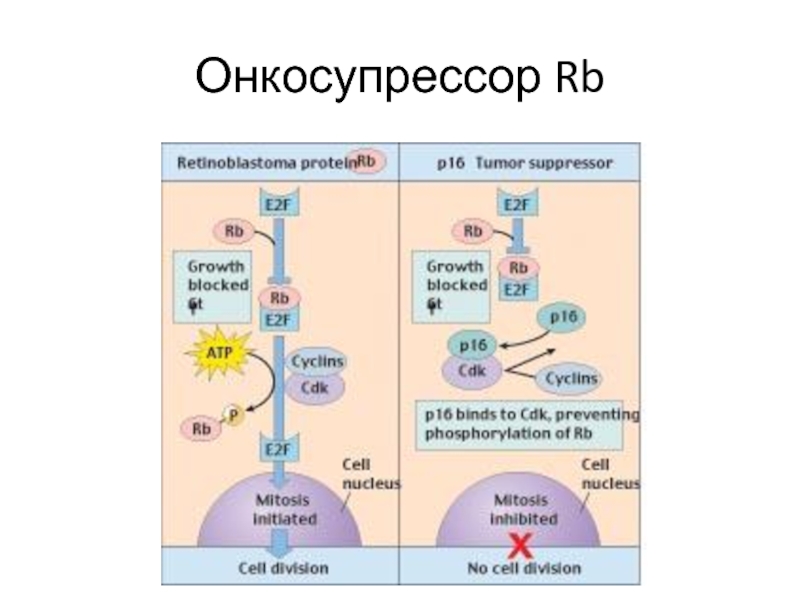
- 16. Избегание супрессоров клеточного роста Действие «каноничных» онкосупрессоров
- 18. Онкосупрессор Rb
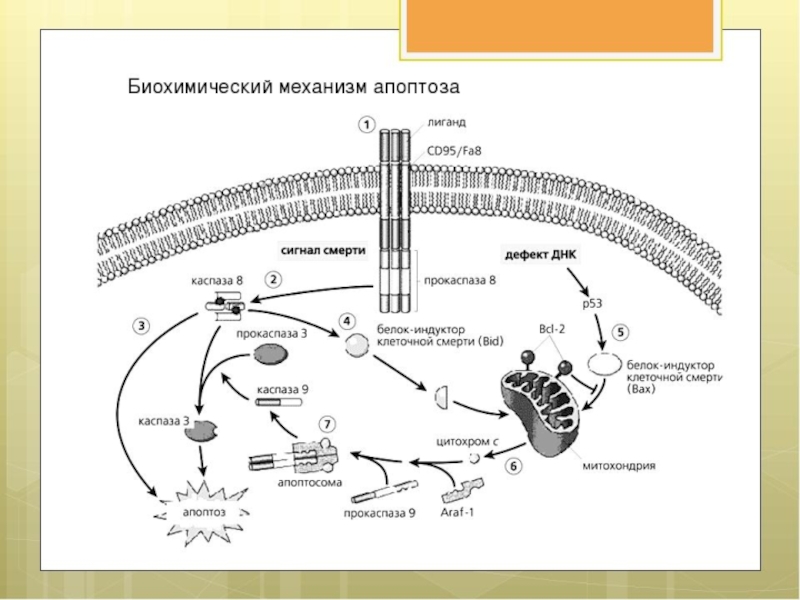
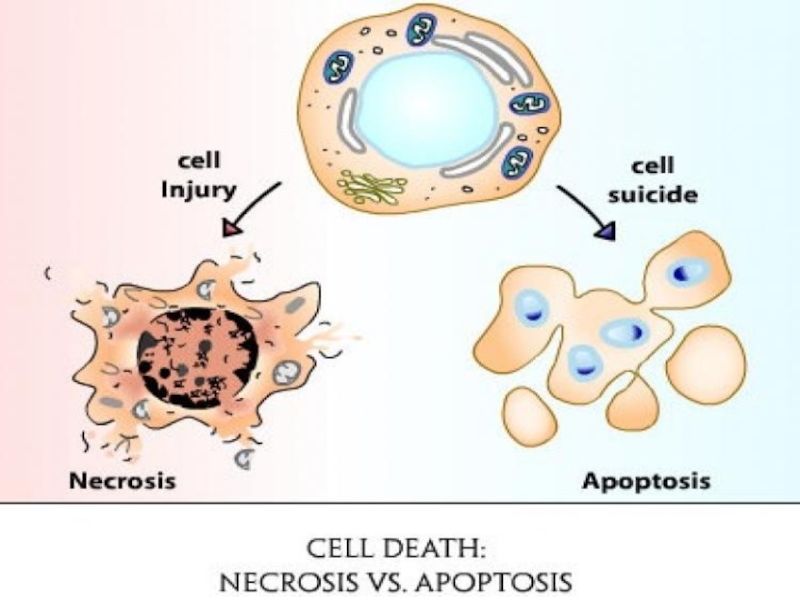
- 19. Сопротивление клеточной гибели Апоптоз – барьер для
- 21. Но не происходит Потому что: Теряется функция
- 22. Аутофагия Также форма клеточной смерти. Разрушаются органеллы
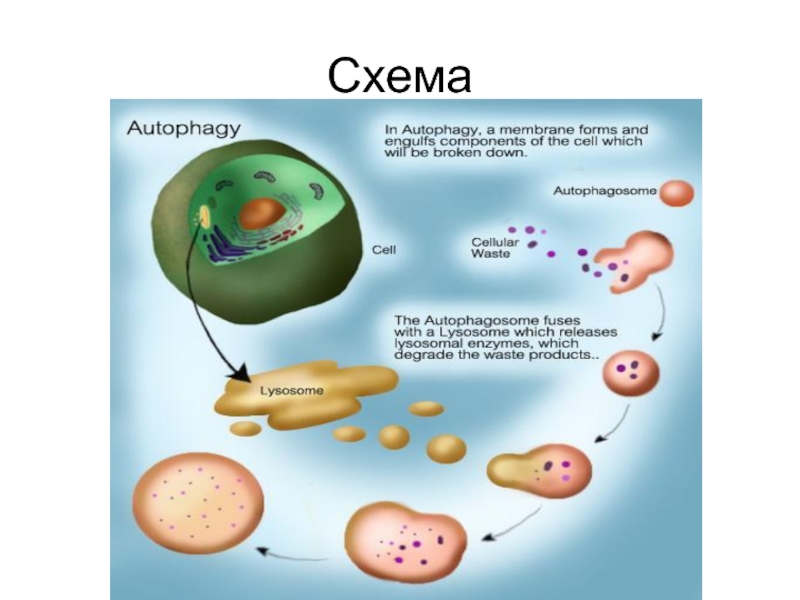
- 23. Схема
- 25. Обретение клеточного бессмертия Или феномен «иммортализации». Нормальные
- 28. Иммортализация Таким образом, теломераза «достраивает» отделенные фрагменты
- 29. Индуцирование ангиогенеза В опухолевой ткани формируется новообразованная
- 31. Характеристики сосудистой сети опухоли Кровеносные сосуды в
- 32. Активация инвазии и метастазирования
- 33. Эпителиально-мезенхимальный переход Приобретение опухолевой клеткой эпителия свойств
- 34. Эпителиально-мезенхимальный переход
- 35. Энергетическое перепрограммирование Длительная гиперпролиферация также включает
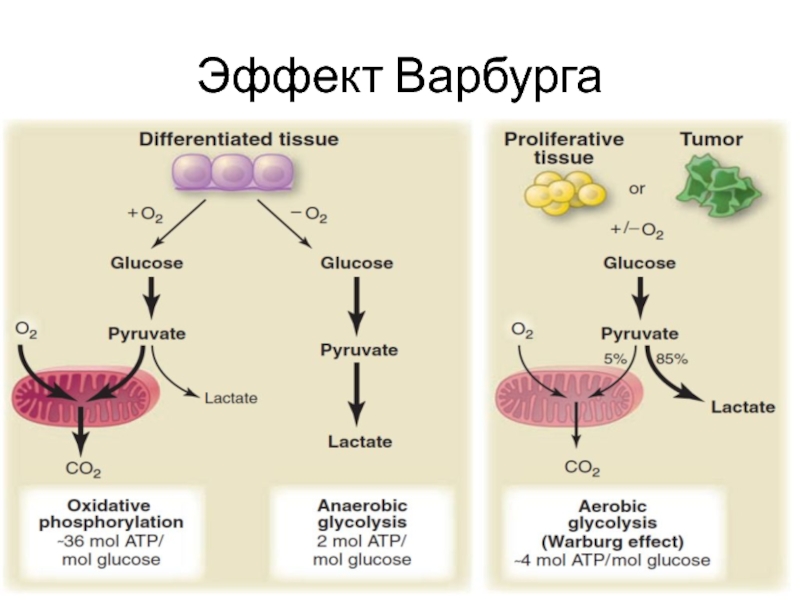
- 36. Эффект Варбурга
- 37. Эффект Варбурга Опухолевые клетки возмещают недостаток энергии,
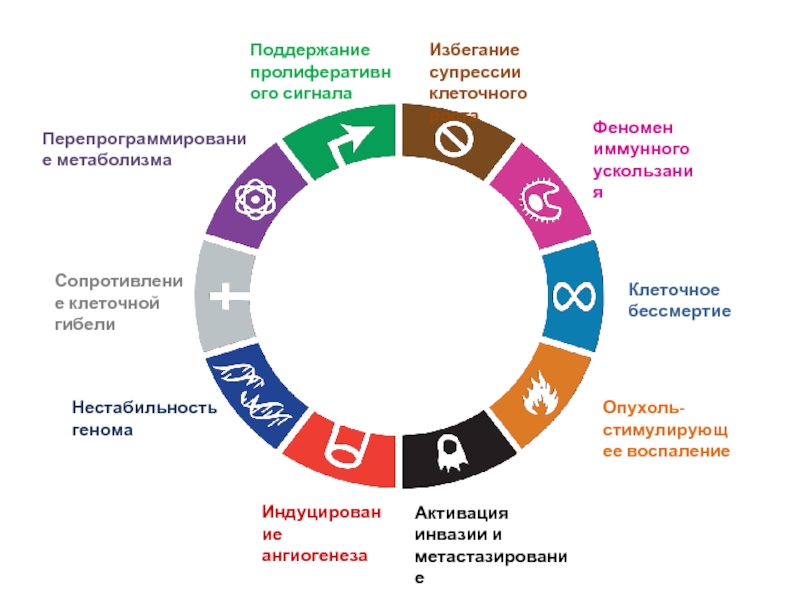
Слайд 2Поддержание пролиферативного сигнала
Избегание супрессии клеточного роста
Сопротивление клеточной гибели
Клеточное бессмертие
Индуцирование ангиогенеза
Активация инвазии
и метастазирование
Перепрограммирование метаболизма
Нестабильность генома
Опухоль-стимулирующее воспаление
Феномен иммунного ускользания
Слайд 3Геномная нестабильность
В результате воздействия:
Экзогенных факторов (ии, инсоляция, бензол, радон, нитрозамины, ВПЧ
16 типа).
Эндогенных факторов (гормональный дисбаланс, хронические воспалительные патологии)
Врожденные мутации (BRCA1 и BRCA2).
Эндогенных факторов (гормональный дисбаланс, хронические воспалительные патологии)
Врожденные мутации (BRCA1 и BRCA2).
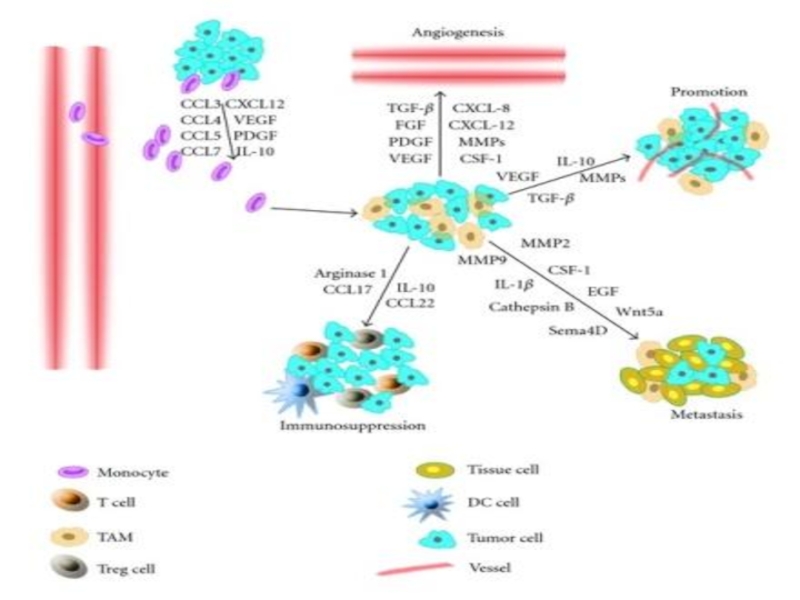
Слайд 6Стимулирующее опухоль воспаление
Хроническое воспаление (бактериальное, аутоиммунное, паразитарное) может обусловливать появление канцерогенных
мутаций в клеточном геноме.
В большинстве опухолевых тканей отмечается гиперэкспрессия ЦОГ-2. PgE2 способствует ангиогенезу (VEGF), ингибирует апоптоз.
Воспаление способствует появлению клеток неспецифического иммунитета в очаге (макрофаги).
В большинстве опухолевых тканей отмечается гиперэкспрессия ЦОГ-2. PgE2 способствует ангиогенезу (VEGF), ингибирует апоптоз.
Воспаление способствует появлению клеток неспецифического иммунитета в очаге (макрофаги).
Слайд 8Иммунное ускользание
Большая часть микроскопических опухолей уничтожаются иммунной системой (CD8+ T-киллеры;
NK-клетки)
Теория иммунного контроля - клетки и ткани постоянно подвергаются мониторингу иммунной системой, контроль ответственен за распознавание и элиминацию большинства ранних опухолевых клеток.
Опухоли, ассоциированный с иммунодефицитом (СПИД-ассоциированная Саркома Капоши, В-клеточная лимфома ЦНС)
Теория иммунного контроля - клетки и ткани постоянно подвергаются мониторингу иммунной системой, контроль ответственен за распознавание и элиминацию большинства ранних опухолевых клеток.
Опухоли, ассоциированный с иммунодефицитом (СПИД-ассоциированная Саркома Капоши, В-клеточная лимфома ЦНС)
Слайд 10Механизмы поддержания пролиферативного сигнала
Аутокринная стимуляция
Паракринная стимуляция опухоль-ассоциированной стромы
Гиперэкспрессия мембранных рецепторов к
факторам роста
Слайд 12Механизмы поддержания пролиферативного сигнала
Аутокринная стимуляция
Паракринная стимуляция опухоль-ассоциированной стромы
Гиперэкспрессия мембранных рецепторов к
факторам роста
Лиганд-независимая активация рецептора (активирующая мутация)
Лиганд-независимая активация рецептора (активирующая мутация)
Слайд 14Механизмы поддержания пролиферативного сигнала
Аутокринная стимуляция
Паракринная стимуляция опухоль-ассоциированной стромы
Гиперэкспрессия мембранных рецепторов к
факторам роста
Лиганд-независимая активация рецептора (активирующая мутация)
Активирующие мутации компонентов сигнального пути
Лиганд-независимая активация рецептора (активирующая мутация)
Активирующие мутации компонентов сигнального пути
Слайд 16Избегание супрессоров клеточного роста
Действие «каноничных» онкосупрессоров (TP53, RB1)
Действие TGF-b (в микроскопических
опухолях – антипролиферативное)
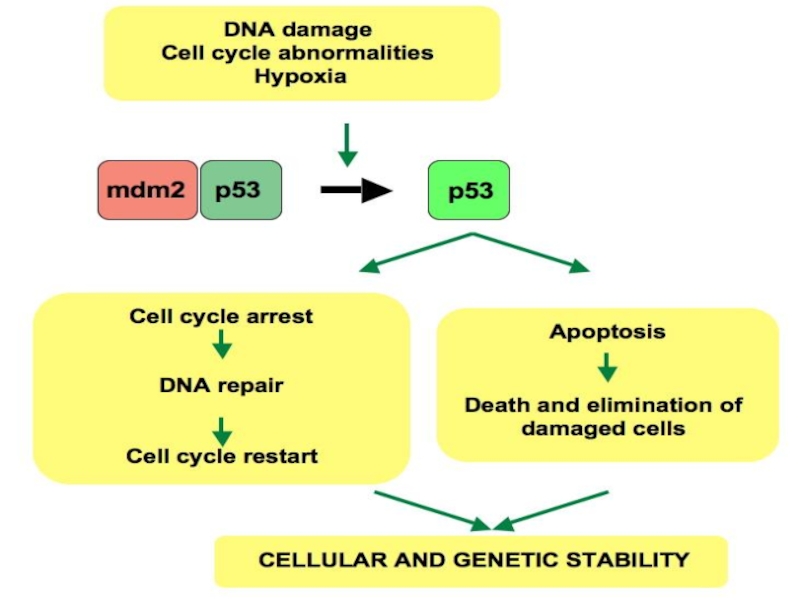
Слайд 19Сопротивление клеточной гибели
Апоптоз – барьер для развития рака.
Должен происходить в опухолевых
клетках, потому что:
Имеется серьезное повреждение генетического материала (опосредованно TP53)
Снижается концентрация факторов выживания в растущей опухолевой массе (ИЛ-3)
Гиперактивация некоторых сигнальных путей может приводить к апоптозу (Myc)
Имеется серьезное повреждение генетического материала (опосредованно TP53)
Снижается концентрация факторов выживания в растущей опухолевой массе (ИЛ-3)
Гиперактивация некоторых сигнальных путей может приводить к апоптозу (Myc)
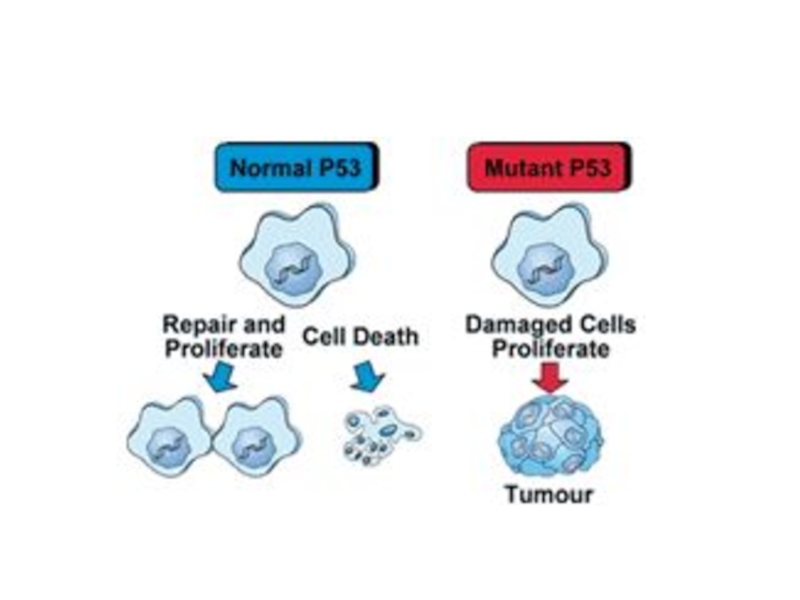
Слайд 21Но не происходит
Потому что:
Теряется функция TP53
Опухолевое микроокружение вырабатывает много ИЛ-3, PgE2
Теряется
функция внешнего контура (FAS-рецептор)
Усиливается экспрессия bcl-2
Усиливается экспрессия bcl-2
Слайд 22Аутофагия
Также форма клеточной смерти.
Разрушаются органеллы клетки, чтобы получившиеся катаболиты были использованы
клеткой для нужд биосинтеза и энергетического метаболизма.
Может способствовать как гибели опухолевых клеток, так и защите от вредных, стрессовых факторов.
Может способствовать как гибели опухолевых клеток, так и защите от вредных, стрессовых факторов.
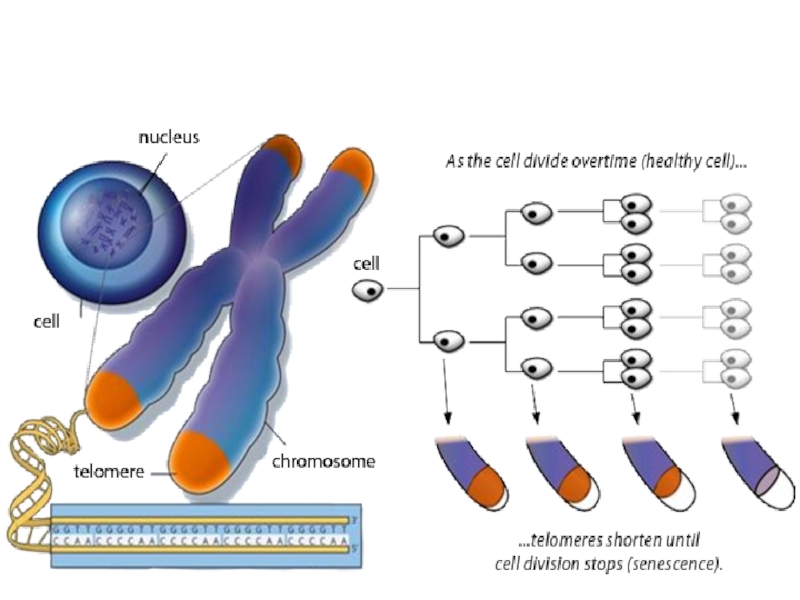
Слайд 25Обретение клеточного бессмертия
Или феномен «иммортализации».
Нормальные клеточные линии организма могут пройти лишь
через ограниченное число последовательных циклов деления (предел Хейфлика).
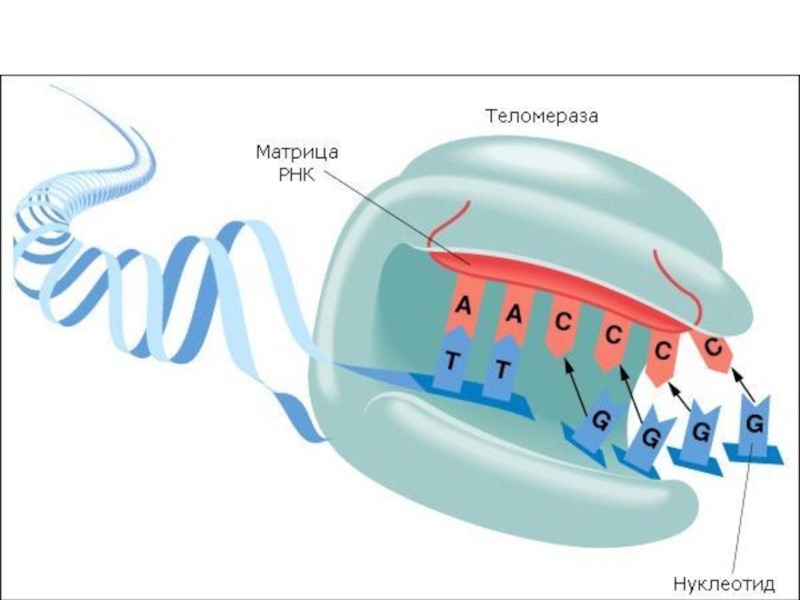
Слайд 28Иммортализация
Таким образом, теломераза «достраивает» отделенные фрагменты теломер в ходе деления, предохраняя
клетку от перехода в непролиферативное состояние (senescence).
Нетипичная функция теломеразы – участие в репаративных процессах (TERT-субъединица)
Нетипичная функция теломеразы – участие в репаративных процессах (TERT-субъединица)
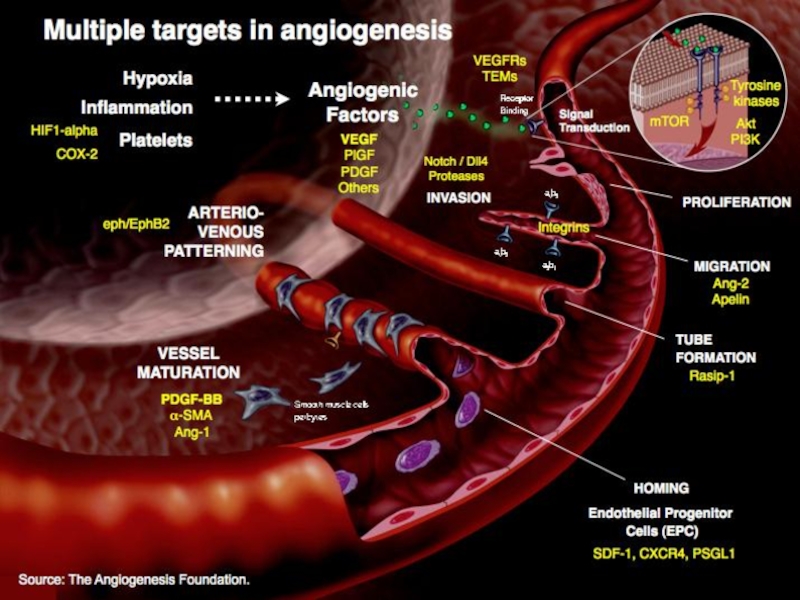
Слайд 29Индуцирование ангиогенеза
В опухолевой ткани формируется новообразованная сосудистая сеть.
Ангиогенез регулируется рядом факторов:
VEGF,
FGF – стимулируют; TSP-1, эндостатин – ингибируют.
Ангиогенез характеризуется хаотичным образованием сосудов, пролиферацией эндотелиоцитов.
Ангиогенез характеризуется хаотичным образованием сосудов, пролиферацией эндотелиоцитов.
Слайд 31Характеристики сосудистой сети опухоли
Кровеносные сосуды в опухолях аномальны:
Они запутанны, чрезмерно
ветвятся, искривлены
Увеличены
Поток крови абсолютно беспорядочный, турбулентный.
Помимо этого, характерен ненормальный уровень клеточной пролиферации и апоптоза эндотелиоцитов.
Увеличены
Поток крови абсолютно беспорядочный, турбулентный.
Помимо этого, характерен ненормальный уровень клеточной пролиферации и апоптоза эндотелиоцитов.
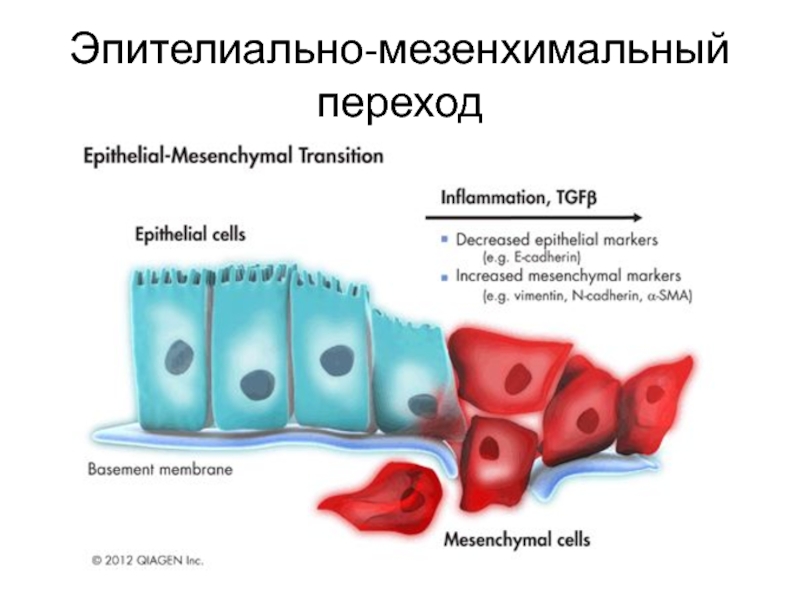
Слайд 33Эпителиально-мезенхимальный переход
Приобретение опухолевой клеткой эпителия свойств фибробласта.
ЭМП – запрограммированный процесс (SNAIL,
SLUG, TWIST).
ЭМП могут способствовать также системы, ответственные за онкосупрессию (TGF-b).
Процесс ЭМП обратим (ЭМП -> МЭП)
ЭМП могут способствовать также системы, ответственные за онкосупрессию (TGF-b).
Процесс ЭМП обратим (ЭМП -> МЭП)
Слайд 35Энергетическое перепрограммирование
Длительная гиперпролиферация также включает в себя корректировки в энергометаболизме,
с ориентировкой на то, чтобы ускорять процессы роста и деления.
Слайд 37Эффект Варбурга
Опухолевые клетки возмещают недостаток энергии, получаемой через аэробный гликолиз, за
счет гиперэкспрессии GLUT1.
А УСИЛЕННЫЙ ГЛИКОЛИЗ переводит многообразие промежуточных метаболитов гликолиза в различные биосинтетические пути, включая ведущие к образованию нуклеозид и аминокислот.
А УСИЛЕННЫЙ ГЛИКОЛИЗ переводит многообразие промежуточных метаболитов гликолиза в различные биосинтетические пути, включая ведущие к образованию нуклеозид и аминокислот.