- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Микрофлора окружающей среды. Нормальная микрофлора человека. Дисбактериоз презентация
Содержание
- 1. Микрофлора окружающей среды. Нормальная микрофлора человека. Дисбактериоз
- 2. Экология микроорганизмов Основные вопросы 1.Роль микроорганизмов в
- 3. «Мы, по сути, совсем не осведомлены
- 4. Они представляют самую древнюю и разнообразную
- 5. Микроорганизмы обитают во всех
- 6. Микрофлора почвы
- 7. В составе микрофлоры почвы выделяют следующие группы:
- 8. бактерии, участвующие в круговороте серы, железа,
- 9. Микрофлора воды
- 10. Вода является древнейшей средой обитания
- 11. Микрофлора воздуха При малейшем дуновении ветра поднимается
- 12. За сутки человек вдыхает около 10 тыс.
- 13. Микрофлора человека
- 14. В настоящее время понятие «микрофлора человека» утратило
- 15. Микробиом распределен в нашем организме неравномерно, по его
- 16. Микрофлора человека и ее значение Аутохтонная (присущая
- 17. Сформировано представление, согласно которому микробиоценоз представляет
- 18. Нормальная микрофлора на различных участках тела (экотопах)
- 20. Микрофлора ЖКТ
- 21. Микрофлора ЖКТ Желудочно-кишечный тракт заселен «по этажам».
- 22. Масса нормальной микрофлоры - 2,5 –
- 23. Микрофлора кишечника Факультативная условно патогенная
- 24. Контакты с бактериальными антигенами определяют созревание
- 25. Кишечник-часть иммунной системы В реализации иммунных механизмов
- 26. взаимодействия иммунной системы хозяина и бактерий-симбионтов. М-клетки
- 27. В состоянии дисбиоза снижение количества бактерий-симбионтов приводит
- 28. Исследуя влияние бактерий на защитные механизмы кишечника
- 29. Вообще, связь колонизации бактериями-симбионтами с развитием как
- 30. Лимфоидная ткань, ассоциированная со слизистой ЖКТ (МАLТ)
- 31. Цитокины и регуляция иммунного ответа в ЖКТ
- 32. Схематическое представление роли нормофлоры в функционировании
- 33. Системообразующие факторы микробиценоза - кворум сенсинг
- 34. Исследование внутрипопуляционных связей микробиоценоза кишечника
- 35. Показано, что при росте в жидких средах
- 36. Исследованиями последних лет установлено, что важным фактором
- 37. Бактериальные аутоиндукторы (язык общения) CH3 R2
- 38. Пример КС для аутоиндукция роста и апоптоза
- 39. ИСТОЧНИКИ КОЛОНИЗАЦИИ НОВОРОЖДЕННОГО
- 40. Еще до недавнего времени считалось, что плод
- 41. ИСТОЧНИКИ КОЛОНИЗАЦИИ НОВОРОЖДЕННОГО Колонизация микроорганизмами новорожденного осуществляется
- 42. Особенности микрофлоры у клинически здоровых детей раннего
- 43. Факторы, обеспечивающие формирование микробиома младенца. Инфекции половых
- 44. Понятно, что условия обитания микробов в
- 45. Микрофлора кожи
- 47. Нормальная микрофлора кожи: грам+ бактерии (пропионибактерии, дифтероиды,
- 48. Микрофлора кожи АНАЭРОБЫ:Propionobacteriumterium, Peptococcus, Streptomyces, Clostridium
- 49. Микрофлора дыхательных путей микрофлора рото- и носоглотки
- 50. Мочеполовой тракт Во влагалище – лактобактерии преобладают-
- 51. Микроэкологические изменения (дисбактериоз)
- 52. ДИСБАКТЕРИОЗ - клинико-лабораторный синдром, возникающий при целом
- 53. Диагноз «дисбактериоз» используется преимущественно отдельными врачами на
- 54. Это интересно! Распространённые методы диагностики дисбактериоза, такие
- 55. Методы исследования микробиоценоза и его нарушений
- 56. Последние исследования «пошатнули» стандартные представления о
- 57. Методы исследования: Метод газовой хроматографии в
- 58. Коррекция дисбактериоза
- 59. В Российской Федерации протокол ведения пациентов
- 60. Обычные методы лечения расстройств, диагностируемых как
- 61. Классификация препаратов 1.Пробиотики 2.Пребиотики 3.Синбиотики Проходят регистрацию
- 62. ПРОБИОТИКИ Живые микроорганизмы и вещества микробного происхождения,
- 63. Пребиотики и Синбиотики
- 64. Пребиотики – неперевариваемые ингредиенты пищи, стимулирующие рост
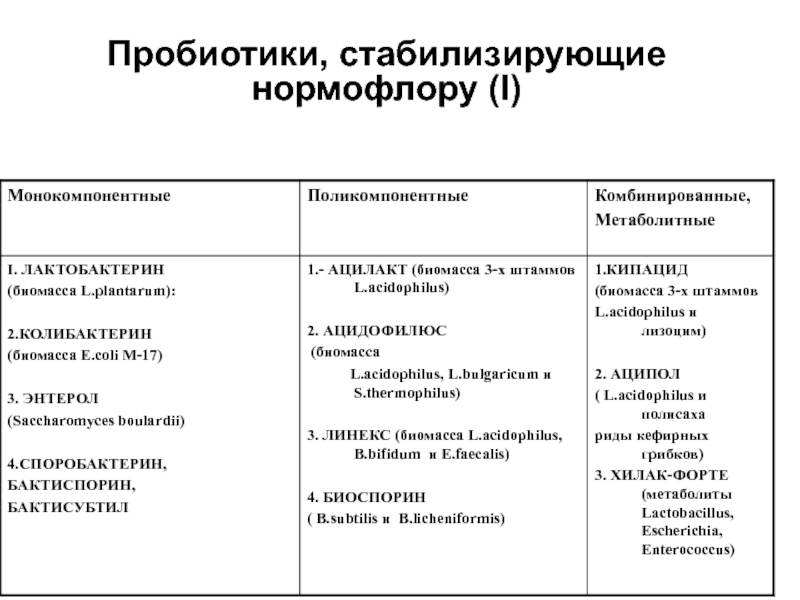
- 65. Пробиотики, стабилизирующие нормофлору (I)
- 66. Бифидосодержащие пробиотики (II)
- 67. Пребиотики, синбиотики, фаги
- 68. Рекомендации к селекции пробиотических штаммов
- 69. Исследование и поиск оригинальных пробиотических штаммов
- 70. СОВРЕМЕННЫЕ ПОДХОДЫ Получение новых препаратов на
- 71. Аутоиндукторы, ассоциированные с функцией “чувство кворума”(QS) “QS”
- 72. ПОЛУЧЕНИЕ НОВЫХ ПРОБИОТИЧЕСКИХ ПРЕПАРАТОВ
- 73. Пробиотики, стабилизирующие нормофлору (I)
- 74. Бифидосодержащие пробиотики (II)
- 75. Пребиотики, синбиотики, фаги
Слайд 1Лекция
Микрофлора окружающей среды. Нормальная микрофлора человека. Дисбактериоз.
Доцент, к.м.н. Темникова Наталья
ОмГМУ
2018
Слайд 2Экология микроорганизмов
Основные вопросы
1.Роль микроорганизмов в поддержании равновесия биосферы.
2.Микрофлора основных сред обитания
3.Микрофлора человека.
4.Гнотобиология и гнотобиологические технологии.
5.Дисбактериозы. Препараты для их коррекции.
Слайд 3
«Мы, по сути, совсем не осведомлены о том какие функции обеспечивает
Слайд 4
Они представляют самую древнюю и разнообразную группу живой природы.
Они являются единственными
Микроорганизмы в соответствии со своими жизненными потребностями заселяют определенные экологические ниши. Они находятся в составе сложных ассоциаций – биоценозов с различными типами синэргических и антагонистических отношений.В.И.Вернадским было сформулировано учение о биосфере как наивысшем уровне экологической интеграции.
Экологическая микробиология изучает микробные сообщества и взаимоотношения микро- и макроорганизмов, совместно обитающих в общих средах обитания.
Слайд 5 Микроорганизмы обитают во всех природных средах и являются
Слайд 6Микрофлора почвы
Почва является главным резервуаром и естественной
Их больше в увлажненной и обработанной почве (5 млрд/г), меньше в лесной почве, в песках (1 млрд/г).
Наиболее обильна микрофлора в верхнем горизонте почвы глубиной 2,5-15 см. Здесь протекают биохимические процессы превращения органических веществ, обусловленные жизнедеятельностью микроорганизмов.
Слайд 7В составе микрофлоры почвы выделяют следующие группы:
бактерии аммонификаторы, вызывающие гниение
нитрифицирующие бактерии: Nitrobacter и Nitrosomonas (Nitrosomonas окисляют аммиак до азотистой кислоты, образуя нитриты, Nitrobacter превращают азотистую кислоту в азотную и нитраты);
азотфиксирующие бактерии: усваивают из воздуха азот и синтезируют белки и другие органические соединения азота, используемые растениями;
Слайд 8
бактерии, участвующие в круговороте серы, железа, фосфора и других элементов -
бактерии, расщепляющие клетчатку, вызывающие брожение (молочнокислые, спиртовые, маслянокислые, уксусные).
С выделениями человека и животных, с фекально-бытовыми сточными водами в почву могут попадать патогенные и условно-патогенные микроорганизмы (возбудители грибковых заболеваний, ботулизма, столбняка, газовой гангрены, сибирской язвы, бруцеллеза, лептоспироза, кишечных инфекций).
Слайд 10
Вода является древнейшей средой обитания микроорганизмов.
Автохтонная (собственная) микрофлора представлена
Аллохтонная (заносная) микрофлора попадает в открытые водоемы из почвы, воздуха, организмов животных и человека и изменяет микробный биоценоз и санитарный режим. Количественный и качественный состав микрофлоры воды зависит от состава и концентрации минеральных и органических веществ, температуры, рН, массивности поступления ливневых, фекально-бытовых и промышленных сточных вод. Количество микробов прямо пропорционально степени загрязненности водоемов.
Вода имеет значение в распространении возбудителей кишечных инфекций, в воде могут сохраняться энтеровирусы, сальмонеллы, лептоспиры, возбудители холеры, дизентерии.
Слайд 11Микрофлора воздуха
При малейшем дуновении ветра поднимается в воздух масса мелких пылинок,
Обычно пребывание микробов в воздухе кратковременно. Для некоторых бактерий и грибов воздушные потоки — основной путь распространения. Споры плесеней нередко разносятся по воздуху на очень большие расстояния.
Чем выше и дальше от земли, тем микробов меньше. В горном воздухе их не так много, как в воздухе узких и пыльных улиц. Очень мало микробов над морем, вдали от берегов. Участникам арктических и антарктических экспедиций приходится иногда работать по колено в ледяной воде, но обычно никто из них не заболевает заразными болезнями, связанными с простудой. Объясняется это тем, что воздух в полярной зоне почти свободен от микроорганизмов, в том числе и от возбудителей болезней.
Слайд 12За сутки человек вдыхает около 10 тыс. л воздуха. Но в
Некоторые микробы (возбудители чумы, коклюша) в воздухе быстро погибают. Но туберкулезная палочка долго переносит высушивание. Туберкулезные палочки остаются жизнеспособными в пыли до 3 месяцев. Вместе с частицами пыли они разносятся по воздуху на большие расстояния.
В каждой капельке брызг от кашля туберкулезных больных обнаружено до 40 тыс. туберкулезных палочек, распространясь на 2—3 м.
Слайд 14
В настоящее время понятие «микрофлора человека» утратило свою актуальность: мы несем в своем организме
Слайд 15
Микробиом распределен в нашем организме неравномерно, по его топографии и видовому составу принято различать
Наиболее крупным микробиомом нашего тела является, несомненно, кишечный. Он может состоять из сотен видов различных микроорганизмов, но у взрослого человека преобладают бактерии двух разделов: Firmicutes и Bacteroidetes.
Кишечный микробиом изучен лучше других бактериальных сообществ человека, и многолетние исследования, о которых будет рассказано ниже, показали, что именно он в большей степени влияет на здоровье своего носителя. ...
Слайд 16Микрофлора человека и ее значение
Аутохтонная (присущая данной области) микрофлора разделена на
Постоянная – на облигатную и факультативную.
На слизистых – просветная и пристеночная микрофлора (мукозный матрикс, биопленка с пристеночной микрофлорой), которая обеспечивает колонизационную резистентность.
Гнотобионты (бесмикробные животные) – для изучения роли нормальной микрофлоры, гнотобиологические технологии – в медицине (лечение ожогов, иммунодефицитов).
Слайд 17
Сформировано представление, согласно которому микробиоценоз представляет собой своеобразный «орган» , высокоорганизованную
Слайд 18Нормальная микрофлора на различных участках тела (экотопах) отличается в количественном и
Основные функции нормальной микрофлоры:
защитная (колонизационная резистентность);
иммуностимулирующая (антигенная стимуляция);
пищеварительная (обмен холестерина и желчных кислот);
метаболическая (синтез витаминов группы В, К, никотиновой, пантотеновой, фолиевой кислот).
Слайд 21Микрофлора ЖКТ
Желудочно-кишечный тракт заселен «по этажам».
В желудке – лактобактерии, энтерококки,
Микрофлора толстого кишечника: до 95% - анаэробные бактерии.
АНАЭРОБЫ: Bacteroides, Bifidobacterium, Coprococcus, Eubacterium, Clostridium
АЭРОБЫ: Escherichia, Staphylococcus (энтерококк), Lactobacillus, Klebsiella, Proteus, дрожжи.
Безусловный рекордсмен по плотности микроскопического населения — кишечник, где находится от 2 до 2,5 кг нормальной микрофлоры. В 1 г содержимого толстой кишки насчитывается до 250 млрд. микроорганизмов
Слайд 22
Масса нормальной микрофлоры - 2,5 – 3,0 кг
Численность микроорганизмов только ЖКТ
Состав : 17 семейств, 45 родов, около 500 видов
Слайд 23
Микрофлора кишечника
Факультативная
условно патогенная
сапрофитная
Транзиторная
бфидо- и лактобактерии
и
эшерихии (кишечные
пептострептококки
энтерококки
бактероиды
пептококки
стрептококки
бациллы
Облигатная
(главная микрофлора)
дрожжеподобные грибы
рода Candida
энтеробактерии
неферментирующие
грамотрицательные
палочки
дрожжи и некоторые дрожжеподобные
грибы
стафилококки
Слайд 24
Контакты с бактериальными антигенами определяют созревание иммунной системы.
Состав микрофлоры кишечника
Слайд 25Кишечник-часть иммунной системы
В реализации иммунных механизмов на уровне интестинального тракта принимают
Нормальная микрофлора.
Лимфоидная ткань, ассоциированная со слизистой оболочкой кишечника
Цитокины, как фактор межклеточного взаимодействия.
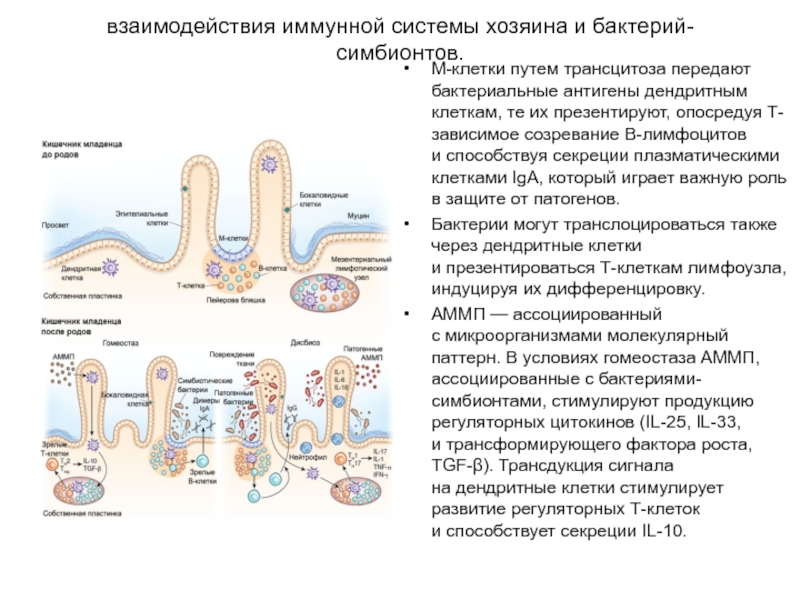
Слайд 26взаимодействия иммунной системы хозяина и бактерий-симбионтов.
М-клетки путем трансцитоза передают бактериальные антигены
Бактерии могут транслоцироваться также через дендритные клетки и презентироваться Т-клеткам лимфоузла, индуцируя их дифференцировку.
АММП — ассоциированный с микроорганизмами молекулярный паттерн. В условиях гомеостаза АММП, ассоциированные с бактериями-симбионтами, стимулируют продукцию регуляторных цитокинов (IL-25, IL-33, и трансформирующего фактора роста, TGF-β). Трансдукция сигнала на дендритные клетки стимулирует развитие регуляторных Т-клеток и способствует секреции IL-10.
Слайд 27
В состоянии дисбиоза снижение количества бактерий-симбионтов приводит к размножению патогенов. Патогенные АММП индуцируют
Слайд 28
Исследуя влияние бактерий на защитные механизмы кишечника (рис. 6), ученые искусственно колонизировали бактерией
Hooper L.V., Wong M.H., Thelin A., Hansson L., Falk P.G., Gordon J.I. (2001). Molecular analysis of commensal host-microbial relationships in the intestine. Science. 291, 881–884;...
Слайд 29
Вообще, связь колонизации бактериями-симбионтами с развитием как приобретенного, так и врожденного иммунитета, демонстрировали
Round J.L. and Mazmanian S.K. (2009). The gut microbiota shapes intestinal responses during health and disease. Nat. Rev. Immunol. 9, 313–323; O’Hara A.M. and Shanahan F. (2007). Gut microbiota: mining for therapeutic potential. Clin. Gastroenterol. Hepatol. 5, 274–284; Abreu M.T., Fukata M., Arditi M. (2005). TLR signaling in the gut in health and disease. J. Immunol. 174, 4453–4460
Слайд 30Лимфоидная ткань, ассоциированная со слизистой ЖКТ (МАLТ)
Иммунокомпетентные клетки распола-гаются или
В тонком кишечнике-пейеровы бляшки
В толстом-солитарные фоликулы
Иммунологически в лимфоидной ткани выделяют индуктивную зону(распознование и презентация антигена) и эффекторная (синтез Ig, цитотоксичность, продукция цитокинов)
Слайд 31Цитокины и регуляция иммунного ответа в ЖКТ
Клетки, вовлекаемые в иммунный ответ
Интерлeйкины
Интерфероны
Факторы некроза опухоли
Хемокины
Факторы роста колониестимулирующего фактора
Биохимический ответ цитокинов реализуется в форме иммунного ответа, толерантности или иммунной патологии
Слайд 34 Исследование внутрипопуляционных связей микробиоценоза кишечника человека и животных показало,
Системообразующие факторы микробиценоза -
кворум сенсинг
Биопленка. Микроорганизмы, в количестве 1011 клеток/см3 распределены в пристеночном слое муцина – относительно прочного геля, состоящего из пептидогликана, продуцируемого бокаловидными клетками эпителия кишечной слизистой оболочки.
Биопленка по химической природе близка полисахаридной защитной капсуле, которой окружают себя многие микробы.
Это псевдоцитологической структура.
Слайд 35Показано, что при росте в жидких средах или на поверхности твердого
Существенно, что стремление к объединению в группы является общей закономерностью в мире микроорганизмов: одиночные микробы в виде взвеси в жидкости или будучи рассеянны по твердой поверхности, как правило, нежизнеспособны.
Прикрепленные к поверхности ассоциации микробов называются биопленками.
В природе часто наблюдается объединение в пределах одного агрегата нескольких видов метаболически взаимосвязанных микроорганизмов (такие ассоциации называются консорциумами). Консорциумы, включающие в себя несколько десятков видов микробов, получили название «бактериальные маты».
Слайд 36Исследованиями последних лет установлено, что важным фактором интеграции сообществ микроорганизмов являются
Показано, что бактериальные олигопептиды не только принимают участие в регуляции таких жизненно важных функций как размножение, но и обеспечивают их коллективное поведение.
Это продемонстрировано на примере колонизации человека патогенными бактериями. Микробы не атакуют клетки хозяина, не вырабатывают факторы патогенности до тех пор, пока плотность их популяции (число на единицу объема) не достигнет необходимой величины. Именно в этот момент происходит освобождение олигопептидов из части бактерий, что является сигналом для активации соответствующих биохимических систем у остальных микроорганизмов.
Слайд 37Бактериальные аутоиндукторы (язык общения)
CH3
R2
R1
O
H
N
H
O
O
H
H
NH
O
O
NH
H
пептиды
лактоны
N
H
OH
O
хинолы
Образование биопленок
Патогенность
Синтез антибиотиков Биолюминисценция
Слайд 38Пример КС для аутоиндукция роста и апоптоза
Культура Micrococcus luteus, голодавшая в
Как пример "бактериального альтруизма«….Голодающая популяция E. coli постепенно разделяется на две субпопуляции, одна из которых гибнет и подвергается автолизу, в то время как другая субпопуляция использует продукты автолиза как субстрат и продолжает расти и создавать колониеобразующие единицы.
Слайд 40
Еще до недавнего времени считалось, что плод в утробе матери полностью огражден от контакта
Слайд 41ИСТОЧНИКИ КОЛОНИЗАЦИИ НОВОРОЖДЕННОГО
Колонизация микроорганизмами новорожденного осуществляется из трех источников:
родового канала матери;
объектов
Грудного вскармливания
Слайд 42Особенности микрофлоры у клинически здоровых детей раннего возраста.
Высокие популяционные уровни бифидобактерий
Лактобактерии не у всех.
К концу первого года жизни происходит полная или частичная элиминация условно-патогенных бактерий
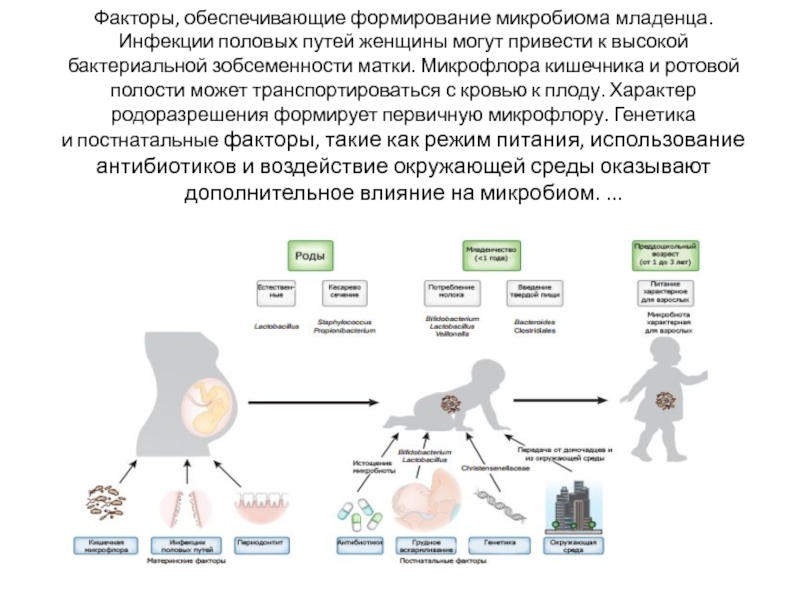
Слайд 43Факторы, обеспечивающие формирование микробиома младенца. Инфекции половых путей женщины могут привести
Слайд 44
Понятно, что условия обитания микробов в человеческом организме не одинаковы. Микрофлора
Микробиотопы организма существенно различаются по газовому составу воздушной среды, спектру ферментов и иммунных факторов, продуктов метаболизма и других биологически активных веществ, уровню рН среды, набору экзогенных веществ - эти и другие параметры различны в ротовой полости, пищеводе, желудке, тонком и толстом кишечнике, влагалище, носу, верхних и нижних дыхательных путях, на коже.
Необходимо учесть разнообразие клеточного состава этих поверхностей, ведь колонизация, т.е. процесс заселения эпителия микробами, невозможен без предварительной адгезии. Адгезия обусловлена лигандно-рецепторным сродством поверхностных структур эпителиальных клеток и микробов.
Поэтому в микроэкологическом отношении организм человека полибиотопен. Каждый биотоп вместе с соответствующим микробиоценозом составляет небольшую экосистему. Естественная аутомикрофлора тела - единый природный комплекс, состоящий из совокупности гетерогенных микробоценозов в различных участках человеческого организма.
Подобная интеграция целесообразна и необходима, она универсальна для живого мира и могла сформироваться только в результате отбора в процессе биологической эволюции.
Слайд 47Нормальная микрофлора кожи: грам+ бактерии (пропионибактерии, дифтероиды, эпидермальные и другие коагулазо-отрицательные
Микрофлора дыхательных путей: микрофлора рото- и носоглотки – бактероиды, зеленящие стрептококки, нейссерии, дифтероиды, стафилококки. Трахея, бронхи и альвеолы в норме стерильны.
Мочеполовой тракт: во влагалище – лактобактерии, бифидобактерии, бактероиды, пропионибактерии, превотеллы, порфиниромонады, дифтероиды. Преобладают анаэробы, могут быть гарднереллы.
Желудочно-кишечный тракт заселен «по этажам». В желудке – лактобактерии, энтерококки, дрожжи, бифидобактерии. Микрофлора толстого кишечника: до 95% - анаэробные бактерии. Преобладают грам+ анаэробные палочки (бифидо- и лактобактерии, эубактерии), грам+ спорообразующие анаэробные палочки (клостридии), энтерококки, грам- анаэробные палочки (бактероиды), гам- факультативно-анаэробные палочкикишечные палочки и близкие энтеробактерии), анаэробные грам+кокки (пептококки, пептострептококки).
Clostridium diffecile – возбудитель псевдомембранозного колита.
Слайд 48Микрофлора кожи
АНАЭРОБЫ:Propionobacteriumterium, Peptococcus, Streptomyces, Clostridium
АЭРОБЫ:Corynebacterium, Micrococcus, Грибки, Staphylococcus, Streptococcus, Pseudomonas, Klebsiella,
Слайд 49Микрофлора дыхательных путей
микрофлора рото- и носоглотки бактероиды, зеленящие стрептококки, нейссерии, дифтероиды,
Трахея, бронхи и альвеолы в норме стерильны.
Слайд 50Мочеполовой тракт
Во влагалище – лактобактерии преобладают- колонизационная резистентность. Обеспечивают кислую РН.
У
АНАЭРОБЫ:Bacteroides, Bifidobacterium, Mobiluncus
АЭРОБЫ:Gardnerella, Lactobacillus, Micoplasma, Candida, Streptococcus
Слайд 52ДИСБАКТЕРИОЗ - клинико-лабораторный синдром, возникающий при целом ряде заболеваний и клинических
изменением качественного и/или количественного состава нормофлоры, а также
метаболическими и иммунными нарушениями, сопровождающимися у части пациентов поражением кишечника, транслокацией бактерий в несвойственные биотопы и их избыточным ростом
(ОСТ № 231“Дисбактериоз кишечника”, 09.06.2003)
Слайд 53 Диагноз «дисбактериоз» используется преимущественно отдельными врачами на территории России; в других странах
За рубежом существует диагноз «синдром избыточного бактериального роста» в тонкой кишке (СИБР), корректно и конкретно определённый.
Он ставится только при обнаружении более 105 микроорганизмов в одном миллилитре аспирата из тонкой кишки и/или появления в ней флоры, характерной для толстой кишки.
Диагноз «дисбактериоз» не указан в Международной классификации болезней-10 ; также он отсутствует в нормативном документе Министерства здравоохранения РФ «Стандарты (протоколы) диагностики и лечения болезней органов пищеварения».
Слайд 54Это интересно!
Распространённые методы диагностики дисбактериоза, такие как копрологическое и микробиологическое исследование кала, не дают
Диагноз «дисбактериоз», как правило, ставится необоснованно, поскольку качественный и количественный состав микрофлоры кишечника обычно мало изменяется на протяжении жизни человека.
Использование термина «дисбактериоз» на территории России активно поддерживается фармацевтическими компаниями (в том числе и западными) — на телевидении и в других средствах массовой информации, в основном в виде рекламы фармацевтических продуктов .
Симптомы, называемые термином «дисбактериоз», встречаются в рамках множества совершенно различных заболеваний и синдромов (в их числе называются синдром раздражённой толстой кишки, синдром избыточного микробного роста, антибиотикоассоциированный колит, диарея); порой они могут быть обусловлены неправильным питанием, ограничениями в питании; функциональные расстройства кишечника в раннем детском возрасте часто обусловлены обычной младенческой коликой, проходящей с взрослением безо всякого лечения.
Слайд 56
Последние исследования «пошатнули» стандартные представления о патогенезе многих заболеваний Тому способствовало и
По сравнению с молекулярно-генетическими методами оказывается, что определение 60-80% их микробиоценоза не доступно для культуральных методов.
Слайд 57Методы исследования:
Метод газовой хроматографии в сочетании с масс-спектрометрией (сокращенно –
Молекулярно-генетические методы: на основе ПЦР, биочипные технологии
Бактериологический и копрологический метод
Слайд 59
В Российской Федерации протокол ведения пациентов с дисбактериозом регламентировался стандартом ОСТ
Слайд 60
Обычные методы лечения расстройств, диагностируемых как дисбактериоз (назначение пробиотиков, бактериофагов и т. п.), являются малоэффективными,
Слайд 61Классификация препаратов
1.Пробиотики
2.Пребиотики
3.Синбиотики
Проходят регистрацию через ГИСК им.Тарасевича и Комитет МИБП
4.Биологически активные добавки
Слайд 62ПРОБИОТИКИ
Живые микроорганизмы и вещества микробного происхождения, оказывающие при естественном способе введения
Слайд 63Пребиотики и Синбиотики
– неперевариваемые ингредиенты продуктов питания немикробного происхождения, способные при оральном назначении оказывать позитивный эффект на организм через селективную стимуляцию роста или метаболической активности нормальной микрофлоры толстой кишки.
Синбиотики
- препараты, полученные в результате рациональной комбинации пробиотиков и пребиотиков (живые бактерии и субстраты, стимулирующие их рост).
Слайд 64 Пребиотики – неперевариваемые ингредиенты пищи, стимулирующие рост собственной нормальной флоры, создающие
Пребиотики находятся в молочных продуктах, кукурузных хлопьях, крупах, хлебе, луке репчатом, цикории полевом, чесноке, фасоли, горохе, артишоке, аспарагусе, бананах и многих других продуктах.
Основными пребиотиками являются инулин, олигосахариды и лактулоза, которая входит в состав препаратов Дюфалак и Лактусан, лизоцим, пантотенат кальция (Кальцидум), пара-амино-метил-бензойная кислота.
Слайд 68
Рекомендации к селекции пробиотических
штаммов (I)
1. Должны быть безвредными (авирулентными,
2. Обладать широким спектром антагонистической и метаболитической активности
3. Индуцировать в организме синтез факторов неспецифической защиты
4. Быть технологичными
Пробиотические бактерии должны обладать устойчивым генотипом, изменение фенотипических свойств должно быть контролируемым
6.Микробы-продуценты не должны ингибировать индигенные бактерии нормальной микрофлоры
7.Обладать устойчивостью к действию неблагоприятных факторов
8. Сохранять свои биологические свойства в течение 1 года при температуре хранения не выше 8о С
Слайд 69Исследование и поиск оригинальных пробиотических штаммов
1. Синтезирующих короткоцепочечные жирные кислоты:
защита от
2. Связывание азота и его выведение:
профилактика печеночной энцефалопатии.
3. Связывание фосфатов и их выведение:
снижение риска хронической почечной недостаточности.
4. Деградация оксалатов: защита от развития почечных камней.
5. Удаление желчных кислот и нейтральных стеролов:
снижение риска сердечно-сосудистых заболеваний.
Слайд 70СОВРЕМЕННЫЕ ПОДХОДЫ
Получение новых препаратов на основе аутоиндукторов “чувства кворума”(QS)
Конструирование препаратов
Создание целевых генетически модифицированных микроорганизмов из представителей нормофлоры
Слайд 71Аутоиндукторы, ассоциированные с функцией “чувство кворума”(QS)
“QS” зависимое увеличение устойчивости к воздействию
Усиление адгезивных свойств нормофлоры
Нарушение действия генов-регуляторов вирулентности у S.aureus, L.monocytogenes, P. aeruginosa, Salmonella enteritidis и др.
Получение новых антимикробных препаратов на основе аутоиндукторов