зав. каф.,
проф., к.м.н. Барычева Л.Ю
Выполнили: студентки 6 курса 62/10 группы
Асханова З.Р.
Тарасова А.Г.
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Характеристика случаев ПИДс в сочетании с другими крупными дефектами презентация
Содержание
- 1. Характеристика случаев ПИДс в сочетании с другими крупными дефектами
- 2. Цель исследования: Дать характеристику первичных иммунодефицитов,
- 3. Задачи: 1.Определить нозологический состав четко очерченных первичных
- 4. Материалы и методы исследования: Под наблюдением находились
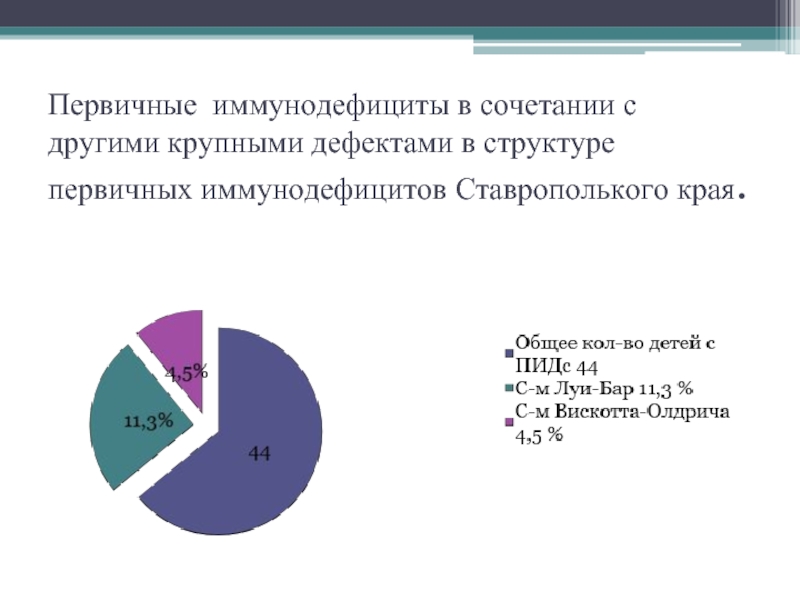
- 5. Первичные иммунодефициты в сочетании с другими крупными дефектами в структуре первичных иммунодефицитов Ставрополького края.
- 6. Этиология синдрома Луи-Бар Мутация гена
- 7. Патогенез синдрома Луи – Бар: Ген ATM
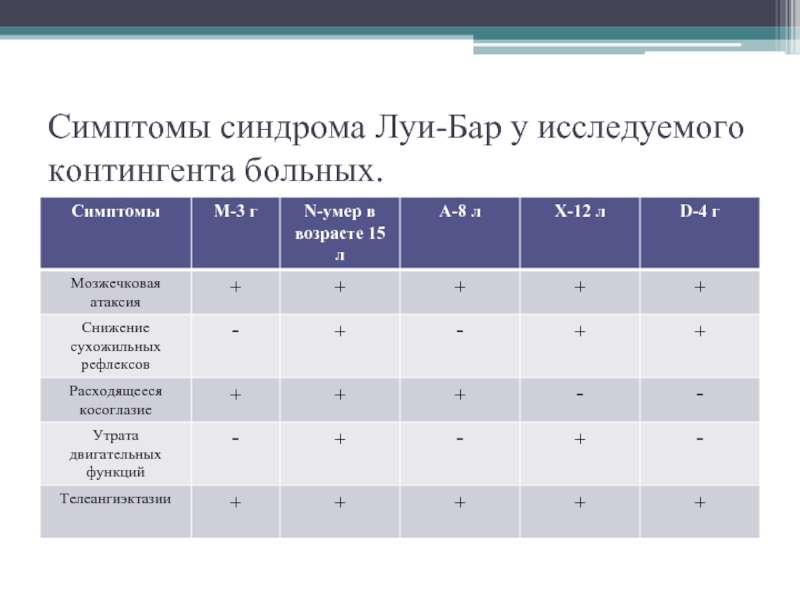
- 8. Симптомы синдрома Луи-Бар у исследуемого контингента больных.
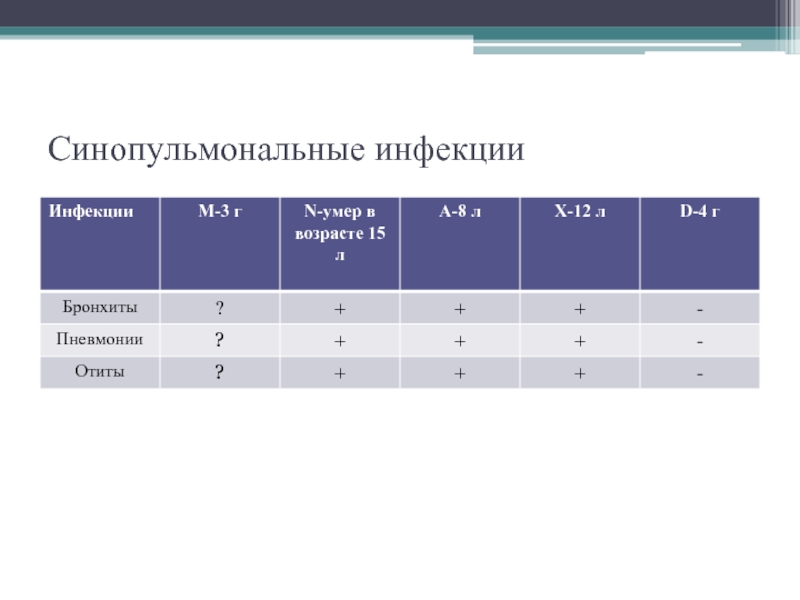
- 9. Синопульмональные инфекции
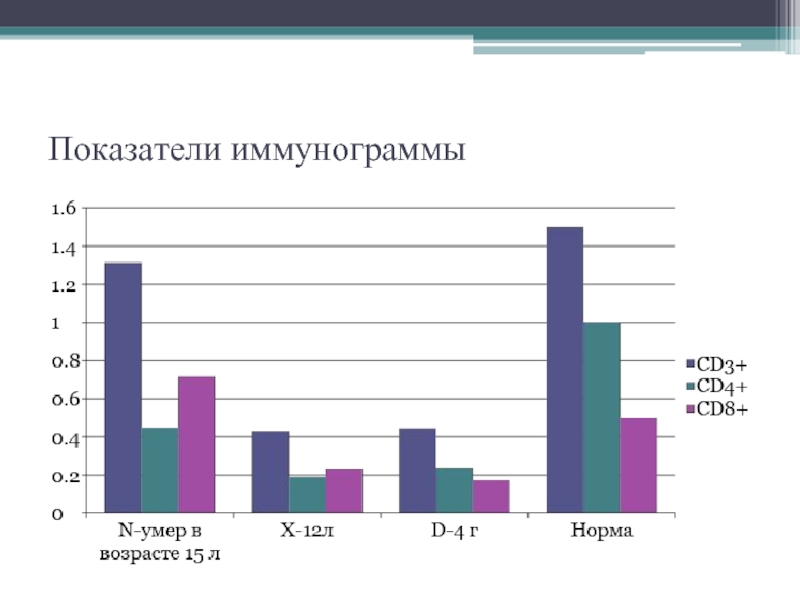
- 10. Показатели иммунограммы
- 11. Показатели Ig A
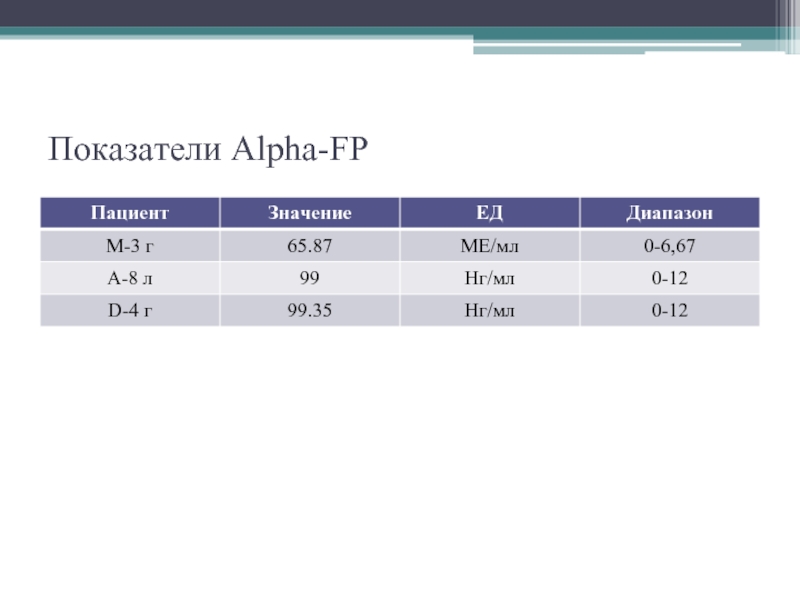
- 12. Показатели Alpha-FP
- 13. Проведено лечение:
- 14. Больной N-умер в возрасте 15 л.
- 15. Этиология синдрома Вискотта-Олдрича Мутация гена
- 16. Патогенез синдрома Вискотта-Олдрича Точная функция гена WASp
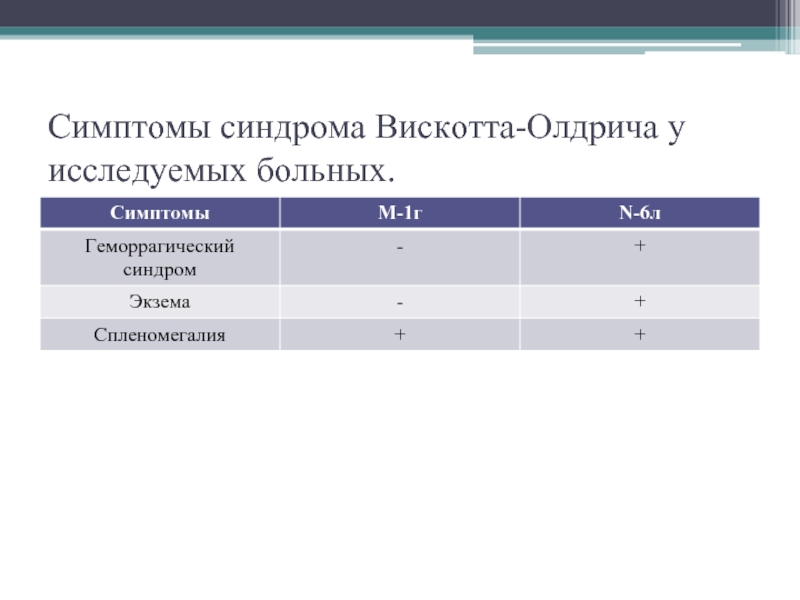
- 17. Симптомы синдрома Вискотта-Олдрича у исследуемых больных.
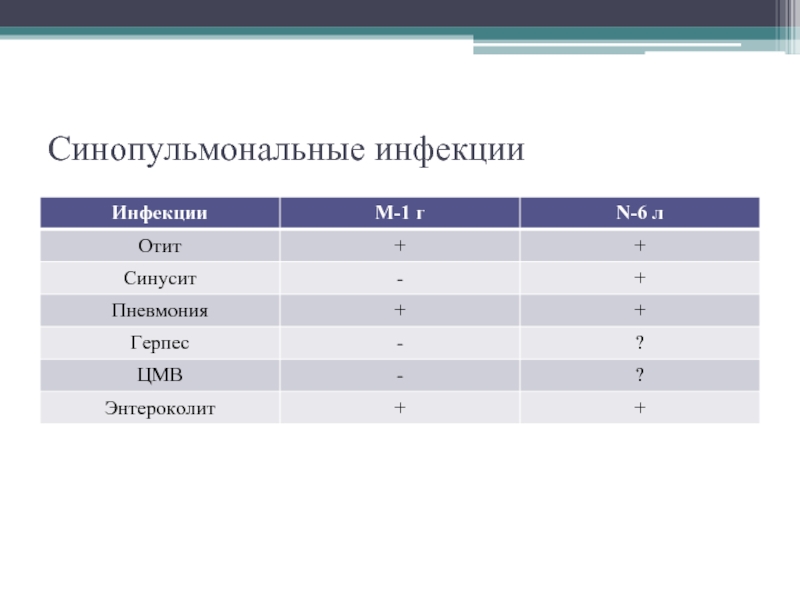
- 18. Синопульмональные инфекции
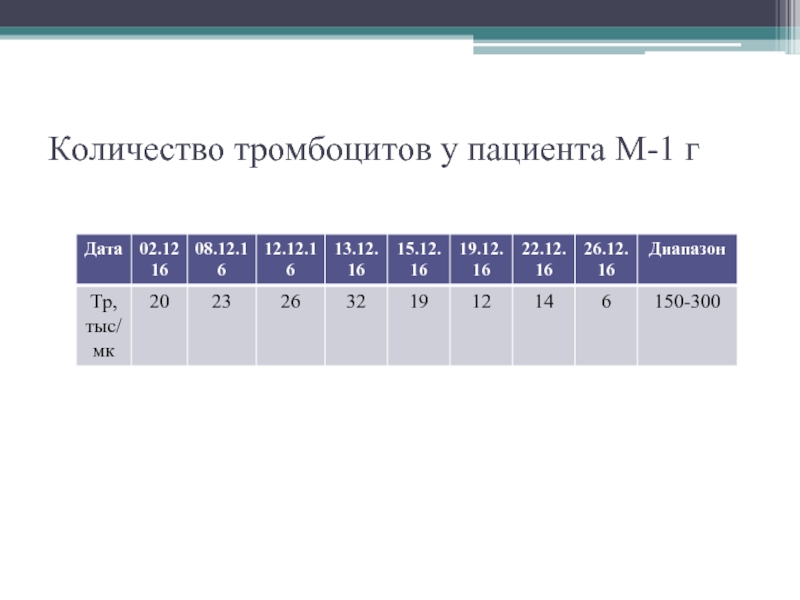
- 19. Количество тромбоцитов у пациента М-1 г
- 20. Количество тромбоцитов у пациента N-6 л.
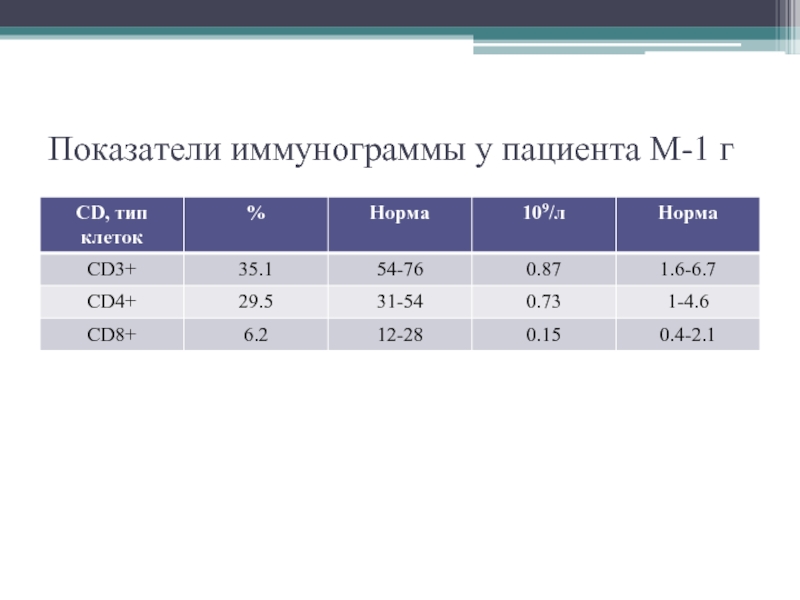
- 21. Показатели иммунограммы у пациента М-1 г
- 22. Проведено лечение пациенту М-1г:
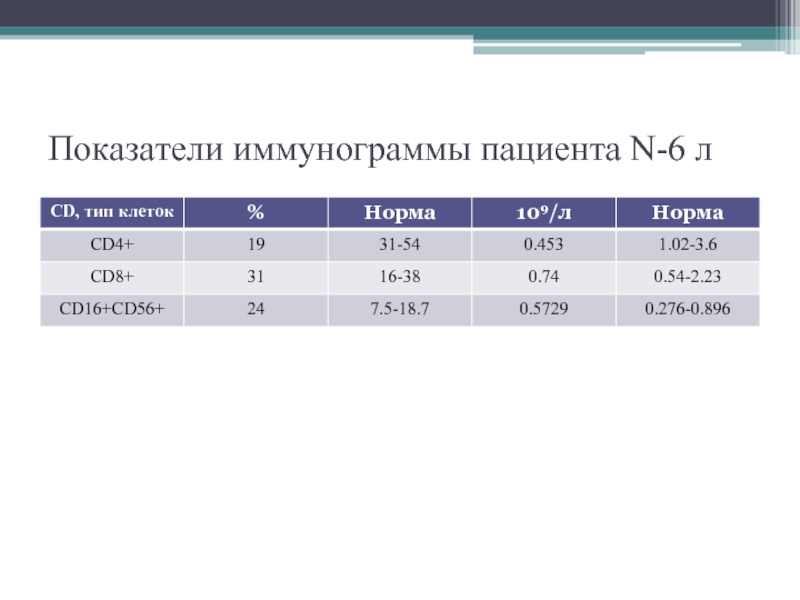
- 23. Показатели иммунограммы пациента N-6 л
- 24. Больной N-6 л. 17.04.2015 г. поступил в
Слайд 2Цель исследования:
Дать характеристику первичных иммунодефицитов, ассоциированных с другими дефектами у
детей в Ставропольском крае.
Слайд 3Задачи:
1.Определить нозологический состав четко очерченных первичных иммунодефицитов.
2.Изучить клинико-иммунологические особенности первичных иммунодефицитов,
ассоциированных с другими главными дефектами.
3.Оценить эффективность терапии и прогноз у пациентов с четко очерченными первичными иммунодефицитами.
4.Сопоставить полученные клинико-иммунологические данные с результатами, представленными в поисковых системах Clinicalkey и Pubmed.
3.Оценить эффективность терапии и прогноз у пациентов с четко очерченными первичными иммунодефицитами.
4.Сопоставить полученные клинико-иммунологические данные с результатами, представленными в поисковых системах Clinicalkey и Pubmed.
Слайд 4Материалы и методы исследования:
Под наблюдением находились 7 пациентов с диагнозом ПИДС
ассоциированных с другими главными дефектами:
Из них 5 детей с диагнозом атаксия – телеангиэктазия (синдром Луи – Бар)
2-е с синдромом Вискотта-Олдрича
Дебют заболевания при синдроме Луи-Бар приходится на возраст от 2-5-ти лет, а при Вискотта-Олдрича с рождения и до 2-х лет.
Из них 5 детей с диагнозом атаксия – телеангиэктазия (синдром Луи – Бар)
2-е с синдромом Вискотта-Олдрича
Дебют заболевания при синдроме Луи-Бар приходится на возраст от 2-5-ти лет, а при Вискотта-Олдрича с рождения и до 2-х лет.
Слайд 5Первичные иммунодефициты в сочетании с другими крупными дефектами в структуре первичных
иммунодефицитов Ставрополького края.
Слайд 6Этиология синдрома Луи-Бар
Мутация гена ATM, регулирующего репарация
ДНК,
приводящая к хромосомным транслокациям в 7 и 14 хромосомах в локусах Т- клеточного рецептора (TCR) и Ig. В основе неврологических нарушений лежит нейродегенеративный процесс, связанный с нарушением репарации ДНК, повреждением мозжечка и исчезновением клеток Пуркинье.
Слайд 7Патогенез синдрома Луи – Бар:
Ген ATM является регулятором клеточного цикла и
клеточного ответа на окислительный процесс, тем самым, восстанавливая поврежденные участки ДНК, при отсутствии гена ATM не происходит восстановления поврежденного ДНК, что приводит к дисрегуляции клеточного цикла и повреждению хромосом.
Белок ATM представляет собой фермент (протеинкиназу), который обычно реагирует на повреждение ДНК, вызывая накопление белка (p53), который предотвращает деление клеток (белок – супрессор опухолей). Однако у лиц с синдромом Луи-Бар мутация гена ATM вызывают отсутствие или дефект белка ATM и замедленное накопление белка p53. В результате клетки с поврежденным ДНК продолжают реплицировать без соответствующего ремонта, вызывая повышенный риск развития рака.
Белок ATM играет ключевую роль в развитии нервной системы, особенно при дифференцировке стволовых клеток.
Белок ATM представляет собой фермент (протеинкиназу), который обычно реагирует на повреждение ДНК, вызывая накопление белка (p53), который предотвращает деление клеток (белок – супрессор опухолей). Однако у лиц с синдромом Луи-Бар мутация гена ATM вызывают отсутствие или дефект белка ATM и замедленное накопление белка p53. В результате клетки с поврежденным ДНК продолжают реплицировать без соответствующего ремонта, вызывая повышенный риск развития рака.
Белок ATM играет ключевую роль в развитии нервной системы, особенно при дифференцировке стволовых клеток.
Слайд 14Больной N-умер в возрасте 15 л.
26.03.11 г. поступил
в ДККБ г. Ставрополь:
С жалобами: на вялость, сонливость, боль в правом подреберье, желтушность кожных покровов, слизистых, увеличение л/у – подчелюстных, ушных, шейных размерами 1.5- 2.5 см., плотные умеренно болезненные.
Температура 37.2 – 37.5, из носовых ходов отделяемое желтого цвета, общая пастозность.
Реаниматолог: 28.03.11 г.: Состояние тяжелое. Тяжесть обусловлена интоксикационным синдромом, метаболическими нарушениями на фоне основной патологии.
31.03.11 г. переведен в ОРИТ: В 17:00 констатирована смерть.
4 из 5 обследуемых больных на сегодняшний день находятся в тяжелом состоянии, обусловленным основным заболеванием: прогрессирующей неврологической симптоматикой, а также присоединением синопульмональных инфекций.
Прогноз неблагоприятный.
С жалобами: на вялость, сонливость, боль в правом подреберье, желтушность кожных покровов, слизистых, увеличение л/у – подчелюстных, ушных, шейных размерами 1.5- 2.5 см., плотные умеренно болезненные.
Температура 37.2 – 37.5, из носовых ходов отделяемое желтого цвета, общая пастозность.
Реаниматолог: 28.03.11 г.: Состояние тяжелое. Тяжесть обусловлена интоксикационным синдромом, метаболическими нарушениями на фоне основной патологии.
31.03.11 г. переведен в ОРИТ: В 17:00 констатирована смерть.
4 из 5 обследуемых больных на сегодняшний день находятся в тяжелом состоянии, обусловленным основным заболеванием: прогрессирующей неврологической симптоматикой, а также присоединением синопульмональных инфекций.
Прогноз неблагоприятный.
Слайд 15Этиология синдрома Вискотта-Олдрича
Мутация гена WASP, кодирующего синтез белка цитоскелета
лимфоцитов и тромбоцитов, что приводит к дефекту межклеточных взаимодействий и активации клеток. Нарушен синтез АТ на полисахаридные антигены. Тромбоцитопения связана с уменьшенным размером тромбоцитов и их повышенным разрушением.
Слайд 16Патогенез синдрома Вискотта-Олдрича
Точная функция гена WASp не полностью выяснена, но, по-видимому,
он служит мостиком между передачей сигналов активных феломентов в цитоскелете.
Слайд 24Больной N-6 л.
17.04.2015 г. поступил в отделение ТГСК №2 для проведения
аллогенной трансплантации костного мозга от родственного полностью совместимого донора (брата).
27.04.15 проведена миелотрансфузия.
В настоящее время состояние удовлетворительное: готовится к проведению прививок согласно календарю прививок.
27.04.15 проведена миелотрансфузия.
В настоящее время состояние удовлетворительное: готовится к проведению прививок согласно календарю прививок.