- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение твердого вещества презентация
Содержание
- 1. Строение твердого вещества
- 2. ПЛАН Свойства твердого состояния вещества. Строение кристаллов.
- 3. Твердое тело сохраняет и свою форму и
- 4. кристаллические вещества состоят из огромного количества очень
- 5. Система атомов или ионов, определенным образом расположенных
- 6. Огромное разнообразие кристаллических решеток подразделено на 7 больших систем, называемых СИНГОНИЯМИ (по геометрической форме кристаллов)
- 7. кристаллы классифицируются на типы по виду связи
- 8. ионные кристаллы - ионная связь между ионами
- 9. Ковалентные кристаллы (атомные решетки): атомы связаны в
- 10. Металлические кристаллы – кристаллы, в которых атомы
- 11. Взаимосвязь между положением металлов в ПСЭ и их кристаллическим строением
- 12. Одно и то же вещество, кристаллизуясь в
- 13. 2 типа плотноупа-кованных структур: кубическая и гекса-гональная.
- 14. Идеальный кристалл может существовать только при температуре
- 15. виды дефектов: точечные - охватывают один-два структурных
- 16. Дислокация – смещение рядов атомов друг
- 17. аморфный в переводе с гре-ческого языка означает
- 18. Аморфные вещества можно рассматривать как переохлажденные жидкости
Слайд 2ПЛАН
Свойства твердого состояния вещества.
Строение кристаллов.
Типы кристаллических решеток.
Упаковка атомов в кристаллах.
Аморфное состояние
Слайд 3Твердое тело сохраняет и свою форму и свой объем, т.к.
молекулы или
Слайд 4кристаллические вещества состоят из огромного количества очень маленьких кристалликов, имеющих абсолютно
кристаллические вещества характеризуются повторяющимся в пространстве расположением атомов или ионов, образующих правильные геометрические тела (куб, параллелепипед, призма и др.)
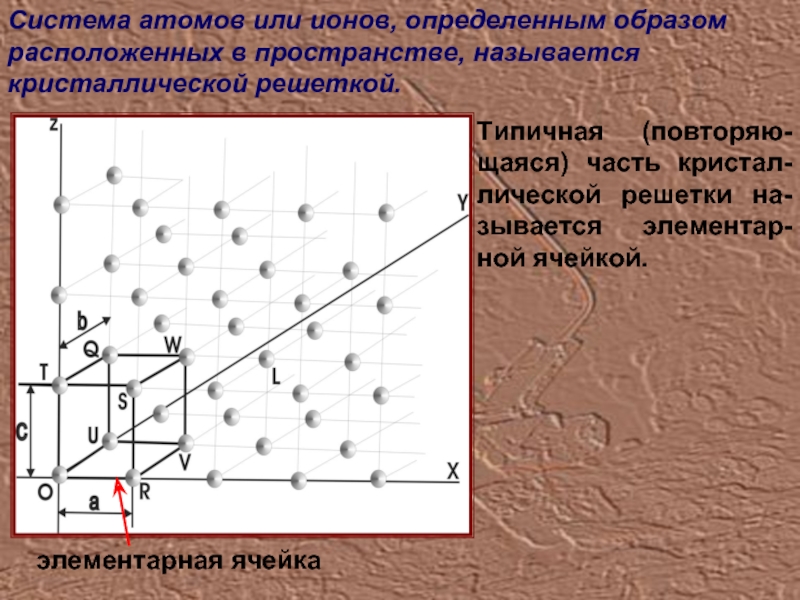
Слайд 5Система атомов или ионов, определенным образом расположенных в пространстве, называется кристаллической
Типичная (повторяю-щаяся) часть кристал-лической решетки на-зывается элементар-ной ячейкой.
элементарная ячейка
Слайд 6Огромное разнообразие кристаллических решеток подразделено на 7 больших систем, называемых СИНГОНИЯМИ
Слайд 7кристаллы классифицируются на типы по виду связи между частицами, составляющими кристалл
Самые слабые силы взаимодействия между молеку-лами в молекулярных кристаллах, к числу которых относятся, например, кристаллы СО2, серы, бензола, йода, нафталина
низкая t0 плавления, электропроводность; мягкость и хрупкость, летучи и пахучи, т.к. молекулы легко испаряются с поверхности кристаллов
кристалл льда
Слайд 8ионные кристаллы - ионная связь между ионами (за счет электростатического взаимодействия
высокие температуры плавления и кипения, чрезвычайно низкое давление паров; растворяются только в наиболее полярных растворителях; диэлектрики,
потому что образующие
их ионы не могут сво-
бодно покидать свои
положения в узлах
решетки
СИЛЫ ВЗАИМОДЕЙСТВИЯ ВЕЛИКИ
NaCl
CsCl
Слайд 9Ковалентные кристаллы (атомные решетки): атомы связаны в кристалле ковалентной связью неполярной
мощные ковалентные связи так близко стягивают соседние атомы, что их электронные облака частично перекрываются. Расстояние между центрами атомов С в алмазе намного меньше, чем известный диаметр атома углерода. Поэтому высокая прочность и химическая инертность алмаза. Он практически не реагирует ни с кислотами, ни со щелочами, и лишь в атмосфере О2 и F2 окисляется до CO2 и CF4. Аналогичной кристаллической структурой обладают и другие представители главной подгруппы IV группы периодической системы: Si, Ge, серое Sn.
Прочные кристаллы образуются лишь в том случае, если число ковалентных связей достаточно для образования пространственных решеток.
алмаз
графит
Слайд 10Металлические кристаллы – кристаллы, в которых атомы металлов образуют плотно упакованные
координационные числа 8-12
Al, Cu, Au, Ag, Fe
Mg, Coα, Zn, Tiα, Cd
Mo, W, V, Fe
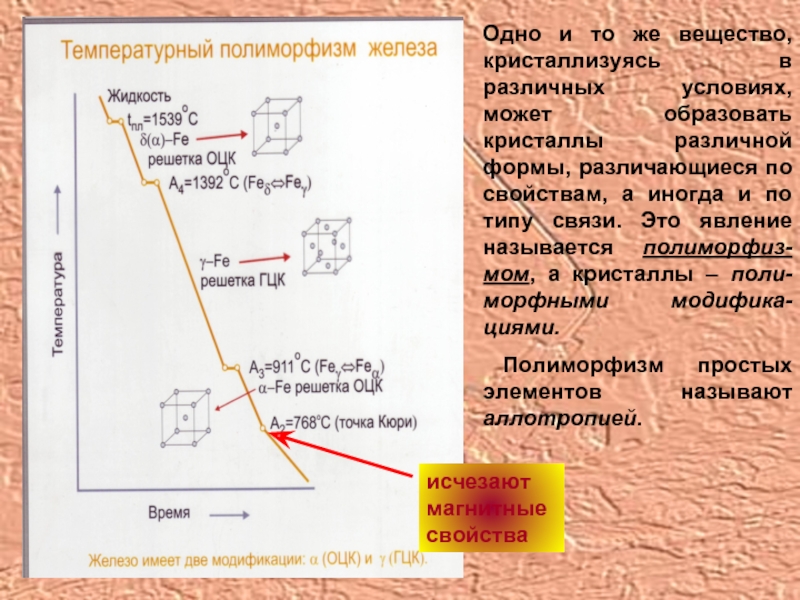
Слайд 12Одно и то же вещество, кристаллизуясь в различных условиях, может образовать
Полиморфизм простых элементов называют аллотропией.
исчезают магнитные свойства
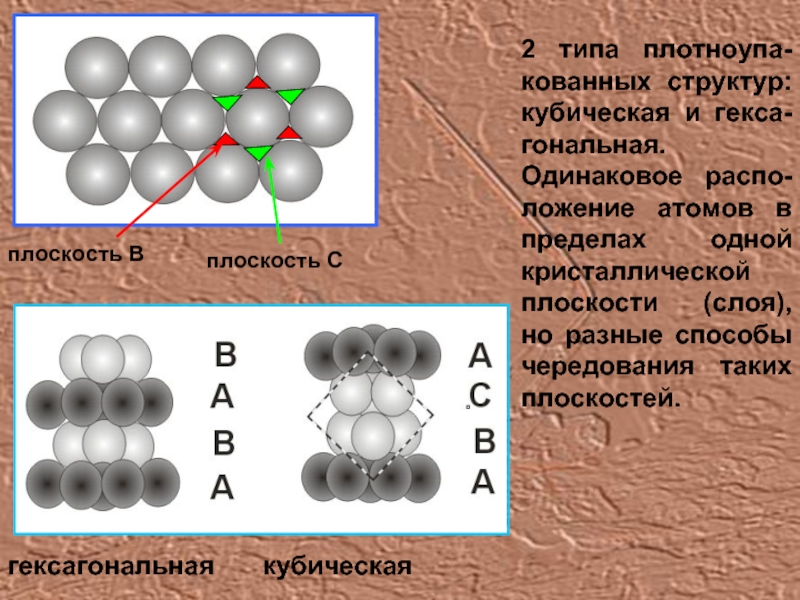
Слайд 132 типа плотноупа-кованных структур: кубическая и гекса-гональная. Одинаковое распо-ложение атомов в
плоскость В
плоскость С
гексагональная
кубическая
Слайд 14Идеальный кристалл может существовать только при температуре абсолютного нуля. При любых
накопление дефектов до определенной концентрации приводит к уменьшению свободной энергии системы
Хотя образование этих дефектов и требует затрат энергии (энтальпия си-стемы возрастает), но оно сопровождается значительным увеличением энтропии системы
изменение энергии при образовании дефектов
Слайд 15виды дефектов: точечные - охватывают один-два структурных узла или междоузлия в
точечные:
1) незанятые узлы решетки – вакан-сии (дефекты Шоттки),
2) атомы, молекулы или ионы, располо-женные не на своих позициях или в междоузлиях (дефекты Френкеля),
3) посторонние атомы – примеси как в узлах, так и в междоузлиях.
вакансии по Шоттки дефекты Френкеля
Окраска драгоценных камней – рубина, изумруда и др. – вызвана примесными ионами (хрома, железа).
ИСКАЖЕНИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ
Слайд 16 Дислокация – смещение рядов атомов друг относительно друга, простирающееся вдоль
обрыв плоскости атомов
взаимный сдвиг плоскостей
краевая дислокация
винтовая дислокация
Слайд 17аморфный в переводе с гре-ческого языка означает «бесформенный».
2 вида твердого
различные физические и меха-нические свойства
аморфные вещества
кристаллические вещества
Слайд 18Аморфные вещества можно рассматривать как переохлажденные жидкости с сильно пониженной подвижностью
Сера кристаллическая S8 и аморфная
Аморфные металлы обладают рядом физических отличий от обычных кристаллических по механическим свойствам, особенно по прочности. В аморфных структурах нет типичных для кристаллов дефектов и внутренних напряжений, способных снизить прочность материала.