Поверхностные свойства малых частиц
Повышенная летучесть и растворимость наноразмерных кристаллов.
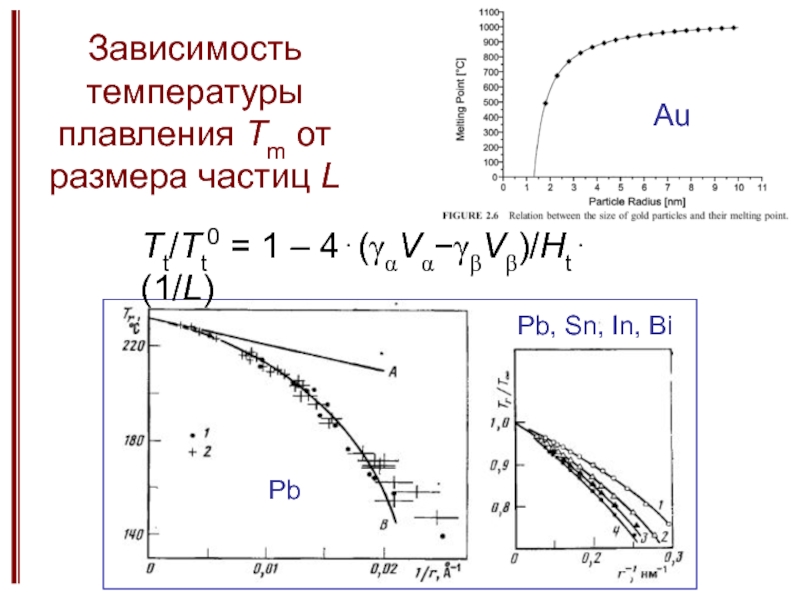
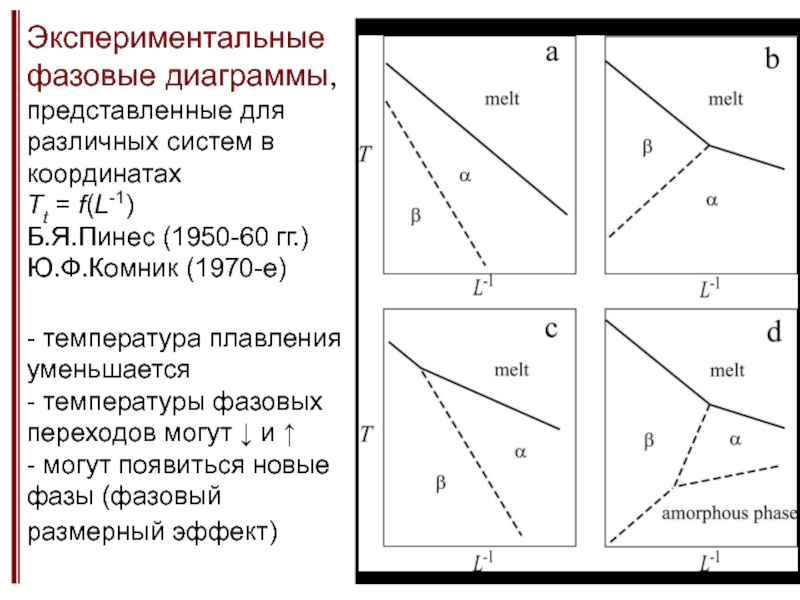
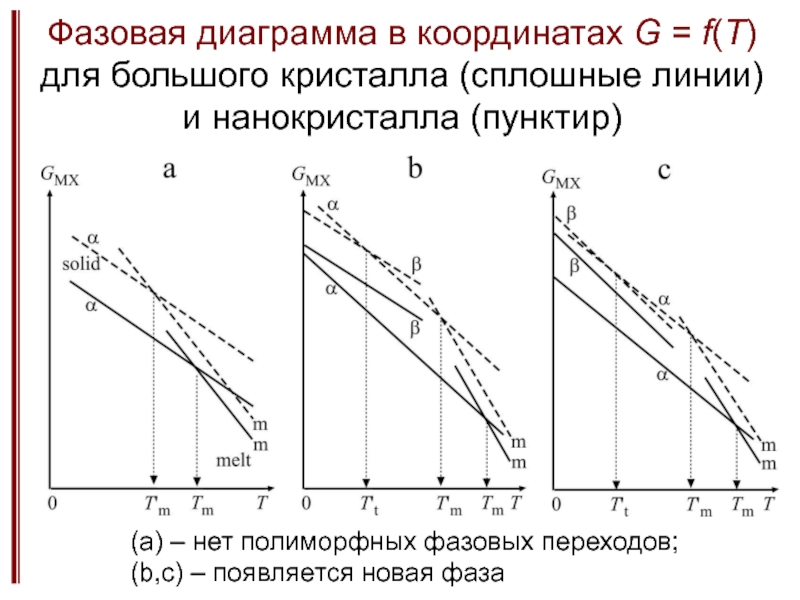
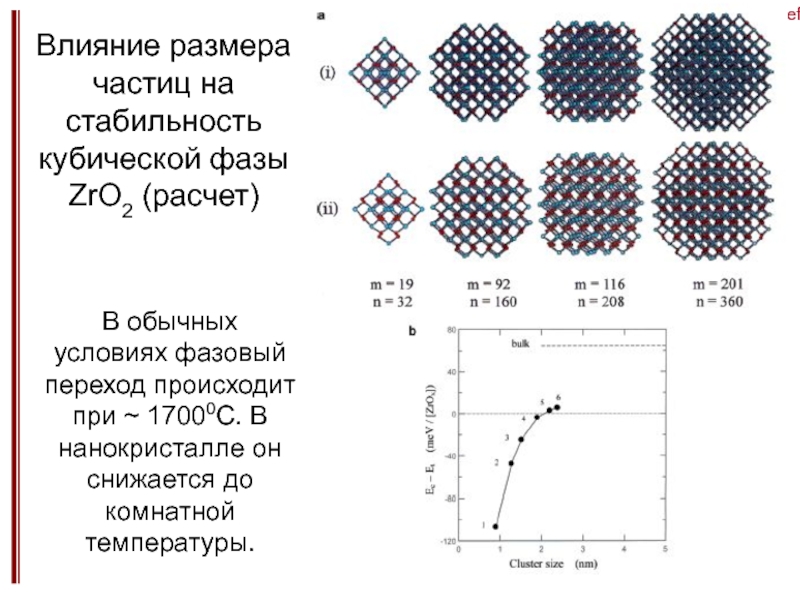
Зависимости температур плавления и фазовых переходов от размера частиц.
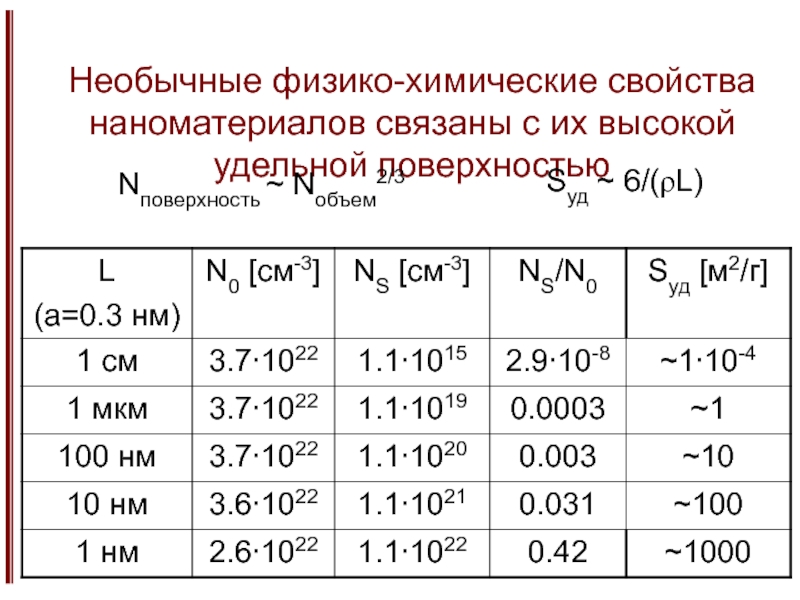
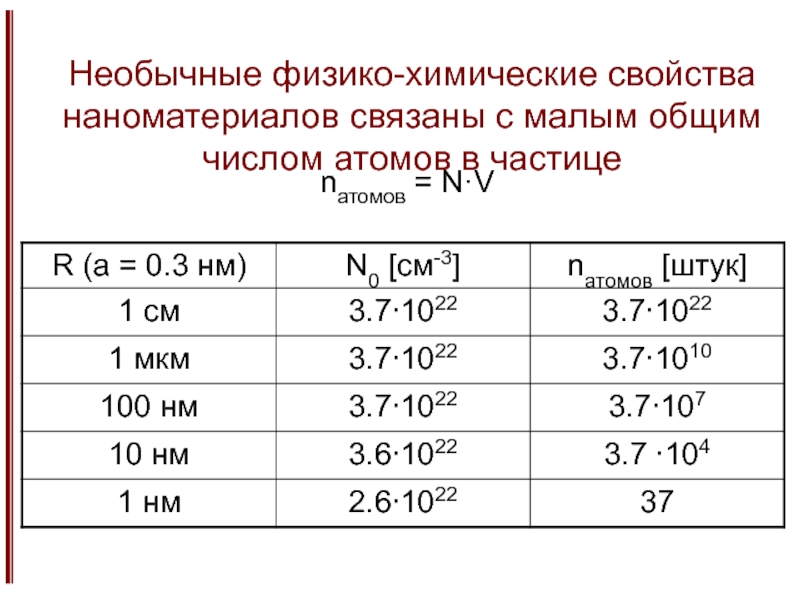
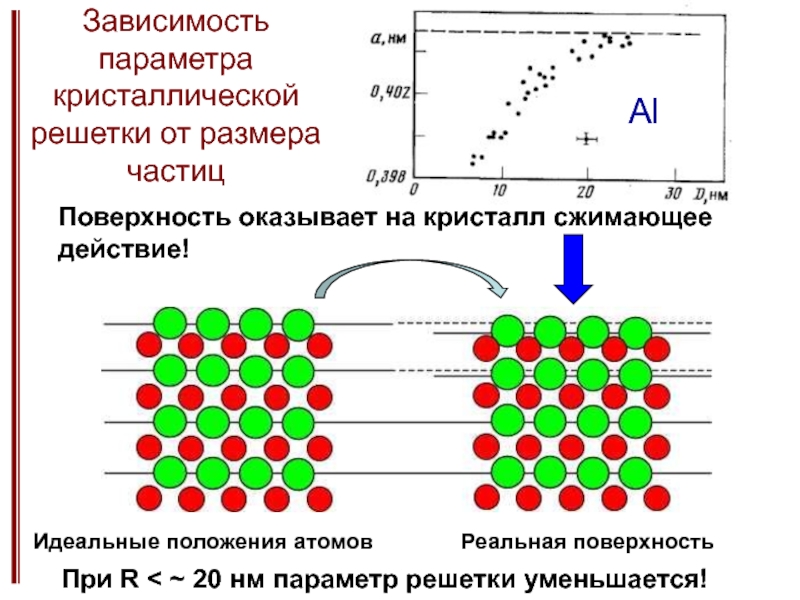
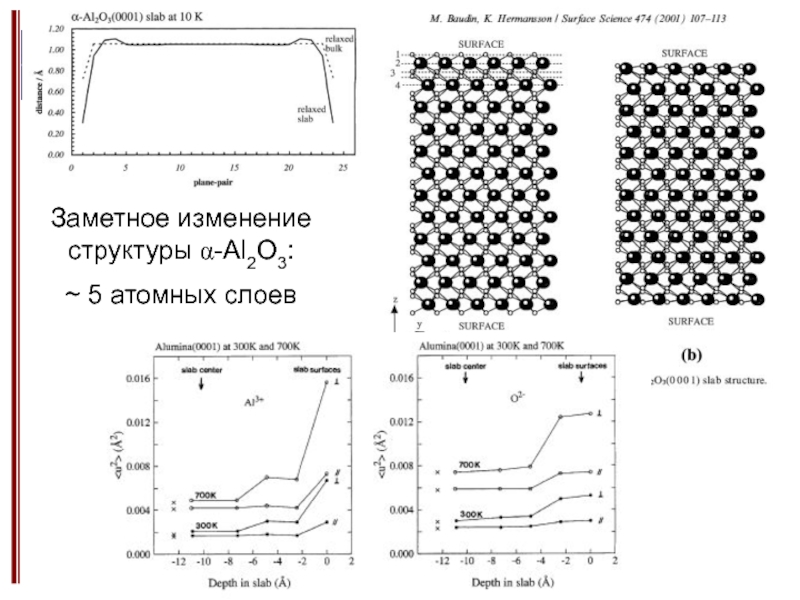
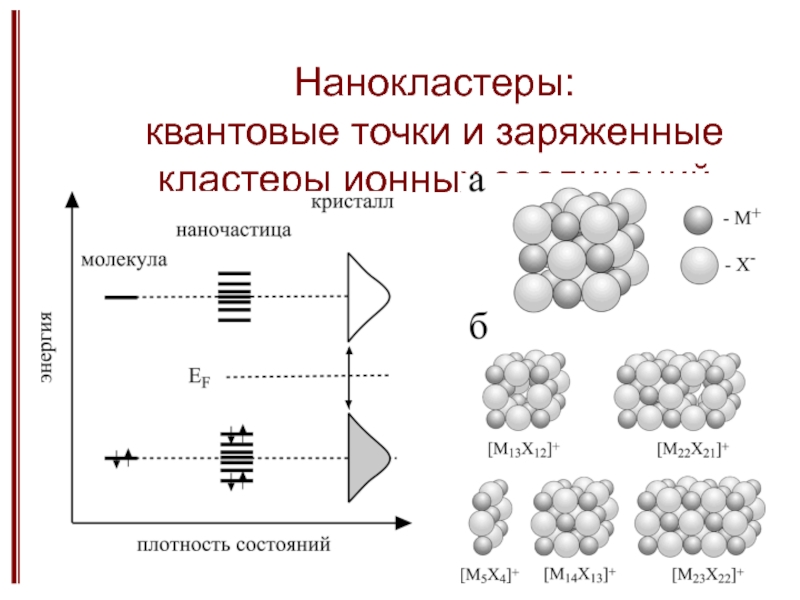
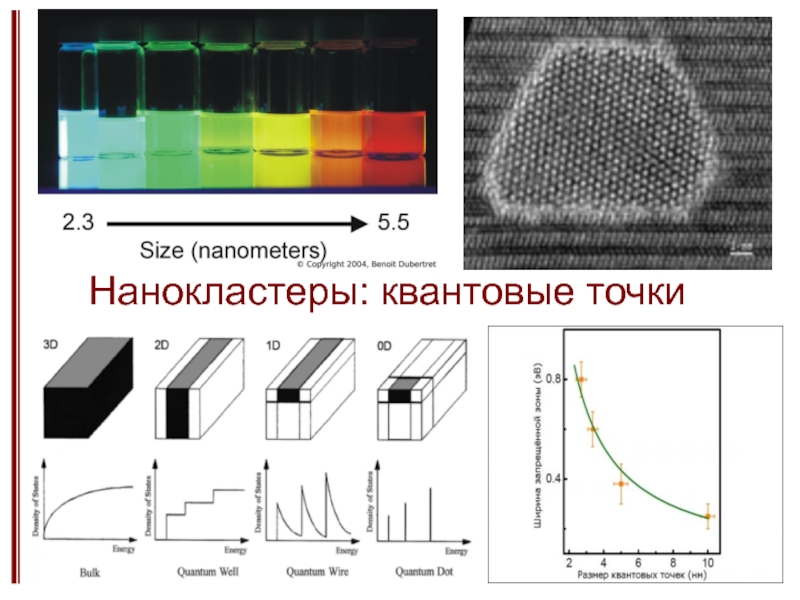
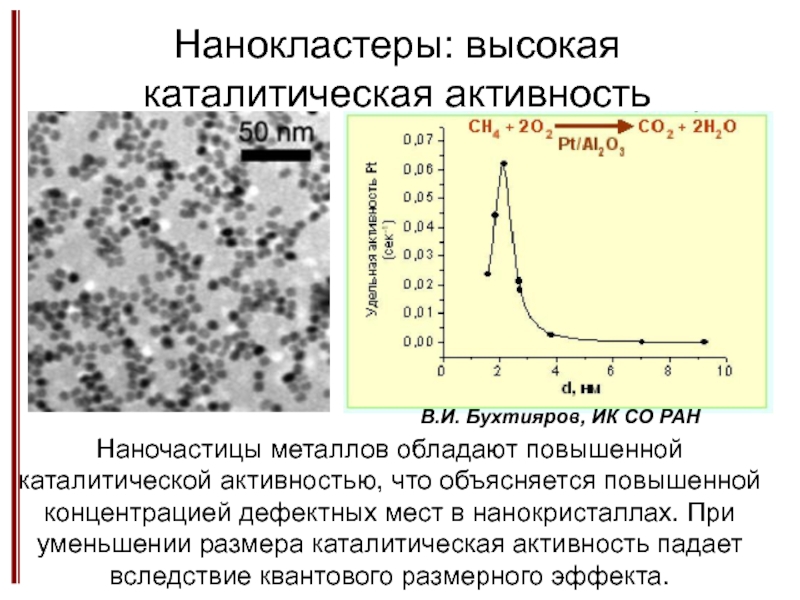
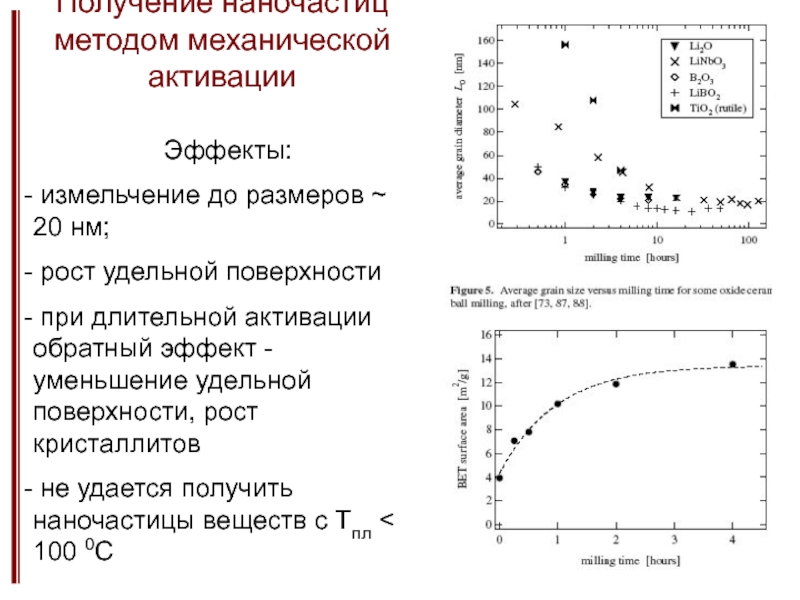
Изменение физико-химических свойств при уменьшенее размера частиц.
Слабые и сильные размерные эффекты.
НАНОКОМПОЗИТНЫЕ МАТЕРИАЛЫ ДЛЯ ЭЛЕКТРОХИМИЧЕСКОЙ ЭНЕРГЕТИКИ