- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Халькогены. Электронное строение кислорода и серы презентация
Содержание
- 1. Халькогены. Электронное строение кислорода и серы
- 2. Электронное строение кислорода и серы Все халькогены
- 3. Озон – аллотропная модификация кислорода. Получение и
- 4. Молекулярный кислород – еще одна аллотропная модификация
- 10. Химические свойства сероводорода Получение из сульфидов Свойства электролита Свойства восстановителя полное сгорание неполное сгорание
- 11. Качественные реакции на сульфид-ион: Большинство сульфидов нерастворимо
- 12. Сера +4: сернистый ангидрид , сернистая кислота, сульфиты.
- 20. Задания 37
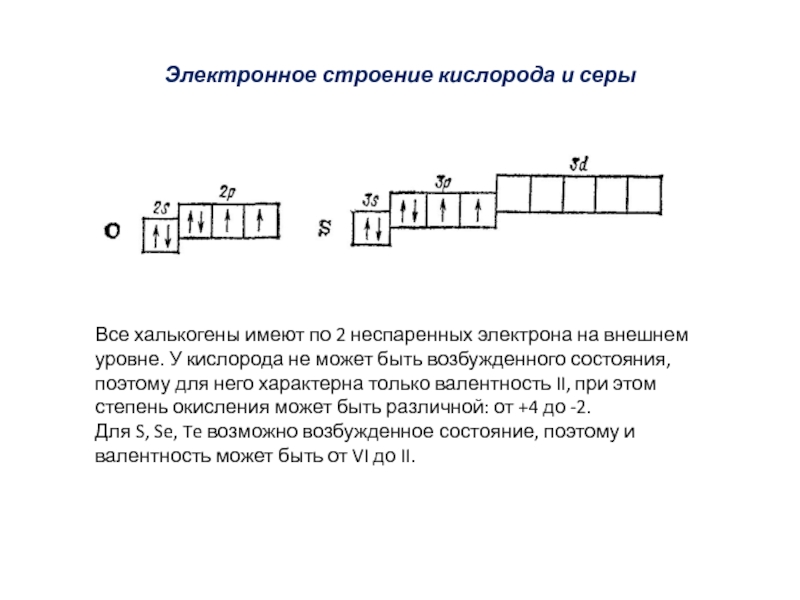
Слайд 2Электронное строение кислорода и серы
Все халькогены имеют по 2 неспаренных электрона
на внешнем уровне. У кислорода не может быть возбужденного состояния, поэтому для него характерна только валентность II, при этом степень окисления может быть различной: от +4 до -2.
Для S, Se, Te возможно возбужденное состояние, поэтому и валентность может быть от VI до II.
Для S, Se, Te возможно возбужденное состояние, поэтому и валентность может быть от VI до II.
Слайд 3Озон – аллотропная модификация кислорода.
Получение и химические свойства озона
Озон имеет
один атом кислорода в степени окисления +4, за счет чего проявляет окислительные свойства.
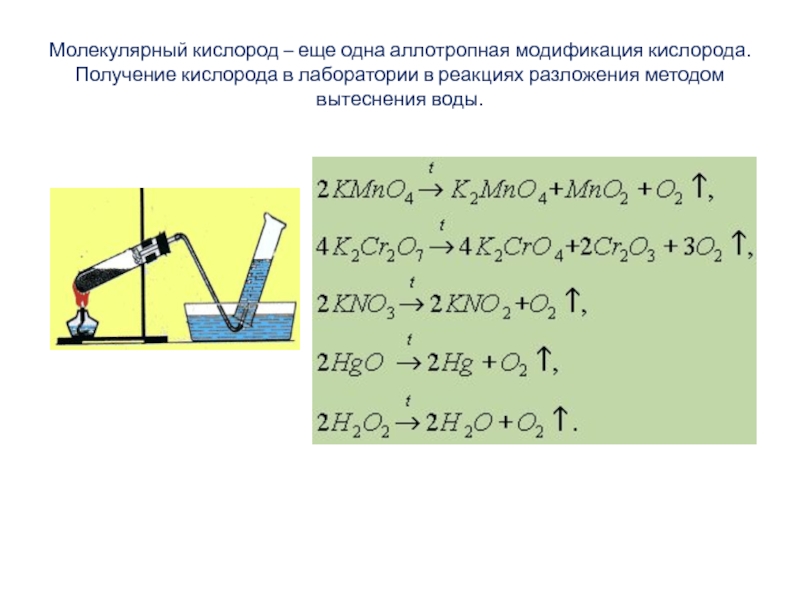
Слайд 4Молекулярный кислород – еще одна аллотропная модификация кислорода. Получение кислорода в лаборатории
в реакциях разложения методом вытеснения воды.
Слайд 10Химические свойства сероводорода
Получение из сульфидов
Свойства электролита
Свойства восстановителя
полное сгорание
неполное сгорание
Слайд 11Качественные реакции на сульфид-ион:
Большинство сульфидов нерастворимо и окрашены в черный цвет,
за исключением сульфида ртути (II). Сульфиды меди, ртути, свинца и серебря не растворяются в растворах сильных кислот.
Потемнение серебра на воздухе