- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Органическая химия – химия соединений углерода презентация
Содержание
- 1. Органическая химия – химия соединений углерода
- 2. Органическая химия – химия соединений углерода Кроме
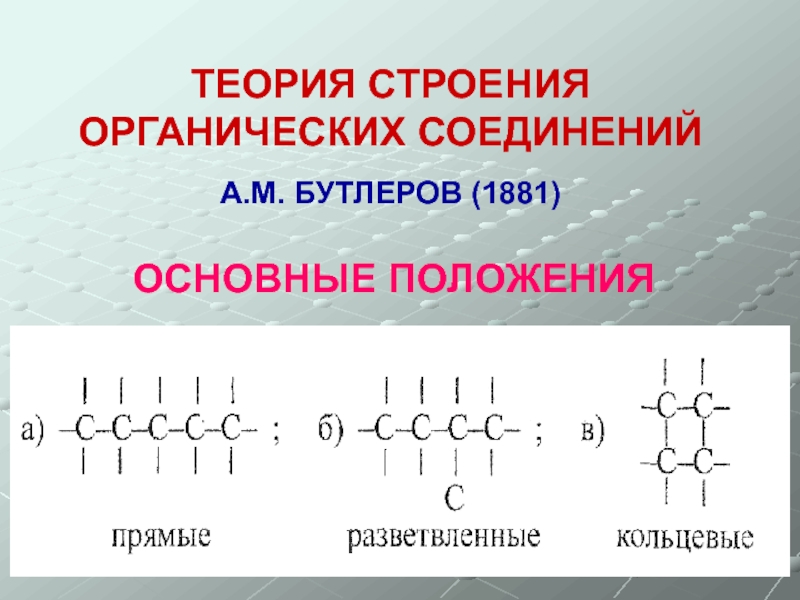
- 3. ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А.М. БУТЛЕРОВ (1881)
- 4. ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А.М. БУТЛЕРОВ (1881)
- 5. ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А.М. БУТЛЕРОВ (1881)
- 6. ИЗОМЕРЫ – вещества, имеющие одинаковый состав, но
- 7. ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А.М. БУТЛЕРОВ (1881)
- 8. Органические соединения Ациклические Циклические Предельные Непредельные Ароматические Алициклические Карбоциклические Гетероциклические
- 9. Органические соединения Ациклические Циклические Предельные Непредельные Ароматические Алициклические Карбоциклические Гетероциклические
- 10. Предельные углеводороды (алканы, насыщенные углеводороды, парафины) Общая формула СnH2n+2
- 11. Предельные углеводороды Физические свойства: До 4
- 12. Предельные углеводороды Химические свойства: 1. Реакции замещения А) галогенирование Б) нитрование
- 13. Предельные углеводороды Химические свойства: 2. Реакции окисления А) горение Б) окисление
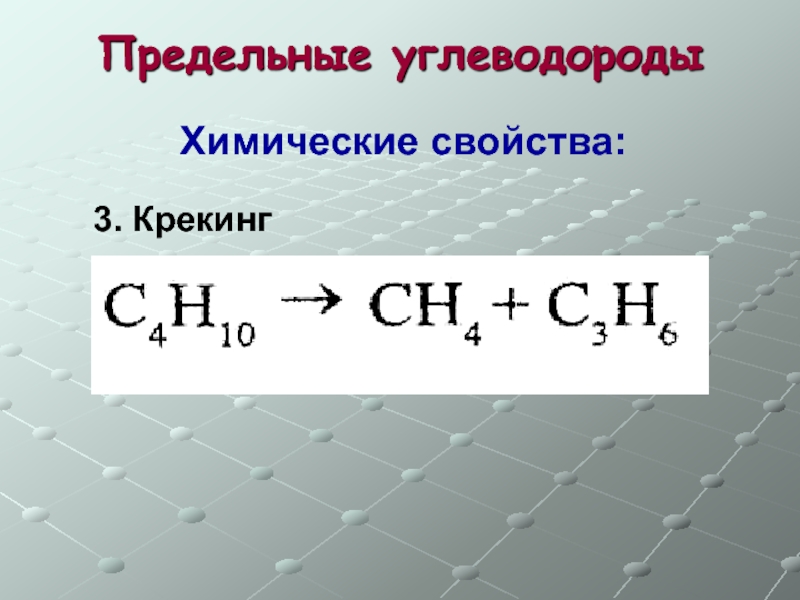
- 14. Предельные углеводороды Химические свойства: 3. Крекинг
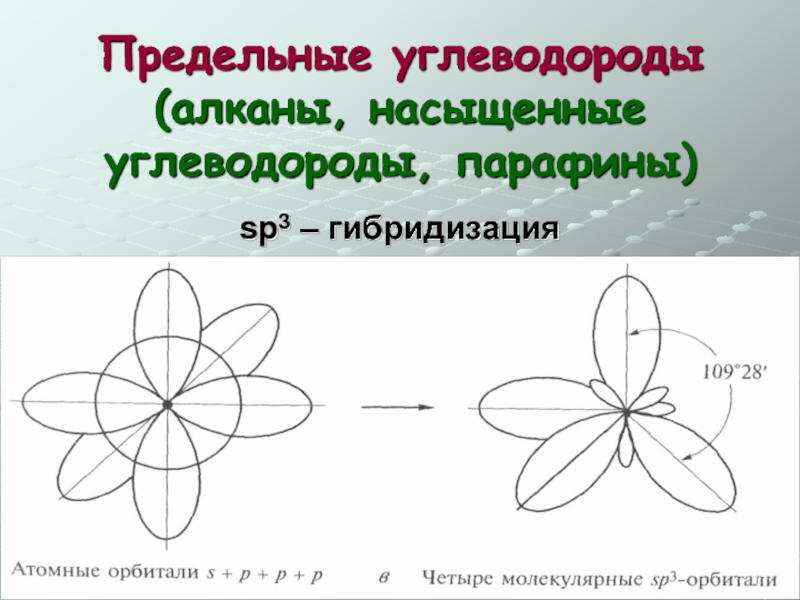
- 15. Предельные углеводороды (алканы, насыщенные углеводороды, парафины) sp3 – гибридизация
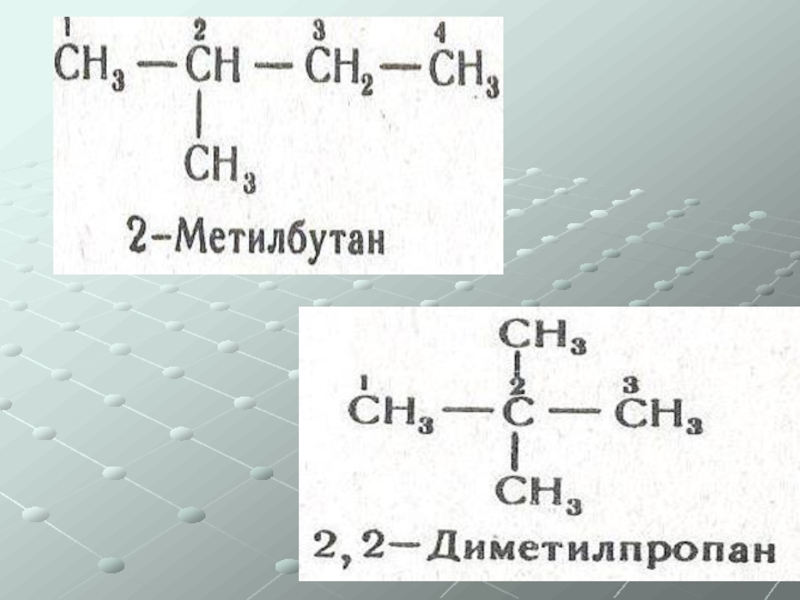
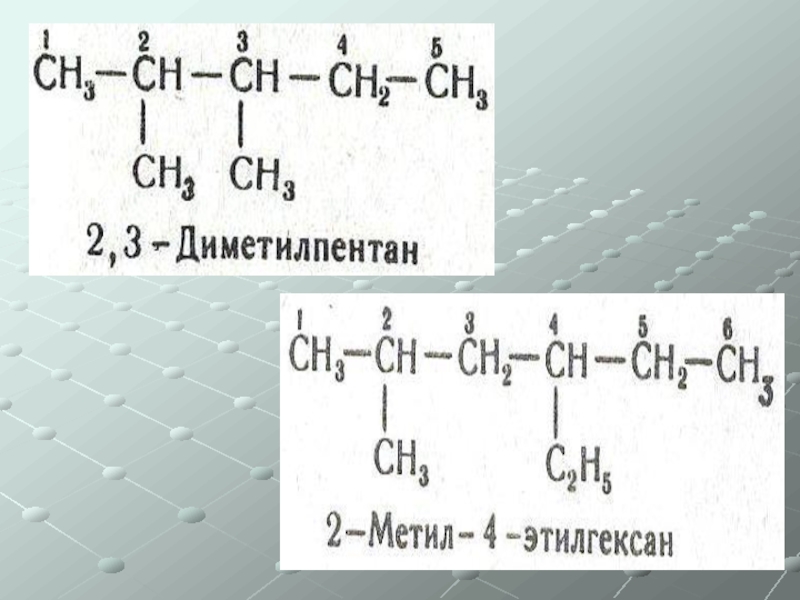
- 16. Предельные углеводороды Характерна изомерия углеродного скелета
- 17. Номенклатура 1. Выбирается самая длинная цепь. 2.
- 20. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n
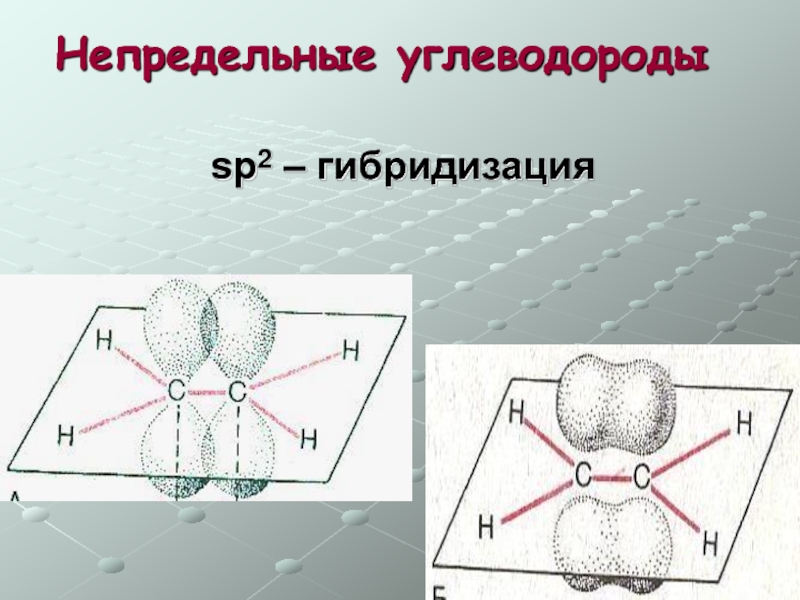
- 21. Непредельные углеводороды sp2 – гибридизация
- 22. Непредельные углеводороды Химические свойства: 1. Реакции присоединения А) гидрирование Б) галогенирование
- 23. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n
- 24. ПРАВИЛО МАРКОВНИКОВА Атом водорода присоединяется к наиболее
- 25. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n
- 26. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n
- 27. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n
- 28. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n
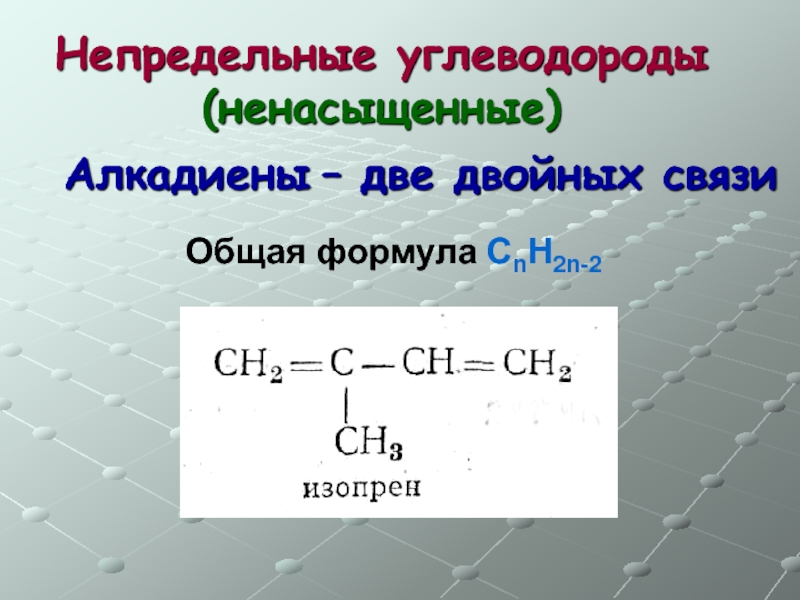
- 32. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n-2 Алкадиены – две двойных связи
- 33. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n-2
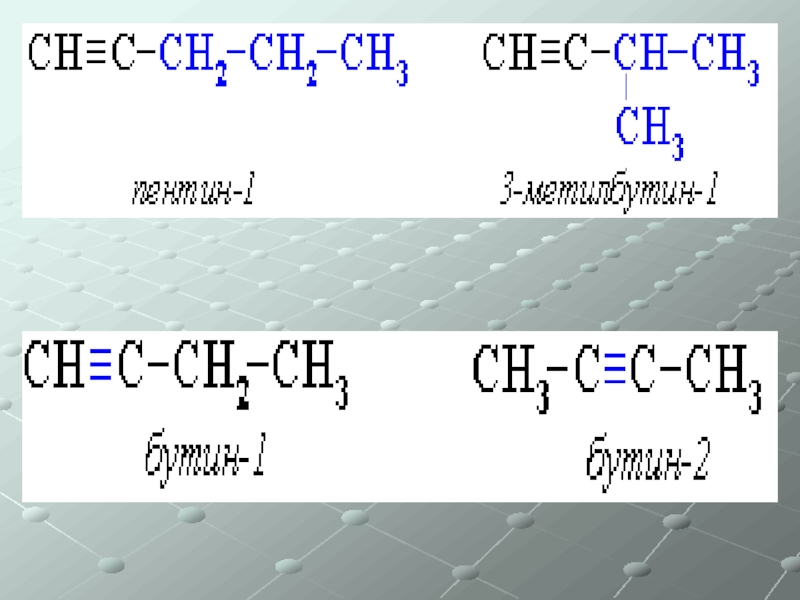
- 35. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n-2 Алкины – одна тройная связь
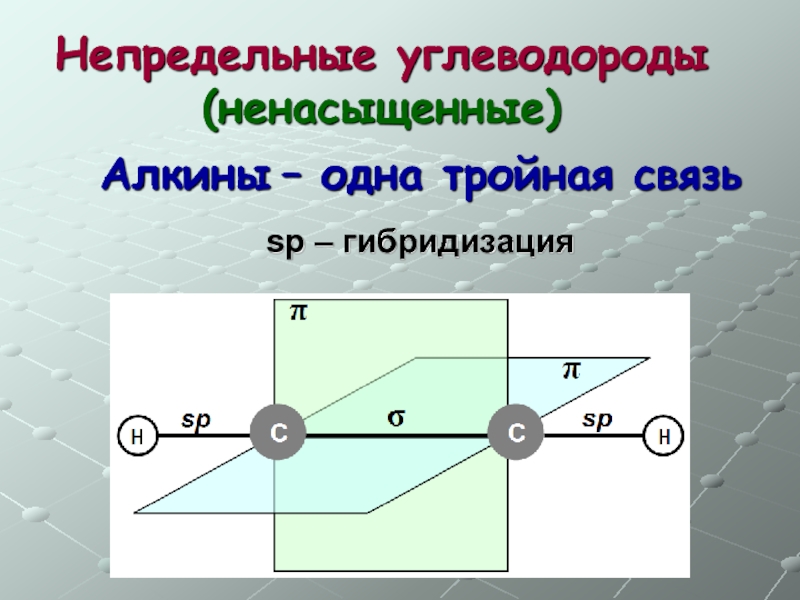
- 36. Непредельные углеводороды (ненасыщенные) Алкины – одна тройная связь sp – гибридизация
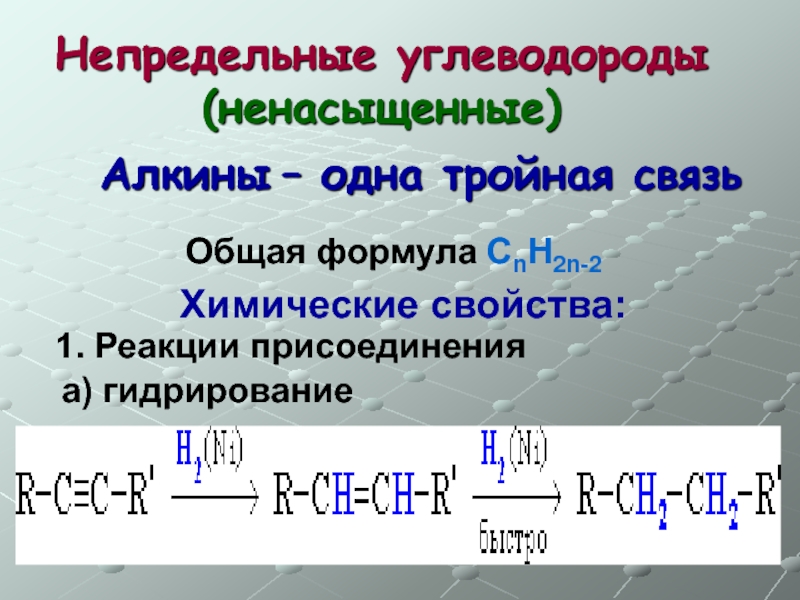
- 37. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n-2
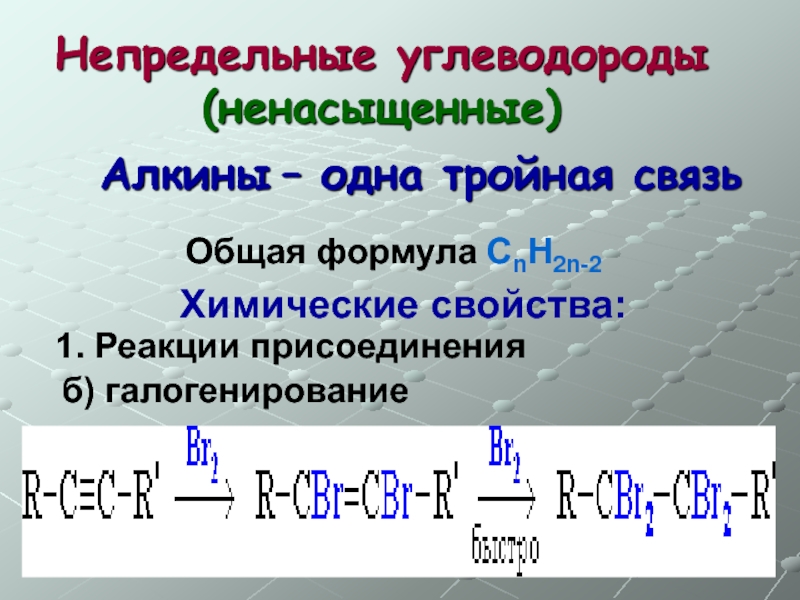
- 38. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n-2
- 39. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n-2
- 40. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n-2
- 41. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n-2
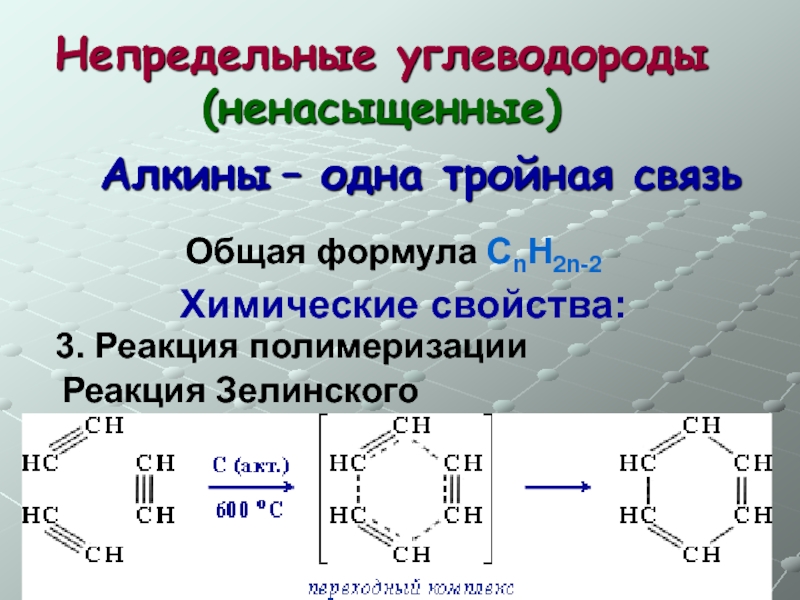
- 42. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n-2
- 43. Непредельные углеводороды (ненасыщенные) Общая формула СnH2n-2
Слайд 2Органическая химия – химия соединений углерода
Кроме углерода и водорода в составе
Слайд 3ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
А.М. БУТЛЕРОВ (1881)
ОСНОВНЫЕ ПОЛОЖЕНИЯ
1. Углерод в органических соединениях
Слайд 4ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
А.М. БУТЛЕРОВ (1881)
ОСНОВНЫЕ ПОЛОЖЕНИЯ
2. Атомы углерода соединяются между
Слайд 5ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
А.М. БУТЛЕРОВ (1881)
ОСНОВНЫЕ ПОЛОЖЕНИЯ
3. Свойства веществ зависят не
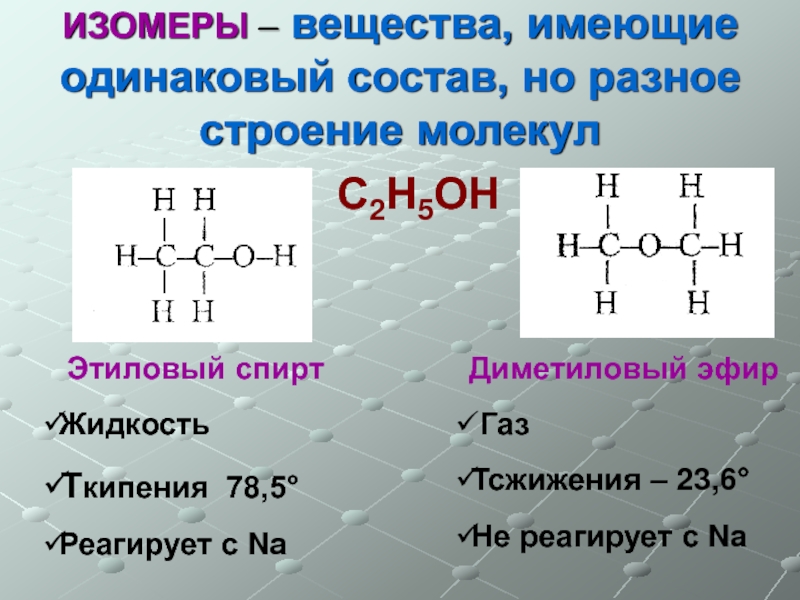
Слайд 6ИЗОМЕРЫ – вещества, имеющие одинаковый состав, но разное строение молекул
С2Н5ОН
Этиловый спирт
Жидкость
Ткипения 78,5°
Реагирует с Na
Диметиловый эфир
Газ
Тсжижения – 23,6°
Не реагирует с Na
Слайд 7ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
А.М. БУТЛЕРОВ (1881)
ОСНОВНЫЕ ПОЛОЖЕНИЯ
4. Атомы в молекуле взаимно
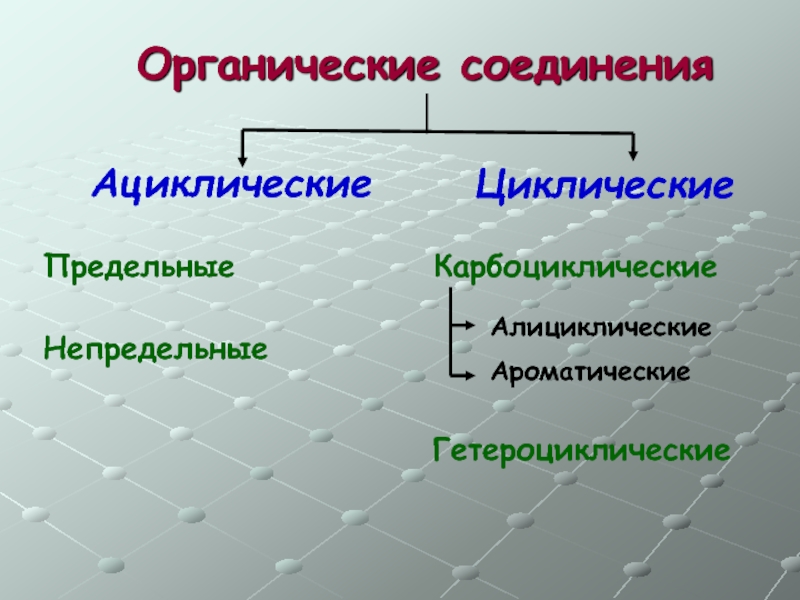
Слайд 8 Органические соединения
Ациклические
Циклические
Предельные
Непредельные
Ароматические
Алициклические
Карбоциклические
Гетероциклические
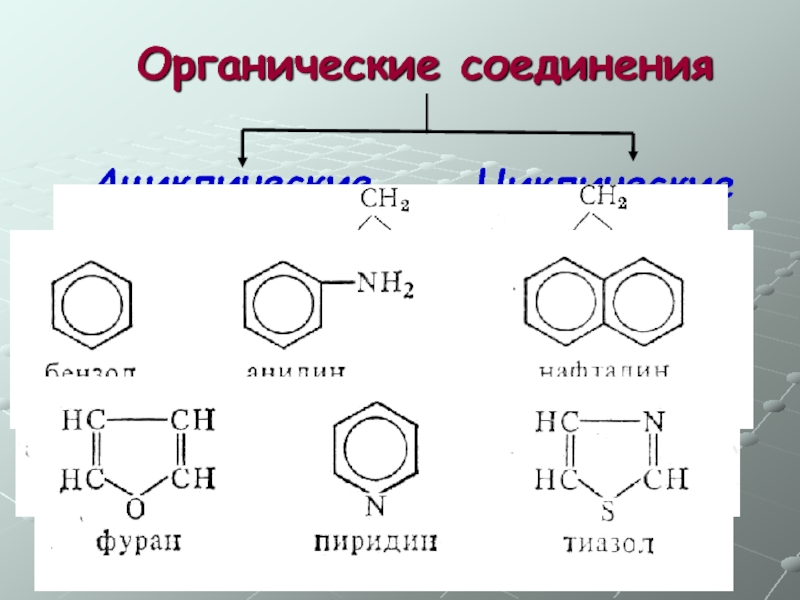
Слайд 9 Органические соединения
Ациклические
Циклические
Предельные
Непредельные
Ароматические
Алициклические
Карбоциклические
Гетероциклические
Слайд 11Предельные углеводороды
Физические свойства:
До 4 С – газы, от 5 до
Слайд 12Предельные углеводороды
Химические свойства:
1. Реакции замещения
А) галогенирование
Б) нитрование
Слайд 17Номенклатура
1. Выбирается самая длинная цепь.
2. Нумеруются атомы в главной цепи, начиная
3. Цифрами указывается месторасположение радикалов.
4. Называются радикалы по старшинству (например, сначала метил, а потом этил).
5. Называется основная углеродная цепь.
Слайд 20Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n
Физические свойства:
До 4 С –
Алкены – одна двойная связь
Слайд 22Непредельные углеводороды
Химические свойства:
1. Реакции присоединения
А) гидрирование
Б) галогенирование
Слайд 23Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n
Алкены – одна двойная связь
Химические свойства:
1. Реакции присоединения
В) гидрогалогенирование
Слайд 24ПРАВИЛО МАРКОВНИКОВА
Атом водорода присоединяется к наиболее гидрированному атому углерода при двойной
Слайд 25Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n
Алкены – одна двойная связь
Химические свойства:
1. Реакции присоединения
Г) гидратация
Слайд 26Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n
Алкены – одна двойная связь
Химические свойства:
2. Реакции полимеризации
Слайд 27Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n
Алкены – одна двойная связь
Химические свойства:
3. Реакции окисления
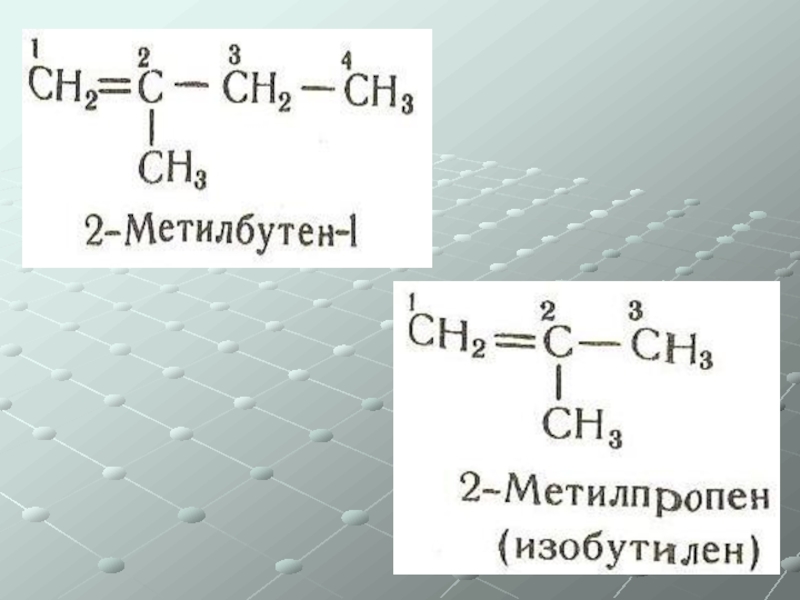
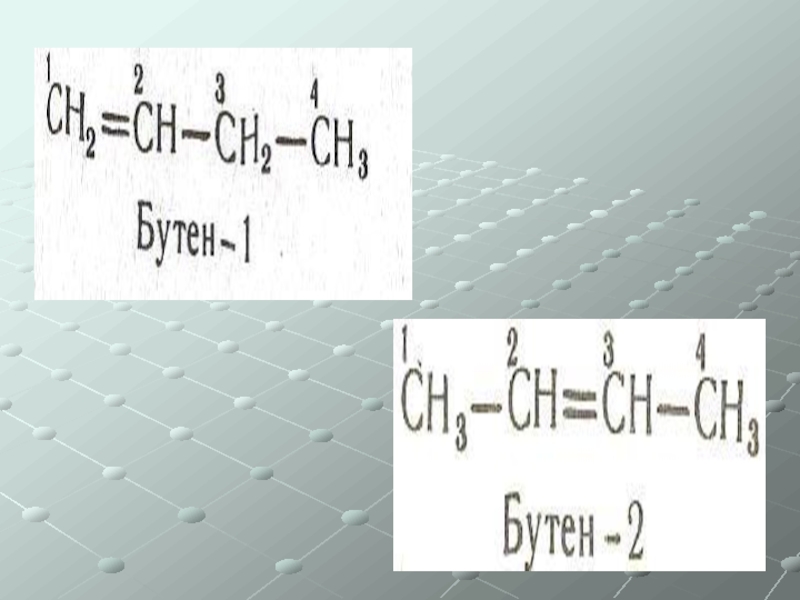
Слайд 28Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n
Алкены – одна двойная связь
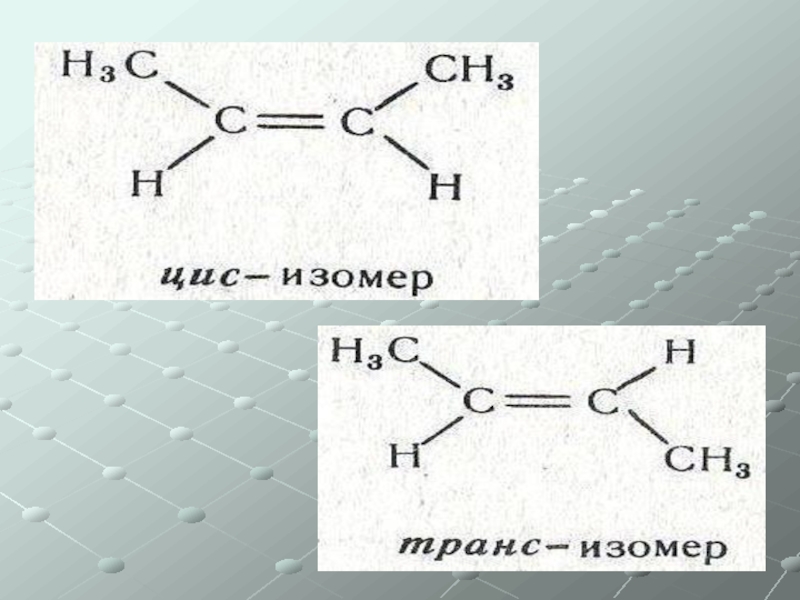
Изомерия:
Углеродного скелета
Положения
Геометрическая
Слайд 33Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n-2
Алкадиены – две двойных связи
Изомерия:
Углеродного скелета
Положения
Слайд 37Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n-2
Алкины – одна тройная связь
Химические свойства:
1. Реакции присоединения
а) гидрирование
Слайд 38Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n-2
Алкины – одна тройная связь
Химические свойства:
1. Реакции присоединения
б) галогенирование
Слайд 39Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n-2
Алкины – одна тройная связь
Химические свойства:
1. Реакции присоединения
в) гидрогалогенирование
Слайд 40Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n-2
Алкины – одна тройная связь
Химические свойства:
1. Реакции присоединения
г) гидратация (реакция Кучерова)
Слайд 41Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n-2
Алкины – одна тройная связь
Химические свойства:
2. Реакция замещения
Реакция «серебряного зеркала» с реактивом Толленса
Слайд 42Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n-2
Алкины – одна тройная связь
Химические свойства:
3. Реакция полимеризации
Реакция Зелинского
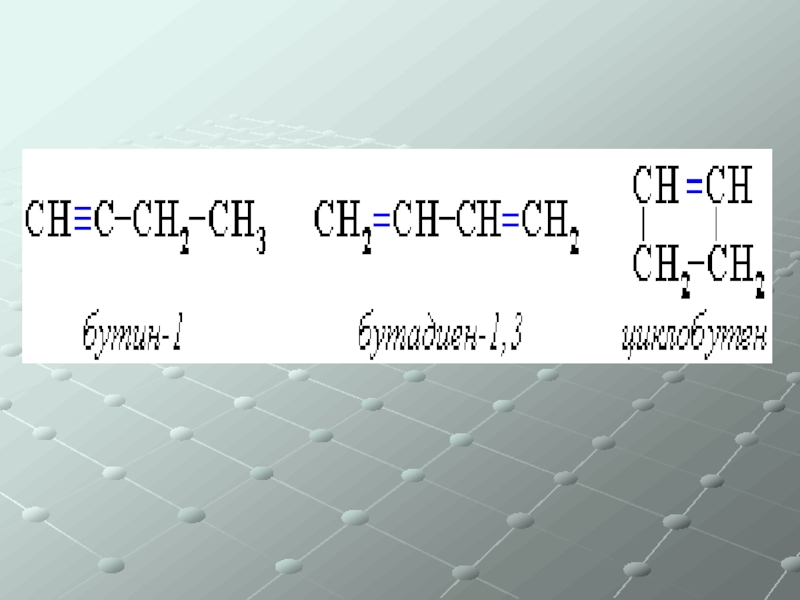
Слайд 43Непредельные углеводороды (ненасыщенные)
Общая формула СnH2n-2
Алкины – одна тройная связь
Изомерия:
Углеродного скелета
Положения
Межклассовая (с алкадиенами и циклоалкенами)