- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Одноатомные спирты презентация
Содержание
- 1. Одноатомные спирты
- 2. Спирты (алканолы) - органические вещества, в молекулах
- 3. и многоатомные спирты - органические соединения, содержащие
- 4. Одноатомные спирты получаются, если в молекулах предельных
- 5. Из метана получаем метанол:
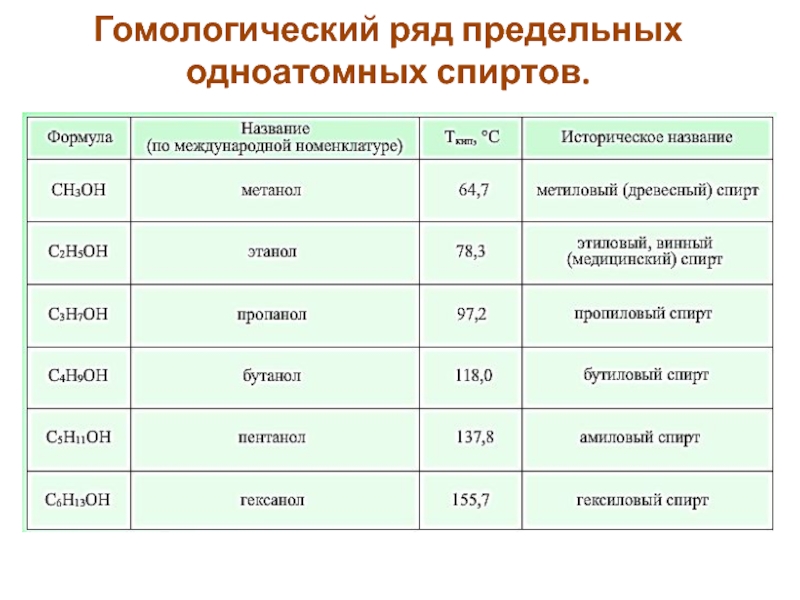
- 6. Гомологический ряд предельных одноатомных спиртов.
- 7. В любом гомологическом ряду существует закономерность.
- 8. Оказывается, атом кислорода в молекулах спиртов, за
- 9. Спирты растворяются в воде. Однако с увеличением
- 10. При растворении спиртов в воде выделяется большое
- 11. Изомерия предельных одноатомных спиртов. От того, к
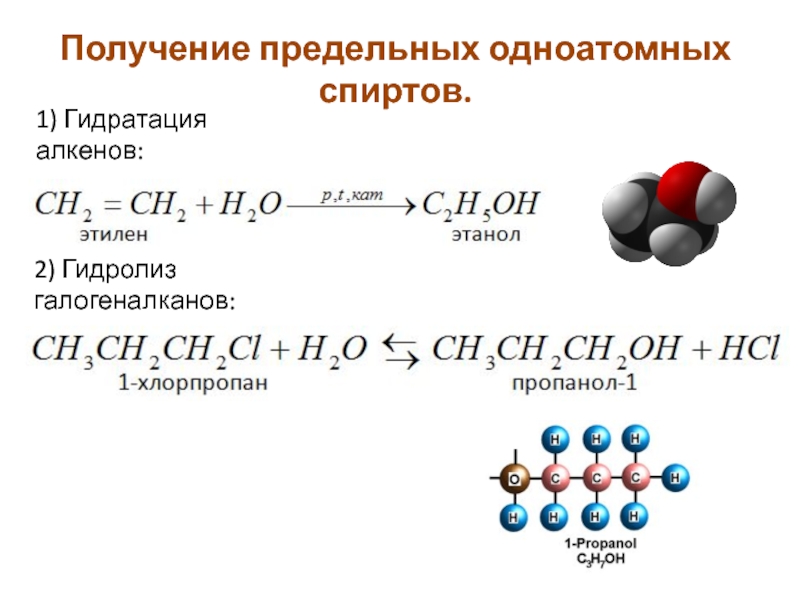
- 12. Получение предельных одноатомных спиртов. 2) Гидролиз галогеналканов: 1) Гидратация алкенов:
- 13. 3) Метанол в промышленности получают из “синтез-газа”-
- 14. Тема: «Многоатомные спирты» 900igr.net
- 15. Домашнее задание
- 16. Содержание 1 этапа: Дать
- 17. Химические свойства многоатомных спиртов Взаимодействие
- 18. Генетическая связь многоатомных спиртов
- 19. Применение спиртов Использование в косметике Использование в
- 20. Представленные вещества
- 21. Тосол ЭТИЛЕНГЛИКОЛЬ - двухатомный спирт. Важным
- 22. Тосол Тосол этиленгликоль Многоатомный спирт
- 23. Мёд
- 24. Мёд Углевод Фруктоза, глюкоза Многоатомный спирт
- 25. Маннит Маннит — шестиатомный спирт, содержится во
- 26. Маннит Сорбит Многоатомный спирт
- 27. Жевательная резинка Жева́тельная рези́нка — вид
- 28. Жевательная резинка Ксилит Многоатомный спирт
- 29. Детский крем (глицерин) Глицерин – трёхатомный спирт.
- 30. Детский крем Глицерин Многоатомный спирт
- 32. Растительное масло Жир Сложный эфир Многоатомный спирт Глицерин
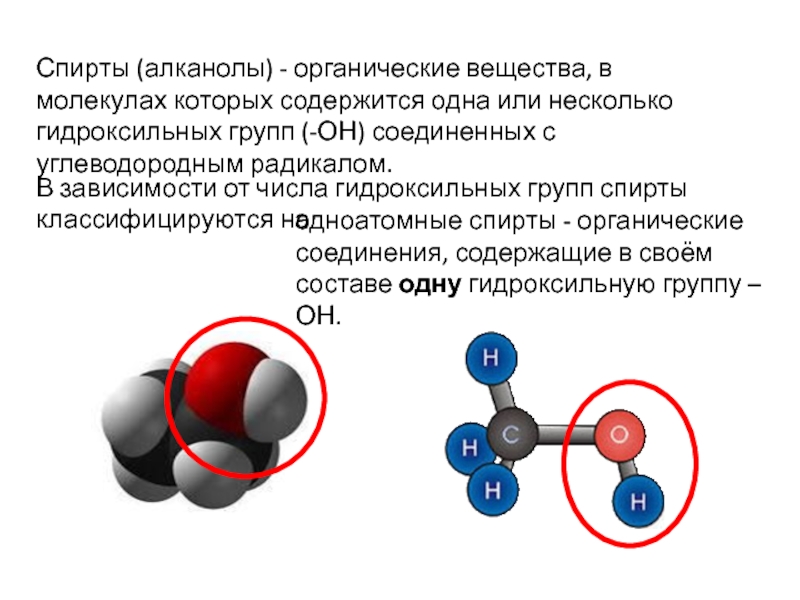
Слайд 2Спирты (алканолы) - органические вещества, в молекулах которых содержится одна или
В зависимости от числа гидроксильных групп спирты классифицируются на
одноатомные спирты - органические соединения, содержащие в своём составе одну гидроксильную группу – ОН.
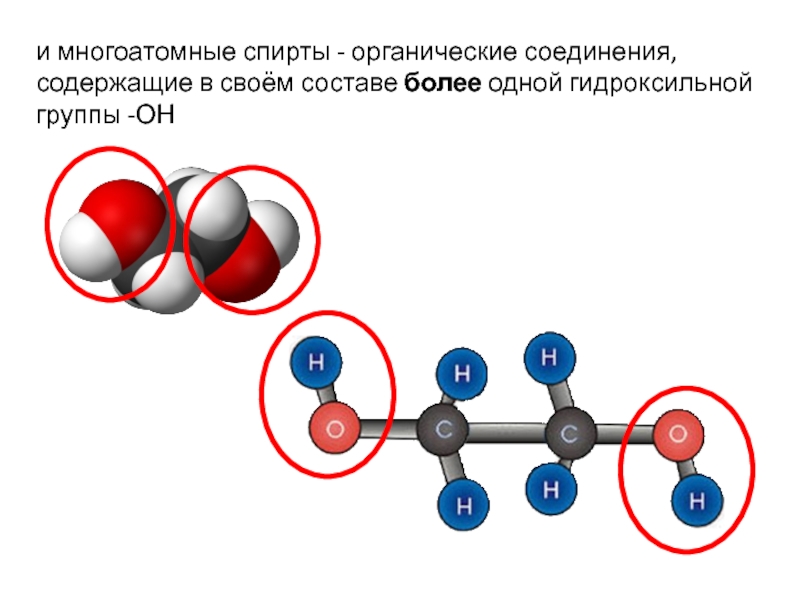
Слайд 3и многоатомные спирты - органические соединения, содержащие в своём составе более
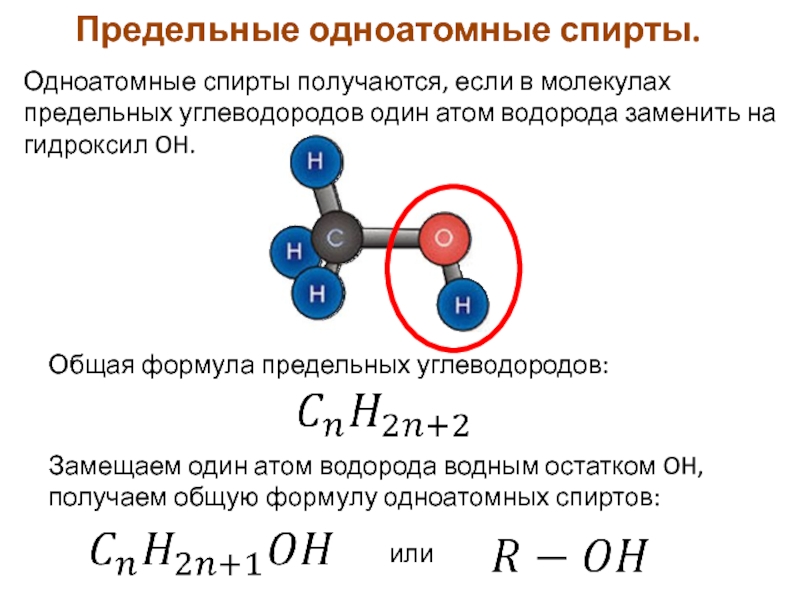
Слайд 4Одноатомные спирты получаются, если в молекулах предельных углеводородов один атом водорода
Общая формула предельных углеводородов:
Замещаем один атом водорода водным остатком OH, получаем общую формулу одноатомных спиртов:
или
Предельные одноатомные спирты.
Слайд 5
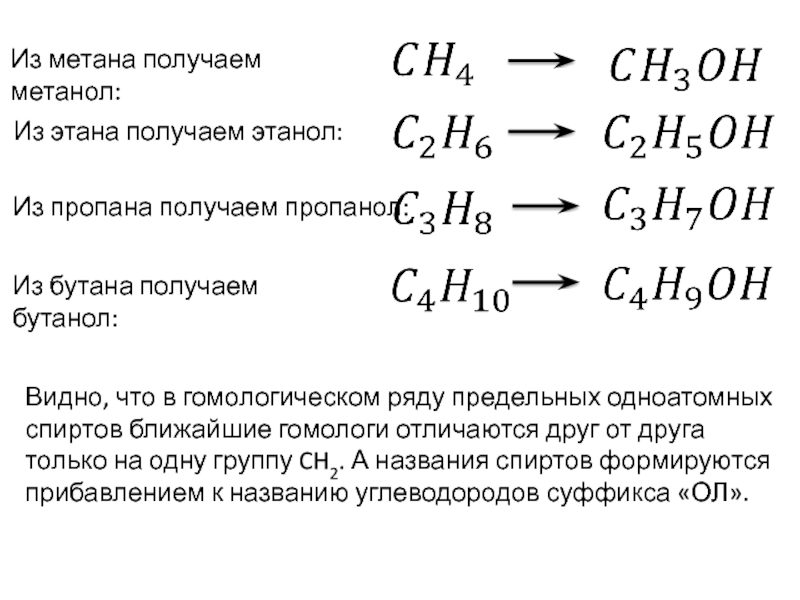
Из метана получаем метанол:
Из этана получаем этанол:
Из пропана получаем пропанол:
Из бутана
Видно, что в гомологическом ряду предельных одноатомных спиртов ближайшие гомологи отличаются друг от друга только на одну группу CH2. А названия спиртов формируются прибавлением к названию углеводородов суффикса «ОЛ».
Слайд 7В любом гомологическом ряду существует закономерность.
С увеличением молекулярной массы предельных
Физические свойства одноатомных спиртов.
Также, to кипения спиртов значительно больше to кипения углеводородов.
Почему?
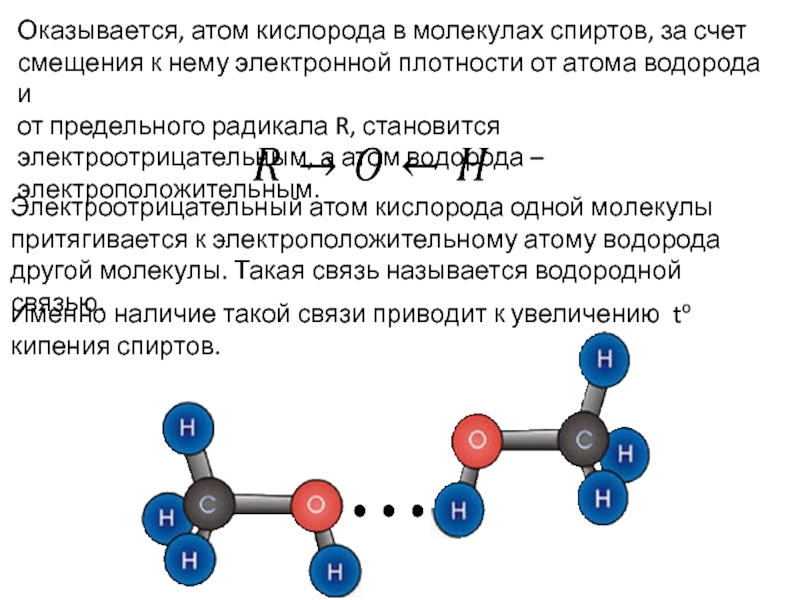
Слайд 8Оказывается, атом кислорода в молекулах спиртов, за счет смещения к нему
от предельного радикала R, становится электроотрицательным, а атом водорода – электроположительным.
Электроотрицательный атом кислорода одной молекулы притягивается к электроположительному атому водорода другой молекулы. Такая связь называется водородной связью.
Именно наличие такой связи приводит к увеличению to кипения спиртов.
Слайд 9Спирты растворяются в воде. Однако с увеличением молекулярной массы спиртов растворимость
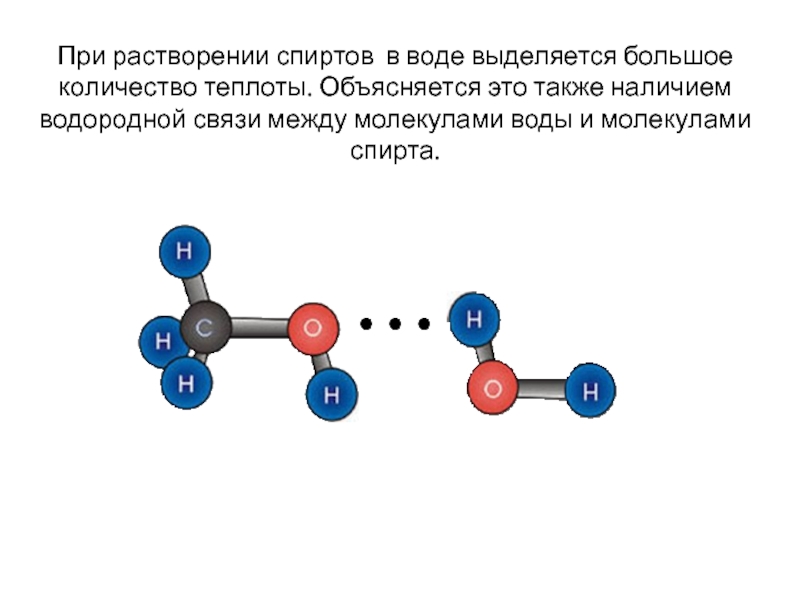
Слайд 10При растворении спиртов в воде выделяется большое количество теплоты. Объясняется это
Слайд 11Изомерия предельных одноатомных спиртов.
От того, к какому атому углерода прикреплена функциональная
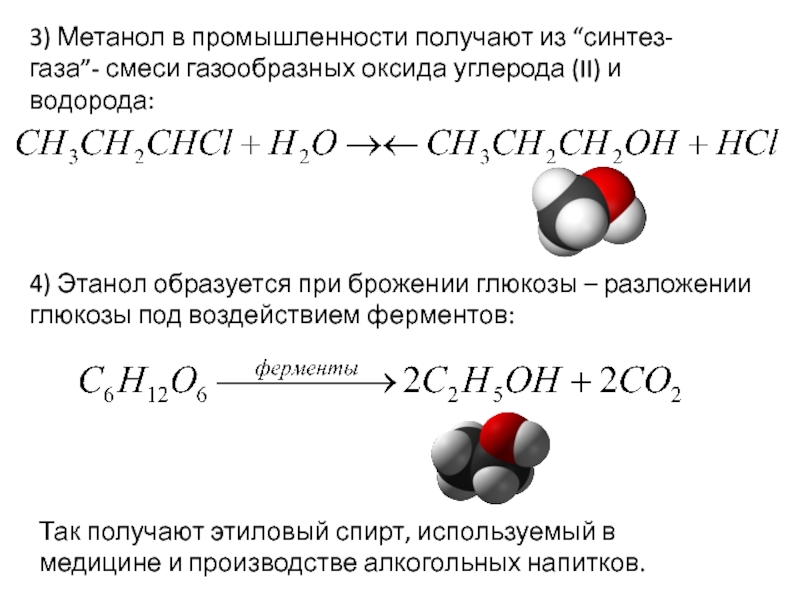
Слайд 133) Метанол в промышленности получают из “синтез-газа”- смеси газообразных оксида углерода
4) Этанол образуется при брожении глюкозы – разложении глюкозы под воздействием ферментов:
Так получают этиловый спирт, используемый в медицине и производстве алкогольных напитков.
Слайд 15Домашнее задание
написать формулу
2-метил бутанола
2-метил-2-бутанола
Осуществить превращение:
C2 H6
↓
C2 H4
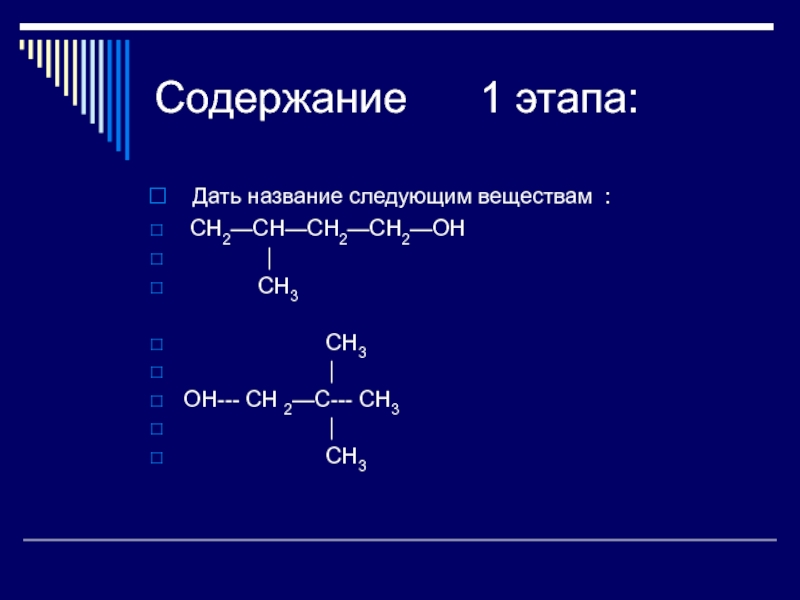
Слайд 16Содержание 1 этапа:
Дать название следующим веществам :
CH2—CH—CH2—CH2—OH
CH3
CH3
⏐
OH--- CH 2—C--- CH3
⏐
CH3
Слайд 17
Химические свойства многоатомных спиртов
Взаимодействие с металлами
Взаимодействие с гидроксидом меди
Взаимодействие с
Слайд 19Применение спиртов
Использование в косметике
Использование в медицине
Использование в текстильной промышленности
Использование в радиаторах
Слайд 21Тосол
ЭТИЛЕНГЛИКОЛЬ - двухатомный спирт.
Важным свойством этиленгликоля является способность понижать температуру замерзания
Он применяется и для получения лавсана (ценного синтетического волокна).
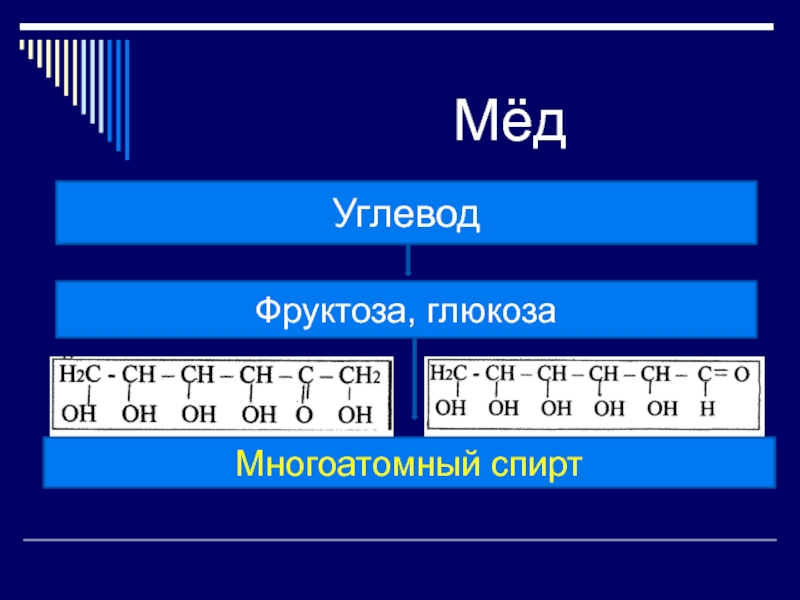
Слайд 23 Мёд
Основной составной частью мёда всех
В процентном отношении глюкоза составляет около 35% и фруктоза около 40%.
Глюкоза - (C6H12O6) («виноградный сахар» встречается в соке многих фруктов и ягод, в том числе и винограда. В организме человека и животных глюкоза является основным и наиболее универсальным источником энергии для обеспечения метаболических процессов
Фруктоза , или плодовый сахар C6H12O6 — моносахарид, который в свободном виде присутствует почти во всех сладких ягодах и плодах. В отличие от глюкозы, фруктоза не поглощается инсулин-зависимыми тканями. Она почти полностью поглощается и метаболизируется клетками печени.
Слайд 25Маннит
Маннит — шестиатомный спирт, содержится во многих растениях.
Сорбит – является составной
Сорбит часто применяется как заменитель сахара, его можно встретить в диетических продуктах и диетических напитках. Вещество считается пищевым подсластителем.
Слайд 27Жевательная резинка
Жева́тельная рези́нка — вид конфеты, которая состоит из несъедобной эластичной
Ксилит - пятиатомный спирт.
По калорийности ксилит идентичен сахару, в два раза слаще его. Биологической ценности не имеет. Отрицательного действия на организм не оказывает. Его применяют в пищевой промышленности, например вместо сахара, в производстве кондитерских изделий для больных диабетом и ожирением
Слайд 29Детский крем (глицерин)
Глицерин – трёхатомный спирт. Это бесцветная, вязкая, гигроскопи-чная, сладкая
Применяется:
При обработке кожи.
Как компонент некоторых клеёв.
При производстве пластмасс глицерин используют в качестве пластификатора.
В производстве кондитерских изделий и напитков (как пищевая добавкаE422).
Слайд 31 Растительное масло
Жиры
глицерина и высших карбоновых кислот.
Насыщенные кислоты образуют
твердые жиры, обычно они животного происхождения.
Непредельные кислоты образуют
жидкие жиры, они обычно растительного происхождения.
Жиры – основной источник энергии в живых организмах.