- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Общая характеристика элементов I группы главной подгруппы Периодической системы химических элементов Д.И. Менделеева презентация
Содержание
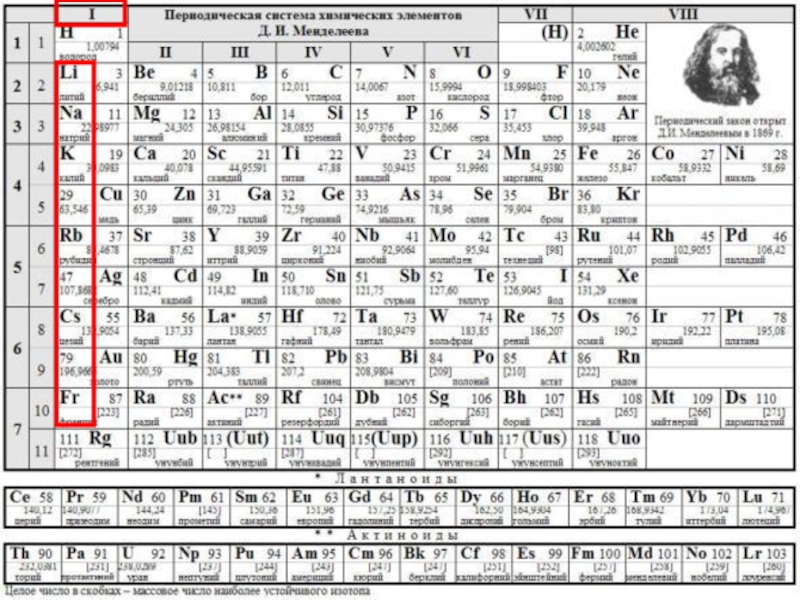
- 1. Общая характеристика элементов I группы главной подгруппы Периодической системы химических элементов Д.И. Менделеева
- 3. СТРОЕНИЕ АТОМА +3 1 +11
- 4. СТЕПЕНЬ ОКИСЛЕНИЯ +3 1 +11
- 5. ЗАПОМНИ! Степень окисления металлов I группы
- 6. ПРОСТЫЕ ВЕЩЕСТВА Серебристо-белые, с характерным металлическим
- 7. ХИМИЧЕСКИЕ СВОЙСТВА Металлы I группы
- 8. ВЗАИМОДЕЙСТВУЮТ С НЕМЕТАЛЛАМИ Li +
- 9. ВЗАИМОДЕЙСТВУЮТ С КИСЛОРОДОМ Li +
- 10. ВНИМАНИЕ! При взаимодействии с кислородом
- 11. A ЗНАЕТЕ ЛИ ВЫ? При взаимодействии
- 12. ВЗАИМОДЕЙСТВУЮТ С ВОДОЙ Металлы I группы
- 13. ВЗАИМОДЕЙСТВУЮТ С ВОДОЙ 2Li +
- 14. ХРАНЕНИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ Так как щелочные
- 15. НАХОЖДЕНИЕ В ПРИРОДЕ Щелочные металлы в
- 16. ПОЛУЧЕНИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ 2NaCl (расплав)
- 17. ПРИМЕНЕНИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ В металлургии в
- 18. ИЗ ИСТОРИИ
Слайд 1«Общая характеристика элементов
I группы главной подгруппы Периодической системы химических
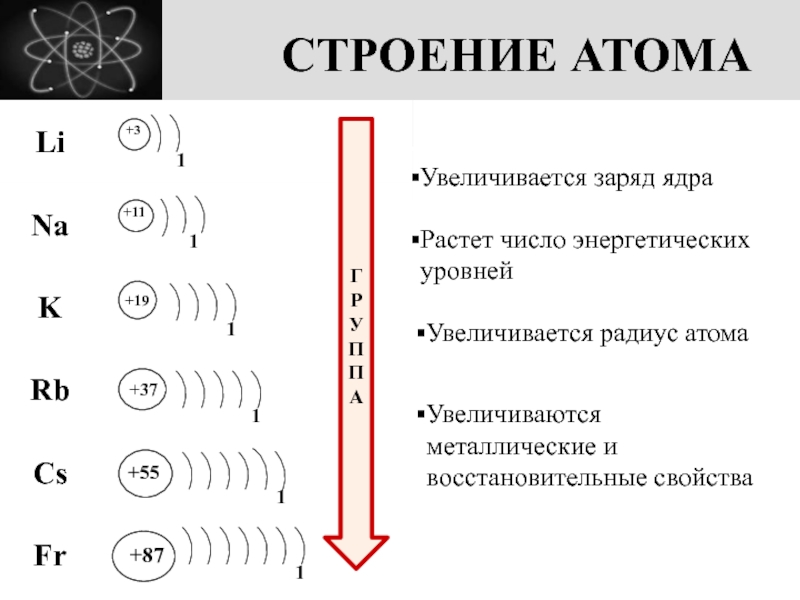
Слайд 3СТРОЕНИЕ АТОМА
+3
1
+11
+19
+37
+55
+87
1
1
1
1
1
ГРУППА
Увеличивается заряд ядра
Увеличивается радиус атома
Увеличиваются металлические и восстановительные свойства
Растет число
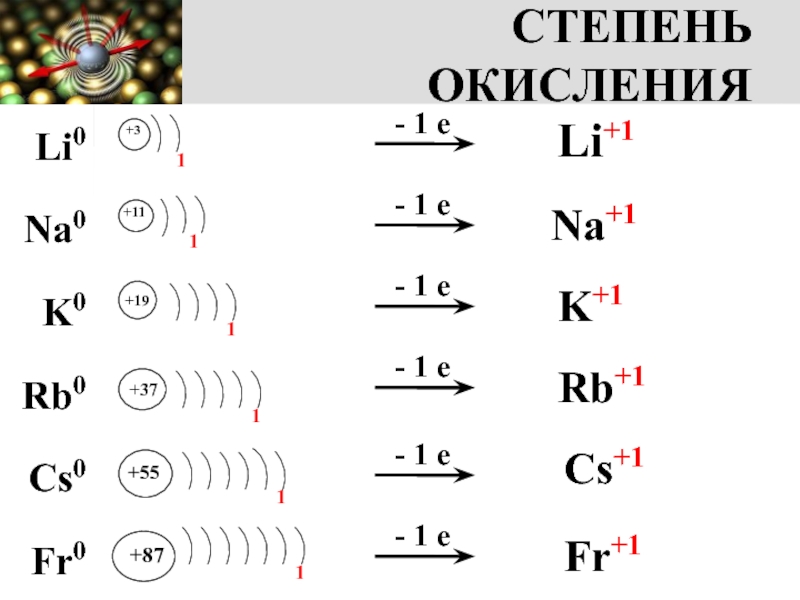
Слайд 4СТЕПЕНЬ ОКИСЛЕНИЯ
+3
1
+11
+19
+37
+55
+87
1
1
1
1
1
- 1 е
- 1 е
- 1 е
- 1 е
- 1
- 1 е
Li+1
Na+1
K+1
Rb+1
Cs+1
Fr+1
Слайд 5ЗАПОМНИ!
Степень окисления металлов I группы главной подгруппы в соединениях постоянная и
NaOH, K2O, Li3PO4,
K2CO3, NaCl, Na2O2
+1
+1
+1
+1
+1
+1
Слайд 6ПРОСТЫЕ ВЕЩЕСТВА
Серебристо-белые, с характерным металлическим блеском, но быстро тускнеют (окисляются) на
Мягкие, легко режутся ножом;
Хорошо проводят тепло и электрический ток;
Легкие (Li, Na, K – легче воды);
Легкоплавкие
температуры плавления и кипения понижаются
плотность металлов увеличивается
Слайд 7ХИМИЧЕСКИЕ СВОЙСТВА
Металлы I группы главной подгруппы –
наиболее активные
обладают высокой восстановительной способностью
В ряду Li - Na - K - Rb - Cs- Fr
химическая активность увеличивается
Образуют соединения с ионной связью и ионной кристаллической решеткой
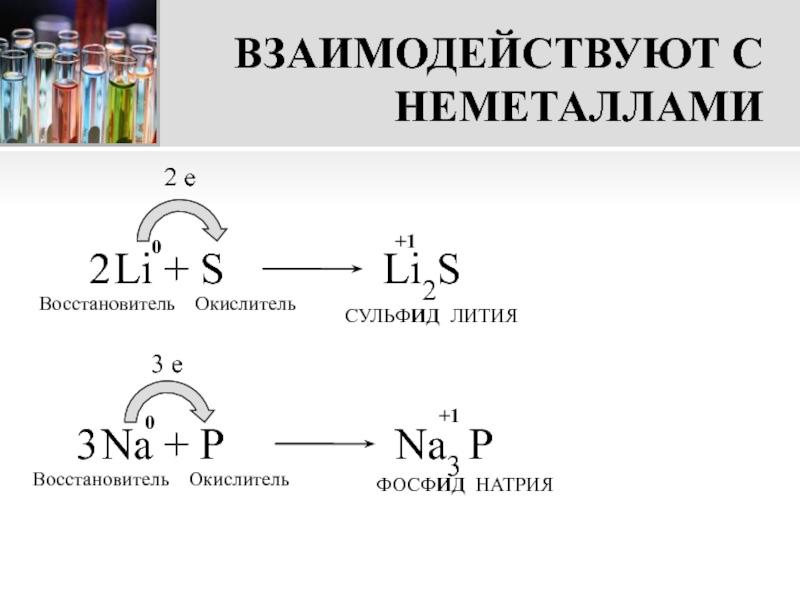
Слайд 8ВЗАИМОДЕЙСТВУЮТ С НЕМЕТАЛЛАМИ
Li + S
2 e
Восстановитель
Окислитель
СУЛЬФИД ЛИТИЯ
Na + P
3
Восстановитель
Окислитель
ФОСФИД НАТРИЯ
+1
0
0
+1
Li2S
2
Na3 P
3
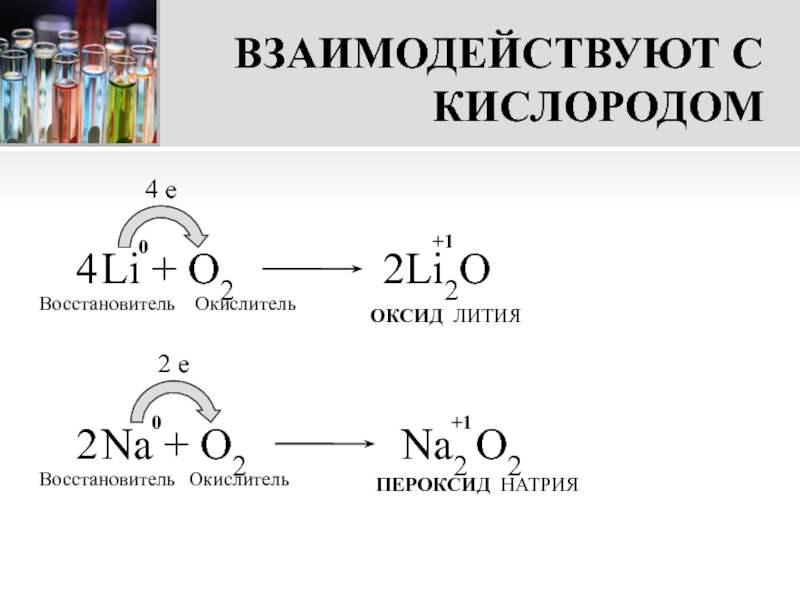
Слайд 9ВЗАИМОДЕЙСТВУЮТ С КИСЛОРОДОМ
Li + О2
4 e
Восстановитель
Окислитель
ОКСИД ЛИТИЯ
Na + O2
2
Восстановитель
Окислитель
ПЕРОКСИД НАТРИЯ
+1
0
0
+1
2Li2O
4
Na2 O2
2
Слайд 10ВНИМАНИЕ!
При взаимодействии с кислородом
только литий образует оксид.
Другие металлы I
ПЕРОКСИД НАТРИЯ
Na O O Na
+1
-1
-1
+1
Слайд 11A ЗНАЕТЕ ЛИ ВЫ?
При взаимодействии пероксида натрия с углекислым газом протекает
2Na2О2 + 2СО2 → 2Na2CО3 + О2
На этой реакции основано применение пероксида натрия для получения кислорода на подводных лодках и для регенерации воздуха в закрытых помещениях.
Слайд 12ВЗАИМОДЕЙСТВУЮТ С ВОДОЙ
Металлы I группы главной подгруппы реагируют с водой бурно,
Так как гидроксиды металлов I группы главной подгруппы образуют щелочи, то их групповое название – ЩЕЛОЧНЫЕ МЕТАЛЛЫ
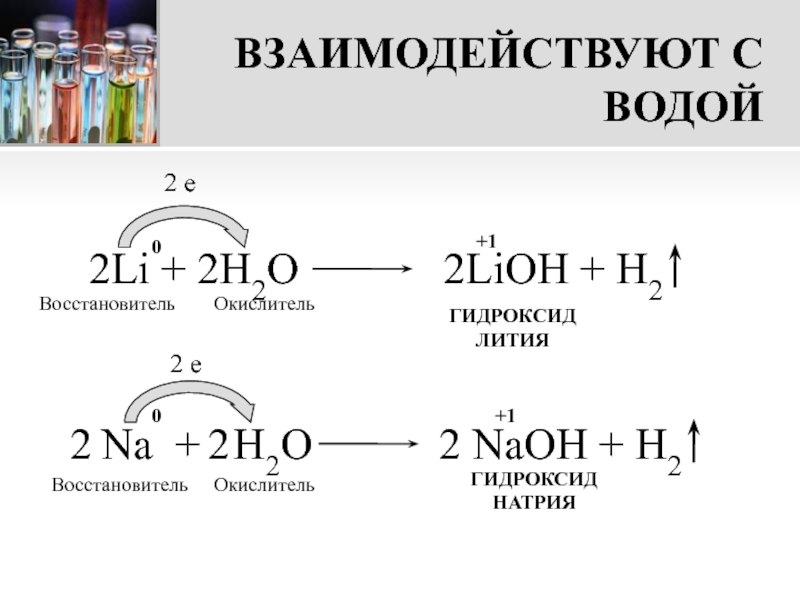
Слайд 13ВЗАИМОДЕЙСТВУЮТ С ВОДОЙ
2Li + 2H2О
2 e
Восстановитель
Окислитель
ГИДРОКСИД ЛИТИЯ
Восстановитель
Окислитель
ГИДРОКСИД НАТРИЯ
+1
0
Na + H2О
2 NaOH + H2
2
2
0
+1
2 e
Слайд 14ХРАНЕНИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ
Так как щелочные металлы легко окисляются и обладают высокой
Беречь от воды
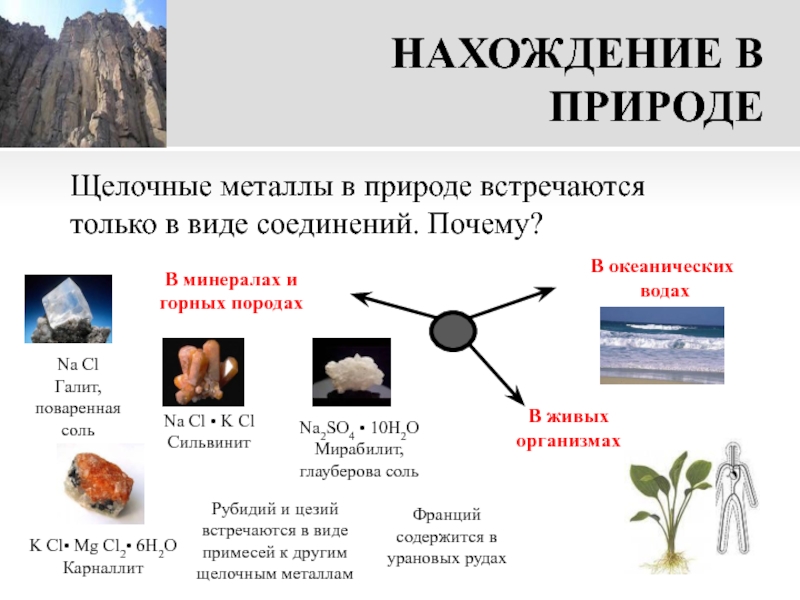
Слайд 15НАХОЖДЕНИЕ В ПРИРОДЕ
Щелочные металлы в природе встречаются только в виде соединений.
Na Cl
Галит, поваренная соль
Na Cl • K Cl
Сильвинит
K Cl• Mg Cl2• 6H2O
Карналлит
Na2SO4 • 10H2O
Мирабилит, глауберова соль
В океанических
водах
В минералах и горных породах
В живых организмах
Рубидий и цезий встречаются в виде примесей к другим щелочным металлам
Франций содержится в урановых рудах
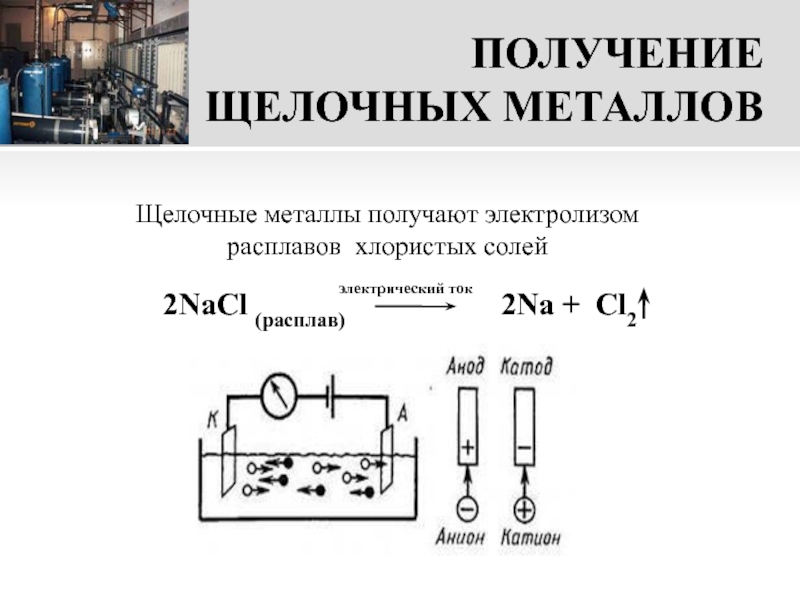
Слайд 16ПОЛУЧЕНИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ
2NaCl (расплав)
Щелочные металлы получают электролизом расплавов хлористых солей
электрический ток
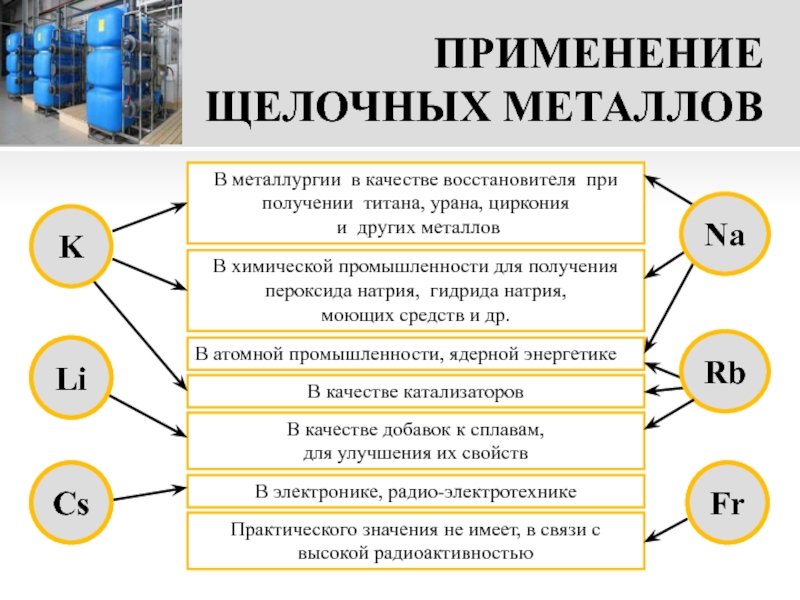
Слайд 17ПРИМЕНЕНИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ
В металлургии в качестве восстановителя при получении титана, урана,
и других металлов
В химической промышленности для получения пероксида натрия, гидрида натрия,
моющих средств и др.
В качестве добавок к сплавам,
для улучшения их свойств
В атомной промышленности, ядерной энергетике
Практического значения не имеет, в связи с высокой радиоактивностью
В качестве катализаторов
В электронике, радио-электротехнике
Na
Rb
Fr
K
Li
Cs