доцент Салищева О.В.
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение мицеллы лиофобного золя презентация
Содержание
- 1. Строение мицеллы лиофобного золя
- 2. ЛИОФОБНЫЕ ЗОЛИ Золи (коллоидные растворы) –
- 3. Как возникает двойной электрический слой 1. Нa
- 4. Избыточный электрический заряд на твердой поверхности, находящейся
- 5. I путь — ионная адсорбция Cl- Cl- Cl-
- 6. II путь —ионизация поверхностных молекул
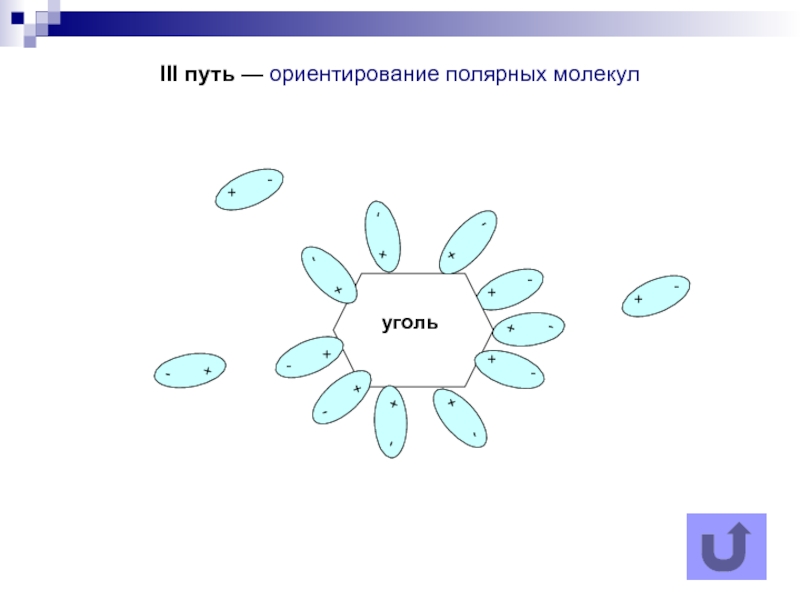
- 7. III путь — ориентирование полярных молекул уголь + -
- 8. Задание 1. Золь карбоната бария BaCO3 получен
- 9. Не верно Согласно правилу адсорбции (правилу Панета-Фаянса)
- 10. Правильно!
- 11. Задание 2. Золь карбоната бария BaCO3 получен
- 12. Не верно Итак, образующиеся в результате
- 13. Правильно!
- 14. AgNO3(изб) + KI ––> AgI +
- 15. AgNO3(изб) + KI ––> AgI + KNO3
- 16. AgNO3(изб) + KI ––> AgI +
- 17. AgNO3(изб) + KI ––> AgI +
- 18. AgNO3(изб) + KI ––> AgI
- 19. AgNO3(изб) + KI ––> AgI
- 20. AgNO3(изб) + KI ––>
- 21. AgNO3(изб) + KI ––> AgI
- 22. Строение мицеллы лиофобного золя В результате реакции
- 23. Образование двойного электрического слоя (ДЭС) Согласно правилу
- 24. Благодаря адсорбции ионов Ag+ поверхность кристалла заряжается
- 25. Слой противоионов, компенсирующих заряд твердой поверхности, имеет
- 26. Задание 4. Напишите формулу мицеллы золя карбоната
- 27. Строение мицеллы лиофобного золя BaCl2 не может
- 28. Строение мицеллы лиофобного золя Свободных ионов
- 29. Строение мицеллы лиофобного золя Обратите вниманием на
- 30. Строение мицеллы лиофобного золя BaCl2 не
- 31. Правильно!
- 32. Задание 5. Обозначьте составные части мицеллы золя
- 33. Задание 5. Обозначьте составные части мицеллы золя
- 34. Задание 5. Обозначьте составные части мицеллы золя
- 35. Задание 5. Обозначьте составные части мицеллы золя
- 36. Мицелла - кристаллик нерастворимого вещества,
- 37. Правильно!
- 38. Задание 6. На рисунке изображена мицелла золя
- 39. Мицелла - кристаллик нерастворимого вещества,
- 40. Правильно!
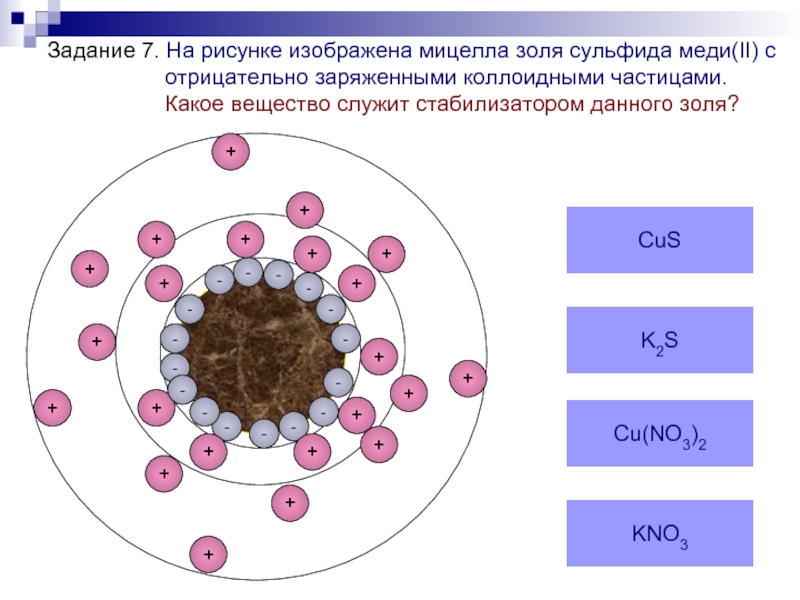
- 41. Задание 7. На рисунке изображена мицелла золя
- 42. Подсказки Стабилизатор – это сильный электролит
- 43. Т Е С Т Если Вы научились
- 44. Выберите номер варианта 1 2 3 4 5 6 7 8 9 10
- 45. Вариант-1 Изобразите формулу мицеллы гидрофобного золя, полученного
- 46. Вариант-1 Золь берлинской лазури Fe4[Fe(CN)6]3 получен конденсационным
- 47. Вариант-1 Напишите формулу мицеллы золя ZnS, стабилизированного
- 48. Вариант-1 На примере мицеллы золя сульфида цинка,
- 49. Вариант-2 Задание 1 Напишите формулу мицеллы гидрофобного
- 50. Вариант-2 Золь Сu2[Fe(CN)6] получен конденсационным методом с
- 51. Вариант-2 Задание 3 Напишите формулу мицеллы золя
- 52. Вариант-2 На примере мицеллы золя гидроксида алюминия,
- 53. Вариант-3 Задание 1 Золь гидроксида железа (III)
- 54. Вариант-3 Напишите формулу мицеллы золя As2S3, стабилизированного
- 55. Вариант-3 На примере мицеллы золя сульфида мышьяка,
- 56. Вариант-3 Золь Co2[Fe(CN)6] получен конденсационным методом с
- 57. Вариант-4 Золь Ag4[Fe(CN)6] получен конденсационным методом с
- 58. Вариант-4 Задание 2 Напишите схему строения мицеллы
- 59. Вариант-4 Напишите формулу мицеллы золя Ni(OH)2, стабилизированного
- 60. Вариант-4 На примере мицеллы золя гидроксида никеля,
- 61. Вариант-5 Напишите формулу мицеллы золя гидроксида бария,
- 62. Вариант-5 На примере мицеллы золя гидроксида бария,
- 63. Вариант-5 Изобразите формулу мицеллы гидрофобного золя, образующегося
- 64. Вариант-5 Золь берлинской лазури Fe4[Fe(CN)6]3 получен конденсационным
- 65. Вариант-6 Золь Cu2[Fe(CN)6] получен конденсационным методом с
- 66. Вариант-6 Изобразите формулу мицеллы гидрофобного золя, полученного
- 67. Вариант-6 Напишите формулу мицеллы золя гидроксида железа(III),
- 68. Вариант-6 На примере мицеллы золя гидроксида железа(III),
- 69. Вариант-7 Золь AgBr получен при добавлении 8
- 70. Вариант-7 Золь Ag4[Fe(CN)6] получен конденсационным методом с
- 71. Вариант-7 Напишите формулу мицеллы золя PbS, стабилизированного
- 72. Вариант-7 На примере мицеллы золя сульфида свинца(II),
- 73. Вариант-8 Золь Co2[Fe(CN)6] получен конденсационным методом с
- 74. Вариант-8 Золь BaSO4 получен при добавлении 10
- 75. Вариант-8 Напишите формулу мицеллы золя диоксида марганца
- 76. Вариант-8 На примере мицеллы золя MnO2, стабилизированного
- 77. Вариант-9 Золь сульфида кобальта CoS получен при
- 78. Вариант-9 Золь сульфида цинка получен конденсационным методом
- 79. Вариант-9 Напишите формулу мицеллы золя золота Au,
- 80. Вариант-9 На примере мицеллы золя золота, стабилизированного
- 81. Вариант-10 Напишите формулу мицеллы золя FeS, стабилизированного
- 82. Вариант-10 На примере мицеллы золя сульфида железа(II),
- 83. Вариант-10 Золь AgSCN получен при добавлении 5
- 84. Вариант-10 Золь гидрофосфата серебра Ag2HPO4 получен конденсационным
- 85. Желаю Вам успехов!!!
Слайд 1Строение мицеллы лиофобного золя
тренажер
начать
Государственное образовательное учреждение высшего профессионального образования
Кемеровский технологический
Слайд 2ЛИОФОБНЫЕ ЗОЛИ
Золи (коллоидные растворы) – высокодисперсные системы с жидкой дисперсионной
Золи, в которых дисперсная фаза не способна взаимодействовать с дисперсионной средой, а, следовательно, растворяться в ней, называются лиофобными.
Многие важные специфические свойства золей: электрические, оптические, молекулярно-кинетические и др., а также их устойчивость, обусловлены возникновением на поверхности частиц двойного электрического слоя.
Слайд 3Как возникает двойной
электрический слой
1. Нa любой твердой поверхности при ее контакте
2. Этот заряд компенсируется, находящимися в жидкой фазе ионами противоположного знака (противоионами). В результате этих процессов на границе раздела твердой и жидкой фаз формируется двойной электрический слой.
3. Образование двойного электрического слоя происходит самопроизвольно, как следствие стремления поверхностной энергии к минимуму.
Слайд 4 Избыточный электрический заряд на твердой поверхности, находящейся в контакте с жидкостью,
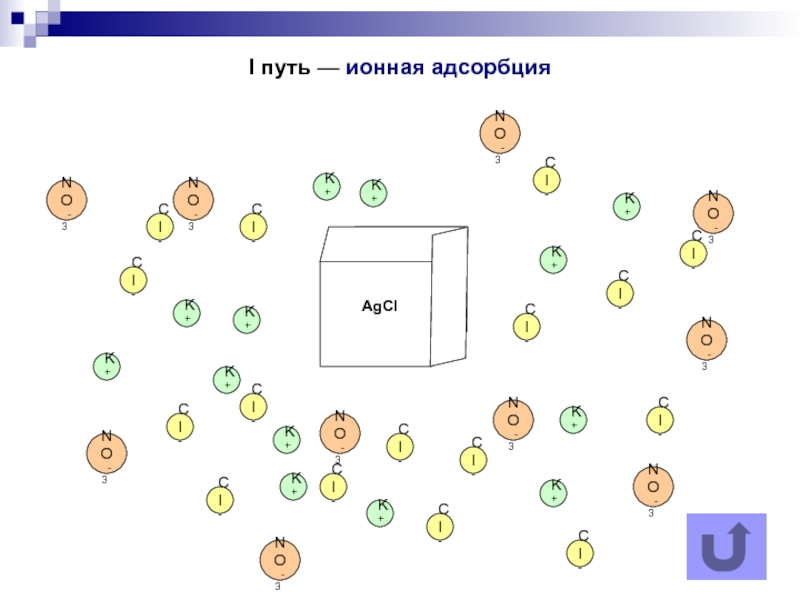
I путь — ионная адсорбция; поверхность кристалла адсорбирует из дисперсионной среды подходящие ионы - это такие анионы или катионы, которые способны достраивать его кристаллическую решетку
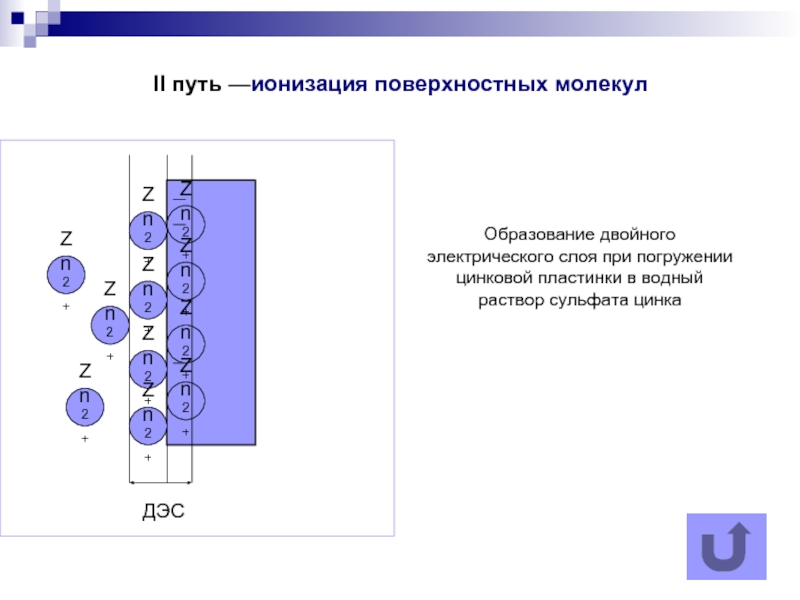
II путь — поверхностная ионизация; в этом случае с поверхности твердого тела в дисперсионную среду переходят ионы одного знака, и поверхность приобретает заряд другого знака
III путь — в тех редких случаях, когда межфазная поверхность образована веществами, не способными обмениваться зарядами, двойной электрический слой может образовываться благодаря ориентированию полярных молекул в поверхностном слое
Показать пример
Показать пример
Показать пример
Слайд 5I путь — ионная адсорбция
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
K+
NO3-
K+
K+
K+
K+
K+
K+
K+
K+
K+
K+
K+
K+
AgCl
NO3-
NO3-
NO3-
NO3-
NO3-
NO3-
NO3-
NO3-
NO3-
Слайд 6II путь —ионизация поверхностных молекул
Zn2+
Zn2+
Zn2+
Zn2+
Zn2+
Zn2+
Zn2+
Zn2+
Zn2+
Zn2+
Zn2+
ДЭС
Образование двойного электрического слоя при погружении цинковой
Слайд 8Задание 1. Золь карбоната бария BaCO3 получен при действии избытка хлорида
[m BaCO3] ·?
BaCl2 (избыток) + Na2CO3 = BaCO3 ↓ + 2NaCl
Какие ионы будут адсорбироваться на поверхности
кристалла BaCO3 ?
Na+
Ba2+
Cl-
CO32-
Слайд 9Не верно
Согласно правилу адсорбции (правилу Панета-Фаянса) на кристалле адсорбируются:
ионы, которые способны
Рассмотрим образование ДЭС на поверхности кристалла BaCO3, полученного при взаимодействии водных растворов хлорида бария и карбоната натрия, причем одно из реагирующих веществ (BaCl2) взято в избытке:
BaCl2 (избыток) + Na2CO3 → BaCO3↓ + 2NaCl,
Образующиеся в результате реакции мелкие кристаллы BaCO3 находятся в растворе, содержащем ионы Ba2+, Cl-, Na+. Ионов CO32- в растворе нет, так как карбонат натрия был взят в недостатке, и все ионы CO32- образовали труднорастворимое соединение BaCO3.
Начинается процесс адсорбции ионов, в котором кристаллы BaCO3 являются адсорбентом.
Слайд 11Задание 2. Золь карбоната бария BaCO3 получен при действии избытка хлорида
[m BaCO3] ·n Ba2+
BaCl2 (избыток) + Na2CO3 = BaCO3 ↓ + 2NaCl
Какие ионы будут компенсировать избыточный электрический заряд поверхности кристалла BaCO3 ?
Na+
Ba2+
Cl-
CO32-
Слайд 12Не верно
Итак, образующиеся в результате реакции :
BaCl2 (избыток) + Na2CO3 →
мелкие кристаллы BaCO3 находятся в растворе, содержащем ионы Ba2+, Cl-, Na+. Так как карбонат натрия был взят в недостатке, то ионов CO32- в растворе нет.
Адсорбция ионов Ba2+ происходит за счет химических сил, приводящих к прочному присоединению их к кристаллу. Поверхность кристалла заряжается положительно. Ионы Ba2+ , сообщившие поверхности этот заряд, называются потенциалобразующими ионами.
Оставшиеся в растворе ионы противоположного знака (противоионы) электростатически притягиваются к твердой поверхности и компенсируют ее заряд.
Слайд 14
AgNO3(изб) + KI ––> AgI + KNO3
Стабилизатор: AgNO3→Ag++NO3-
{[
Задание 3. Изобразите формулу мицеллы золя иодида серебра, полученного по реакции:
?
AgNO3
AgI
KI
KNO3
Слайд 15AgNO3(изб) + KI ––> AgI + KNO3
Стабилизатор: AgNO3→Ag++NO3-
{[
Изобразите формулу мицеллы золя иодида серебра, полученного по реакции:
AgNO3
AgI
KI
KNO3
Слайд 16
AgNO3(изб) + KI ––> AgI + KNO3
Стабилизатор: AgNO3→Ag++NO3-
{[
Изобразите формулу мицеллы золя иодида серебра, полученного по реакции:
?
AgI
NO3-
K+
I-
Ag+
Слайд 17
AgNO3(изб) + KI ––> AgI + KNO3
Стабилизатор: AgNO3→Ag++NO3-
{[
Изобразите формулу мицеллы золя иодида серебра, полученного по реакции:
AgI
NO3-
K+
I-
Ag+
Слайд 18
AgNO3(изб) + KI ––> AgI + KNO3
Стабилизатор: AgNO3→Ag++NO3-
{[
Изобразите формулу мицеллы золя иодида серебра, полученного по реакции:
?
AgI
NO3-
K+
I-
Ag+
Ag+
Слайд 19
AgNO3(изб) + KI ––> AgI + KNO3
Стабилизатор: AgNO3→Ag++NO3-
{[
Изобразите формулу мицеллы золя иодида серебра, полученного по реакции:
AgI
NO3-
K+
I-
Ag+
Ag+
Слайд 20
AgNO3(изб) + KI ––> AgI + KNO3
Стабилизатор: AgNO3→Ag++NO3-
{[
Изобразите формулу мицеллы золя иодида серебра, полученного по реакции:
?
AgI
NO3-
K+
I-
Ag+
Ag+
NO3-
Слайд 21
AgNO3(изб) + KI ––> AgI + KNO3
Стабилизатор: AgNO3→Ag++NO3-
{[
Изобразите формулу мицеллы золя иодида серебра, полученного по реакции:
AgI
NO3-
K+
I-
Ag+
Ag+
NO3-
Слайд 22Строение мицеллы лиофобного золя
В результате реакции ионного обмена образуется трудно растворимое
Слайд 23Образование двойного электрического слоя (ДЭС)
Согласно правилу адсорбции (правилу Панета-Фаянса) на кристалле
ионы, которые способны достраивать его кристаллическую решетку, т.е. ионы, из которых построена данная решетка или изоморфные им;
ионы, которые могут образовывать с ионами кристаллической решетки малорастворимые соединения.
Обратите внимание на вещество, взятое в избытке
(оно является стабилизатором)
Слайд 24Благодаря адсорбции ионов Ag+ поверхность кристалла заряжается положительно. Ионы Ag+, сообщившие
Оставшиеся в растворе ионы противоположного знака (противоионы) электростатически притягиваются к поверхности и нейтрализуют ее заряд.
Образование двойного электрического слоя (ДЭС)
Обратите внимание на уравнение электролитической диссоциации электролита, взятого в избытке
Слайд 25Слой противоионов, компенсирующих заряд твердой поверхности, имеет сложное строение и состоит
Образование двойного электрического слоя (ДЭС)
Слайд 26Задание 4. Напишите формулу мицеллы золя карбоната бария BaCO3, стабилизированного хлоридом
{ [m BaCl2] · n Ba2+ · (2n-x) Cl-} x+ · x Cl-
{ [m BaCO3] · n Ba2+ · (n-x) CO32-} 2x+ · x CO32-
{ [m BaCO3] · n Ba2+ · (n-x) Cl-} x+ · x Cl-
{ [m BaCO3] · n Ba2+ · (2n-x) Cl-} x+ · x Cl-
{ [m BaCl2] · n Ba2+ · (n-x) CO32-} 2x+ · x CO32-
ВЫБЕРИТЕ ПРАВИЛЬНУЮ ЗАПИСЬ
Слайд 27Строение мицеллы лиофобного золя
BaCl2 не может быть центром адсорбции, так как
Слайд 28Строение мицеллы лиофобного золя
Свободных ионов CO32- в растворе нет (все карбонат-ионы
Слайд 29Строение мицеллы лиофобного золя
Обратите вниманием на заряд потенциалопределяющих ионов. Так как
Слайд 30Строение мицеллы лиофобного золя
BaCl2 не может быть центром адсорбции, так как
Слайд 32Задание 5. Обозначьте составные части мицеллы золя сульфата бария, стабилизированного сульфатом
{ [BaSO4]m∙nSO42-·(2n-x)K+}x-∙xK+
1
4
3
2
Потенциалобразующие ионы
Агрегат
Противоионы адсорбционного слоя
Противоионы диффузионного слоя
Слайд 33Задание 5. Обозначьте составные части мицеллы золя сульфата бария, стабилизированного сульфатом
{ [BaSO4]m∙nSO42-·(2n-x)K+}x-∙xK+
1
4
3
2
Потенциалобразующие ионы
Агрегат
Противоионы адсорбционного слоя
Противоионы диффузионного слоя
Слайд 34Задание 5. Обозначьте составные части мицеллы золя сульфата бария, стабилизированного сульфатом
{ [BaSO4]m∙nSO42-·(2n-x)K+}x-∙xK+
1
4
3
2
Потенциалобразующие ионы
Агрегат
Противоионы адсорбционного слоя
Противоионы диффузионного слоя
Слайд 35Задание 5. Обозначьте составные части мицеллы золя сульфата бария, стабилизированного сульфатом
{ [BaSO4]m∙nSO42-·(2n-x)K+}x-∙xK+
1
4
3
2
Потенциалобразующие ионы
Агрегат
Противоионы адсорбционного слоя
Противоионы диффузионного слоя
Слайд 36Мицелла - кристаллик нерастворимого вещества, окруженный двойным электрическим слоем.
Коллоидная частица - кристаллик вместе с прочно удерживаемыми на его поверхности ионами адсорбционного слоя. Коллоидная частица заряжена.
Агрегат - мелкие кристаллы труднорастворимого соединения, выступающие в роли адсорбента.
Потенциалобразующие ионы – ионы, прочно присоединеные к кристаллу за счет химических сил, и, сообщившие поверхности свой знак заряда.
Ядро - кристаллик вместе с прочно удерживаемыми на его поверхности потенциалобразующими ионами.
Противоионы - ионы противоположного знака по отношению к потенциалобразующим ионам.
Противоионы адсорбционного слоя - это противоионы, которые непосредственно примыкают к заряженной поверхности твердой частицы и удерживаются на ней не только электростатическими, но и адсорбционными силами.
Противоионы диффузионного слоя - это остальные противоионы, которые совершают тепловое движение около заряженной поверхности коллодной чкастицы и удерживаются вблизи неё только электростатическими силами.
Адсорбционный слой – слой, образованный потенциалобразующими ионами и противоионами, которые непосредственно примыкают к заряженной поверхности твердой частицы (к ядру).
Граница скольжения – граница между адсорбционным и диффузионным слоями.
Строение мицеллы лиофобного золя
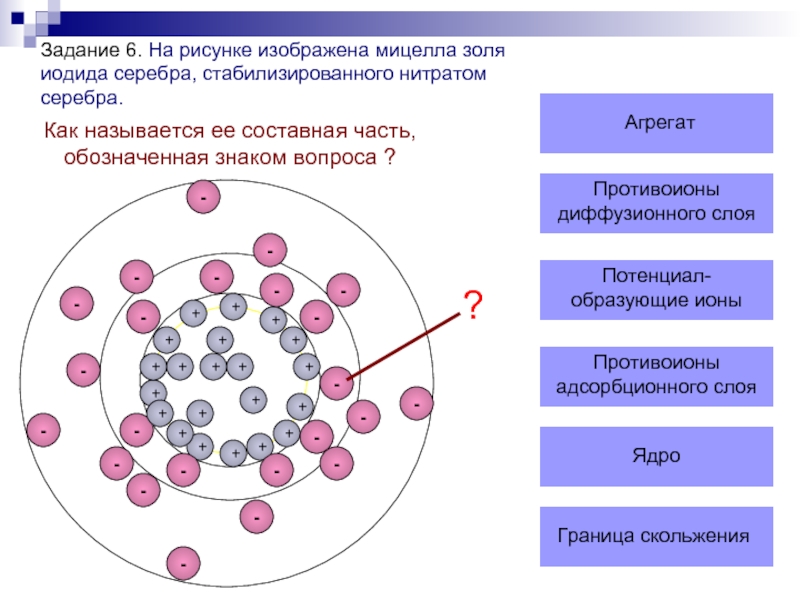
Слайд 38Задание 6. На рисунке изображена мицелла золя иодида серебра, стабилизированного нитратом
Как называется ее составная часть, обозначенная знаком вопроса ?
?
Слайд 39Мицелла - кристаллик нерастворимого вещества, окруженный двойным электрическим слоем.
Коллоидная частица - кристаллик вместе с прочно удерживаемыми на его поверхности ионами адсорбционного слоя. Коллоидная частица заряжена.
Агрегат - мелкие кристаллы труднорастворимого соединения, выступающие в роли адсорбента.
Потенциалобразующие ионы – ионы, прочно присоединеные к кристаллу за счет химических сил, и, сообщившие поверхности свой знак заряда.
Ядро - кристаллик вместе с прочно удерживаемыми на его поверхности потенциалобразующими ионами.
Противоионы - ионы противоположного знака по отношению к потенциалобразующим ионам. Слой противоионов, компенсирующих заряд твердой поверхности, имеет сложное строение и состоит из двух частей.
Противоионы адсорбционного слоя - это противоионы, которые непосредственно примыкают к заряженной поверхности твердой частицы и удерживаются на ней не только электростатическими, но и адсорбционными силами.
Противоионы диффузионного слоя - это остальные противоионы, которые совершают тепловое движение около заряженной поверхности коллодной чкастицы и удерживаются вблизи неё только электростатическими силами.
Адсорбционный слой – слой, образованный потенциалобразующими ионами и противоионами, которые непосредственно примыкают к заряженной поверхности твердой частицы (к ядру).
Граница скольжения – граница между адсорбционным и диффузионным слоями.
Строение мицеллы лиофобного золя
Слайд 41Задание 7. На рисунке изображена мицелла золя сульфида меди(II) c отрицательно
-
-
-
-
-
-
-
-
-
-
-
-
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
-
-
-
-
CuS
K2S
Cu(NO3)2
KNO3
Слайд 42Подсказки
Стабилизатор – это сильный электролит
Один из ионов (катион или анион)
Этот ион придает свой знак заряда твердой поверхности кристалла
Слайд 43Т Е С Т
Если Вы научились составлять формулы мицелл гидрофобных золей,
Слайд 45Вариант-1
Изобразите формулу мицеллы гидрофобного золя, полученного при действии избытка гидроксида калия
Каков знак заряда коллоидной частицы этого золя?
Задание 1
Слайд 46Вариант-1
Золь берлинской лазури Fe4[Fe(CN)6]3 получен конденсационным методом с помощью реакции ионного
Напишите формулу мицеллы золя с положительно заряженными коллоидными частицами. Какая соль является стабилизатором такого золя? Как следует проводить реакцию, чтобы получить золь с положительными частицами.
Задание 2
Слайд 47Вариант-1
Напишите формулу мицеллы золя ZnS, стабилизированного ZnCl2. К какому электроду будут
Задание 3
Слайд 48Вариант-1
На примере мицеллы золя сульфида цинка, стабилизированного хлоридом цинка, расскажите о
Задание 4
Слайд 49Вариант-2
Задание 1
Напишите формулу мицеллы гидрофобного золя, полученного при взаимодействии сульфата цинка
Каков знак заряда коллоидной частицы этого золя?
Слайд 50Вариант-2
Золь Сu2[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:
Напишите формулу мицеллы золя с положительно заряженными коллоидными частицами. Какая соль является стабилизатором такого золя? Как следует проводить реакцию, чтобы получить именно такой золь?
Задание 2
Слайд 51Вариант-2
Задание 3
Напишите формулу мицеллы золя Al(OH)3, стабилизированного AlCl3.
К какому электроду
Слайд 52Вариант-2
На примере мицеллы золя гидроксида алюминия, стабилизированного хлоридом алюминия, расскажите о
Задание 4
Слайд 53Вариант-3
Задание 1
Золь гидроксида железа (III) получен при добавлении к 85 мл
Слайд 54Вариант-3
Напишите формулу мицеллы золя As2S3, стабилизированного Na2S. К какому электроду будут
Задание 2
Слайд 55Вариант-3
На примере мицеллы золя сульфида мышьяка, стабилизированного сульфидом натрия, расскажите о
Задание 3
Слайд 56Вариант-3
Золь Co2[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:
Напишите формулу мицеллы золя с положительно заряженными коллоидными частицами. Какая соль является стабилизатором такого золя? Как следует проводить реакцию, чтобы получить именно такой золь?
Задание 4
Слайд 57Вариант-4
Золь Ag4[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:
Напишите формулу мицеллы золя с положительно заряженными коллоидными частицами. Какая соль является стабилизатором такого золя? Как следует проводить реакцию, чтобы получить именно такой золь?
Задание 1
Слайд 58Вариант-4
Задание 2
Напишите схему строения мицеллы золя сульфата бария, получающегося при взаимодействии
Каков знак заряда коллоидной частицы этого золя?
Слайд 59Вариант-4
Напишите формулу мицеллы золя Ni(OH)2, стабилизированного Ni(NO3)2. К какому электроду будут
Задание 3
Слайд 60Вариант-4
На примере мицеллы золя гидроксида никеля, стабилизированного нитратом никеля, расскажите о
Задание 4
Слайд 61Вариант-5
Напишите формулу мицеллы золя гидроксида бария, стабилизированного хлоридом бария. К какому
Задание 1
Слайд 62Вариант-5
На примере мицеллы золя гидроксида бария, стабилизированного хлоридом бария, расскажите о
Задание 2
Слайд 63Вариант-5
Изобразите формулу мицеллы гидрофобного золя, образующегося при действии избытка сульфата цинка
Каков знак заряда коллоидной частицы этого золя?
Задание 3
Слайд 64Вариант-5
Золь берлинской лазури Fe4[Fe(CN)6]3 получен конденсационным методом с помощью реакции ионного
Напишите формулу мицеллы золя с отрицательно заряженными коллоидными частицами. Какая соль является стабилизатором такого золя? Как следует проводить реакцию, чтобы получить именно такой золь?
Задание 4
Слайд 65Вариант-6
Золь Cu2[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:
Напишите формулу мицеллы золя с положительно заряженными коллоидными частицами. Какая соль является стабилизатором такого золя? Как следует проводить реакцию, чтобы получить именно такой золь?
Задание 1
Слайд 66Вариант-6
Изобразите формулу мицеллы гидрофобного золя, полученного при взаимодействии сульфата цинка с
Каков знак заряда коллоидной частицы этого золя?
Задание 2
Слайд 67Вариант-6
Напишите формулу мицеллы золя гидроксида железа(III), стабилизированного хлоридам железа(III). К какому
Задание 3
Слайд 68Вариант-6
На примере мицеллы золя гидроксида железа(III), стабилизированного хлоридам железа(III), расскажите о
Задание 4
Слайд 69Вариант-7
Золь AgBr получен при добавлении 8 мл водного раствора КBr концентрацией
Задание 1
Слайд 70Вариант-7
Золь Ag4[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:
Напишите формулу мицеллы золя с отрицательно заряженными коллоидными частицами. Какая соль является стабилизатором такого золя? Как следует проводить реакцию, чтобы получить именно такой золь?
Задание 2
Слайд 71Вариант-7
Напишите формулу мицеллы золя PbS, стабилизированного Pb(NO3)2. К какому электроду будут
Задание 3
Слайд 72Вариант-7
На примере мицеллы золя сульфида свинца(II), стабилизированного нитратом свинца(II), расскажите о
Задание 4
Слайд 73Вариант-8
Золь Co2[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:
Напишите формулу мицеллы золя с отрицательно заряженными коллоидными частицами. Какая соль является стабилизатором такого золя? Как следует проводить реакцию, чтобы получить именно такой золь?
Задание 1
Слайд 74Вариант-8
Золь BaSO4 получен при добавлении 10 мл водного раствора Na2SO4 концентрацией
Задание 2
Слайд 75Вариант-8
Напишите формулу мицеллы золя диоксида марганца MnO2, стабилизированного перманганатом калия KMnO4.
Задание 3
Слайд 76Вариант-8
На примере мицеллы золя MnO2, стабилизированного KMnO4, расскажите о строении двойного
Задание 4
Слайд 77Вариант-9
Золь сульфида кобальта CoS получен при добавлении 5 мл водного раствора
Задание 1
Слайд 78Вариант-9
Золь сульфида цинка получен конденсационным методом с помощью реакции ионного обмена:
Напишите формулу мицеллы золя с положительно заряженными коллоидными частицами. Какая соль является стабилизатором такого золя? Как следует проводить реакцию, чтобы получить именно такой золь?
Задание 2
Слайд 79Вариант-9
Напишите формулу мицеллы золя золота Au, стабилизированного KAuO2. К какому электроду
Задание 3
Слайд 80Вариант-9
На примере мицеллы золя золота, стабилизированного KAuO2, расскажите о строении двойного
Задание 4
Слайд 81Вариант-10
Напишите формулу мицеллы золя FeS, стабилизированного Na2S. К какому электроду будут
Задание 1
Слайд 82Вариант-10
На примере мицеллы золя сульфида железа(II), стабилизированного сульфидом натрия, расскажите о
Задание 2
Слайд 83Вариант-10
Золь AgSCN получен при добавлении 5 мл водного раствора КSCN концентрацией
Задание 3
Слайд 84Вариант-10
Золь гидрофосфата серебра Ag2HPO4 получен конденсационным методом с помощью реакции ионного
Напишите формулу мицеллы золя с положительно заряженными коллоидными частицами. Какая соль является стабилизатором такого золя? Как следует проводить реакцию, чтобы получить именно такой золь?
Задание 4










![AgNO3(изб) + KI ––> AgI + KNO3Стабилизатор: AgNO3→Ag++NO3-{[ ]m·n ·(n-x)](/img/tmb/1/57799/d6debbe3bf8eaad5aa10752233646233-800x.jpg)
![AgNO3(изб) + KI ––> AgI + KNO3Стабилизатор: AgNO3→Ag++NO3-{[ ]m·n ·(n-x) }x+](/img/tmb/1/57799/efbfe8b2c3b1f4cb28ef9368e98a8a4f-800x.jpg)
![AgNO3(изб) + KI ––> AgI + KNO3Стабилизатор: AgNO3→Ag++NO3-{[ ]m·n ·(n-x) }x+](/img/tmb/1/57799/5995d4737889a462fd515c31cfc3fcfd-800x.jpg)
![AgNO3(изб) + KI ––> AgI + KNO3Стабилизатор: AgNO3→Ag++NO3-{[ ]m·n ·(n-x) }x+](/img/tmb/1/57799/df2b362d10b39dfe39fd58c86924d29e-800x.jpg)
![AgNO3(изб) + KI ––> AgI + KNO3Стабилизатор: AgNO3→Ag++NO3-{[ ]m·n ·(n-x) }x+](/img/tmb/1/57799/1efa48a4ca01396c2e4526f8e75152e4-800x.jpg)
![AgNO3(изб) + KI ––> AgI + KNO3Стабилизатор: AgNO3→Ag++NO3-{[ ]m·n ·(n-x) }x+](/img/tmb/1/57799/81e04437c7a5bf575b93fefa407c8914-800x.jpg)
![AgNO3(изб) + KI ––> AgI + KNO3Стабилизатор: AgNO3→Ag++NO3-{[ ]m·n ·(n-x) }x+](/img/tmb/1/57799/2c923b2b9061e5c120ce597f30797e4a-800x.jpg)
![AgNO3(изб) + KI ––> AgI + KNO3Стабилизатор: AgNO3→Ag++NO3-{[ ]m·n ·(n-x) }x+](/img/tmb/1/57799/2842811f5218c1c7352ea375b32dc5e5-800x.jpg)




![Задание 4. Напишите формулу мицеллы золя карбоната бария BaCO3, стабилизированного хлоридом бария BaCl2{ [m BaCl2]](/img/tmb/1/57799/80f46456be1beeb9b2c90e2be0177b68-800x.jpg)





![Задание 5. Обозначьте составные части мицеллы золя сульфата бария, стабилизированного сульфатом калия{ [BaSO4]m∙nSO42-·(2n-x)K+}x-∙xK+1432Потенциалобразующие ионыАгрегатПротивоионы адсорбционного](/img/tmb/1/57799/05562e779e476b28aa7ef136c5ee9a3c-800x.jpg)
![Задание 5. Обозначьте составные части мицеллы золя сульфата бария, стабилизированного сульфатом калия{ [BaSO4]m∙nSO42-·(2n-x)K+}x-∙xK+1432Потенциалобразующие ионыАгрегатПротивоионы адсорбционного](/img/tmb/1/57799/974c9463285aca4c2ac18c88a267e248-800x.jpg)
![Задание 5. Обозначьте составные части мицеллы золя сульфата бария, стабилизированного сульфатом калия{ [BaSO4]m∙nSO42-·(2n-x)K+}x-∙xK+1432Потенциалобразующие ионыАгрегатПротивоионы адсорбционного](/img/tmb/1/57799/6a33f77e1993c013562a8a8b811adc4f-800x.jpg)
![Задание 5. Обозначьте составные части мицеллы золя сульфата бария, стабилизированного сульфатом калия{ [BaSO4]m∙nSO42-·(2n-x)K+}x-∙xK+1432Потенциалобразующие ионыАгрегатПротивоионы адсорбционного](/img/tmb/1/57799/7ba39a767a6dfa8c6fb7048f3da1b27f-800x.jpg)








![Вариант-1Золь берлинской лазури Fe4[Fe(CN)6]3 получен конденсационным методом с помощью реакции ионного обмена:](/img/tmb/1/57799/705a6f1e63e1ebffeededb7cbc46ee3c-800x.jpg)



![Вариант-2Золь Сu2[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:](/img/tmb/1/57799/1228377109e287e4f3d8e8bdae339009-800x.jpg)





![Вариант-3Золь Co2[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:](/img/tmb/1/57799/22580fe9efe1c7c65a19a15ddf945312-800x.jpg)
![Вариант-4Золь Ag4[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:](/img/tmb/1/57799/4152e86c6d05fdee85a3991ee4311efd-800x.jpg)






![Вариант-5Золь берлинской лазури Fe4[Fe(CN)6]3 получен конденсационным методом с помощью реакции ионного обмена:](/img/tmb/1/57799/9bd5409e5ce4676a32b1d8df7dcfcff0-800x.jpg)
![Вариант-6Золь Cu2[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:](/img/tmb/1/57799/e85196e75a50a3747e59390f2785011e-800x.jpg)




![Вариант-7Золь Ag4[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:](/img/tmb/1/57799/abc9244fe9df50e7a06bf3cc3d3a6d1d-800x.jpg)


![Вариант-8Золь Co2[Fe(CN)6] получен конденсационным методом с помощью реакции ионного обмена:](/img/tmb/1/57799/55acc396f9e14cb559be4cf96f2ec5ba-800x.jpg)

















