- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Многоатомные спирты презентация
Содержание
- 1. Многоатомные спирты
- 2. Вопросы для повторения Какими способами может быть
- 3. Задания Напишите структурные формулы пропанола-2, 2,2-диметилпропанола-1; На
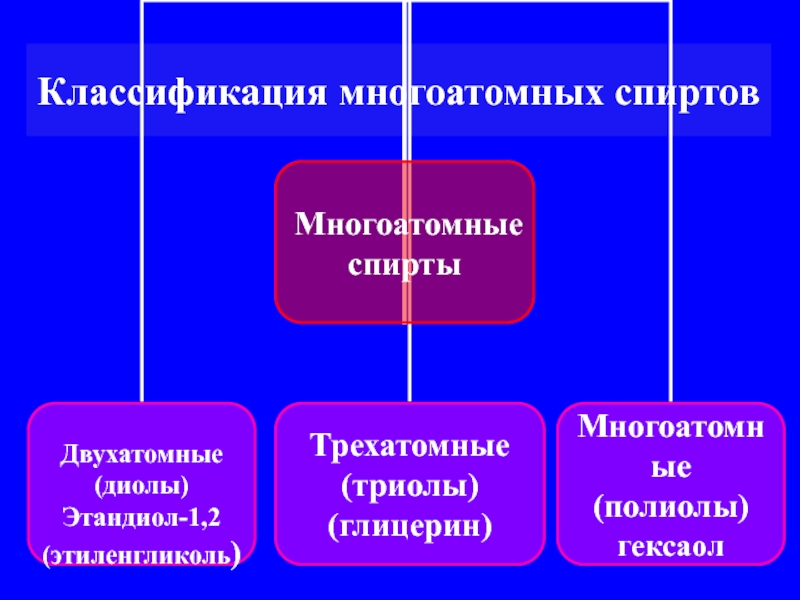
- 4. Классификация многоатомных спиртов
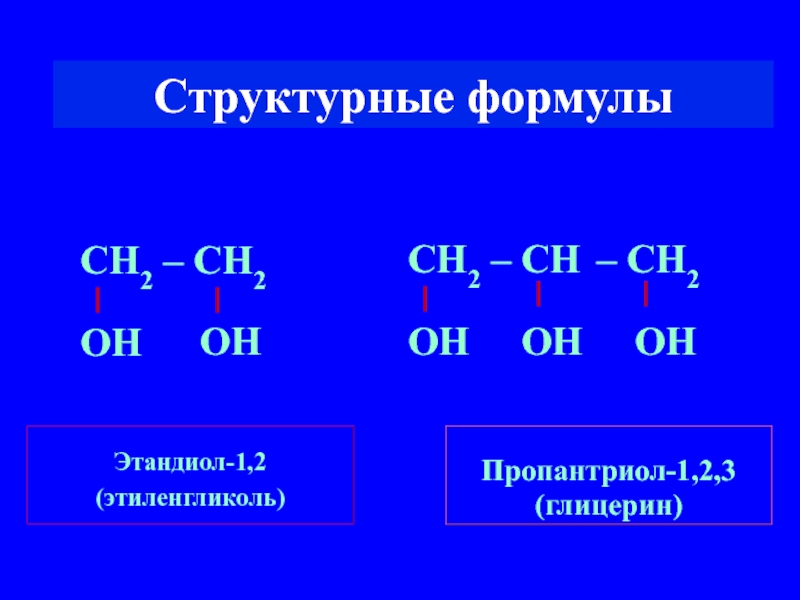
- 5. Структурные формулы Этандиол-1,2 (этиленгликоль) Пропантриол-1,2,3 (глицерин) СН2 – СН2 ОН ОН
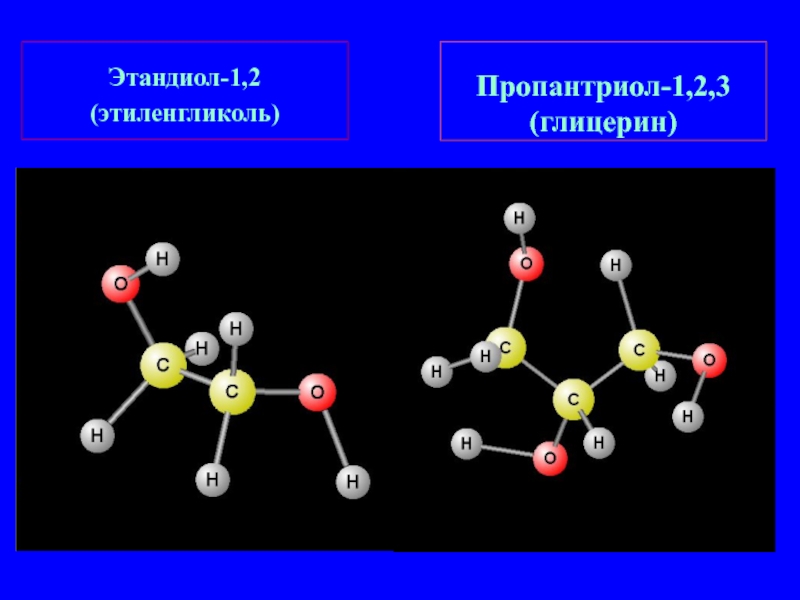
- 6. Этандиол-1,2 (этиленгликоль) Пропантриол-1,2,3 (глицерин)
- 7. Бесцветная, прозрачная, вязкая, сиропообразная жидкость, сладкая
- 8. Физические свойства этиленгликоля бесцветная вязкая жидкость со
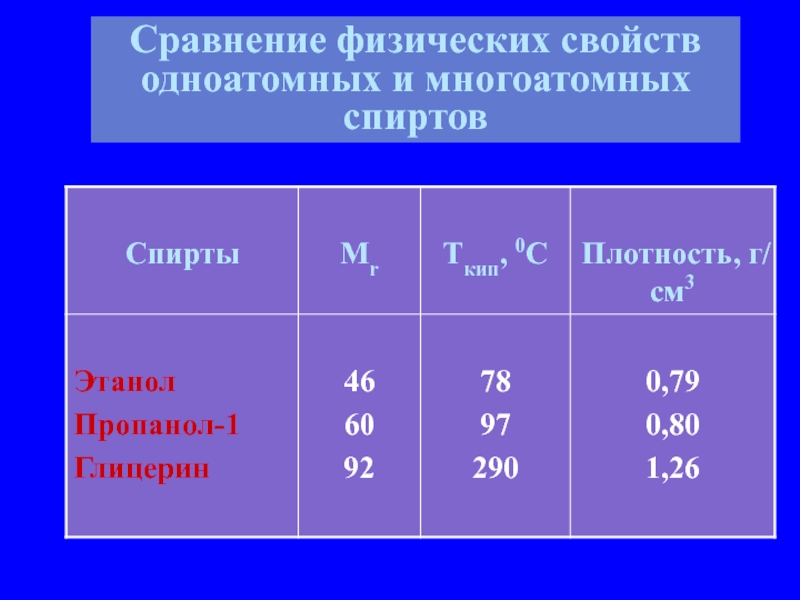
- 9. Сравнение физических свойств одноатомных и многоатомных спиртов
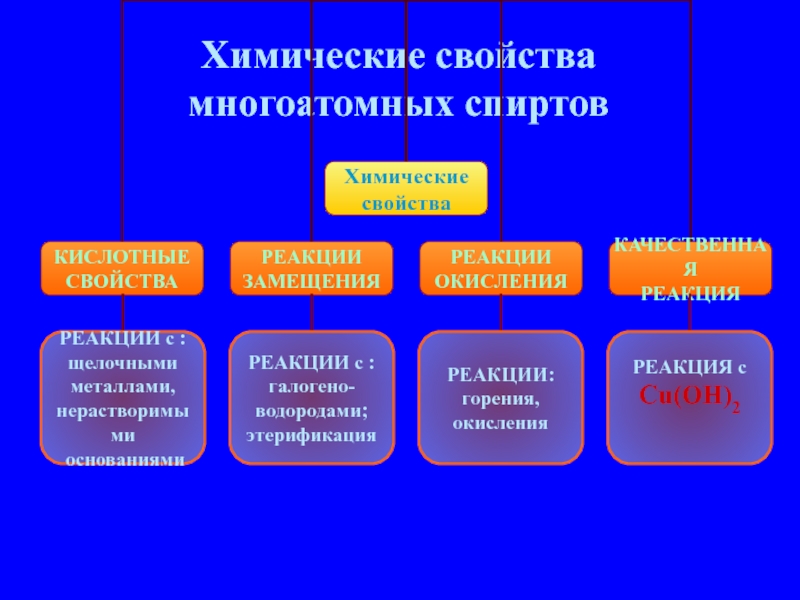
- 10. Химические свойства многоатомных спиртов РЕАКЦИИ с :
- 11. СН – ОН СН2 –
- 12. Задание Получите гидроксид меди (II), путем
- 13. Взаимодействие глицерина с гидроксидом меди (II)
- 14. Получение 3CH2=CH2 + 2KMnO4 + 4H2O →
- 15. Применение этиленгликоля Антифризы – незамерзающие жидкости Пластиковые бутылки Синтетическое волокно лавсан
- 16. Применение глицерина Крема Мыло Помады Зубные пасты Кондитерские изделия Изделия из кожи Нитроглицерин Пластмассовые изделия
- 17. Применение многоатомных спиртов
- 18. Применение многоатомных спиртов
- 19. Выводы Во всех многоатомных спиртах гидроксильные группы
Слайд 2Вопросы для повторения
Какими способами может быть получен этиловый спирт?
Назовите условия промышленного
Слайд 3Задания
Напишите структурные формулы пропанола-2, 2,2-диметилпропанола-1;
На примере пропилового спирта охарактеризуйте химические свойства
Слайд 7Бесцветная, прозрачная, вязкая, сиропообразная жидкость,
сладкая на вкус.
не ядовит
t кип=
Неограниченно растворим в воде,
очень гигроскопичен
Физические свойства
глицерина
Слайд 8Физические свойства этиленгликоля
бесцветная вязкая жидкость со своеобразным запахом, сладкого вкуса ядовит
t
С водой смешивается в любых соотношениях, причем эти растворы имеют очень низкую температуру замерзания.
Слайд 10Химические свойства
многоатомных спиртов
РЕАКЦИИ с :
щелочными
металлами,
нерастворимыми
основаниями
РЕАКЦИИ с :
галогено-
водородами;
этерификация
РЕАКЦИИ:
горения,
окисления
РЕАКЦИЯ
Cu(OH)2
Слайд 11СН –
ОН
СН2 –
СН2 –
ОН
ОН
СН –
О
СН2 –
СН2 –
О
О
HO-NO2
HO-NO2
HO-NO2
-NO2
-NO2
-NO2
+ 3 H2O
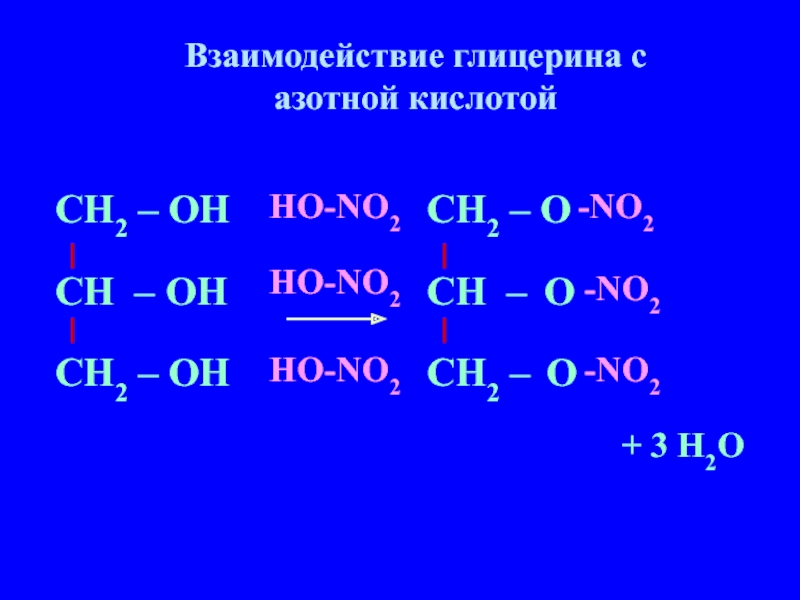
Взаимодействие глицерина с азотной кислотой
Слайд 12Задание
Получите гидроксид меди (II), путем сливания растворов гидроксида натрия и сульфата
Постарайтесь составить уравнение химической реакции.
Взаимодействие многоатомных спиртов с гидроксидом меди (II)
Осадок гидроксида меди растворяется и образуется темно-синий раствор глицерата меди (II).
Слайд 13Взаимодействие глицерина с гидроксидом меди (II)
Вывод: многоатомные спирты лучше реагируют с
СН2 –
СН2 –
СН2 –
О
О
ОН
+Cu(OH)2
НOH
Cu
Слайд 14Получение
3CH2=CH2 + 2KMnO4 + 4H2O → 3HO–CH2–CH2–OH + 2MnO2 + 2KOH
Этиленгликоль
из этилена различными способами
Глицерин (пропантриол -1,2,3) получают гидролизом
жиров или из пропилена
Слайд 15Применение этиленгликоля
Антифризы – незамерзающие жидкости
Пластиковые бутылки
Синтетическое волокно лавсан
Слайд 16Применение глицерина
Крема
Мыло
Помады
Зубные пасты
Кондитерские изделия
Изделия из кожи
Нитроглицерин
Пластмассовые изделия
Слайд 19Выводы
Во всех многоатомных спиртах гидроксильные группы находятся при разных атомах углерода;
число
свойства, общие с одноатомными спиртами, объясняются наличием функциональной группы ОН;
число гидроксильных групп в молекуле обусловило, в результате их взаимного влияния, появление у многоатомных спиртов новых свойств по сравнению с одноатомными спиртами (к примеру – взаимодействие с нерастворимыми основаниями).