- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Отримання нанопорошків. Класифікація. Фізичні методи отримання нанопорошків. . Хімічні методи отримання наноматеріалів презентация
Содержание
- 1. Отримання нанопорошків. Класифікація. Фізичні методи отримання нанопорошків. . Хімічні методи отримання наноматеріалів
- 2. Отримання нанопорошків. Класифікація. Фізичні методи отримання нанопорошків.
- 3. - порошкові методи; - методи
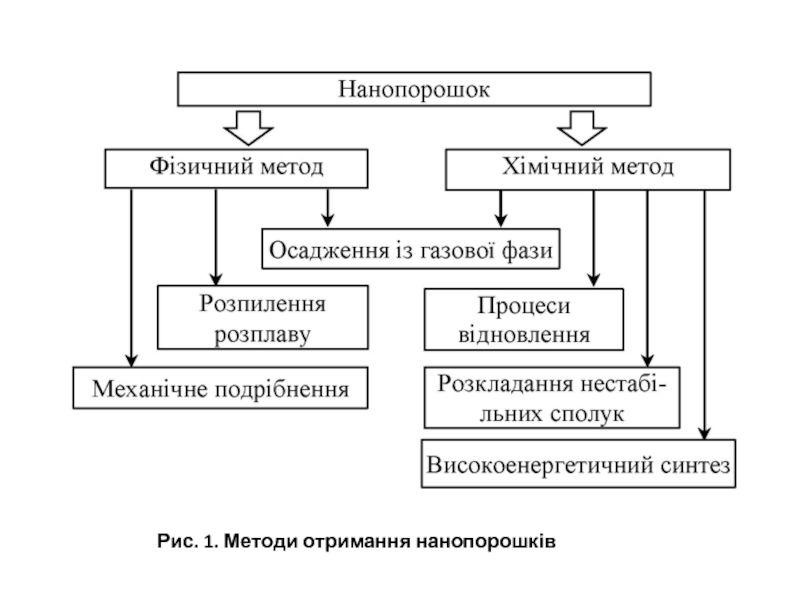
- 4. Рис. 1. Методи отримання нанопорошків
- 5. Таблиця 1. Основні методи отримання порошків для виготовлення наноматеріалів
- 6. 2. Фізичні методи отримання нанопорошків Осадження
- 7. Рис. 2. Класифікація дисперсних матеріалів за розміром дисперсної фази
- 8. При термічному випаровуванні напилюваний матеріал нагрівають до
- 9. Рис. 3. Схема отримання нанопорошків шляхом конденсації
- 10. 4. Випаровування в електричній дузі (arc-PVD-процес). Між
- 11. Розпилення розплаву. Ця група методів базується
- 12. а б Рис. 3. Принципова схема отримання
- 13. Рис. 4. Установка для отримання нанопо-рошку в
- 14. 3. Хімічні методи отримання наноматеріалів В даний
- 15. Хімічні методи отримання нанорозмірних матеріалів можна розділити
- 16. Зазвичай золь-гель метод включає в себе формування
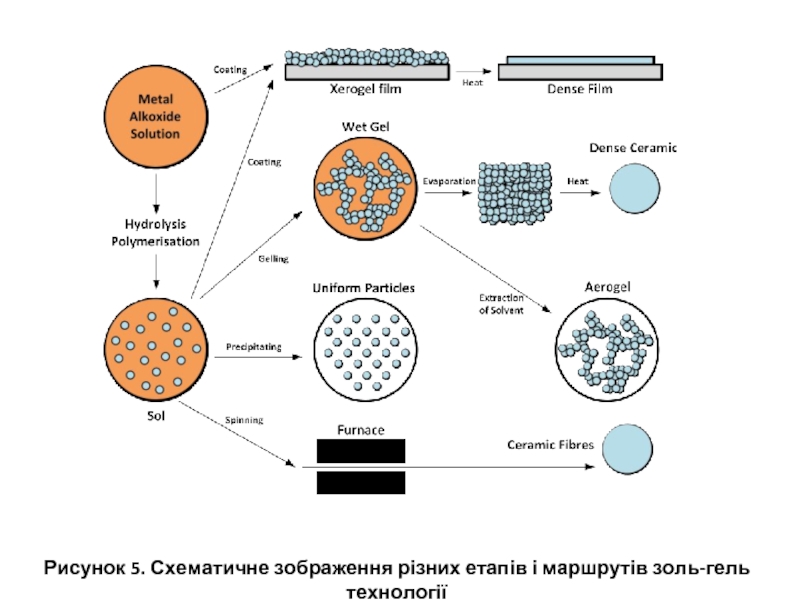
- 17. Рисунок 5. Схематичне зображення різних етапів і маршрутів золь-гель технології
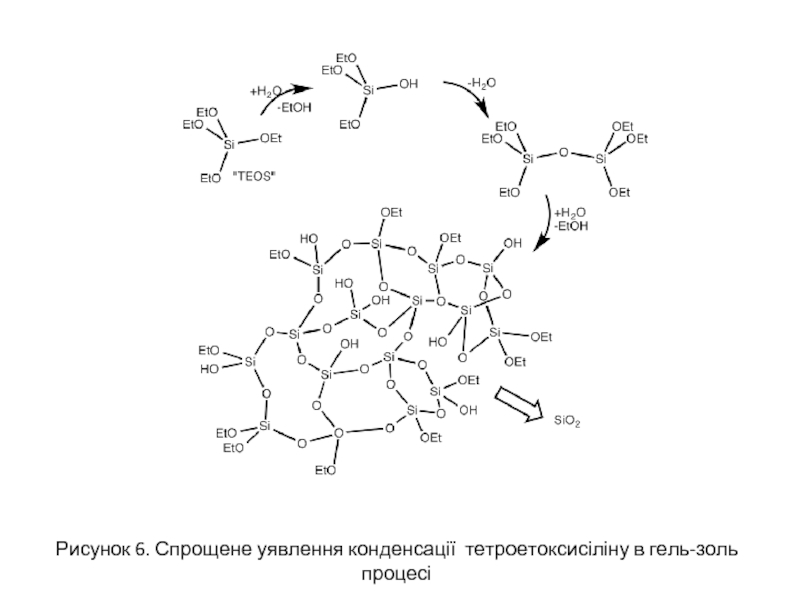
- 18. Рисунок 6. Спрощене уявлення конденсації тетроетоксисіліну в гель-золь процесі
- 19. Відновлення оксидів і інших твердих сполук металів
- 20. Вибір розчинника не обмежується лише водою, а
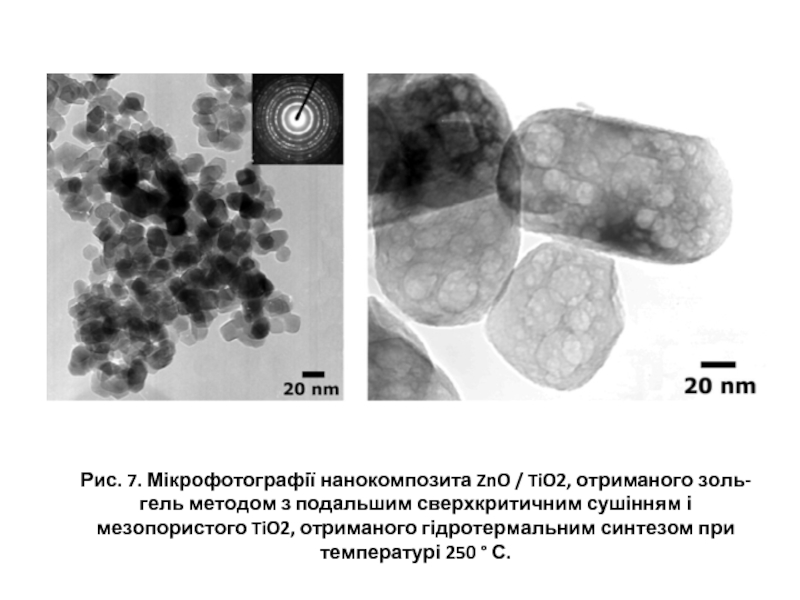
- 21. Рис. 7. Мікрофотографії нанокомпозита ZnO / TiO2,
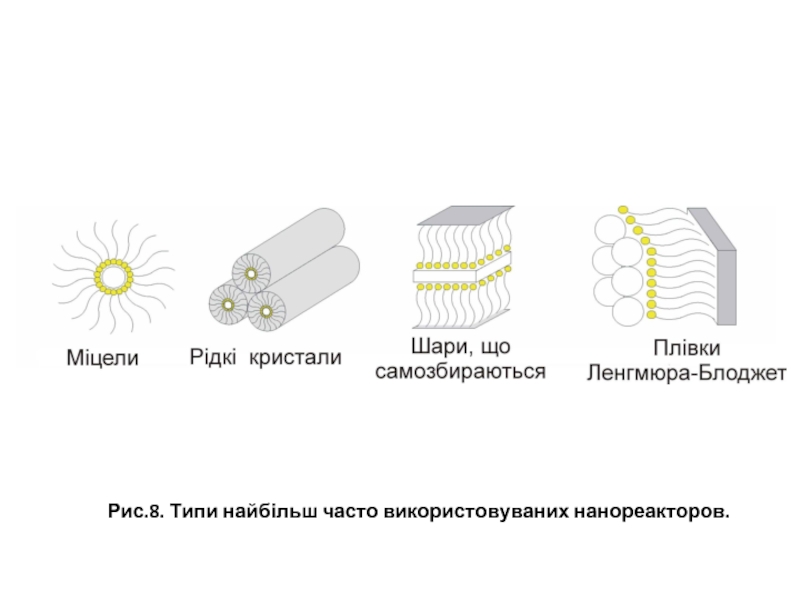
- 22. Рис.8. Типи найбільш часто використовуваних нанореакторов.
- 23. Формування просторово-обмеженою реакційної зони в колоїдних системах
- 24. Термічне випаровування. Процес термічного випаровування здійснюють у
- 25. До технологій на основі хімічних процесів належать:
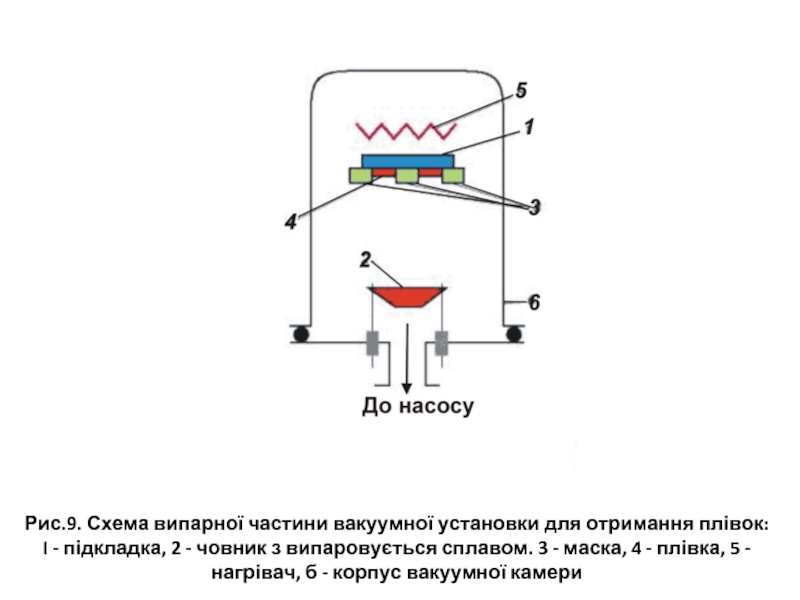
- 26. Рис.9. Схема випарної частини вакуумної установки для
- 27. Рис. 10. Схема формування наноструктури в аморфному
- 28. Питання для самоперевірки 1. Методи для отримання
Слайд 2Отримання нанопорошків. Класифікація. Фізичні методи отримання нанопорошків. . Хімічні методи отримання
У технологіях отримання наноматеріалів використовують два підходи. Ці підходи прийнято називати технологіями «зверху-вниз» і «знизу-вгору».
Нанотехнології типу «знизу-вгору» (англ. «Bottom-up» nanotechnology) - Технологія отримання наноструктурованих матеріалів, в якій реалізується утворення наночастинок з атомів і молекул, тобто досягається укрупнення вихідних елементів структури до частинок нанометрового розміру. Цей процес в основному відбувається шляхом самозборки або каталітичних хімічних реакцій. Вони поширені в біологічних системах і їх можна побачити на кожному кроці в живій природі. Наприклад, за допомогою біологічних каталізаторів - ферментів амінокислоти збираючись в послідовність формують живу тканину.
Нанотехнології типу «зверху-вниз» (англ. «Top-down» nanotechnology) - технологія отримання наноструктурованих матеріалів, в якій нанометровий розмір часток досягається за допомогою подрібнення крупних частинок, порошків або зерен твердого тіла. Наочним прикладом може служити процес літографії.
У вихідному стані НМ можуть являти собою порошок із наночастинок, тонкі плівки/покриття з кристалічною чи аморфною структурою та формені матеріали з поруватою або щільною структурою, що складаються із дрібнодисперсних зерен. В основу методів отримання НМ покладені фізичні або хімічні процеси, які поділяють на[1]:
Слайд 3- порошкові методи;
- методи отримання тонких плівок/покриттів;
- кристалізацію
- методи інтенсивної пластичної деформації;
- комплексні методи - використання декількох підходів.
1. Отримання нанопорошків. Класифікація.
Методи отримання нанопорошків повинні відповідати таким загальним вимогам (рис. 1 та табл..1):
- високій швидкості утворення центрів зародження частинок;
- повільному росту частинок;
- можливості контролю розміру частинок;
- найбільшому розміру частинок, що не перевищує 100 нм;
- малим значенням дисперсії, стабільності отримання частинок заданого розмірного діапазону;
- повторюваності хімічного і фазового складу частинок;
- контрольованості параметрів процесу отримання.
Слайд 62. Фізичні методи отримання нанопорошків
Осадження з газової фази. Ці методи
У залежності від типу методу і технологічних параметрів розмір частинок порошку може становити від 5 до 100 нм, класифікація дисперсних матеріалів наведена на рис. 2.
Змінюючи інертний газ у камері від гелію до ксенону при підтримці однакового значення тиску (змінюється густина газу), розмір частинок може змінюватися в декілька разів. За однакових умов випаровування частинки, отримані із тугоплавких металів, будуть мати менший розмір.
Фізичне осадження з газової фази скор., (англ. physical vapour deposition або PVD-process) - технологія нанесення покриттів (тонких плівок) в вакуумі з парової (газової) фази, при якій покриття виходить шляхом прямої конденсації пари, що наноситься.
Ці методи можна розділити на дві групи: 1) термічне випаровування і 2) іонно-плазмове розпилення.
Слайд 8При термічному випаровуванні напилюваний матеріал нагрівають до досить високої температури, при
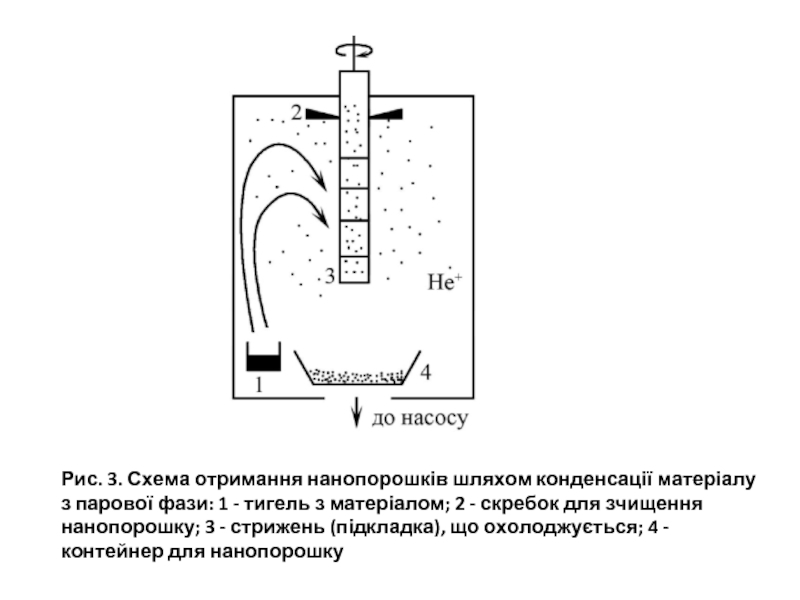
Масивний матеріал розігрівається (резистивним, високочастотно-індукційним, електронно-променевим, електродуговим, плазмовим або лазерним методами). Формування нанопорошку відбувається за такою схемою: підведення теплової енергії до матеріалу, який необхідно розпилити -> переведення його в газову фазу -> конденсація на охолоджену підкладку -> зчищення порошку в ємність для зберігання. Приклад установки наведено на рис. 3. Частинки порошку мають сферичну або ограновану форму і можуть бути металевими, інтерметалідними та неметалевими. Перевагою методу є отримання чистих порошків із вузьким розподілом частинок за розміром, а недоліком - низька продуктивність процесу, через відсутність установок великих розмірів для використання в промисловому виробництві.
За способами нагріву розрізняють наступні процеси.
1. Термічне випаровування (резистивний нагрів) (TVD-процес). У надвисокому вакуумі (≤1,3 · 10-8 Па) речовина термічно нагрівається до необхідної температури випаровування, при цьому її атоми і молекули потрапляють на підкладку, де відбувається їх конденсація.
2. Електронно-променеве випаровування (EBVD-процес). На зразок металу, що є анодом, спрямований потік електронів з енергією в декілька кілоелектронвольт, емітованих катодом, що призводить до неперервного випаровуванню атомів.
3. Лазерна абляція . Мішень опромінюється імпульсним УФ випромінюванням ексимерного або Nd:YAG лазера. Інтенсивність випромінювання становить 108-109 Вт/см2, тривалість - декілька наносекунд, що досить для абляції речовини (металів, оксидів металів) в точці нагріву мішені.
термін Ексімер (англ. excited dimer) позначає збуджений димер і позначає тип матеріалу, використовуваного як робоче тіло лазера. Nd: YAG лазер - твердотільний лазер, в якості активного середовища використовується алюмо-ітрієві гранат ( «YAG», Y3Al5O12) легований іонами неодиму (Nd).
винесення речовини з поверхні твердого тіла під впливом випромінювання
Слайд 9Рис. 3. Схема отримання нанопорошків шляхом конденсації матеріалу з парової фази:
Слайд 104. Випаровування в електричній дузі (arc-PVD-процес). Між катодом і анодом ініціюється
При іонно-плазмовому розпиленні поверхню мішені бомбардують атомами, іонами або молекулами, що мають енергію, що перевищує енергію зв'язку атомів мішені. Для бомбардування, як правило, використовують іони благородних газів, так як їх легко розганяти до потрібної енергії в електричному полі і вони хімічно інертні.
Різновидом методу термічного випаровування є вибуховий випар (випаровування «спалахом»), що застосовується для випаровування матеріалів складного складу (складної будови). При цій процедурі температуру підтримують значно вище необхідної для випаровування компонента з найменшим тиском пару, а матеріал подають у вигляді порошку або гранул за допомогою спеціального дозуючого пристрою. В результаті дрібні крупинки порошку випаровуються практично миттєво, і всі компоненти досягають підкладки одночасно, зберігаючи вихідну стехіометрію. Недоліками методу є значні витрати енергії, які приводять до високої собівартості порошку, нерівномірність розміру частинок, внаслідок чого виникає необхідність їх сортування. Через те, що частина матеріалу може не встигнути перейти в газову фазу, відбувається формування рідких крапель мікронних розмірів
В окрему групу можна умовно виділити наступні фізичні методи отримання наноматеріалів:
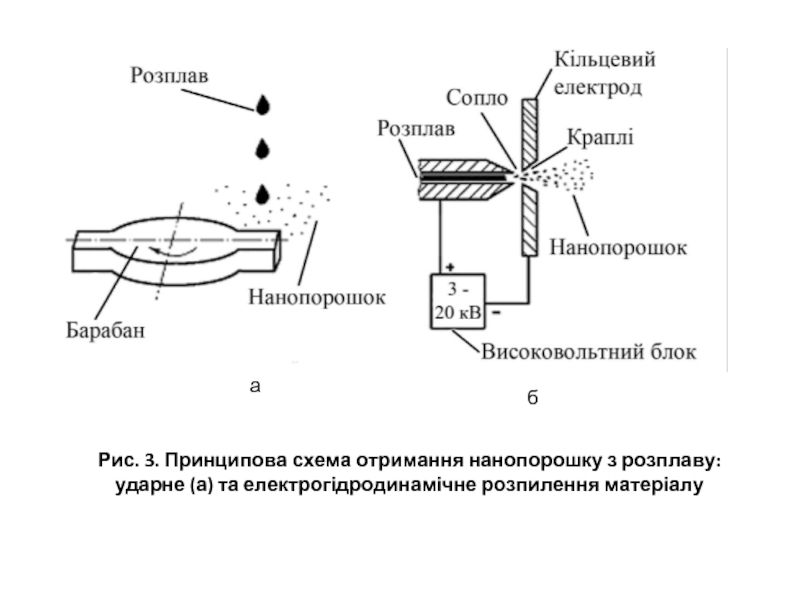
Слайд 11 Розпилення розплаву. Ця група методів базується на швидкому розпиленні та
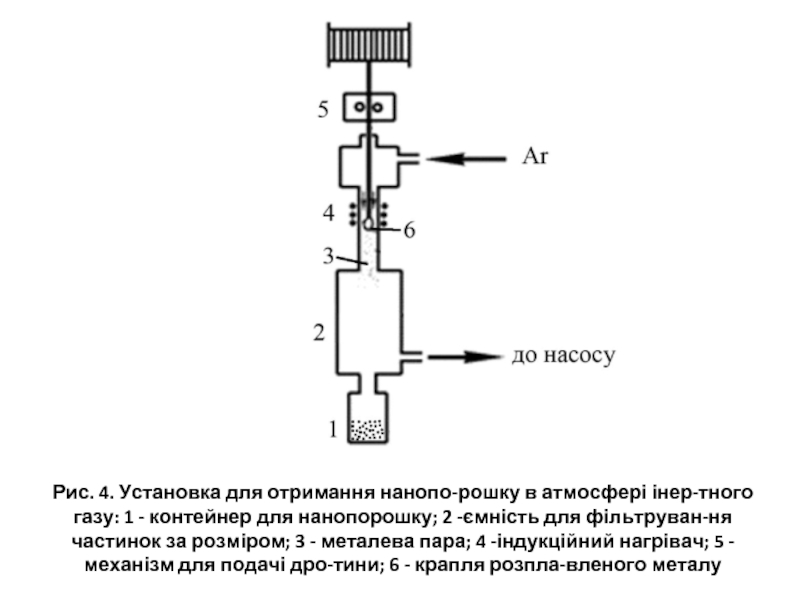
Випаровування в потоці інертного газу (левітаційно-струминний метод). При цьому методі випаровування металу проводиться в потоці інертного газу, наприклад із краплі розплаву на кінці дротини, що розігрівається високочастотним магнітним полем (рис. 4). Розмір сформованих частинок залежить від швидкості потоку газу - зі збільшенням швидкості він може зменшуватися від 500 до 10 нм.
Механічне подрібнення використовується для розмелювання (подрібнення) матеріалу на частинки малих розмірів (5-200 нм), із використанням жорен. Розмір частинок залежить від температури плавлення металу і часу подрібнення (від декількох годин до декількох діб). Чим вища температура плавлення металу і більший час розмелювання, тим менший розмір частинок може бути отриманий. Наприклад, за однакових умов подрібнення мінімальний розмір частинок алюмінію (температура плавлення 660 0C) становив 20 нм, а вольфраму (температура плавлення 3395 0C) - 6 нм. Основний недолік методу - забруднення порошку внаслідок зношення робочих частин устаткування
Слайд 12а
б
Рис. 3. Принципова схема отримання нанопорошку з розплаву: ударне (а) та
Слайд 13Рис. 4. Установка для отримання нанопо-рошку в атмосфері інертного газу: 1
Слайд 143. Хімічні методи отримання наноматеріалів
В даний час розроблені методи отримання наноматеріалів
Нерівноважність систем. Практично всі наносистеми термодинамічно нестійкі, і їх отримують в умовах, далеких від рівноважних, що дозволяє домогтися спонтанного зародкоутворення і уникнути зростання і агрегації сформувалися наночастинок.
Висока хімічна однорідність. Однорідність наноматериал забезпечується, якщо в процесі синтезу не відбувається поділу компонентів як в межах однієї наночастинки, так і між частинками.
Монодисперсність. Так як властивості наночастинок надзвичайно сильно залежать від їх розміру, для отримання матеріалів з хорошими функціональними характеристиками необхідно синтезувати частинки з досить вузьким розподілом за розмірами.
Однак виконання цих умов при синтезі наночастинок не завжди виявляється обов'язковим. Наприклад, розчини поверхнево активних речовин (міцелярні структури, плівки Ленгмюра-Блоджетт, рідкокристалічні фази), являються термодинамічно стабільними і тим не менш є основою для формування різноманітних наноструктур.
хімічної реакції, в яких беруть участь певні класи речовин. В іншу можна віднести різні варіанти електрохімічних реакцій.
Слайд 15Хімічні методи отримання нанорозмірних матеріалів можна розділити на групи, до одної
Метод осадження полягає в осадженні різних сполук металів з розчинів їх солей за допомогою осаджувачей. Продуктом осадження є гідроксиди металів. Регулюванням рН і температури розчину можливе створення оптимальних для отримання наноматеріалів умов осадження, при яких підвищуються швидкості кристалізації і утворюється високодисперсний гідроксид. Потім продукт прокаливают і, при необхідності, відновлюють. Отримувані нанопорошки металів мають розмір часток від 10 до 150 нм. Форма окремих частинок зазвичай близька до сферичної. Однак, цим методом, варіюючи параметри процесу осадження, можна отримувати порошки голчастої, лускатої, неправильної форми.
Золь-гельний метод
Традиційно під терміном "золь-гель метод" розуміють сукупність стадій, що включають приготування розчину прекурсору, послідовне перетворення його спочатку в золь, а потім в гель за рахунок процесів гідролізу і конденсації, подальше «старіння», висушування і термообробку продукту. Однак, останнім часом цей термін часто використовується для позначення процесів, в яких відсутня одна з цих стадій. При уявній простоті і універсальності цієї схеми властивості оксидного матеріалу виявляються надзвичайно чутливими до умов процесу на всіх його етапах.
Слайд 16Зазвичай золь-гель метод включає в себе формування металлооксополімерних ланцюгів - золю
Слайд 19Відновлення оксидів і інших твердих сполук металів є одним з найбільш
Гідротермальний і сольвотермальний синтез наночастинок.
В основі гидротермального методу синтезу лежить висока розчинність великої кількості неорганічних речовин у воді при підвищених температурі і тиску і можливість подальшої кристалізації розчиненого матеріалу з рідкої фази. Висока температура води відіграє важливу роль у трансформації матеріалу прекурсора, оскільки при цьому створюється підвищений тиск парів, а сама структура води відрізняється від такої при кімнатній температурі. До того ж при високій температурі змінюються властивості самих реагентів (розчинність, швидкості дифузії, реакційна здатність). Контроль тиску парів, температури і часу реакції надає широкі можливості для синтезу високоякісних наночастинок і нанотрубок. В ході процесу ці параметри можуть варіюватися для досягнення максимально високої швидкості спонтанного зародкоутворення і вузького розподілу наночастинок за розмірами.
Слайд 20Вибір розчинника не обмежується лише водою, а включає й інші полярні
Гідротермальний синтез ведеться, як правило, при температурах 100-370 ° С (критична точка води: 374,2 ºС, 21,4 МПа). У разі використання висококиплячих розчинників температура синтезу може досягати 600 ºС. При більш високих температурах реалізують синтез в надкритичних умовах.
Методи сольвотермального синтезу і синтезу в надкритичних розчинниках дозволяють отримувати самі різні типи наноструктур, починаючи від простих речовин (Ge, Si), оксидів і халькогенидов металів, таких як SiO2, TiO2, ZnO, PbS, ZnS, CdS і закінчуючи складними оксидними сполуками (SrFe12O19, LaMnO3, і т.д.) і наноструктурами (цеоліти, мезопористі оксиди) . Нанокристали, отримані цим методом звичайно добре закристалізовані, але мають широкий розподіл за розмірами.
Колоїдні нанореактори
Колоїдні розчини наночастинок (наприклад, колоїдні розчини золота - пурпурне золото) були першими відомими людині наноструктурами. Вони застосовувалися в технології задовго до відкриття поверхнево-активних речовин - основних стабілізаторів колоїдних розчинів.
Синтез наноструктур в просторово-обмежених колоїдних системах, так званих нанореакторах, є очевидним, і, на сьогоднішній день, найбільш поширеним підходом до отримання нанорозмірних систем. Як колоїдні нанореактори найбільш часто використовують звичайні та звернені (обратные) міцели, рідкі кристали, адсорбційні шари, плівки Ленгмюра-Блоджетт, мікроемульсії і т.д (рис. 5.1).
Слайд 21Рис. 7. Мікрофотографії нанокомпозита ZnO / TiO2, отриманого золь-гель методом з
Слайд 23Формування просторово-обмеженою реакційної зони в колоїдних системах відбувається, головним чином, в
4 Методи отримання тонких плівок/покриттів
Технологічні методи отримання тонких плівок і покриттів умовно можна розділити на методи, зав тоновані на фізичних і хімічних процесах.
До першої групи відносять:
- осадження із газової фази (PVD – Physical Vapour Deposition): термічне випарування, катодне та магнетронне розпилення, іонна імплантація;
- газотермічне (плазмове) напилення;
- лазерні методи: легування або імплантація, аморфізація поверхні з використанням лазерного випромінювання. Недоліками цієї групи методів є складність розроблення
технологічного режиму для конкретного випадку отримання покриття, особливо для одержання покриттів із сполук, де необхідна висока точність хімічного складу; необхідність спеціальної підготовки покриття поверхонь.
Слайд 24Термічне випаровування. Процес термічного випаровування здійснюють у вакуумі при тиску порядку
Метод термічного випаровування досить широко використовується під час виробництва жорстких магнітних дисків для комп’ютерів. Підкладкою є алюмінієвий диск із шорсткістю менше 20 нм із нанесеним аморфним нікель-фосфорним підшаром товщиною порядку 20 мкм (для поліпшення адгезії і компенсації відмінностей коефіцієнтів термічного розширення підкладки та покриття). Спочатку напилюється проміжний металевий шар, наприклад Ni-Fе, товщиною 500-1000 нм, а вже потім - основний шар з магнітного матеріалу, наприклад сплаву на основі Co або Co-Cr, товщиною 100-500 нм. Поверх всього покриття наноситься зносостійкий захисний вуглецевий шар товщиною 30-50 нм. Також термічне напилення використовують і при виробництві CD-дисків. На диск з пластмаси наносять алюмінієве основне покриттів з товщиною нанометрового діапазону. В обох випадках для забезпечення високої чистоти матеріалів тиск у вакуумній камері становить не менше 10-5 Па.
Слайд 25До технологій на основі хімічних процесів належать:
- хімічне осадження із
- осадження з використанням плазми тліючого розряду;
- світлова та електронна літографія;
- осадження із розчинів;
- хімічне та електрохімічне окиснення (анодування).
Ця група методів базується на осадженні плівок на поверхню нагрітих деталей, де в газоподібному стані перебу- вають сполуки металів. Найбільш оптимальне проходження хімічних реакцій відбувається найчастіше при температурах 500-1500 оС. Осадження, як правило, проводять у спеціальній камері при зниженому тиску за допомогою використання хімічних реакцій відновлення, піролізу, дис-пропорціонування. У ряді випадків можуть використовуватися реакції взаємодії основного газоподібного реагенту з додатковим. Найбільш часто використовують сполуки карбонілів, галогенідів, металоорганічні сполуки.
5 Кристалізація аморфних сплавів
Аморфні металеві сплави характеризуються відсутністю дальнього порядку атомів, що досягається надшвидким (≥ 106 К/с) охолодженням підкладки, на яку спрямовується матеріал в газоподібному, рідкому чи іонізованому стані. Можливість отримання аморфного стану визначається хімічним складом і швидкістю охолодження. Для створення нанокристалічної структури в аморфному сплаві він підлягає спеціальній термообробці. При цьому процес виконується таким чином, щоб виникала велика кількість центрів кристалізації, але швидкість росту кристалітів була низькою.
Слайд 26Рис.9. Схема випарної частини вакуумної установки для отримання плівок: I -
Слайд 27Рис. 10. Схема формування наноструктури в аморфному сплаві системи Fe-Cu-Nb- Si-B
Слайд 28Питання для самоперевірки
1. Методи для отримання наноматеріалів та вимоги до них.
2.
3. Методи отримання нанопорошків з найменшим/найбільшим розміром частинок, переваги і недоліки.
4. Опишіть метод отримання нанопорошку з газової фази.
5. Які фактори впливають на дисперсність матеріалів?
6. Які існують методи отримання тонких плівок/покриттів?
7. Яким чином можна отримати аморфний сплав?
8. Переваги і недоліки методу інтенсивної пластичної деформації.