- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химические соединения в живых организмах. Неорганические вещества презентация
Содержание
- 1. Химические соединения в живых организмах. Неорганические вещества
- 2. Вещества, входящие в состав живых организмов: Неорганические соединения Органические соединения
- 3. Неорганические соединения Вода Минеральные соли Неорганические (минеральные) кислоты и др.
- 4. Вода Содержание воды в живых организмах составляет 60-75% их массы.
- 5. Вода У медузы – 98% массы тела вода.
- 6. Вода В листьях и сочных плодах растений – до 98%.
- 7. Вода У человека в сером веществе головного мозга 85% воды.
- 8. Вода В костной ткани человека – 22% воды.
- 9. Вода Наибольшее содержание воды в организме наблюдается
- 10. Вода Без употребления воды человек может прожить не более 5-7 дней
- 11. Вода Молекула воды состоит из двух атомов водорода, соединенных ковалентными полярными связями с атомом кислорода.
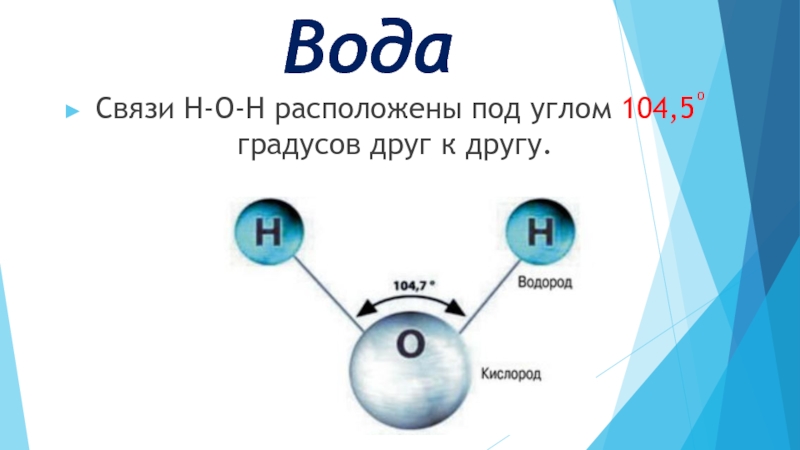
- 12. Вода Связи Н-О-Н расположены под углом 104,5 градусов друг к другу. о
- 13. Вода Молекула является полярной, т.к. кислород обладает
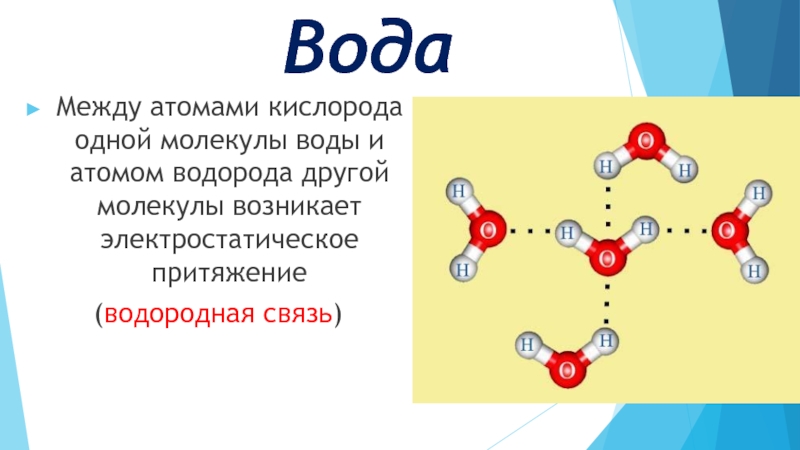
- 14. Вода Между атомами кислорода одной молекулы воды
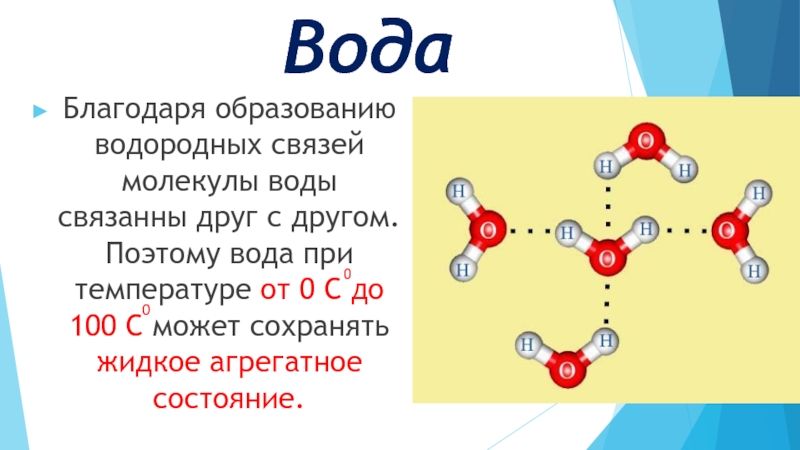
- 15. Вода Благодаря образованию водородных связей молекулы воды
- 16. Вода Вода определяет объем клеток и внутриклеточное давление (тургор)
- 17. Вода Благодаря полярности молекулы воды способны формировать
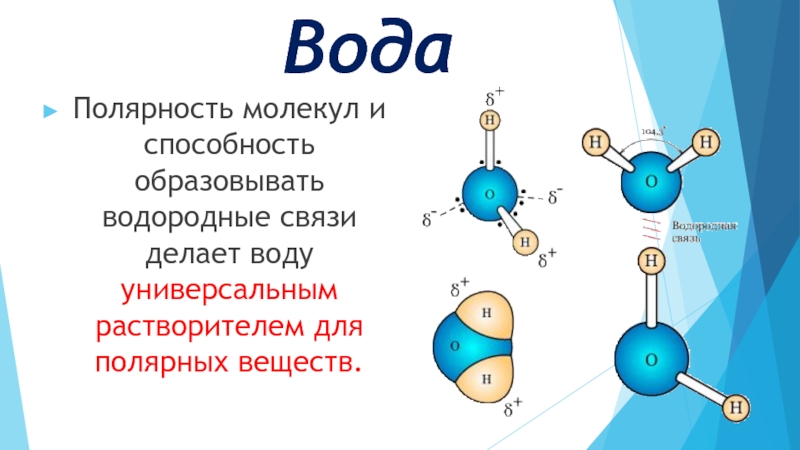
- 18. Вода Полярность молекул и способность образовывать водородные связи делает воду универсальным растворителем для полярных веществ.
- 19. Соединения (в зависимости от растворимости в воде): Гидрофильные Гидрофобные
- 20. Гидрофильные вещества – это вещества хорошо растворимые
- 21. Гидрофобные вещества – это вещества не растворимые
- 22. Вода Вода как растворитель принимает участие в явлениях осмоса.
- 23. Осмос – это перемещение молекул воды через
- 25. Изотонические растворы – это растворы, осмотическое давление которых такое же, как в клетках.
- 26. Гипертонические растворы – это растворы, осмотическое давление которых выше, чем в клетках.
- 27. Гипотонические растворы – это растворы, осмотическое давление которых ниже, чем в клетках.
- 28. Вода Свойственна высокая теплоемкость – способность поглощать большое количество теплоты при незначительных изменениях собственной температуры.
- 29. Домашнее задание: Параграф 2, стр. 11-15
Слайд 2Вещества, входящие в состав живых организмов:
Неорганические соединения
Органические соединения
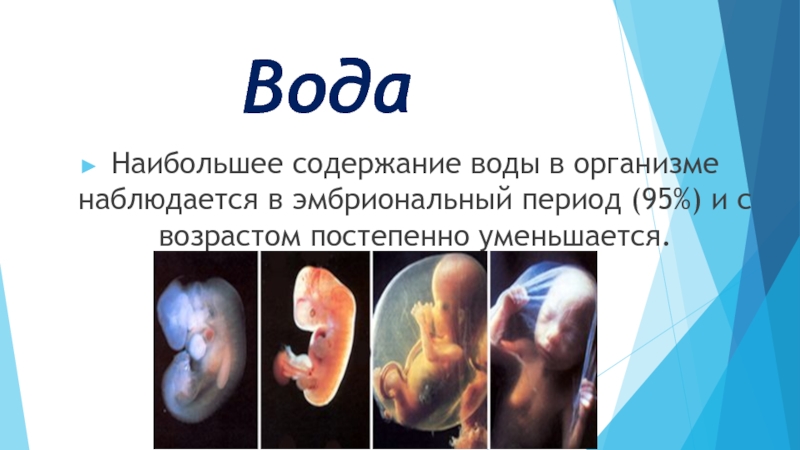
Слайд 9Вода
Наибольшее содержание воды в организме наблюдается в эмбриональный период (95%) и
с возрастом постепенно уменьшается.
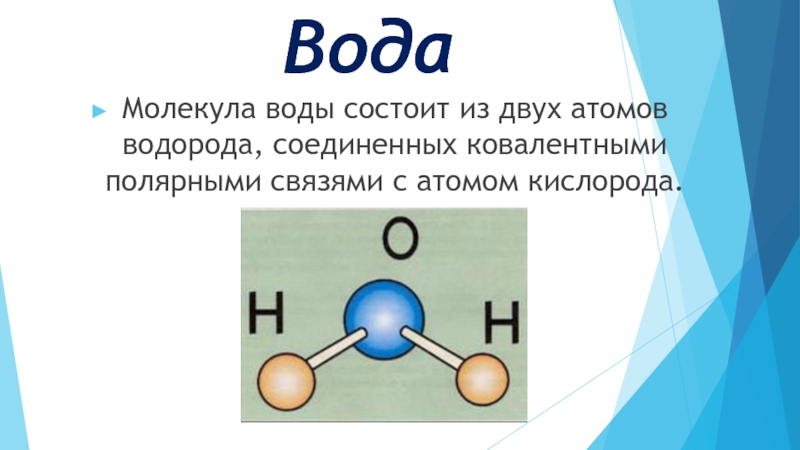
Слайд 11Вода
Молекула воды состоит из двух атомов водорода, соединенных ковалентными полярными связями
с атомом кислорода.
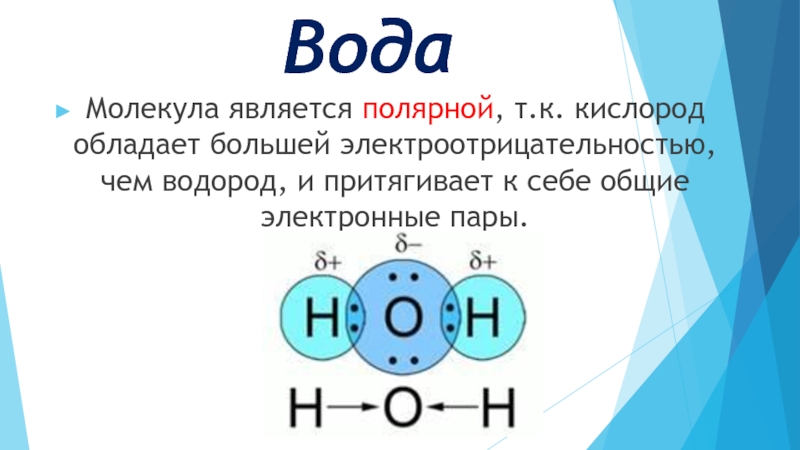
Слайд 13Вода
Молекула является полярной, т.к. кислород обладает большей электроотрицательностью, чем водород, и
притягивает к себе общие электронные пары.
Слайд 14Вода
Между атомами кислорода одной молекулы воды и атомом водорода другой молекулы
возникает электростатическое притяжение
(водородная связь)
(водородная связь)
Слайд 15Вода
Благодаря образованию водородных связей молекулы воды связанны друг с другом. Поэтому
вода при температуре от 0 С до 100 С может сохранять жидкое агрегатное состояние.
0
0
Слайд 17Вода
Благодаря полярности молекулы воды способны формировать так называемые гидратные оболочки вокруг
ионов и полярных молекул.
Слайд 18Вода
Полярность молекул и способность образовывать водородные связи делает воду универсальным растворителем
для полярных веществ.
Слайд 20Гидрофильные вещества – это вещества хорошо растворимые в воде.
Моно- и дисахариды
Соли
Низшие
спирты
Низшие карбоновые кислоты
Минеральные соли
Низшие карбоновые кислоты
Минеральные соли
Слайд 21Гидрофобные вещества – это вещества не растворимые в воде.
Высшие карбоновые кислоты
Жиры
Некоторые
белки
Слайд 23Осмос – это перемещение молекул воды через полупроницаемую мембрану из области
с меньшей концентрацией растворенных веществ в область с более высокой концентрацией этих веществ.
Слайд 25Изотонические растворы – это растворы, осмотическое давление которых такое же, как
в клетках.
Слайд 28Вода
Свойственна высокая теплоемкость – способность поглощать большое количество теплоты при незначительных
изменениях собственной температуры.