- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Коллоидная химия презентация
Содержание
- 1. Коллоидная химия
- 2. Признаки объектов коллоидной химии Коллоидную химию иногда называют физикохимией дисперсных систем
- 3. Виды дисперсных систем
- 4. Классификация по степени взаимодействия дисперсной фазы
- 5. Особенности коллоидных систем 2. Термодинамическая неустойчивость 3. Невоспроизводимость 4. Способность к структурообразованию
- 6. Получение дисперсных систем -измельчение крупных образцов вещества до частиц дисперсных размеров;
- 7. Позволяют достигать более тонкого измельчения
- 8. ИНТЕНСИФИКАЦИЯ ПРОЦЕССОВ ДИСПЕРГИРОВАНИЯ ВВЕДЕНИЕМ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ
- 9. основаны на ассоциации молекул в
- 10. Стадии конденсации 2. Рост зародышей. 3. Формирование слоя стабилизатора (ДЭС).
- 11. Физические конденсационные методы
- 12. СТРОЕНИЕ КОЛЛОИДНОЙ МИЦЕЛЛЫ Согласно общепринятой мицеллярной
- 13. СТРОЕНИЕ КОЛЛОИДНОЙ МИЦЕЛЛЫ Строение мицеллы может
- 14. Некоторая часть противоионов адсорбируется на поверхности
- 15. Правило Панета-Фаянса Определить
- 16. Химические конденсационные методы
- 17. {[mFe4[Fe(CN)6]3·n[Fe(CN)6]4-]4n-·4 (n-х)K+}4x-·4xK+ {[m Fe4[Fe(CN)6]3·nFe3+] 3n+·3(n-х)Сl-}3x+·3xCl-
- 19. 3. Реакции окисления Образование золя
- 20. 4. Реакции гидролиза Получение золя гидроксида
- 21. Метод пептизации
- 22. Низкомолекулярные примеси разрушают коллоидные системы.
- 23. Опреснение методом электродиализа. Под действием электрического
- 24. Низкомолекулярные примеси разрушают коллоидные системы.
- 25. Молекулярно-кинетические свойства дисперсных систем Запорожский государственный медицинский университет Кафедра физической и коллоидной химии
- 26. Броуновское движение Коллоидные частицы по молекулярно-кинетическим
- 27. Броуновское движение При столкновении частиц происходит обмен
- 28. Диффузия Диффузия – самопроизвольный процесс выравнивания концентрации
- 29. Осмотическое давление Осмотическое давление в коллоидных системах
- 30. Седиментация Седиментацией (от лат. sedimentum – осадок)
- 31. Седиментационный анализ Для проведения седиментационного анализа кинетически
- 32. Ультрацентрифуги Современные ультрацентрифуги дают возможность получить центробежную
- 33. Оптические свойства дисперсных систем Запорожский государственный медицинский университет Кафедра физической и коллоидной химии
- 34. Рассеяние света Это наиболее характерное оптическое
- 35. Рассеяние света Тиндаль обнаружил, что при
- 36. Электрические свойства дисперсных систем Запорожский государственный медицинский университет Кафедра физической и коллоидной химии
- 37. ДЭС. Образование двойного электрического слоя Существование ДЭС
- 38. При погружении металлической пластинки в воду часть
- 39. Двойной электрический слой 2-й вариант. При образовании
- 40. Двойной электрический слой 3-й вариант. При ориентации
- 41. Строение ДЭС. Впервые представление о ДЭС было
- 43. Строение ДЭС По современным представлениям (теория Штерна)
- 44. В пределах ДЭС действует электрическое поле,
- 45. Для характеристики электрических свойств поверхности используют
- 46. Электрокинетические явления. Классификация. Электрокинетические явления 1-го рода
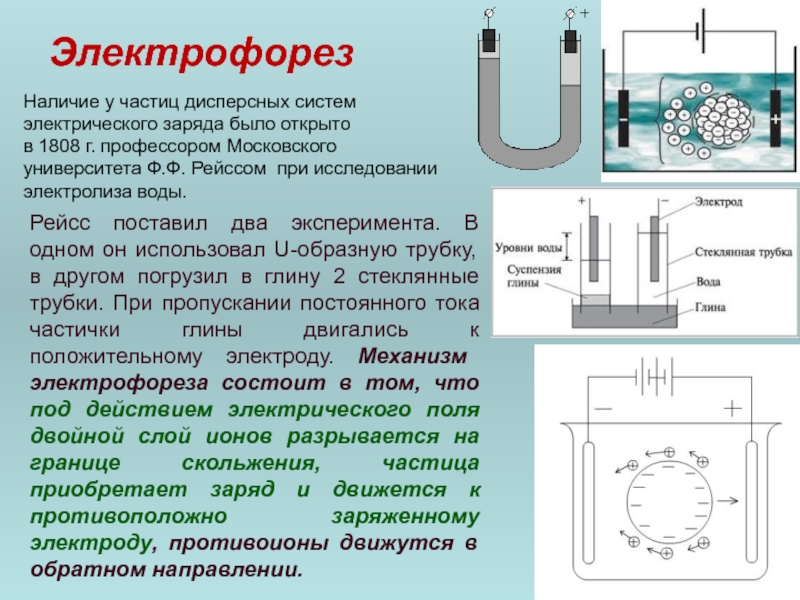
- 47. Электрофорез Наличие у частиц дисперсных систем электрического
- 48. Электрофорез Скорость движения частиц дисперсной фазы при
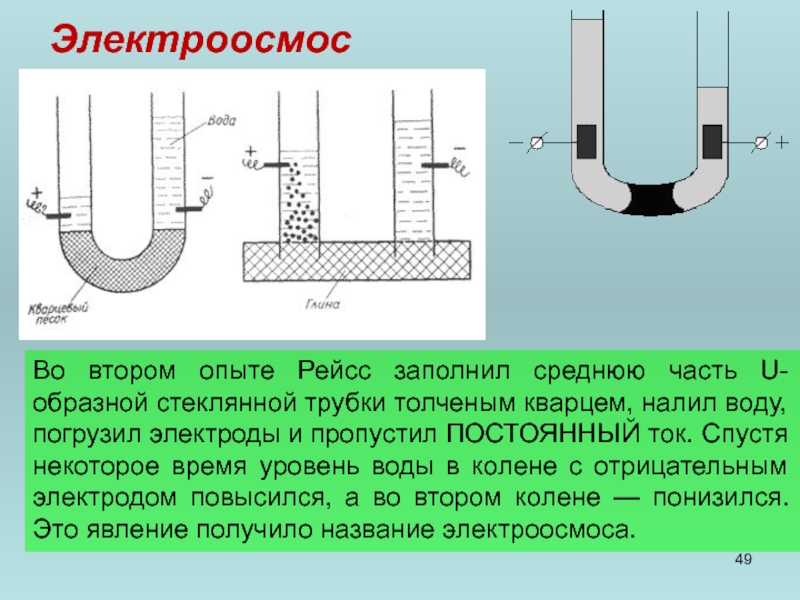
- 49. Электроосмос Во втором опыте Рейсс заполнил среднюю
- 50. Потенциал протекания и седиментации Потенциал
- 51. Устойчивость и коагуляция коллоидных систем Запорожский государственный
- 52. Устойчивость дисперсных систем По предложению Н.П.
- 53. Коагуляция процесс слипания коллоидных частиц с образованием
- 54. Коагуляция золей электролитами Все электролиты при
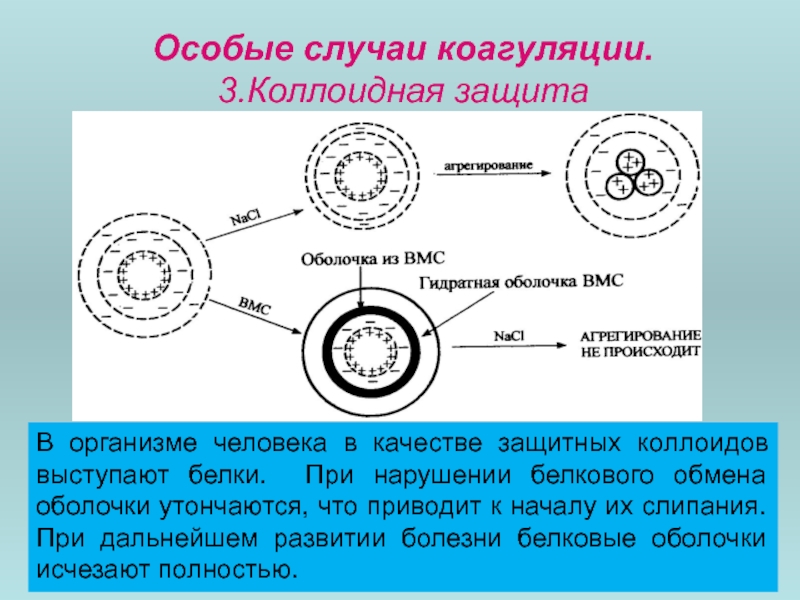
- 55. Особые случаи коагуляции. 3.Коллоидная защита
Слайд 1Запорожский государственный
медицинский университет
Кафедра физической и
коллоидной химии
КОЛЛОИДНАЯ ХИМИЯ
Слайд 2
Признаки объектов коллоидной химии
Коллоидную химию иногда называют
физикохимией дисперсных систем
Слайд 4
Классификация по степени взаимодействия дисперсной фазы с дисперсионной средой
Лиофильные - системы
Лиофобные - дисперсная фаза слабо взаимодействует с дисперсионной средой.
Гидрофильная (а) и гидрофобная (б) поверхности в трёхфазной системе вода - твёрдое тело - воздух; 1 - вода; 2 - твёрдое тело; 3 - воздух; a - краевой угол смачивания.
Слайд 5
Особенности коллоидных систем
2. Термодинамическая неустойчивость
3. Невоспроизводимость
4. Способность к структурообразованию
Слайд 6
Получение дисперсных систем
-измельчение крупных образцов вещества до частиц дисперсных размеров;
Слайд 8ИНТЕНСИФИКАЦИЯ ПРОЦЕССОВ ДИСПЕРГИРОВАНИЯ ВВЕДЕНИЕМ
ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ И ИОНОВ ЭЛЕКТРОЛИТОВ
ИСПОЛЬЗУЕТСЯ, ТАКЖЕ, ДЛЯ
ДИСПЕРСНЫХ СИСТЕМ
Механизм действия заключается в образовании на
границе раздела частица-среда адсорбционных
слоев.
Интенсификация диспергирования
Слайд 9
основаны на ассоциации молекул в агрегаты из истинных растворов;
используют для
не требуют затраты внешней работы;
появление новой фазы происходит при пересыщении среды.
Конденсационные методы
Слайд 12
СТРОЕНИЕ КОЛЛОИДНОЙ МИЦЕЛЛЫ
Согласно общепринятой мицеллярной теории золь состоит из 2-х частей:
Мицелла
Интермицеллярная жидкость – дисперсионная среда, разделяющая мицеллы, в которой растворены электролиты, не электролиты и ПАВ.
Слайд 13
СТРОЕНИЕ КОЛЛОИДНОЙ МИЦЕЛЛЫ
Строение мицеллы может быть рассмотрено лишь в первом приближении,
Слайд 14
Некоторая часть противоионов адсорбируется на поверхности ядра, образуя т.н. адсорбционный слой
При избытке одного из реагентов микрокристалл адсорбирует его ионы не образующие осадок. В результате этого микрокристалл приобретает заряд; ионы, сообщающие ему этот заряд, называются потенциалопределяющими, а сам заряженный кристалл – ядром мицеллы.
Заряженное ядро притягивает из раствора ионы с противоположным зарядом – противоионы; на поверхности раздела фаз образуется двойной электрический слой.
I
Слайд 15Правило Панета-Фаянса
Определить знак заряда поверхности AgI(крист.) полученного по реакции:
АgNО3(р) +
а) nАgNО3 = nКI : поверхность осадка не заряжена;
б) nАgNO3 > nКI : в) nАgNО3 < nКI :
избыток АgNO3 ⬄ Аg+ + NО3- избыток КI ⬄ К+ + I-
АgI + АgI -
+ -
+ -
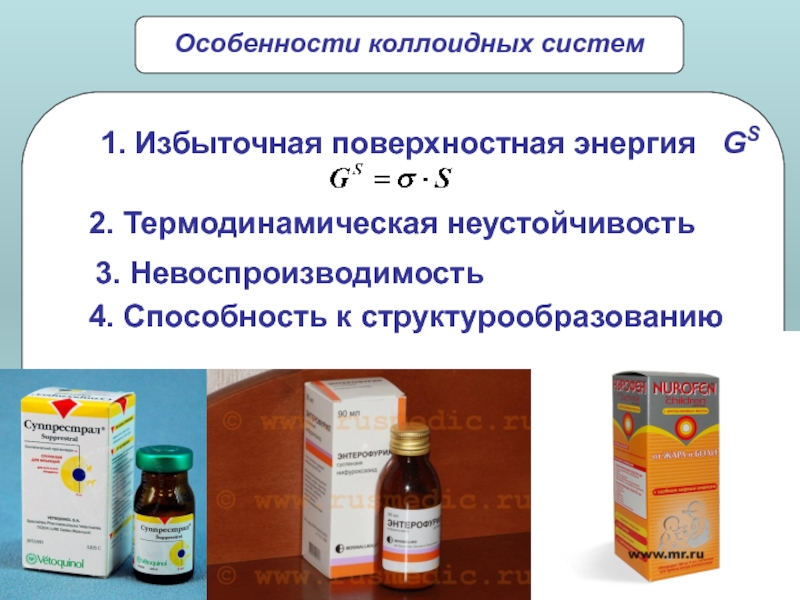
Слайд 17{[mFe4[Fe(CN)6]3·n[Fe(CN)6]4-]4n-·4 (n-х)K+}4x-·4xK+
{[m Fe4[Fe(CN)6]3·nFe3+] 3n+·3(n-х)Сl-}3x+·3xCl-
Слайд 20
4. Реакции гидролиза
Получение золя гидроксида железа.
FeCl3 + 3H2O = Fe(OH)3 ↓
Cтроение мицеллы:
Слайд 22
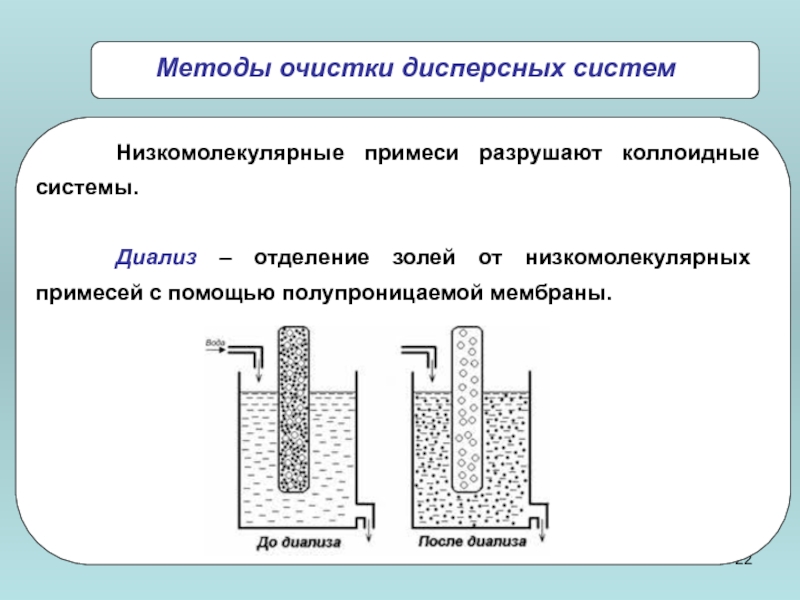
Низкомолекулярные примеси разрушают коллоидные системы.
Диализ – отделение золей от низкомолекулярных
Методы очистки дисперсных систем
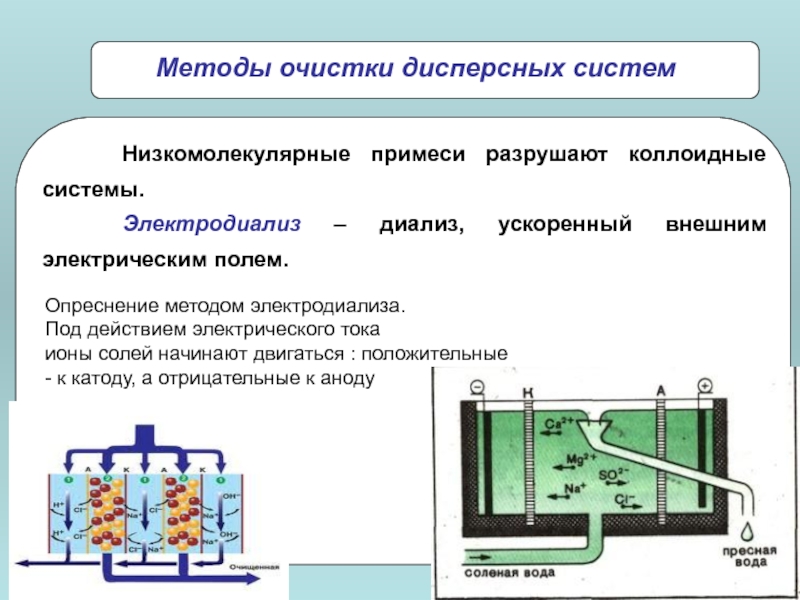
Слайд 23Опреснение методом электродиализа.
Под действием электрического тока
ионы солей начинают двигаться
- к катоду, а отрицательные к аноду
Низкомолекулярные примеси разрушают коллоидные системы.
Электродиализ – диализ, ускоренный внешним электрическим полем.
Методы очистки дисперсных систем
Слайд 24
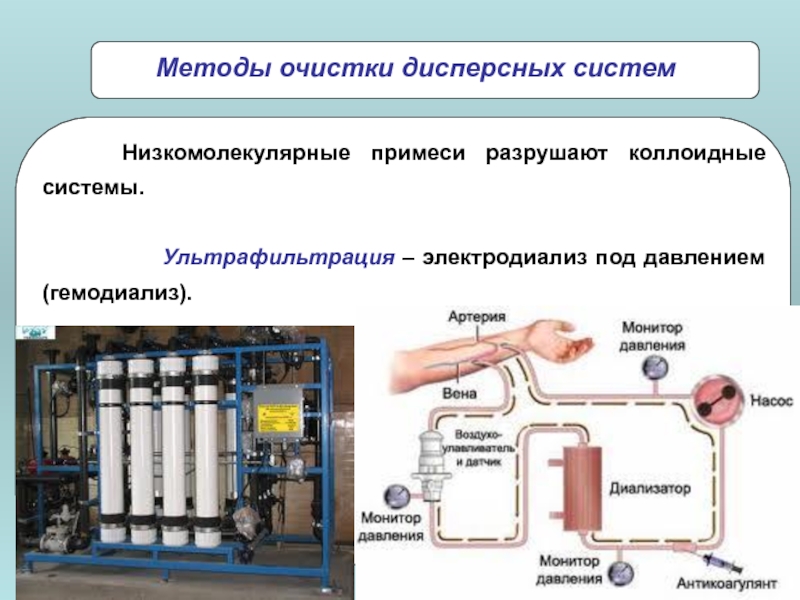
Низкомолекулярные примеси разрушают коллоидные системы.
Ультрафильтрация – электродиализ под давлением (гемодиализ).
Методы
Слайд 25Молекулярно-кинетические свойства дисперсных систем
Запорожский государственный
медицинский университет
Кафедра физической и
коллоидной химии
Слайд 26Броуновское
движение
Коллоидные частицы по молекулярно-кинетическим свойствам принципиально не отличаются от истинных
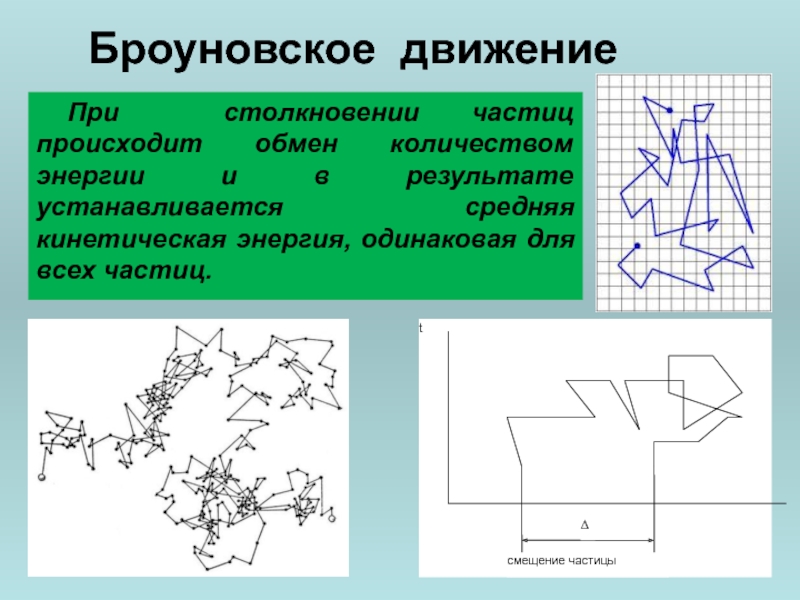
Слайд 27Броуновское движение
При столкновении частиц происходит обмен количеством энергии и в результате
Слайд 28Диффузия
Диффузия – самопроизвольный процесс выравнивания концентрации частиц по всему объему раствора
Эйнштейн, изучая броуновское движение, установил связь коэффициента диффузии – D со средним сдвигом:
Эйнштейн показал, что коэффициент диффузии D связан с размерами диффундирующих частиц уравнением:
r – радиус сферических частиц, размер которых намного больше, чем размер молекул растворителя
Слайд 29Осмотическое давление
Осмотическое давление в коллоидных системах составляет очень малую величину, трудно
Осмотическое давление в коллоидных системах убывает обратно пропорционально кубу радиуса частиц:
– осмотическое давление в золях одного итого же вещества с различной дисперсностью частиц
Слайд 30Седиментация
Седиментацией (от лат. sedimentum – осадок) называют процесс оседания частиц дисперсной
Всплывание частиц носит название обратной седиментации.
Скорость оседания частиц подчиняется закону Стокса:
ρ, ρ0 - плотности частиц и среды;
ή вязкость среды;
r- радиус;
g-ускорение силы тяжести
Если разность ρ-ρ0 имеет знак «-», частицы легче среды и всплывают
Слайд 31Седиментационный анализ
Для проведения седиментационного анализа кинетически устойчивых систем с целью определения
Русский ученый А.В. Думанский (1912) предложил подвергать коллоидные системы центрифугированию.
Сведберг (1923г.) разработал специальные центрифуги с огромным числом оборотов, названные ультрацентрифугами.
Слайд 32Ультрацентрифуги
Современные ультрацентрифуги дают возможность получить центробежную силу, превышающую ускорение силы тяжести
Современная ультрацентрифуга – сложный аппарат, центральная часть которого ротор (с частотой вращения 20-60000 об/мин и выше).
Слайд 33Оптические свойства дисперсных систем
Запорожский государственный
медицинский университет
Кафедра физической и
коллоидной химии
Слайд 34Рассеяние
света
Это наиболее характерное оптическое свойство для коллоидных систем. Свет рассеивается
Это явление наблюдал Фарадей (1857) при исследовании золя золота. Описано явление Тиндалем в 1868 году.
Через чистые жидкости и молекулярные растворы свет просто проходит. Через коллоидно-дисперсные системы луч света, встречая на своем пути частицу, не отражается, как бы огибает ее, отклоняется и несколько изменяет свое направление (дифракция).
Фарадей
Тиндаль
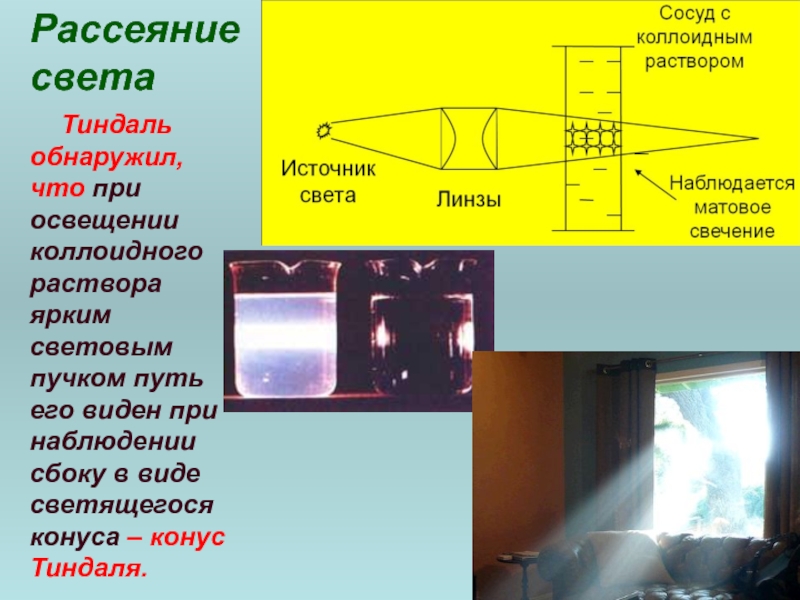
Слайд 35Рассеяние
света
Тиндаль обнаружил, что при освещении коллоидного раствора ярким световым пучком
Слайд 36Электрические свойства дисперсных систем
Запорожский государственный
медицинский университет
Кафедра физической и
коллоидной химии
Слайд 37ДЭС. Образование двойного электрического слоя
Существование ДЭС ионов и скачка потенциала на
Различают три возможных механизма образования ДЭС:
- в результате перехода ионов или электронов из одной фазы в другую (1-й вариант);
- в результате избирательной адсорбции в межфазном слое ионов электролитов (2-й вариант);
- в результате ориентирования полярных молекул сопряженных фаз при их взаимодействии (3-й вариант).
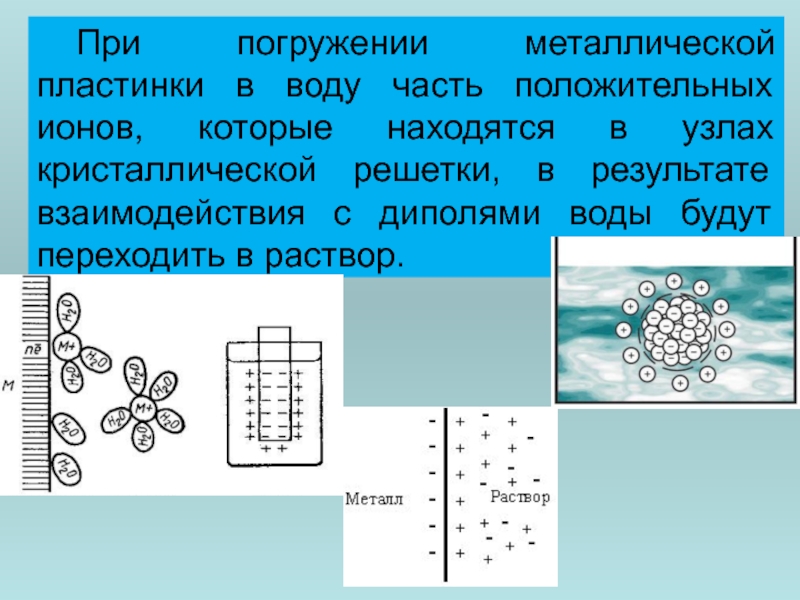
Слайд 38 При погружении металлической пластинки в воду часть положительных ионов, которые находятся
Слайд 39Двойной электрический слой 2-й вариант. При образовании золя AgI по реакции между
Соль
Соль
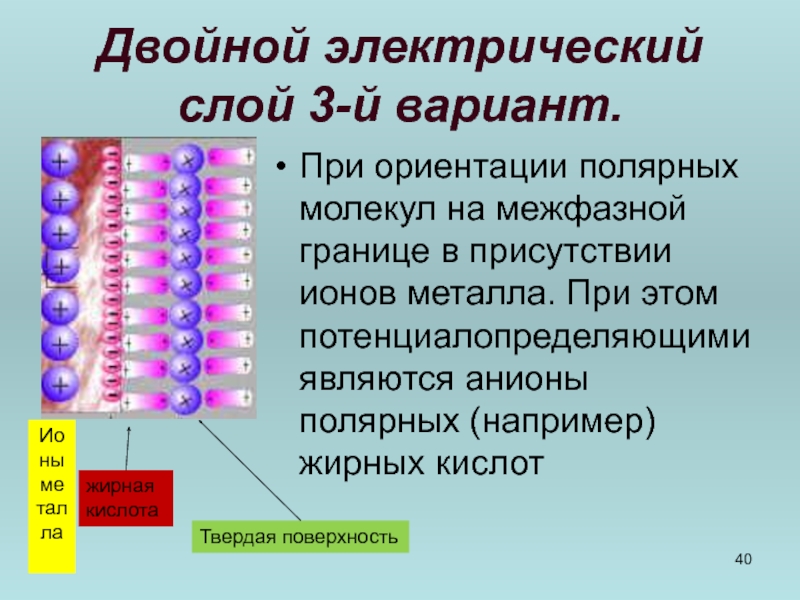
Слайд 40Двойной электрический слой 3-й вариант.
При ориентации полярных молекул на межфазной границе
Ионы металла
жирная кислота
Твердая поверхность
Слайд 41Строение ДЭС.
Впервые представление о ДЭС было высказано Квинке (1859) и развито
Теория ДЭС получила развитие в трудах ученых СССР А.Н. Фрумкина и Б.В. Дерягина.
Первой теорией строения ДЭС была теория Гельмгольца: ДЭС состоит из двух плоских зарядов, расположенных на молекулярном расстоянии один от другого и взаимодействующих между собой только за счет электростатических сил притяжения.
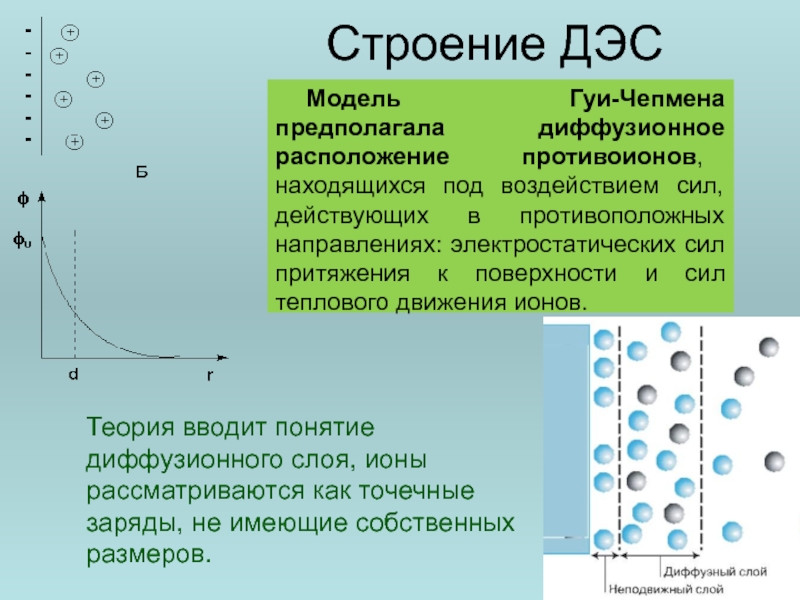
Слайд 42 Строение ДЭС
Модель Гуи-Чепмена предполагала
Теория вводит понятие диффузионного слоя, ионы рассматриваются как точечные заряды, не имеющие собственных размеров.
Слайд 43Строение ДЭС
По современным представлениям (теория Штерна) строение ДЭС: ионы входящие в
Слайд 44
В пределах ДЭС действует электрическое поле, интенсивность которого характеризуется значением потенциала.
При этом падение потенциала в пределах плотного слоя происходит линейно, а в диффузном слое – по экспоненте.
Потенциал на поверхности раздела Δ и потенциал так называемой плоскости максимального приближения (расположенной на расстоянии δ порядка молекулярных размеров) φ0 принадлежат к разряду практически неизмеримых величин.
На твердой поверхности возникает заряд, называемый φ-потенциал.
Знак φ-потенциала совпадает со знаком заряда потенцалобразующих ионов и его рассчитуют по уравнению Нернста. φ-потенциал равен работе переноса единичного (элементарного) заряда из бесконечно удаленной точки объема раствора на поверхность твердой фазы
Слайд 45
Для характеристики электрических свойств поверхности используют ζ-потенциал– потенциал границы скольжения фаз,
ξ = η*U0/ε0*ε*E
U0 – скорость движения жидкости, ε0 – константа, ε - диэлектрическая проницаемость жидкости, E – напряженность электрического поля,
ξ - потенциал, η- вязкость жидкости.
Слайд 46Электрокинетические явления.
Классификация.
Электрокинетические явления 1-го рода – относительное перемещение фаз под действием
Электрокинетические явления 2-го рода – возникновение разности потенциалов вследствие вынужденного относительного перемещения фаз
Электрофорез - движение частиц дисперсной фазы в электрическом поле
Электроосмос - движение дисперсной среды в электрическом поле относительно неподвижной дисперсной фазы
Потенциал седиментации – возникновение разности потенциалов при движении частиц в неподвижной жидкости
Потенциал протекания – возникновение разности потенциалов при движении жидкости относительно неподвижной твердой поверхности
Слайд 47Электрофорез
Наличие у частиц дисперсных систем электрического заряда было открыто
в 1808
Рейсс поставил два эксперимента. В одном он использовал U-образную трубку, в другом погрузил в глину 2 стеклянные трубки. При пропускании постоянного тока частички глины двигались к положительному электроду. Механизм электрофореза состоит в том, что под действием электрического поля двойной слой ионов разрывается на границе скольжения, частица приобретает заряд и движется к противоположно заряженному электроду, противоионы движутся в обратном направлении.
Слайд 48Электрофорез
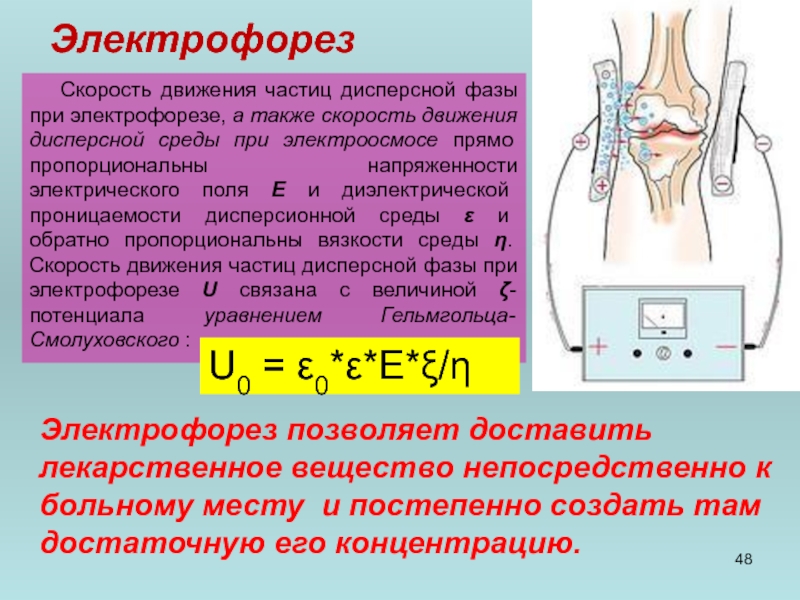
Скорость движения частиц дисперсной фазы при электрофорезе, а также скорость движения
U0 = ε0*ε*E*ξ/η
Электрофорез позволяет доставить лекарственное вещество непосредственно к больному месту и постепенно создать там достаточную его концентрацию.
Слайд 49Электроосмос
Во втором опыте Рейсс заполнил среднюю часть U- образной стеклянной трубки
Слайд 50Потенциал
протекания
и седиментации
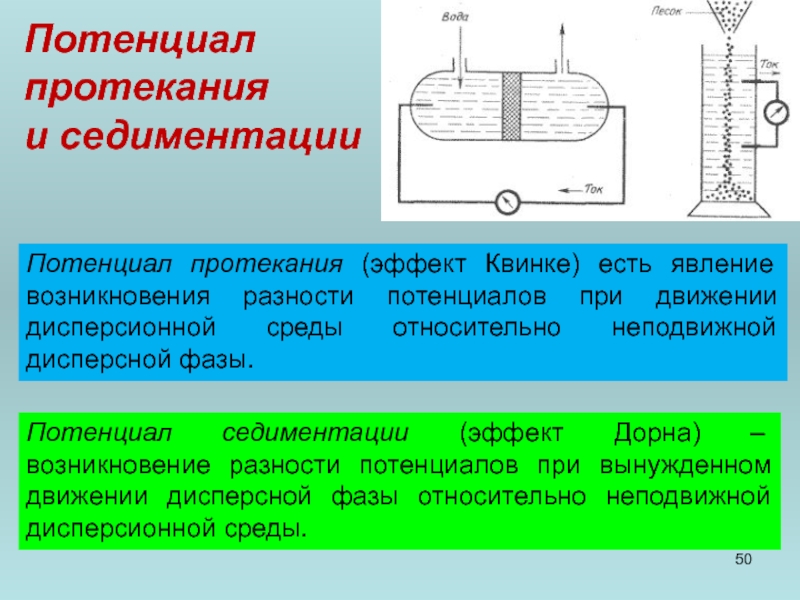
Потенциал протекания (эффект Квинке) есть явление возникновения разности
Потенциал седиментации (эффект Дорна) – возникновение разности потенциалов при вынужденном движении дисперсной фазы относительно неподвижной дисперсионной среды.
Слайд 51Устойчивость и коагуляция коллоидных систем
Запорожский государственный
медицинский университет
Кафедра физической и
коллоидной
Слайд 52
Устойчивость дисперсных систем
По предложению Н.П. Пескова (1920г) устойчивость дисперсных систем подразделяют
Кинетическая устойчивость – свойство дисперсных частиц удерживаться во взвешенном состоянии, не оседая.
Агрегативная устойчивость – способность частиц дисперсной фазы оказывать сопротивление слипанию и тем самым сохранять определенную степень дисперсности этой фазы в целом.
Слайд 53Коагуляция процесс слипания коллоидных частиц с образованием более крупных агрегатов с
введением электролитов;
нагреванием или замораживанием дисперсной системы;
механическим воздействием;
высокочастотными колебаниями;
ультрацентрифугированием.
Слайд 54
Коагуляция золей электролитами
Все электролиты при определенной концентрации могут вызвать коагуляцию золя.
Правило
Этот ион называют ионом-коагулятором.
Каждый электролит по отношению к коллоидному раствору обладает порогом коагуляции.















![{[mFe4[Fe(CN)6]3·n[Fe(CN)6]4-]4n-·4 (n-х)K+}4x-·4xK+{[m Fe4[Fe(CN)6]3·nFe3+] 3n+·3(n-х)Сl-}3x+·3xCl-](/img/tmb/3/263819/5688b3309b9254f7175189604385b59f-800x.jpg)