- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Классификация кристаллов по силам связи презентация
Содержание
- 1. Классификация кристаллов по силам связи
- 2. Кристаллические вещества состоят из огромного количества
- 3. Система атомов или ионов, определенным образом
- 4. Огромное разнообразие кристаллических решеток подразделено на
- 5. Самые слабые силы взаимодействия между молекулами
- 6. Ионная Составляющая кристаллической решетки – ионы с
- 7. Ковалентная Нейтральные атомы в результате превращения электронной оболочки в общий для обоих партнеров
- 8. Металлическая Металлическая структура может быть представлена как
- 9. Межмолекулярная Осуществляется нейтральными молекулами, сила притяжения и
Слайд 2
Кристаллические вещества состоят из огромного количества очень маленьких кристалликов, имеющих абсолютно
одинаковое строение. Кристаллические вещества характеризуются повторяющимся в пространстве расположением атомов или ионов, образующих правильные геометрические тела
Слайд 3
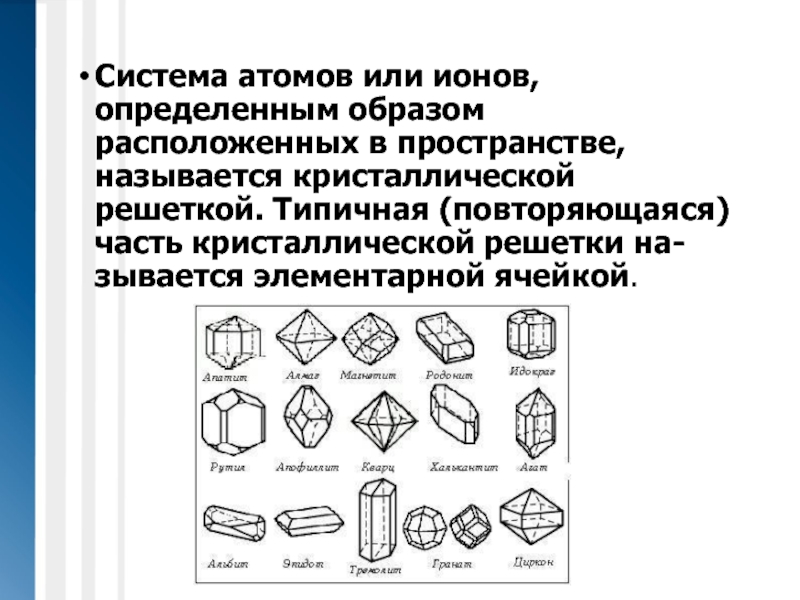
Система атомов или ионов, определенным образом расположенных в пространстве, называется кристаллической
решеткой. Типичная (повторяющаяся) часть кристаллической решетки на-зывается элементарной ячейкой.
Слайд 4
Огромное разнообразие кристаллических решеток подразделено на 7 больших систем, называемых СИНГОНИЯМИ
(по геометрической форме кристаллов)
Слайд 5
Самые слабые силы взаимодействия между молекулами в молекулярных кристаллах, к числу
которых относятся, например, кристаллы СО2, серы, бензола, йода, нафталина
Слайд 6Ионная
Составляющая кристаллической решетки – ионы с противоположными зарядами, взаимодействуют через электростатические
силы притяжения и электростатические силы отталкивания, а также квантовые силы, препятствующие сближению ионов с противоположным по знаку зарядами.
Слайд 7Ковалентная
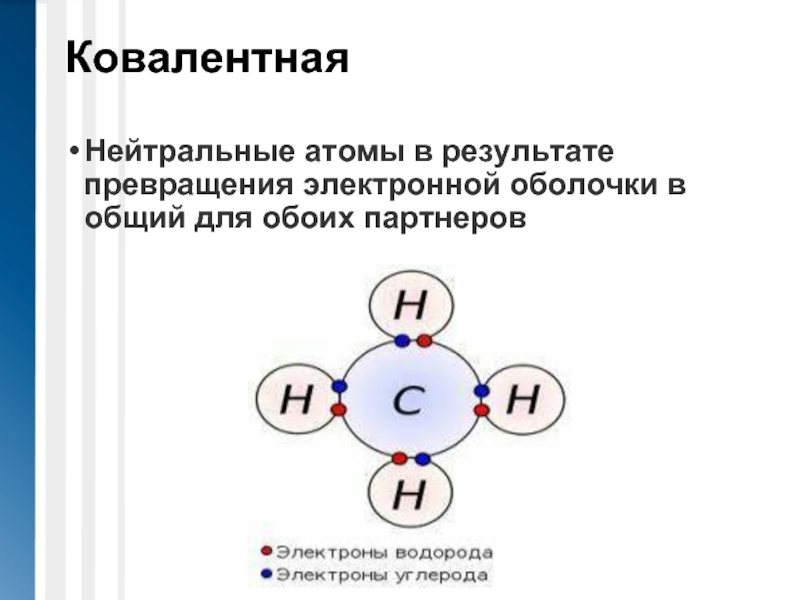
Нейтральные атомы в результате превращения электронной оболочки в общий для обоих
партнеров
Слайд 8Металлическая
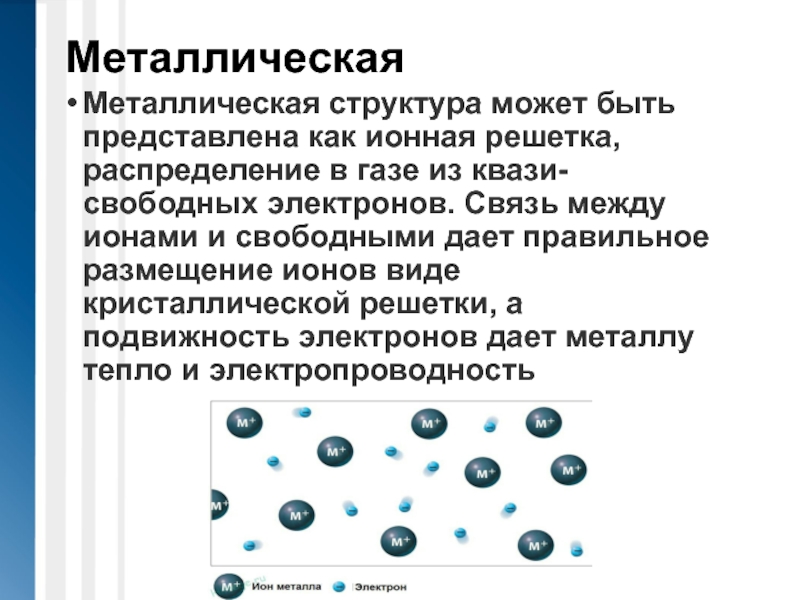
Металлическая структура может быть представлена как ионная решетка, распределение в газе
из квази-свободных электронов. Связь между ионами и свободными дает правильное размещение ионов виде кристаллической решетки, а подвижность электронов дает металлу тепло и электропроводность
Слайд 9Межмолекулярная
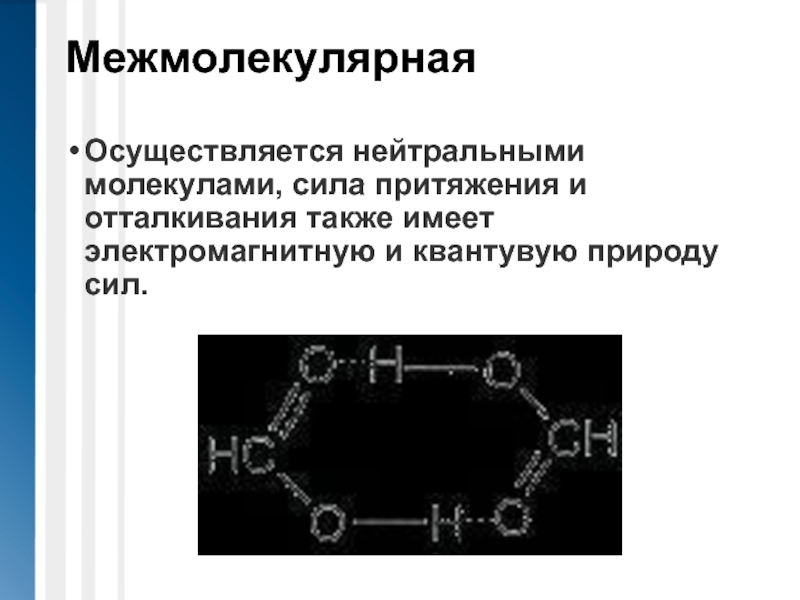
Осуществляется нейтральными молекулами, сила притяжения и отталкивания также имеет электромагнитную и
квантувую природу сил.