- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Жесткость воды и способы ее устранения презентация
Содержание
- 1. Жесткость воды и способы ее устранения
- 2. Вода́ —химическое вещество в виде прозрачной жидкости, не имеющей цвета, запаха и вкуса.
- 3. Жесткость воды обуславливается большим содержанием растворенных в
- 4. Жесткая и мягкая вода Жесткость и мягкость
- 5. Способы устранения жесткости воды: В природной
- 6. 4. Добавление умягчителей. Снижение общей жёсткости достигает
- 7. Спасибо за внимание
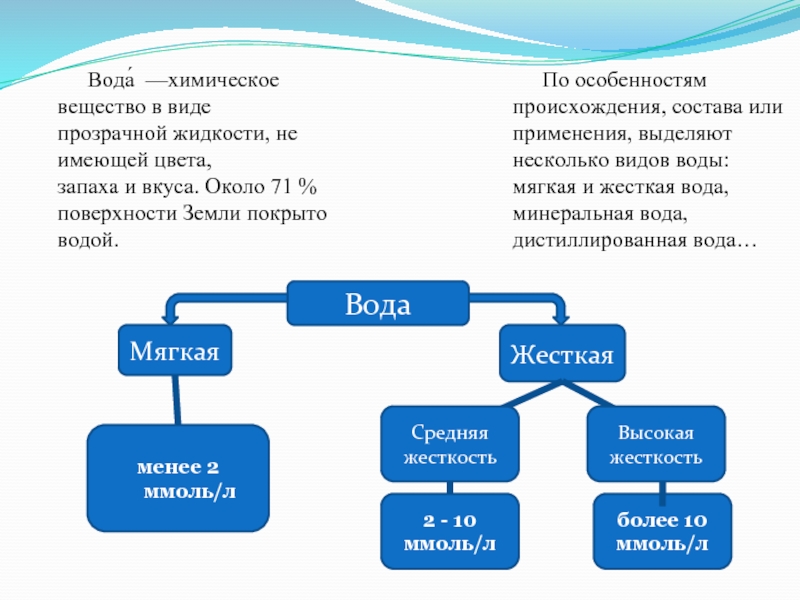
Слайд 2Вода́ —химическое вещество в виде прозрачной жидкости, не имеющей цвета, запаха и вкуса. Около 71 % поверхности Земли покрыто водой.
По
Слайд 3Жесткость воды обуславливается большим содержанием растворенных в ней солей щелочноземельных металлов,
Употребление жесткой или мягкой воды несет незначительный вред здоровью. При высоком содержании солей могут образовываться мочевые камни, а низкий уровень ненамного повышает риск появления сердечно-сосудистых заболеваний. Вкус родниковой воды обуславливается именно ее жесткостью.
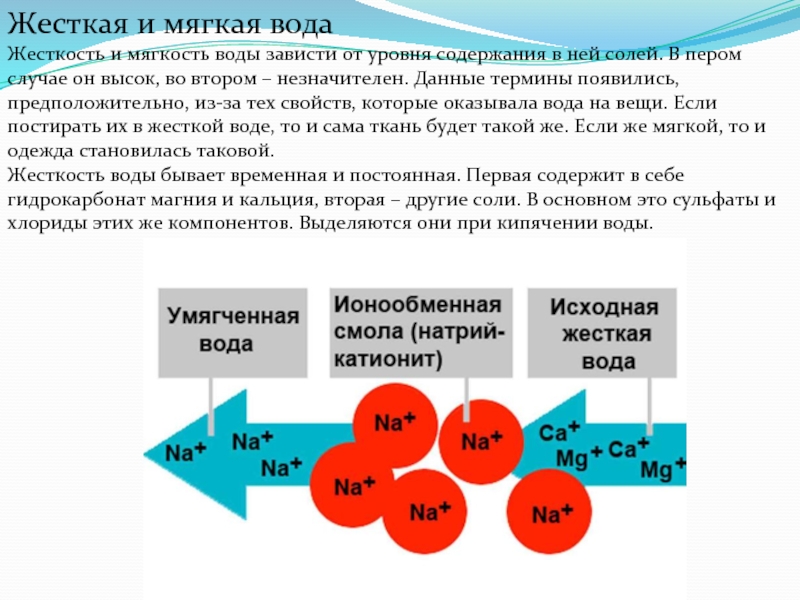
Слайд 4Жесткая и мягкая вода Жесткость и мягкость воды зависти от уровня содержания
Слайд 5Способы устранения жесткости воды:
В природной воде растворены соли кальция и
Слайд 64. Добавление умягчителей. Снижение общей жёсткости достигает 100%. Умягчители предназначены для
5.Фильтрование . Фильтрование снижает общую жесткость до 80%.Внутри картриджа фильтра содержится смесь из активированного угля и катионообменники. Уголь адсорбирует вредные органические вещества и хлориды. Катионообменники снижают общую жесткость. Теперь мы знаем, как уменьшить жесткость воды. Накипь внутри чайника ‑ это осадок карбонатов кальция и магния с примесью сульфата кальция. Накипь можно удалить со стенок, используя разбавленный раствор уксусной кислоты.