- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Кислород. Историческая справка презентация
Содержание
- 1. Кислород. Историческая справка
- 2. Кислород – это вещество,
- 3. Докажите, что кислород - невидимка, но находится везде и может все» .
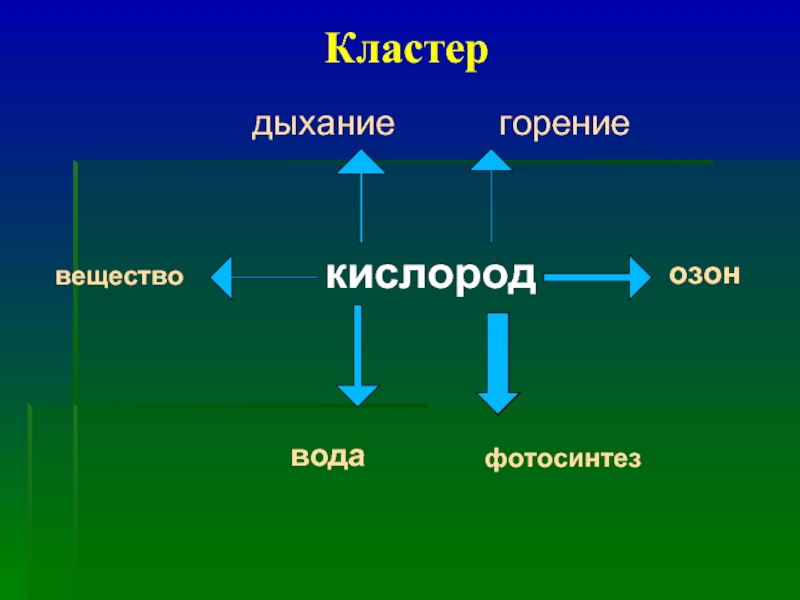
- 4. Кластер кислород
- 5. Актуализация опорных знаний Определенный вид атомов
- 6. План изучения нового материала 1. История открытия
- 7. Историческая справка В1774г.
- 8. О своем открытии Пристли сообщил другу
- 9. 1. Кислород как химический элемент План
- 10. Кислород как элемент Элемент кислород находится
- 11. 2. Кислород как вещество План характеристики
- 12. Кислород в природе В земной коре его
- 13. Жидкий кислород Твердый кислород
- 14. Физические свойства кислорода. Признаки Кислород-простое вещество Формула
- 15. Способы получения и собирания кислорода. Кислород в
- 16. В лаборатории кислород получают реакциями разложения: а)
- 17. назад
- 18. назад
- 19. назад
- 20. Получение кислорода , проверка его наличия тлеющей лучиной
- 21. старт Кислород – это простое вещество, состоящее
- 22. Домашнее задание Домашнее задание. Выберете то задание,
Слайд 5Актуализация опорных знаний
Определенный вид атомов — ….
Свойство атомов удерживать определенное число других атомов в соединении — ….
валентность
Вещества, образованные одним видом атомов, называются...
простыми
Самое распространенное вещество на Земле –
вода
Явления, при которых происходит превращение одних веществ в другие, называются...
химическими
Слайд 6План изучения нового материала
1. История открытия кислорода.
2. Кислород как химический элемент
3.
4. Физические свойства кислорода.
5. Получение кислорода в лаборатории и промышленности.
Слайд 7 Историческая справка
В1774г. англичанин Джозеф Пристли (пастор по
Слайд 8
О своем открытии Пристли сообщил другу - французу А. Л. Лавуазье.
Слайд 9
1. Кислород как химический элемент
План
характеристики химического элемента
1. Химический знак.
природе.
Слайд 10Кислород как элемент
Элемент кислород находится
в VI группе, главной подгруппе,
II
порядковый номер №8, Ar = 16.
2. Валентность II, степень окисления -2
(редко +2; -1).
3. Входит в состав оксидов, оснований, солей, кислот, органических веществ, в том числе живых организмов.
Слайд 112. Кислород как вещество
План
характеристики простого вещества
1. Химическая
5. Способы получения в лаборатории и в
промышленности.
Слайд 12Кислород в природе
В земной коре его 49%, в воде – 89%.
Состав воздуха:
О2 – 20-21 %; N2 – 78%; CO2 – 0,03%,
остальное приходится на инертные газы, пары воды, примеси.
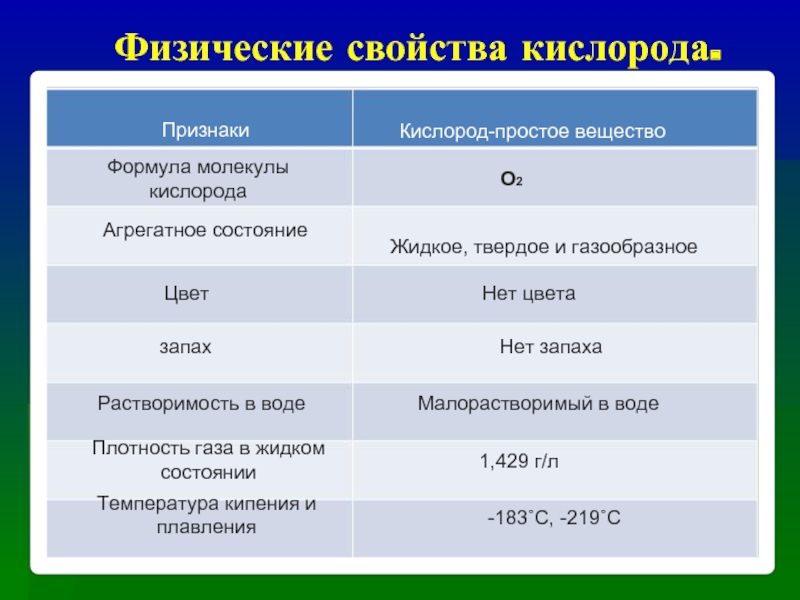
Слайд 14Физические свойства кислорода.
Признаки
Кислород-простое вещество
Формула молекулы кислорода
Агрегатное состояние
Цвет
Растворимость в воде
Плотность газа в жидком состоянии
Температура кипения и плавления
О2
Жидкое, твердое и газообразное
Нет цвета
Нет запаха
Малорастворимый в воде
1,429 г/л
-183˚С, -219˚С
Слайд 15Способы получения и собирания кислорода.
Кислород в природе образуется в
процессе фотосинтеза.
В промышленности
его получают перегонкой
сжиженного воздуха при t = - 1830
С.
Слайд 16В лаборатории
кислород получают реакциями разложения:
а) воды под действием электрического тока (электролиз):
б) пероксида водорода под действием MnO2 :
MnO2
2Н2О2 → 2Н2О + О2
в) перманганата калия при нагревании:
2KMnO4 → K2MnO4 + MnO2 + O2
Разложение этой соли идёт при нагревании её выше 2000 С.
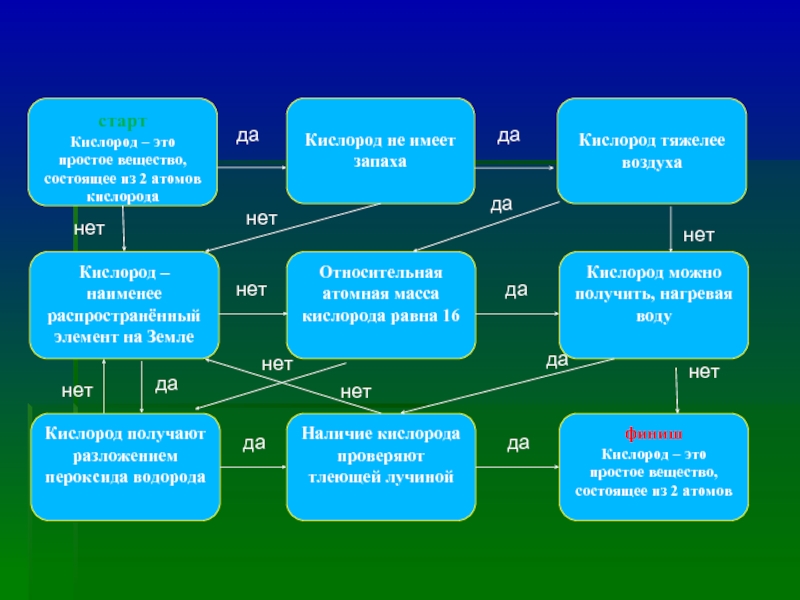
Слайд 21старт
Кислород – это простое вещество, состоящее из 2 атомов кислорода
Кислород не
Кислород тяжелее воздуха
Кислород – наименее распространённый элемент на Земле
Относительная атомная масса кислорода равна 16
Кислород можно получить, нагревая воду
Кислород получают разложением пероксида водорода
Наличие кислорода проверяют тлеющей лучиной
финиш
Кислород – это простое вещество, состоящее из 2 атомов
да
да
нет
нет
нет
да
нет
нет
да
да
да
да
да
нет
нет
нет
Слайд 22Домашнее задание
Домашнее задание.
Выберете то задание, которое вам больше нравится:
1. Ответить на вопросы:
• На
• Какие факты доказывают, что кислород хоть и плохо, но растворяется в воде?
2. У мальчика Пети была шпаргалка, которую ему отдал папа. Но так как этой шпаргалке уже много лет часть информации стерлась. Помоги Пете, восстанови шпаргалку:
… →K2MnO4 + … + O2
KCIO3 →KCI + …
HgO → … + O2
… → H2O + O2
Задача: При разложении 16 г бертолетовой соли
образовалось 4 г хлорида калия(KCI). Найдите массу выделившегося при этом кислорода?
KCIO3 → KCI + O2
________________________________________