- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Хімічні властивості кисню презентация
Содержание
- 1. Хімічні властивості кисню
- 2. Мета уроку: ознайомитись з хімічними властивостями кисню;
- 3. Експрес-контроль Оксиген – це проста речовина чи
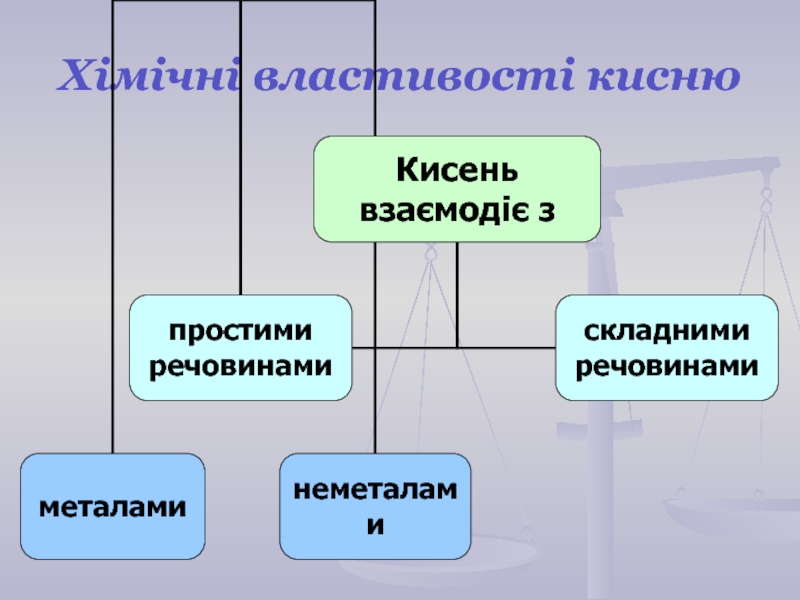
- 4. Хімічні властивості кисню
- 5. Хімічні властивості кисню Унаслідок взаємодії речовин із
- 6. Горіння простих речовин в кисні
- 7. Горіння неметалів Взаємодія кисню з сіркою: S
- 8. Горіння металів Взаємодія кисню з магнієм: 2Mg
- 9. Взаємодія кисню зі складними речовинами Горіння складних
- 10. Горіння бензену в кисні
- 11. Горіння складних речовин Взаємодія кисню з бензеном
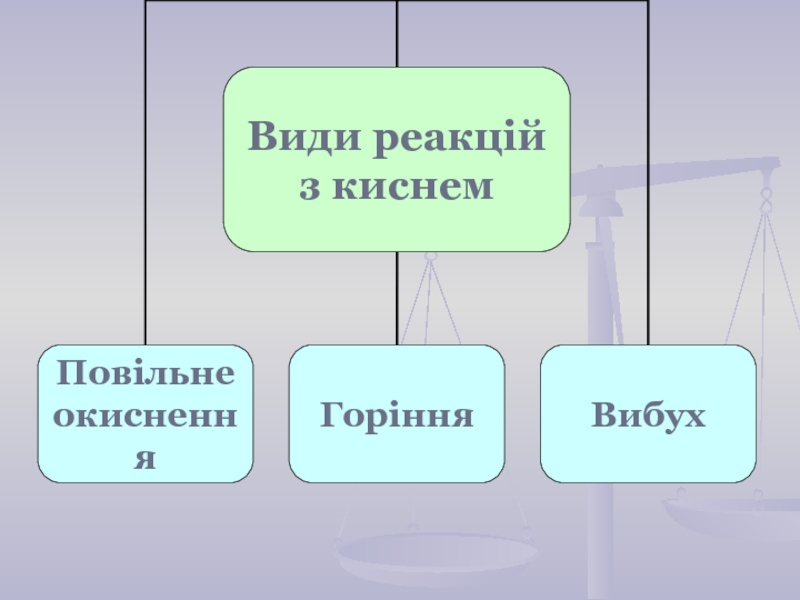
- 13. Повільне окиснення Відбувається повільно. Теплота виділяється поступово.
- 14. Вибух Відбувається дуже швидко. Енергія, що виділяється,
- 15. Горіння Відбувається швидко. Виділяється велика кількість теплоти.
- 17. Завдання 1. Скласти формули оксидів Калію, Карбону
Слайд 2Мета уроку:
ознайомитись з хімічними властивостями кисню;
сформувати поняття про оксиди, окиснення, горіння;
з’ясувати
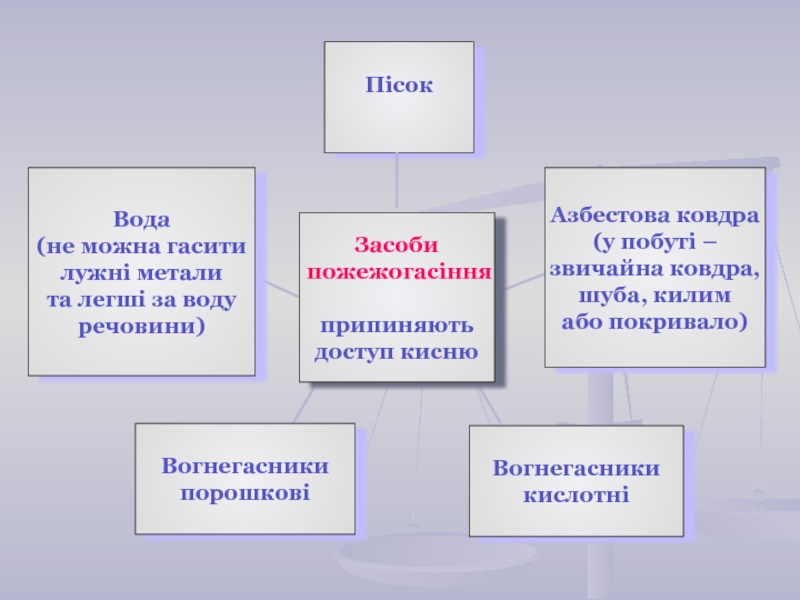
умови виникнення та припинення горіння;
ознайомитись з заходами протипожежної безпеки.
ознайомитись з заходами протипожежної безпеки.
Слайд 3Експрес-контроль
Оксиген – це проста речовина чи хімічний елемент?
Яка валентність Оксигену?
Молекула кисню
складається з …
В якій групі Періодичної системи розташований Оксиген?
Оксиген відносять до металічних чи неметалічних елементів?
Найпоширеніша сполука Оксигену на Землі – це …
В якій групі Періодичної системи розташований Оксиген?
Оксиген відносять до металічних чи неметалічних елементів?
Найпоширеніша сполука Оксигену на Землі – це …
Слайд 5Хімічні властивості кисню
Унаслідок взаємодії речовин із киснем утворюються бінарні сполуки, до
складу яких входить Оксиген. Такі сполуки називають оксидами.
Взаємодія речовин з киснем належить до реакцій окиснення.
Горіння – це хімічна реакція, під час якої відбувається окиснення речовин з виділенням тепла і світла.
Взаємодія речовин з киснем належить до реакцій окиснення.
Горіння – це хімічна реакція, під час якої відбувається окиснення речовин з виділенням тепла і світла.
Слайд 7Горіння неметалів
Взаємодія кисню з сіркою:
S + О2 → SO2
Взаємодія кисню з
фосфором:
4P + 5О2 → 2P2O5
Завдяки утворенню густого білого диму Р2О5 цю реакцію використовують для створення димової завіси
4P + 5О2 → 2P2O5
Завдяки утворенню густого білого диму Р2О5 цю реакцію використовують для створення димової завіси
Слайд 8Горіння металів
Взаємодія кисню з магнієм:
2Mg + О2 → 2MgO
Цю
реакцію раніше використовували фотографи для створення спалаху.
Взаємодія кисню з залізом:
2Fe + О2 → 2FeO
Цю реакцію можна спостерігати на будівництвах під час різання та зварюванню металів.
Взаємодія кисню з залізом:
2Fe + О2 → 2FeO
Цю реакцію можна спостерігати на будівництвах під час різання та зварюванню металів.
Слайд 9Взаємодія кисню зі складними речовинами
Горіння складних речовин принципово не відрізняється від
горіння простих речовин.
При горінні складних речовин утворюються оксиди всіх елементів, які входять до складу цієї речовини.
При горінні складних речовин утворюються оксиди всіх елементів, які входять до складу цієї речовини.
Слайд 11Горіння складних речовин
Взаємодія кисню з бензеном С6Н6:
2C6H6 + 15О2 → 12CO2
+ 6H2O
Взаємодія кисню з метаном СН4 (природним газом):
CH4 + 2О2 → CO2 + 2H2O
Взаємодія кисню зі спиртом С16Н34О :
C16H34O + 24О2 → 16CO2 + 17H2O
Взаємодія кисню з метаном СН4 (природним газом):
CH4 + 2О2 → CO2 + 2H2O
Взаємодія кисню зі спиртом С16Н34О :
C16H34O + 24О2 → 16CO2 + 17H2O
Слайд 13Повільне окиснення
Відбувається повільно.
Теплота виділяється поступово.
Не супроводжується полум’ям.
Приклади:
Залізні предмети з
часом вкриваються іржею.
Скисання молока або сока.
Ваші приклади.
Скисання молока або сока.
Ваші приклади.
Слайд 14Вибух
Відбувається дуже швидко.
Енергія, що виділяється, призводить до руйнівних наслідків.
Супроводжується вибуховою хвилею
та іноді короткочасним спалахом.
Приклади:
Суміш кисню з воднем (гримучий газ).
Суміші природного газу або вугільного пилу з повітрям.
Тирса, просочена рідким киснем (вибухівка).
Приклади:
Суміш кисню з воднем (гримучий газ).
Суміші природного газу або вугільного пилу з повітрям.
Тирса, просочена рідким киснем (вибухівка).
Слайд 15Горіння
Відбувається швидко.
Виділяється велика кількість теплоти.
Найчастіше супроводжується полум’ям.
Умови виникнення:
вільний доступ
кисню;
досягнення температури займання;
наявність горючої речовини.
досягнення температури займання;
наявність горючої речовини.
Слайд 17Завдання
1. Скласти формули оксидів Калію, Карбону (IV), Алюмінію.
K2O CO2
Al2O3
2. Скласти рівняння реакцій горіння Натрію, Кальцію, Нітрогену (I).
4Na + О2 → 2Na2O
2Ca + О2 → 2CaO
N2 + О2 → 2NO
2. Скласти рівняння реакцій горіння Натрію, Кальцію, Нітрогену (I).
4Na + О2 → 2Na2O
2Ca + О2 → 2CaO
N2 + О2 → 2NO