- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Гідроліз солей презентация
Содержание
- 1. Гідроліз солей
- 2. ГІДРОЛІЗ - це реакція
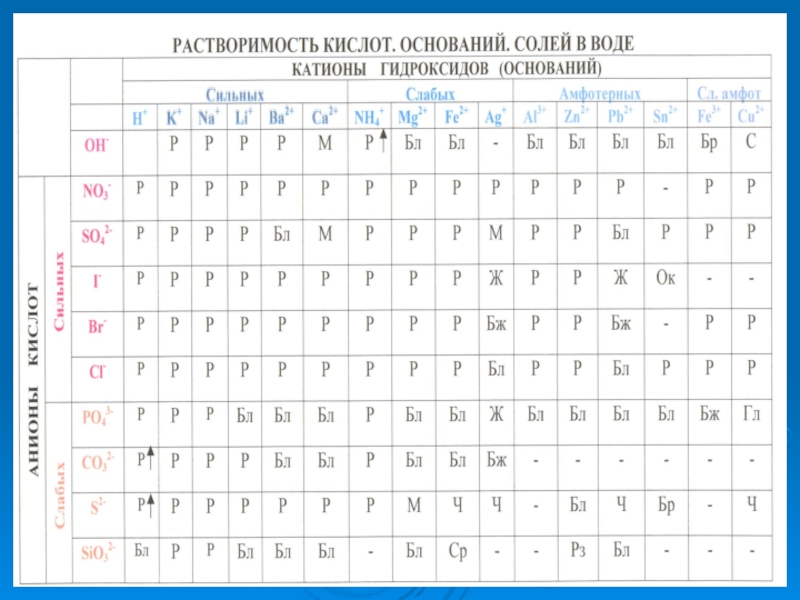
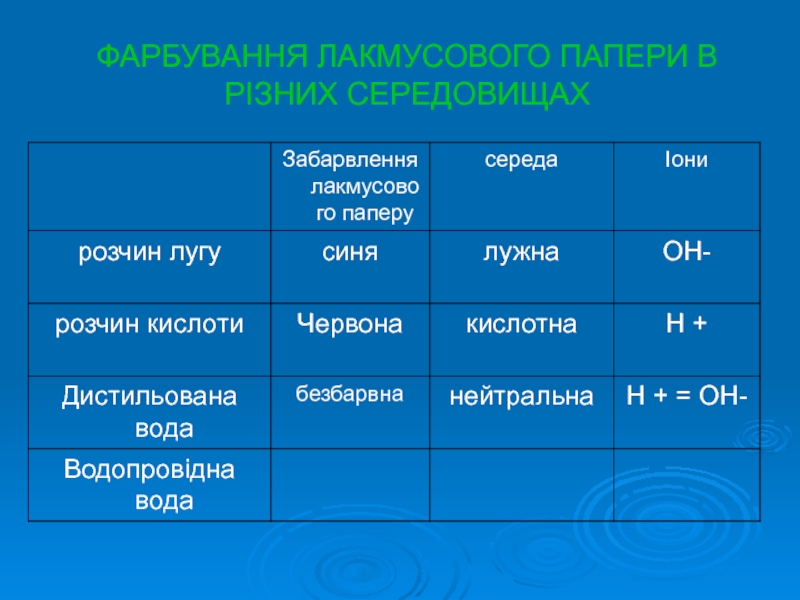
- 4. ФАРБУВАННЯ ЛАКМУСОВОГО ПАПЕРИ В РІЗНИХ СЕРЕДОВИЩАХ
- 5. Тема: Гідроліз солей Мета: вивчити сутність гідролізу
- 6. « ГІДРОЛІЗ » - від грецького «
- 7. Забарвлення лакмоіда в розчинах солей : хлориду
- 8. Механізм гідролізу хлориду алюмінію H2O H+ +
- 9. Схема гідролізу хлориду алюмінію
- 10. АЛГОРИТМ СКЛАДАННЯ РІВНЯНЬ реакції гідролізу СОЛЕЙ
- 11. Механізм гідролізу карбонату натрію H2O H+ +
- 12. Механізм гідролізу хлориду натрію H2O H+ +
- 13. Сформулируем определение понятия «гидролиз»: К какому
- 14. Роль гідролізу в природі Перетворення земної кори Забезпечення середовища морської води
- 15. Роль гідролізу в народному господарстві Псування виробничого
- 16. Роль гідролізу в повсякденному житті людини Прання
Слайд 2
ГІДРОЛІЗ - це реакція обміну між деякими солями і
водою приводить до утворення слабкого електроліту.
Слайд 5Тема: Гідроліз солей
Мета: вивчити сутність гідролізу солей у водних розчинах .
завдання: сформулювати визначення поняття « гідроліз » навчитися пояснювати хімічні процеси, що протікають у водних розчинах солей записувати рівняння реакцій гідролізу пророкувати і пояснювати зміна кислотності середовища і утворення кислих і основних солей у цьому процесі познайомитися з роллю гідролізу солей в природі, господарської діяльності та повсякденному житті людини .
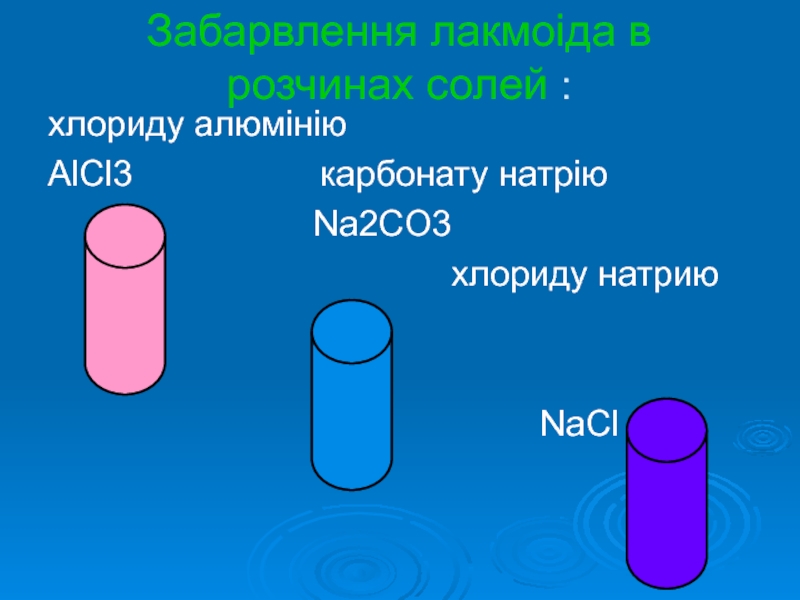
Слайд 7Забарвлення лакмоіда в розчинах солей :
хлориду алюмінію
AlCl3
карбонату натрію
Na2CO3
хлориду натрию
NaCl
Na2CO3
хлориду натрию
NaCl
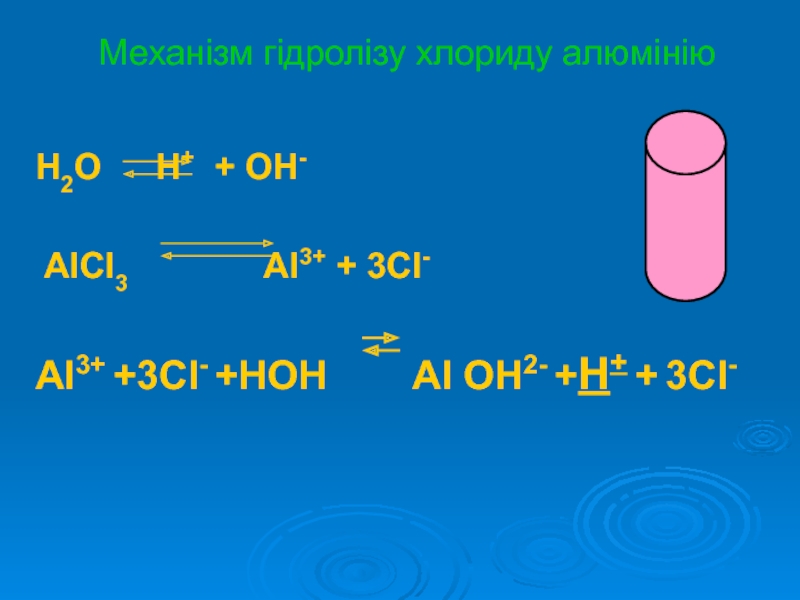
Слайд 8Механізм гідролізу хлориду алюмінію
H2O H+ + OH-
AlCl3
Al3+ + 3Cl-
Al3+ +3Cl- +HOH Al OH2- +H+ + 3Cl-
Al3+ +3Cl- +HOH Al OH2- +H+ + 3Cl-
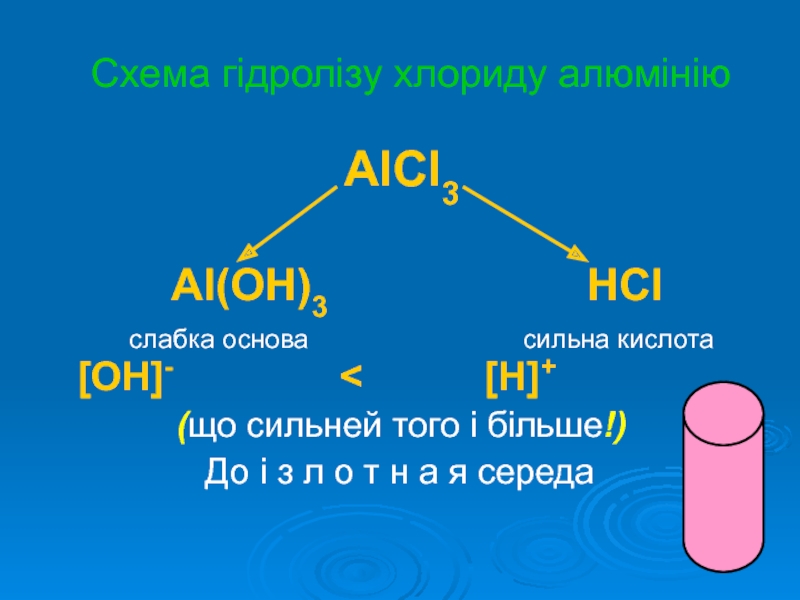
Слайд 9Схема гідролізу хлориду алюмінію
AlCl3
Al(OH)3 HCl
слабка основа сильна кислота [OH]- < [H]+
(що сильней того і більше!)
До і з л о т н а я середа
Al(OH)3 HCl
слабка основа сильна кислота [OH]- < [H]+
(що сильней того і більше!)
До і з л о т н а я середа
Слайд 10
АЛГОРИТМ СКЛАДАННЯ РІВНЯНЬ реакції гідролізу СОЛЕЙ
Визначити склад солі, тобто вказати, яким
по силі підставою і який за силою кислотою утворена дана сіль.
Взяти іон слабкого електроліту і написати рівняння взаємодії його з складовими частинами однієї молекули води ; в результаті отримати короткий іонне рівняння гідролізу.
Написати на підставі короткого іонного рівняння молекулярне рівняння.
Вихідні речовини відомі - сіль і вода. Продукти гідролізу скласти , пов'язуючи утворилися іони з тими іонами солі, які не беруть участь у реакції гідролізу.
Взяти іон слабкого електроліту і написати рівняння взаємодії його з складовими частинами однієї молекули води ; в результаті отримати короткий іонне рівняння гідролізу.
Написати на підставі короткого іонного рівняння молекулярне рівняння.
Вихідні речовини відомі - сіль і вода. Продукти гідролізу скласти , пов'язуючи утворилися іони з тими іонами солі, які не беруть участь у реакції гідролізу.
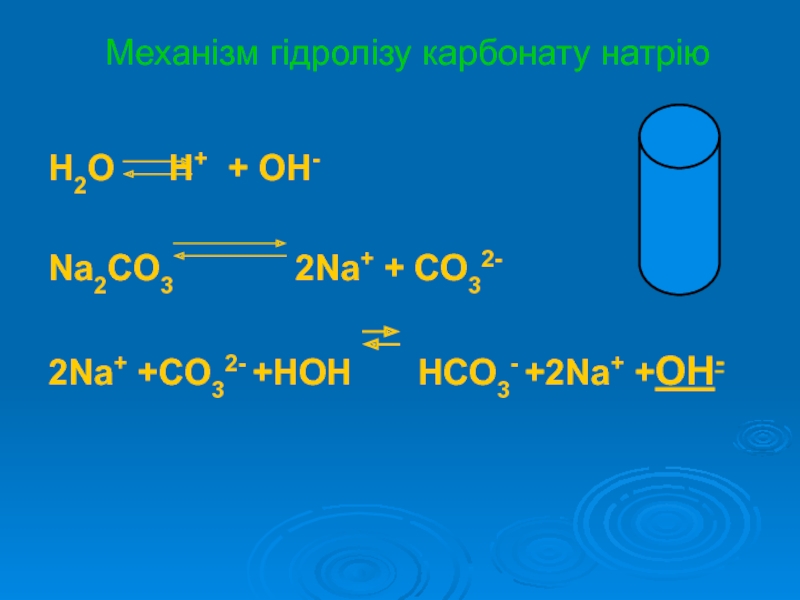
Слайд 11Механізм гідролізу карбонату натрію
H2O H+ + OH-
Na2CO3
2Na+ + CO32-
2Na+ +CO32- +HOH HCO3- +2Na+ +OH-
2Na+ +CO32- +HOH HCO3- +2Na+ +OH-
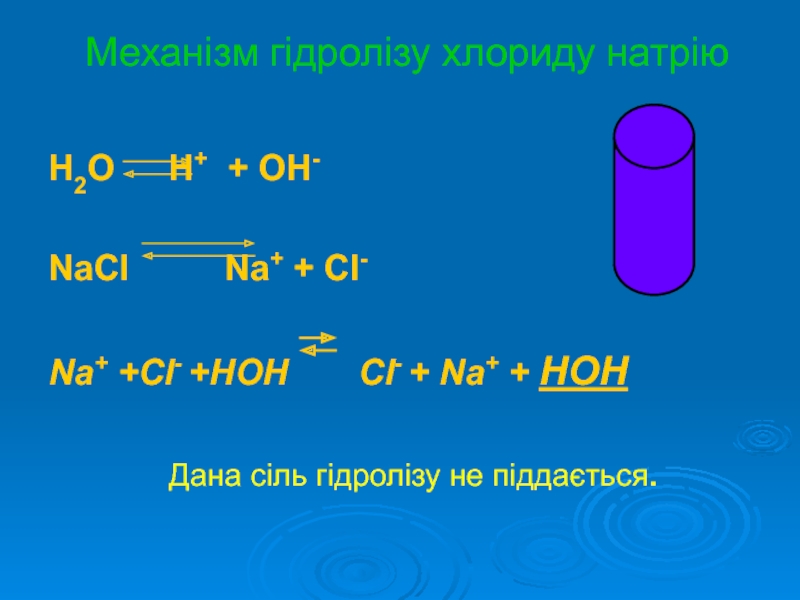
Слайд 12Механізм гідролізу хлориду натрію
H2O H+ + OH-
NaСl Na+
+ Cl-
Na+ +Cl- +HOH Cl- + Na+ + HOH
Дана сіль гідролізу не піддається.
Na+ +Cl- +HOH Cl- + Na+ + HOH
Дана сіль гідролізу не піддається.
Слайд 13Сформулируем
определение понятия «гидролиз»:
К какому типу мы отнесем данные реакции?
Какие вещества
в них участвуют?
В чем заключается сущность гидролиза? Какие продукты данных взаимодействий с точки зрения теории электролитической диссоциации мы получили
В чем заключается сущность гидролиза? Какие продукты данных взаимодействий с точки зрения теории электролитической диссоциации мы получили
Слайд 15Роль гідролізу в народному господарстві
Псування виробничого обладнання Вироблення з нехарчової сировини
цінних продуктів (папір , мило, спирт , глюкоза , білкові дріжджі) Очищення промислових стоків та питної води (сульфат алюмінію + вода гідроксид алюмінію) Підготовка тканин до фарбування Вапнування грунтів засноване на гідролізі
Слайд 16Роль гідролізу в повсякденному житті людини
Прання
Миття посуду Умивання з милом процеси травлення