- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Фенолы: понятие, классификация, номенклатура, изомерия, получение, физические свойства, химические свойства, применение презентация
Содержание
- 1. Фенолы: понятие, классификация, номенклатура, изомерия, получение, физические свойства, химические свойства, применение
- 2. Общая формула:
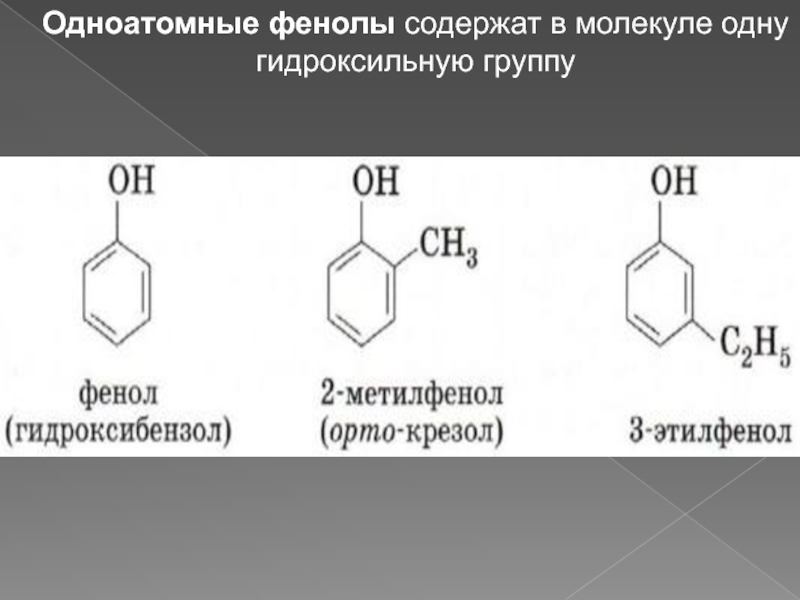
- 3. Одноатомные фенолы содержат в молекуле одну гидроксильную группу
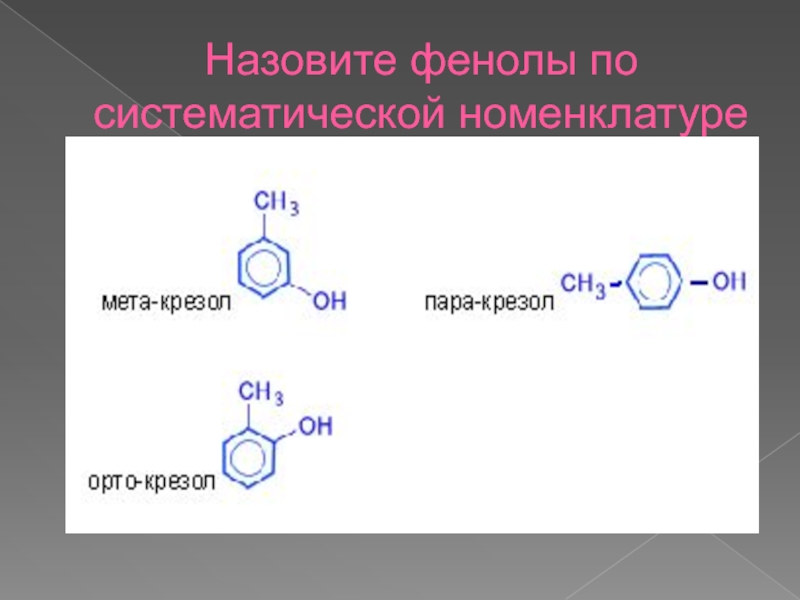
- 6. Назовите фенолы по систематической номенклатуре
- 7. Изомерия фенолов Изомерия положения гидроксигруппы Изомерия углеродного скелета
- 8. Напишите и назовите изомеры фенолов с общей формулой С8Н10О С9Н12О
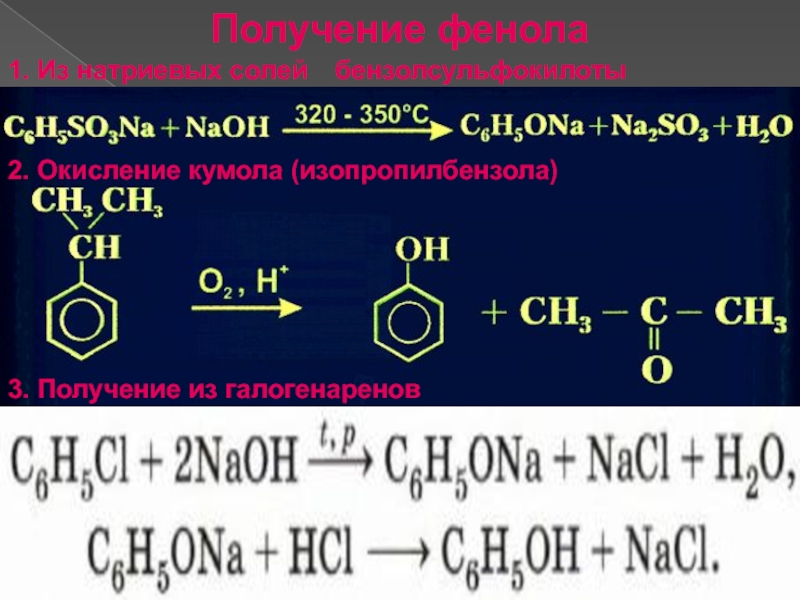
- 9. Получение фенола 1. Из натриевых солей бензолсульфокилоты 2. Окисление кумола (изопропилбензола) 3. Получение из галогенаренов
- 10. Фенол - бесцветные, розовеющие при хранении на
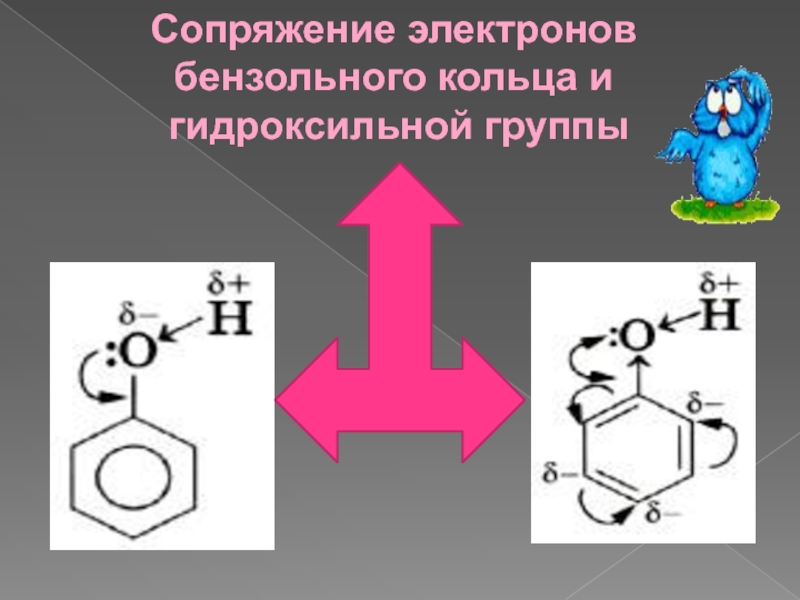
- 11. Сопряжение электронов бензольного кольца и гидроксильной группы
- 12. I. Кислотные свойства 1. Фенол реагирует с щелочными металлами, с щелочами с образованием фенолятов
- 13. I. Кислотные свойства 2. Фенол реагирует
- 14. II. Реакции бензольного кольца 3. Бромирование фенола (образуется белый осадок 2,4,6-трибромфенола) Качественная реакция
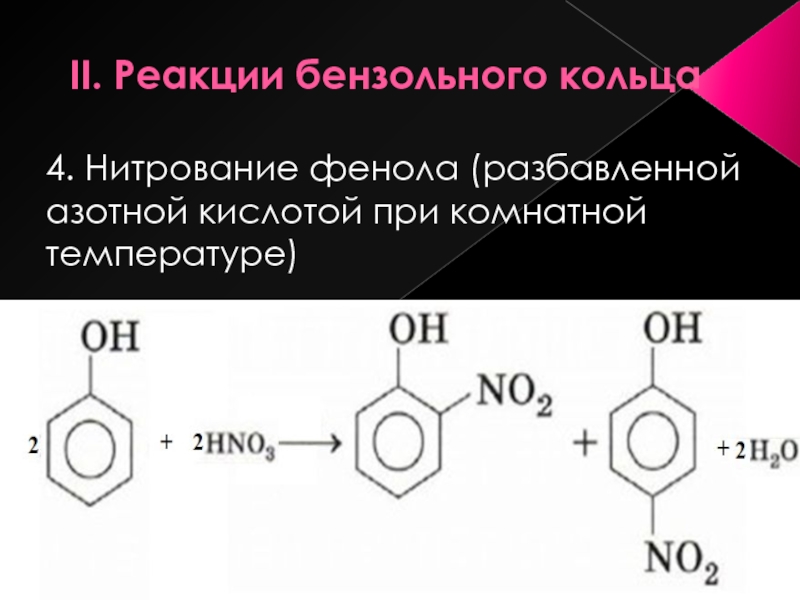
- 15. II. Реакции бензольного кольца 4. Нитрование фенола (разбавленной азотной кислотой при комнатной температуре)
- 16. II. Реакции бензольного кольца Нитрование фенола концентрированной
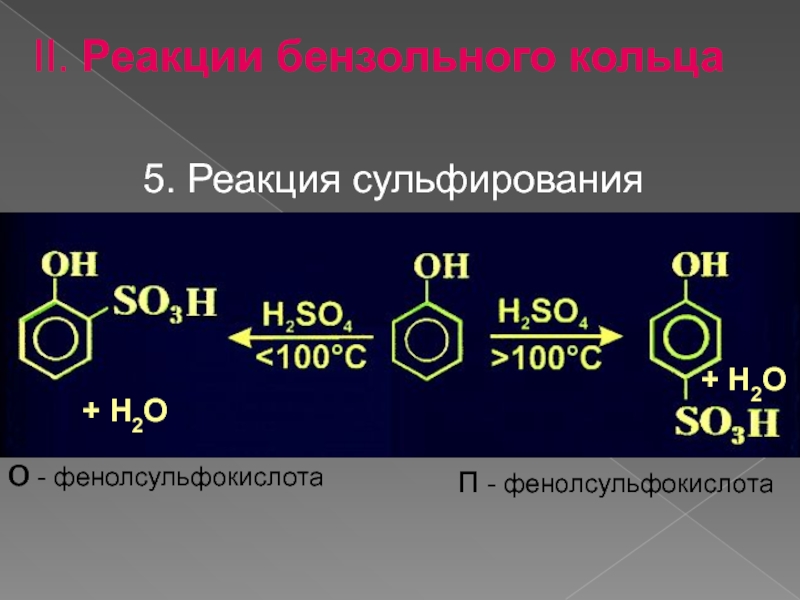
- 17. + H2O + H2O 5. Реакция сульфирования
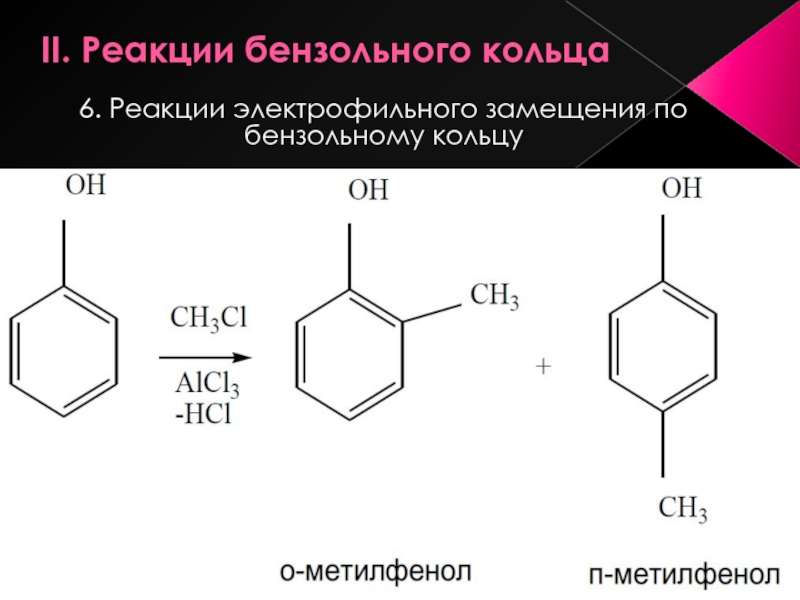
- 18. II. Реакции бензольного кольца 6. Реакции электрофильного замещения по бензольному кольцу
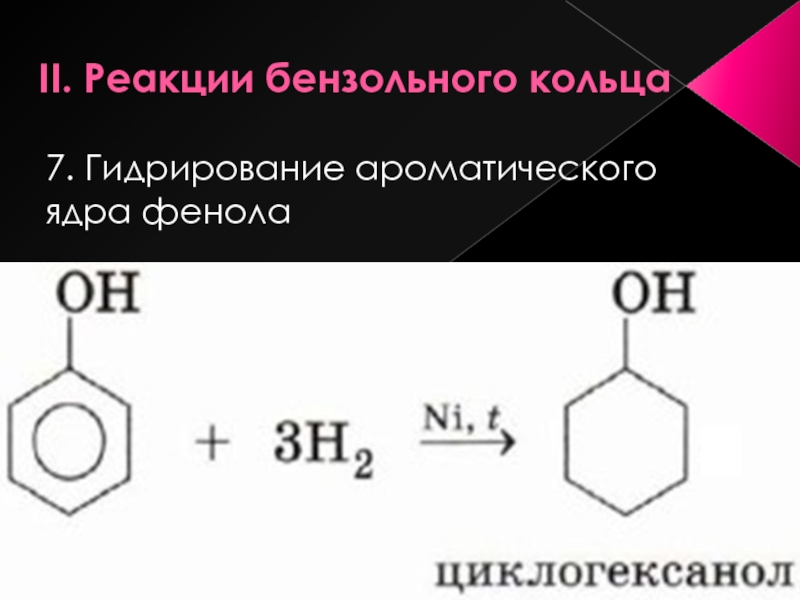
- 19. II. Реакции бензольного кольца 7. Гидрирование ароматического ядра фенола
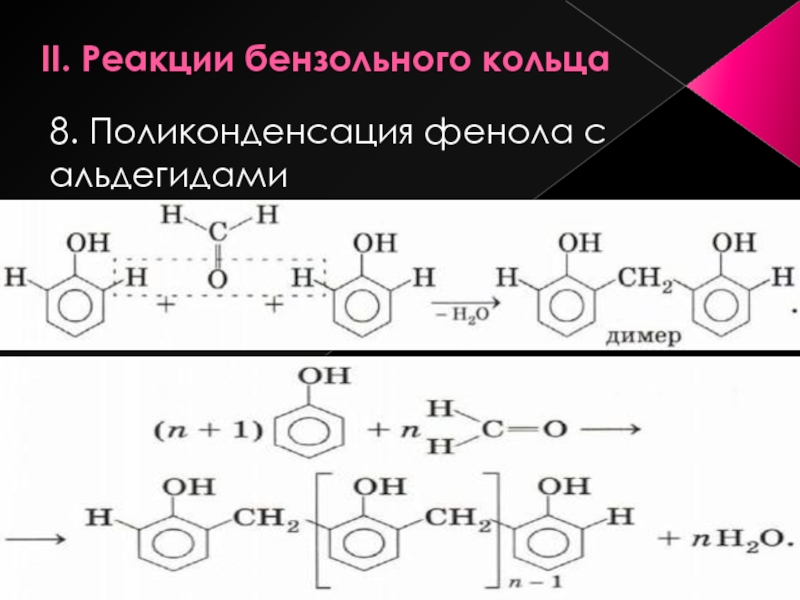
- 20. II. Реакции бензольного кольца 8. Поликонденсация фенола с альдегидами
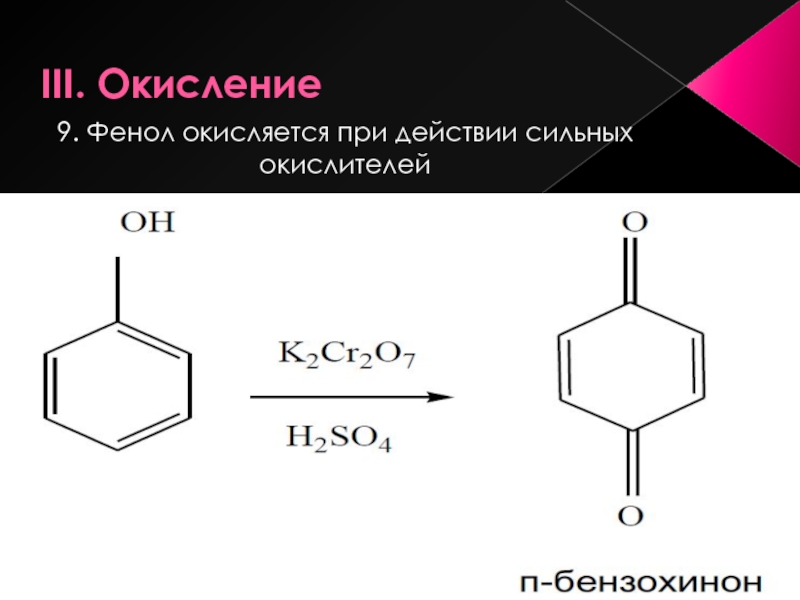
- 21. III. Окисление 9. Фенол окисляется при действии сильных окислителей
- 22. III. Окисление 10. Фенол горит С6Н5ОН+ 7О2 =6СО2 + 3Н2О
- 24. В трёх пробирках без подписи находятся водные
- 25. Массовые доли углерода и водорода в гомологе
- 26. Расположите указанные вещества в порядке усиления кислотных
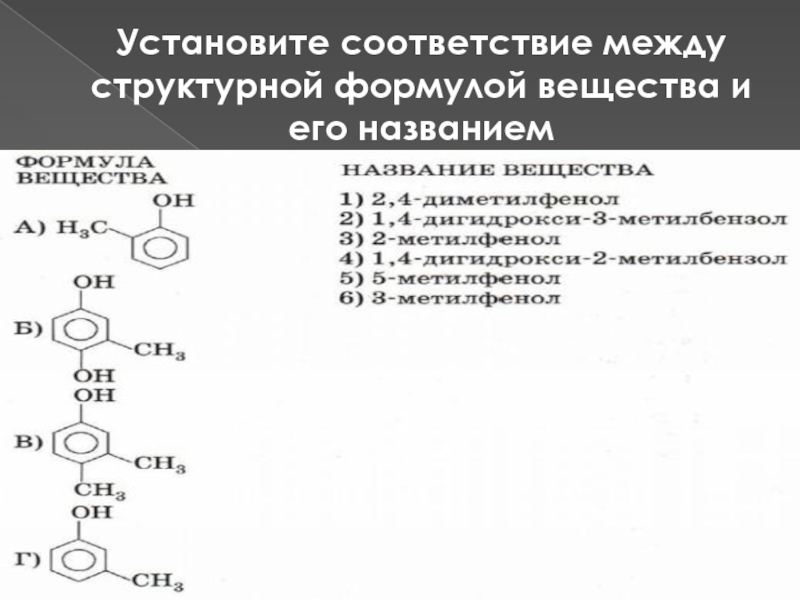
- 27. Установите соответствие между структурной формулой вещества и его названием
- 28. Смесь предельного одноатомного спирта и фенола массой
Слайд 1ФЕНОЛЫ
Понятие
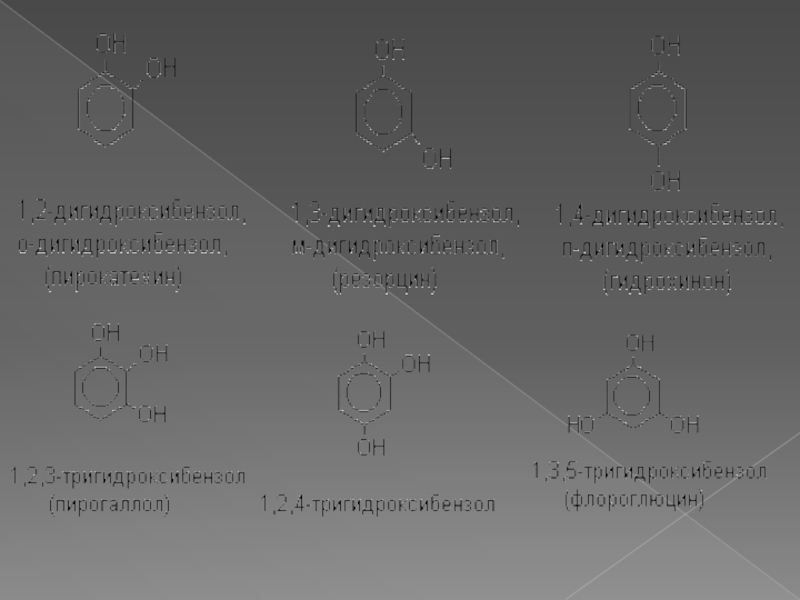
Классификация
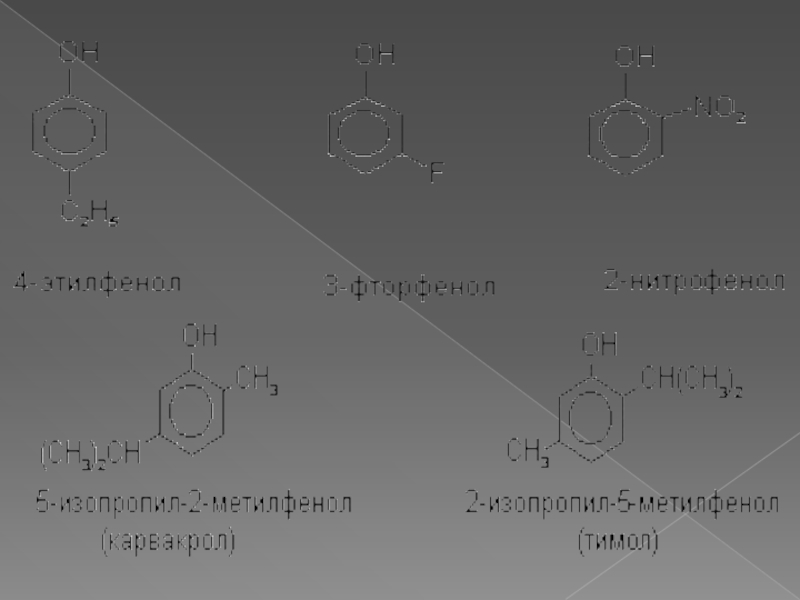
Номенклатура
Изомерия
Получение
Физические свойства
Химические свойства
Применение
Слайд 9Получение фенола
1. Из натриевых солей бензолсульфокилоты
2. Окисление кумола (изопропилбензола)
3. Получение из
галогенаренов
Слайд 10Фенол - бесцветные, розовеющие при хранении на воздухе, кристаллы с характерным
запахом.
Хорошо растворим в ацетоне, и других органических растворителях, умеренно - в воде при температуре выше 66 0C растворяется.
При попадании на кожу вызывает ожоги. Ядовит.
Хорошо растворим в ацетоне, и других органических растворителях, умеренно - в воде при температуре выше 66 0C растворяется.
При попадании на кожу вызывает ожоги. Ядовит.
Физические свойства
Слайд 12I. Кислотные свойства
1. Фенол реагирует с щелочными металлами, с щелочами с
образованием фенолятов
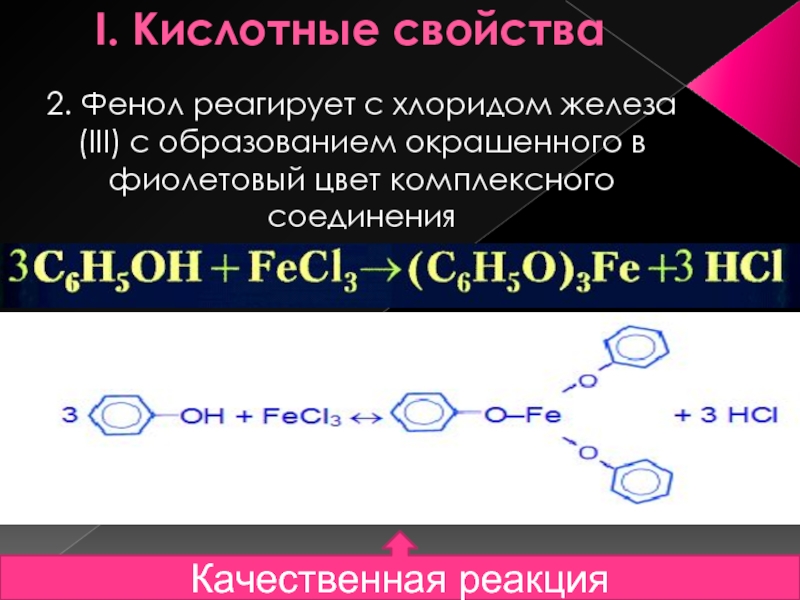
Слайд 13I. Кислотные свойства
2. Фенол реагирует с хлоридом железа (III) с образованием
окрашенного в фиолетовый цвет комплексного соединения
Качественная реакция
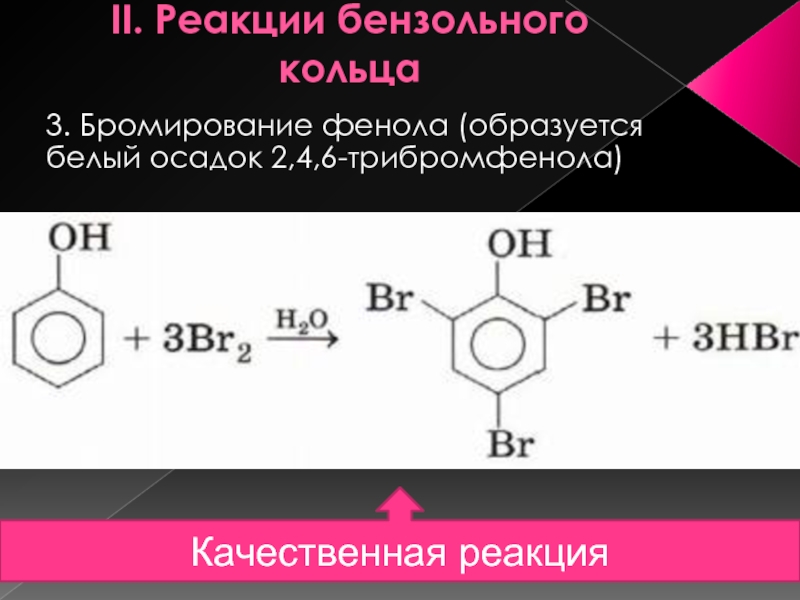
Слайд 14II. Реакции бензольного кольца
3. Бромирование фенола (образуется белый осадок 2,4,6-трибромфенола)
Качественная реакция
Слайд 15II. Реакции бензольного кольца
4. Нитрование фенола (разбавленной азотной кислотой при комнатной
температуре)
Слайд 16II. Реакции бензольного кольца
Нитрование фенола концентрированной азотной кислотой (образуется 2,4,6-тринитрофенол —
пикриновая кислота, взрывчатое вещество)
Слайд 17+ H2O
+ H2O
5. Реакция сульфирования
о - фенолсульфокислота
п - фенолсульфокислота
II. Реакции бензольного
кольца
Слайд 24В трёх пробирках без подписи находятся водные растворы пропанола-1, глицерина и
фенола. С помощью каких реагентов можно определить каждый из растворов?
Напишите уравнения соответствующих реакций.
Слайд 25Массовые доли углерода и водорода в гомологе фенола равны соответственно 77,78
и 7,41%. Определите формулу вещества. Сколько изомерных фенолов имеют такую формулу?
Слайд 26Расположите указанные вещества в порядке усиления кислотных свойств: а) фенол; б)
2-метилфенол;
в) 2,4,6-триметилфенол;
г) 2,4,6-тринитрофенол;
д) 4-нитрофенол.
Слайд 28Смесь предельного одноатомного спирта и фенола массой 3,25 г реагирует с
600 г 2%-й бромной воды. Такая же смесь реагирует с избытком натрия, при этом образуется 448 мл газа (н. у.). Определите молекулярную формулу предельного одноатомного спирта и массовые доли веществ в смеси.
Ответ: С3Н7ОН; 27,7% С3Н7ОН, 72,3% С6Н5ОН.