- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Етилен і ацетилен – ненасичені вуглеводні презентация
Содержание
- 1. Етилен і ацетилен – ненасичені вуглеводні
- 2. Щоб пізнати – треба навчитися спостерігати
- 3. М е т а ознайомитися із
- 4. План 1. Поняття про ненасичені вуглеводні.
- 5. Ненасичені вуглеводні – органічні сполуки, що мають
- 6. Будова етилену СН2 = СН2
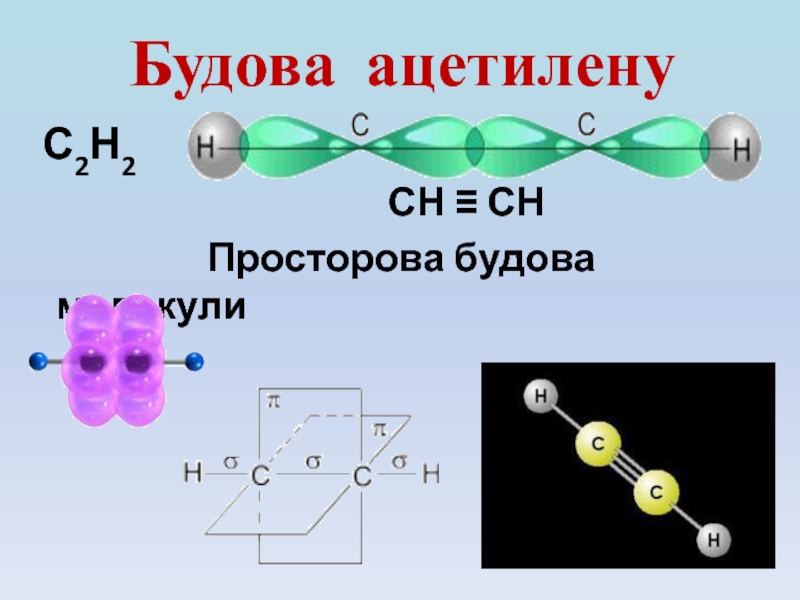
- 7. Будова ацетилену С2Н2
- 8. Фізичні властивості етилену С2Н4 безбарвний газ; добре
- 9. Добування етилену В лабораторії добувають: 1) дегідратація
- 10. Фізичні властивості С2Н2 безбарвний газ; майже
- 11. Добування ацетилену 1836р. - відкритий Е. Деві
- 12. Хімічні властивості етилену Горіння (з виділенням великої
- 13. Хімічні властивості ацетилену Горіння (яскравим кіптявим полум’ям):
- 14. Застосування Етилен Ацетилен Висока реакційна здатність зумовлює
- 15. Дайте відповіді на питання 1. Ацетилен у
- 16. Заплановані результати
- 17. Домашнє завдання Вивчити відповідний матеріал підручника. Вивчити основні поняття теми. Виконати письмове завдання.
Слайд 1Етилен і ацетилен – ненасичені вуглеводні
Міщук Сергій Леонідович,
вчитель хімії
Трифонівської
школи I-III ступенів
Слайд 3 М е т а
ознайомитися із основними фізико-хімічними властивостями, будовою та
навчитися складати рівняння реакцій, що характеризують хімічні властивості ненасичених вуглеводнів;
навчитися встановлювати причинно-наслідкові зв’язки між будовою і властивостями
Слайд 4 План
1. Поняття про ненасичені вуглеводні. Номенклатура.
2. Будова молекул етену та
3. Фізичні властивості, добування.
4. Хімічні властивості етену та етину.
5. Застосування ненасичених вуглеводнів.
Слайд 5Ненасичені вуглеводні – органічні сполуки, що мають кратні зв’язки між атомами
Етиленові вуглеводні - органічні сполуки, що мають один подвійний зв’язок між атомами Карбону.
Загальна формула СnH2n
С2Н4 - етен (етилен)
С3Н6 - пропен
С4Н8 - бутен
Ацетиленові вуглеводні - органічні сполуки, що мають один потрійний зв’язок між атомами Карбону.
Загальна формула - СnH2n - 2
С2Н2 - етин (ацетилен)
С3Н4 - пропін
С4Н6 - бутин
Слайд 8Фізичні властивості етилену
С2Н4
безбарвний газ;
добре розчинний в органічних розчинниках;
tплавл = - 169,2
вибухонебезпечний
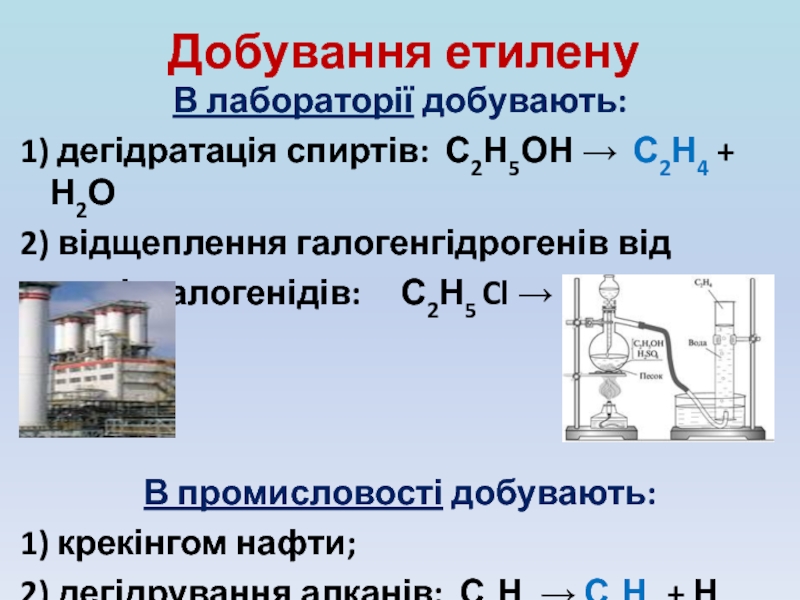
Слайд 9Добування етилену
В лабораторії добувають:
1) дегідратація спиртів: С2Н5ОН → С2Н4 + Н2О
2)
алкілгалогенідів: С2Н5 Cl → С2Н4 + НCl
В промисловості добувають:
1) крекінгом нафти;
2) дегідрування алканів: С2Н6 → С2Н4 + Н2
Слайд 10Фізичні властивості
С2Н2
безбарвний газ;
майже без запаху;
малорозчинний у воді, але під тиском
tкип = - 84 ̊С;
легший за повітря;
вибухонебезпечний
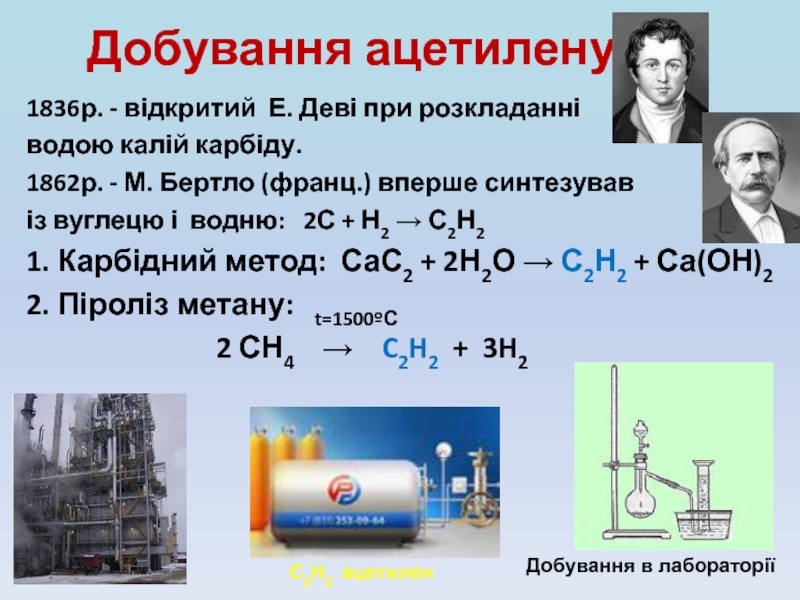
Слайд 11Добування ацетилену
1836р. - відкритий Е. Деві при розкладанні
водою калій карбіду.
1862р.
із вуглецю і водню: 2С + Н2 → С2Н2
1. Карбідний метод: СаС2 + 2Н2О → С2Н2 + Са(ОН)2
2. Піроліз метану: t=1500ºС
2 СН4 → C2H2 + 3H2
Добування в лабораторії
C2H2 ацетилен
Слайд 12Хімічні властивості етилену
Горіння (з виділенням великої кількості теплоти): С2Н4 + 3O2
2. Реакції приєднання по місцю розриву
π - зв’язку: СН2 = СН2
а) гідрування - приєднання водню: С2Н4 + Н2→ С2Н6
б) галогенування - приєднання галогенів:
С2Н4 + Br2 →С2Н4Br2
Якісне визначення ненасичених
вуглеводнів - знебарвлення розчину
калій перманганату і бромної води
Слайд 13Хімічні властивості ацетилену
Горіння (яскравим кіптявим полум’ям):
2С2Н2 + 5O2 → 4СО2
2. Реакції приєднання по місцю розриву
π - зв’язків відбуваються у дві стадії
а) гідрування (каталітичне): kat
С2Н2 + Н2→ С2Н4
С2Н4 + Н2→ С2Н6
б) галогенування: С2Н2 + Cl2 → С2Н2 Cl2 (дихлороетен)
С2Н2Cl 2 + Cl2 →С2Н2Cl4 (дихлороетан)
Якісне визначення ненасичених вуглеводнів - знебарвлення бромної води розчину калій перманганату.
Слайд 14Застосування
Етилен
Ацетилен
Висока реакційна здатність зумовлює використання в хімічній промисловості для добування етанолу
Використовують для дозрівання плодів
Використовують для добування полімеру поліетилену
70% ацетилену використовується для потреб органічного синтезу: виробництво етанолу, ацетальдегіду, оцтової кислоти, полімерів, синтетичних каучуків, органічних розчинників
30% ацетилену використовується для автогенного зварювання і різання металів
Слайд 15Дайте відповіді на питання
1. Ацетилен у лабораторії добувають взаємодією:
в) кальцій карбіду і води; г) етену та води.
2. Скільки спільних ковалентних електронних пар є між атомами Карбону в молекулі етилену ?
а) одна; б) дві; в) три; г) чотири
3. Яка загальна формула ненасичених вуглеводнів ряду ацетилену?
а) СnH2n; б) СnH2n+2; в) СnH2n+4; г) СnH2n-2
4. Яка речовина належить до ненасичених вуглеводнів ряду етилену?
а) С2Н2; б) С4Н10; в) С2Н6; г) С3Н6
5. Ненасичені вуглеводні можуть приєднувати:
а) галогени; б) галоген гідрогени;
в) лише водень; г) натрій хлорид
6. Вкажіть продукти реакції, що утворюються при гідруванні ацетилену:
а) етан; б) пропан; в) етен; г) метан
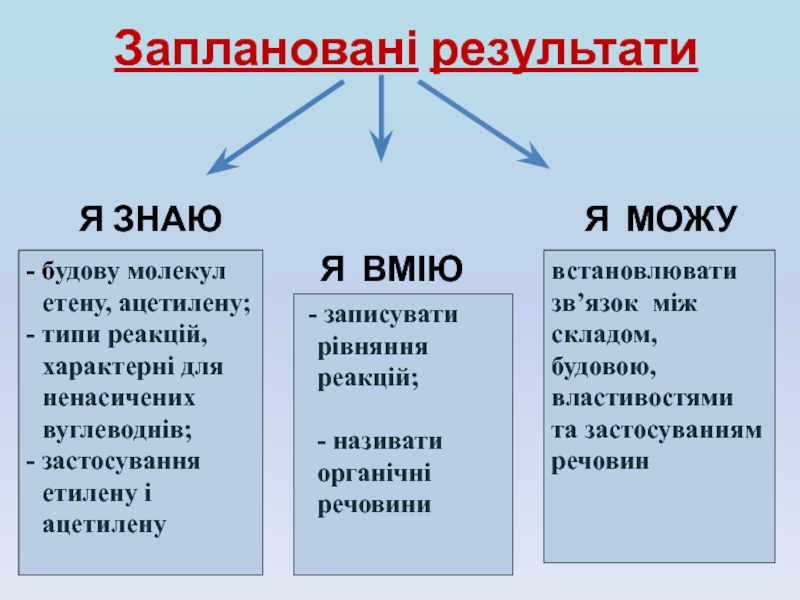
Слайд 16Заплановані результати
Я ЗНАЮ
Я ВМІЮ
- будову молекул етену, ацетилену;
- типи реакцій, характерні для ненасичених вуглеводнів;
- застосування етилену і ацетилену
записувати рівняння реакцій;
- називати органічні речовини
встановлювати зв’язок між складом, будовою, властивостями та застосуванням речовин