- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Электролиз презентация
Содержание
- 1. Электролиз
- 2. УМК «ХИМИЯ» Тема лекции:
- 4. СОДЕРЖАНИЕ Основные понятия
- 5. Основные понятия Электролиз – это совокупность окислительно-восстановительных
- 6. содержание Е = -nF/ΔG
- 7. Электролиз расплавов электролитов содержание В
- 10. Электролиз расплавов электролитов содержание При
- 14. Катодные процессы На катоде идет процесс восстановления
- 16. Катодные процессы содержание При электролизе
- 19. Электролиз с растворимым анодом
- 20. Катодные процессы содержание Выделение водорода
- 21. Анодные процессы содержание Red
- 22. содержание С
- 23. содержание Анионы кислородсодержащих кислот SO42-,
- 24. содержание Пpи высоких анодных
- 26. Законы электролиза содержание Установил (1833-1834)
- 28. Законы электролиза содержание I
- 29. содержание Число Фарадея F
- 33. 1. Ахметов Н.С. Общая и неорганическая химия.
Слайд 3 Цель
Компетенции, формируемые у студента:
Умения:
прогнозировать на основе современных представлений о строении атомов и химической связи, реакции, протекающие при электролизе в расплавах и растворах электролитов.
Слайд 4СОДЕРЖАНИЕ
Основные понятия
Электролиз расплавов электролитов
Электролиз
Катодные процессы
Поведение ионов металлов
Перенапряжение
Анодные процессы
Перенапряжение
Поведение анионов
Электролиз с растворимым анодом
Законы электролиза
Литература
Слайд 5Основные понятия
Электролиз – это совокупность окислительно-восстановительных процессов, которые протекают на электродах,
Основные понятия:
содержание
Отрицательный полюс источника постоянного тока присоединяют к электроду, который называют катодом;
положительный полюс к электроду, который называют анодом.
Слайд 6
содержание
Е = -nF/ΔG
Если ЭДС будет отрицательной, то самопроизвольное протекание ОВР
Основные понятия
E > 0, ΔG < 0 - самопроизвольный процесс протекает в прямом направлении (гальванический элемент).
E < 0, ΔG > 0 - для проведения реакции в прямом направлении необходимо приложить внешнюю ЭДС (электролиз).
Слайд 7Электролиз расплавов электролитов
содержание
В простейших бинарных электролитах типа MeHal , MeHal2 (Me
При этом на катоде протекает полуреакция восстановления катиона металла:
на аноде - полуреакция окисления галогенид-аниона:
Men+ + ne = Me
2Cl- - 2e = Cl2
Слайд 10Электролиз расплавов электролитов
содержание
При электролизе расплава гидродифторида калия (анод – угольный, катод
2НF2- + 2е = Н2 + 4F-
2НF2- - 2е = F2 + 2HF
2F2- - 2е = F2
2НF + 2е = Н2 + 2F-
На аноде:
На катоде:
Слайд 14Катодные процессы
На катоде идет процесс восстановления окислителя:
содержание
Ox + ne = Red
Men+
2Н+ + 2е = Н2
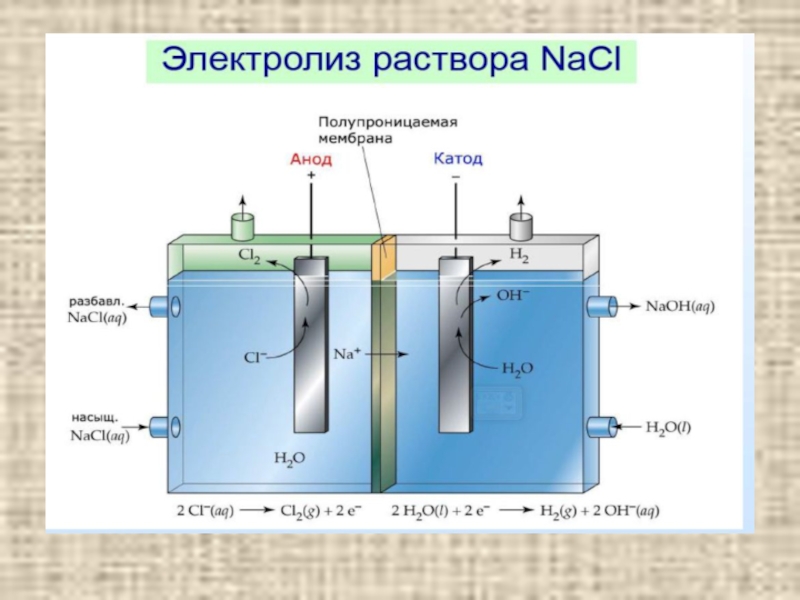
2Н2О + 2е = 2ОН- + Н2
(в кислой среде)
(в нейтральной и щелочной средах)
Слайд 16Катодные процессы
содержание
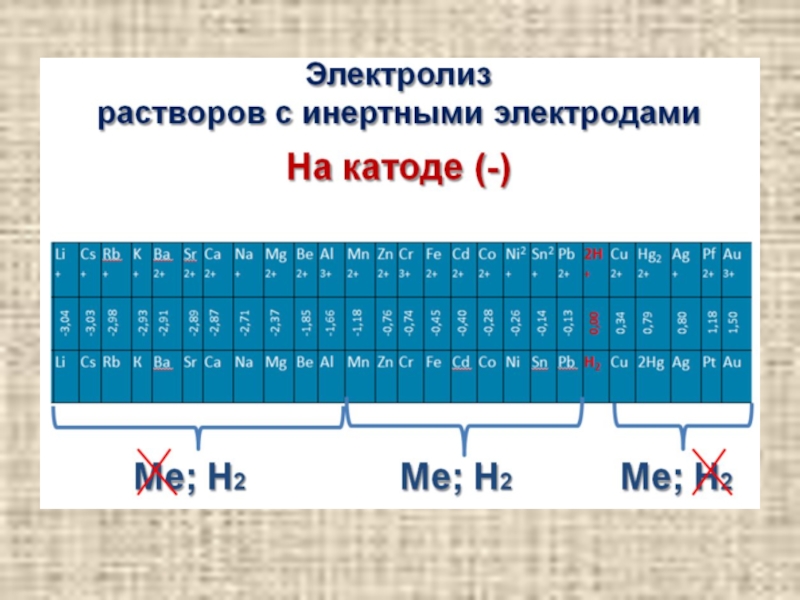
При электролизе водных растворов все металлы можно разделить на три
1. Металлы, осаждение которых на катоде не сопровождается выделением водорода. К ним относятся металлы, стоящие в ряду стандартных потенциалов за водородом (медь, серебро, золото и др.).
2. Металлы, осаждение которых на катоде сопровождается выделением водорода. В ряду стандартных потенциалов эти металлы находятся между марганцем и водородом
(-1,0 < ЕОМеn+/Ме< 0).
3. Металлы, которые в водных растворах не могут быть получены. В эту группу входят щелочные, щелочноземельные металлы, а также магний и алюминий.
Слайд 19Электролиз с растворимым анодом
содержание
Электролиз с растворимым анодом используют для рафинирования некоторых
Процесс электролитического рафинирования состоит в анодном растворении загрязненного примесями (чернового) металла и последующем его катодном осаждении.
Me - ne = Men+
Слайд 20Катодные процессы
содержание
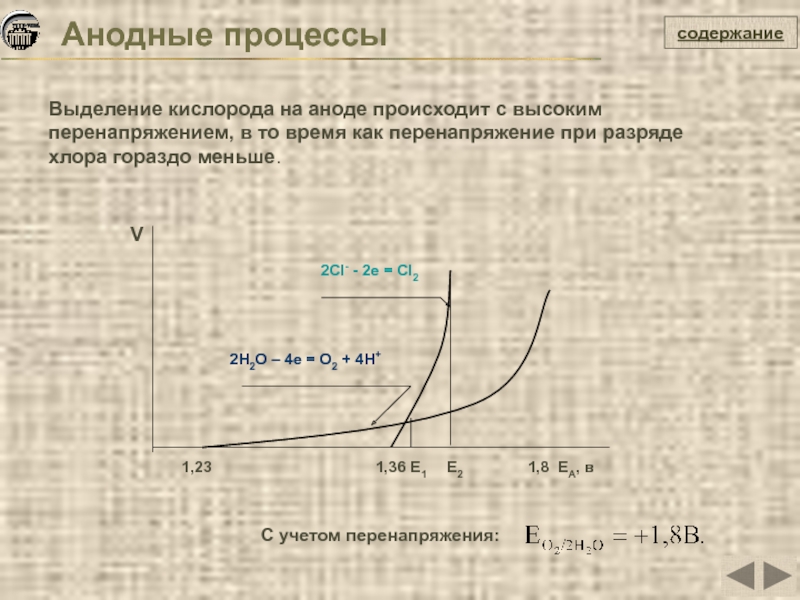
Выделение водорода на катоде происходит с высоким перенапряжением, в то
С учетом перенапряжения:
Слайд 21
Анодные процессы
содержание
Red – ne = Ох
На аноде идет процесс окисления восстановителя:
2Н2О
4ОН- - 4е = О2 + 2Н2О
В щелочной среде
В кислой и нейтральной среде
Me - ne = Men+
Растворимый анод
2Cl- - 2e = Cl2
Разряд анионов
Слайд 22
содержание
С учетом перенапряжения:
Выделение кислорода на аноде происходит с высоким перенапряжением,
Анодные процессы
Слайд 23
содержание
Анионы кислородсодержащих кислот SO42-, PO43-, NO3- и др., в которых центральный
Анодные процессы
Фтор электролизом водных растворов получить невозможно:
Ионы галогенов: Cl-, Br-, I- в водном растворе легко разряжаются:
2Hal- - 2e = Hal2
Слайд 24
содержание
Пpи высоких анодных плотностях тока некотоpые анионы могут окисляться до пеpоксоанионов,
2SO42− − 2e = S2O82−
Анодные процессы
H2PO4− + 2OH−−2e = H2PO5− +H2O
Слайд 26Законы электролиза
содержание
Установил (1833-1834) законы электролиза, названные его именем.
Фарадей (Faraday) Майкл
Слайд 28Законы электролиза
содержание
I закон. Масса вещества, окисленного на аноде или восстановленного на
m = kQ
II закон. Массы окисляющихся или восстанавливающихся на электродах веществ при пропускании одного и того же количества электричества пропорциональны их химическим эквивалентам.
M(г) = MIT/nF
V(л) = 22,4IT/nF
Слайд 29
содержание
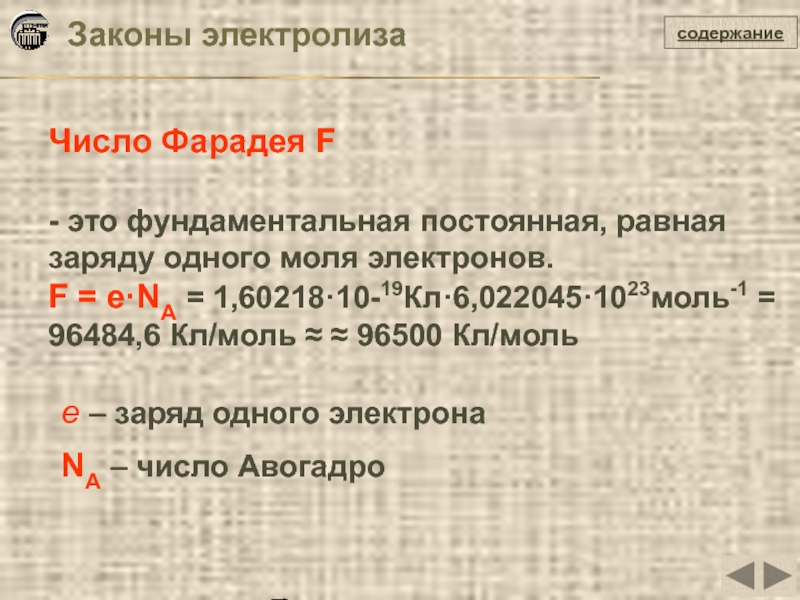
Число Фарадея F
- это фундаментальная постоянная, равная заряду одного моля
F = e·NA = 1,60218·10-19Кл·6,022045·1023моль-1 = 96484,6 Кл/моль ≈ ≈ 96500 Кл/моль
e – заряд одного электрона
NA – число Авогадро
Законы электролиза
Слайд 331. Ахметов Н.С. Общая и неорганическая химия. М.: Высшая школа. 2002.
2. О.М. Полторак, Л.М. Ковба. «Физико-химические основы неорганической химии». М.: МГУ, 1994.
3. В.И. Горшков, И.А. Кузнецов. «Физическая химия». М.: МГУ, 1993.
4. А. Джонсон. Термодинамические аспекты в курсе неорганической химии. М.: Мир. 1985.
5. Анорганикум. Под ред. Л. Кольдица. М. Мир. 1984. Т.1. 6.
Хьюи Дж. Неорганическая химия. Строение вещества и реакционная способность. М., Химия, 1987.
7. Фичини Ж., Ламброзо-Бадер Н., Депезе Ж.-К. Основы физической химии. М. Мир. 1972. стр.276-283.
8. Дж. Кемпбел. Современная общая химия. М.:Мир. 1975г. Т.2. стр.90. гл.20., Т3.
9. Дикерсон Р., Грей Г., Хейт Дж. Основные законы химии. М.: Мир,1982. Т. 2.
10. Б.Б.Дамаскин, О.А.Петрий. Электрохимия. М: Высшая школа, 1987.
11. CRC Hand book of Chemistry and Physics. 82 издание. 2001-2002.
Список литературы
содержание