- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Электролитическая диссоциация. Реакции ионного обмена презентация
Содержание
- 1. Электролитическая диссоциация. Реакции ионного обмена
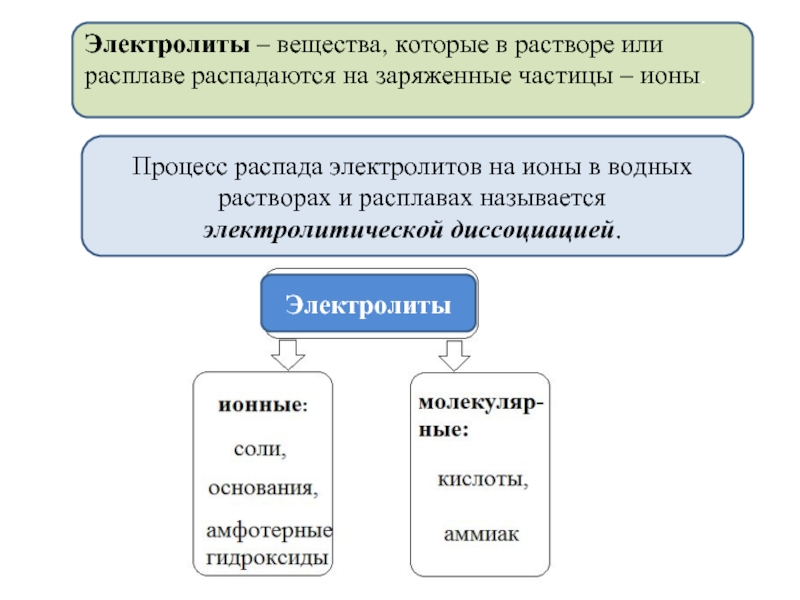
- 2. Электролиты – вещества, которые в растворе или
- 3. Ионные кристаллы (истинные электролиты) Ион-дипольное взаимодействие
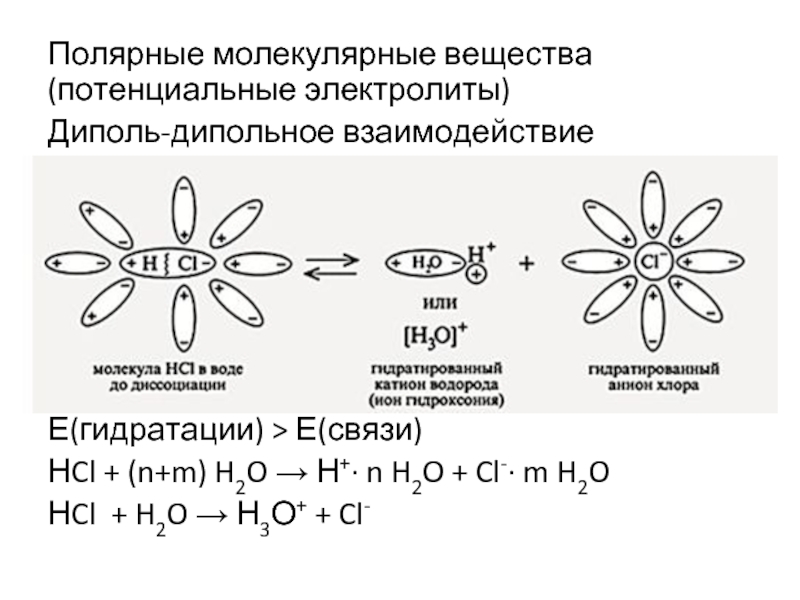
- 4. Полярные молекулярные вещества (потенциальные электролиты) Диполь-дипольное взаимодействие
- 5. Для молекулярных электролитов Степень диссоциации (ионизации):
- 7. Кислоты – электролиты, которые при диссоциации в
- 8. Основания – электролиты, которые при диссоциации в
- 9. Амфотерные гидроксиды (амфолиты) – электролиты, которые могут
- 10. Ступенчато диссоциируют кислые, оснóвные и комплексные соли:
- 11. Средние, двойные и смешанные соли диссоциируют в
- 12. Диссоциация воды H2O ↔ H+ + OH−
- 13. При [H+]=[OH−] =10-7, рН = –
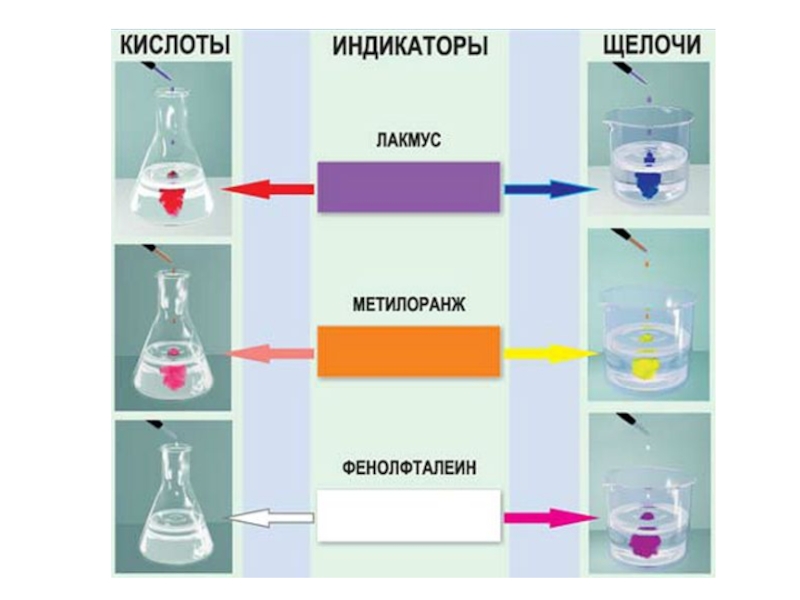
- 14. Окраска лакмуса:
- 15. Реакции ионного обмена
- 16. Реакция нейтрализации 1) Сильная кислота + щелочь
- 17. 2) Сильная кислота + щелочь с образованием
- 18. H2S + 2KOH → K2S + 2
- 19. 4) H2S + 2NH3 →
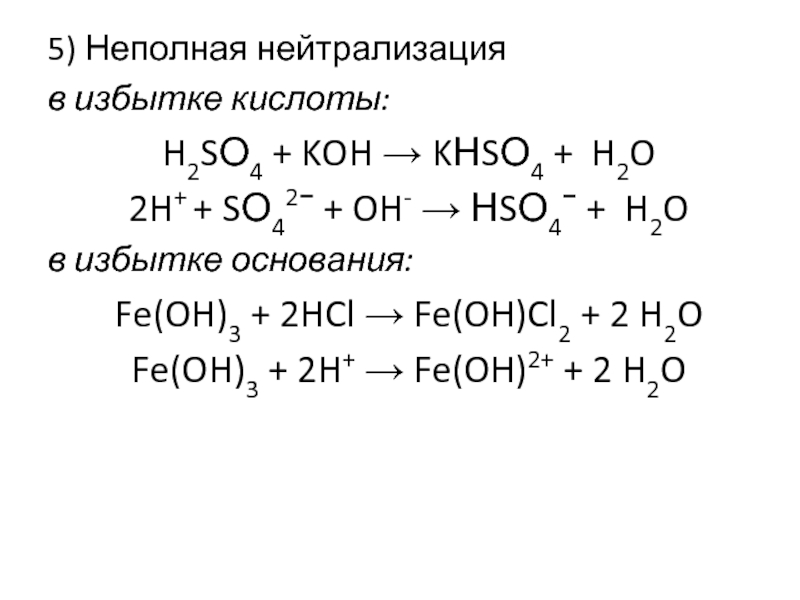
- 20. 5) Неполная нейтрализация в избытке кислоты:
- 21. Гидролиз солей Не
- 22. 1) Соль, образованная сильным основанием и слабой
- 23. 2) Соль, образованная слабым основанием и сильной
- 24. 3) Соль, образованная слабым основанием и слабой
- 25. Совместный гидролиз 1) Соли металлов со степенью
- 26. 2) Соли металлов со степенью окисления +2
- 27. Гидролиз - эндотермический процесс
Слайд 2Электролиты – вещества, которые в растворе или расплаве распадаются на заряженные
Процесс распада электролитов на ионы в водных растворах и расплавах называется электролитической диссоциацией.
Электролиты
Слайд 3Ионные кристаллы (истинные электролиты)
Ион-дипольное взаимодействие
Е(гидратации) > Е(решетки)
NaCl + (n+m) H2O →
NaCl → Na+ + Cl-
Слайд 4Полярные молекулярные вещества (потенциальные электролиты)
Диполь-дипольное взаимодействие
Е(гидратации) > Е(связи)
НCl + (n+m) H2O
НCl + H2O → Н3О+ + Cl-
Слайд 5Для молекулярных электролитов
Степень диссоциации (ионизации):
Сильные электролиты:
1) соли;
2) щелочи – LiOH, NaOH,
3) кислоты (α = 1) – H2SO4, HCl, HNO3, HBr, HI, HClO4, HМnO4;
Слайд 7Кислоты – электролиты, которые при диссоциации в качестве катионов образуют только
HCl → H+ + Cl–
H2SO4 → H+ + HSO4− (I ступень)
HSO4− H+ + SO42- (II ступень)
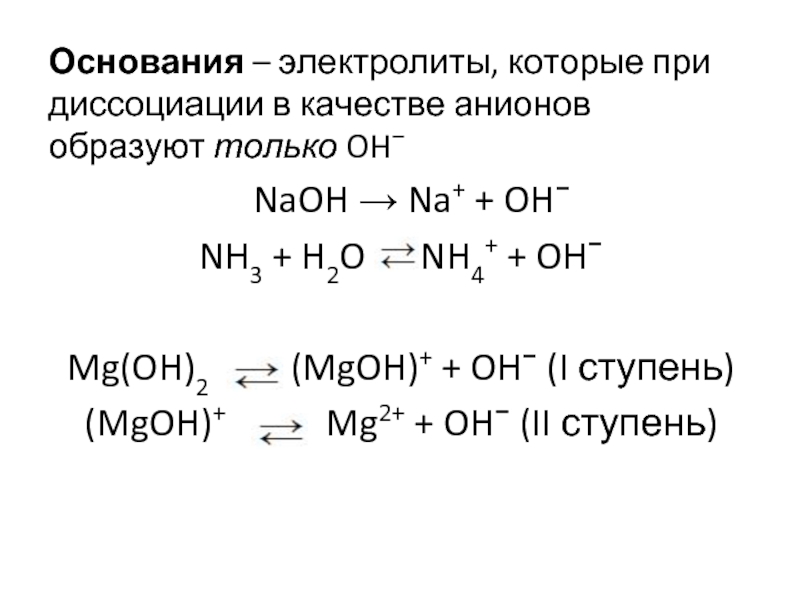
Слайд 8Основания – электролиты, которые при диссоциации в качестве анионов образуют только
NaOH → Na+ + OH−
NH3 + H2O NH4+ + OH−
Mg(OH)2 (MgOH)+ + OH− (I ступень)
(MgOH)+ Mg2+ + OH− (II ступень)
Слайд 9Амфотерные гидроксиды (амфолиты) – электролиты, которые могут диссоциировать как по кислотному,
Be(OH)2 ↔ Be2+ + 2OH− (основный тип)
Be(OH)2 + 2H2O 2H+ + [Be(OH)4]2-
(кислотный тип)
Слайд 10Ступенчато диссоциируют кислые, оснóвные и комплексные соли:
КНСО3 → К+ + НСО3−
НСО3−
(CuOH)NO3 → Сu(OH)+ + NO3−
(CuOH)+ Cu2+ + OH−
Na2[Zn(OH)4] → 2 Na+ + [Zn(OH)4]2−
[Zn(OH)4]2− Zn2+ + 4 OH−
Слайд 11Средние, двойные и смешанные соли диссоциируют в одну стадию!
CaCl2 → Ca2+
Al2(SO4)3 → 2Al3+ +3SO42–
КFe(SO4)2 → К+ + Fe3+ + SO42-
Слайд 12Диссоциация воды
H2O ↔ H+ + OH−
[H+]·[OH−] = KW – константа
KW = 10-14 при 250С
следовательно, [H+]=[OH−] =10-7
Водородный показатель (рН) – десятичный логарифм молярной концентрации ионов водорода, взятый со знаком «минус»
рН = – lg[H+]
Слайд 13При [H+]=[OH−] =10-7,
рН = – lg10-7 =7 – нейтральная среда
при
при [H+] < 10-7, рН > 7 – среда щелочная
Слайд 15Реакции ионного обмена
В виде ионов записываются только сильные и растворимые в
Реакции ионного обмена всегда протекают в сторону связывания ионов.
Ионы связываются с образованием газа; осадка; слабого электролита.
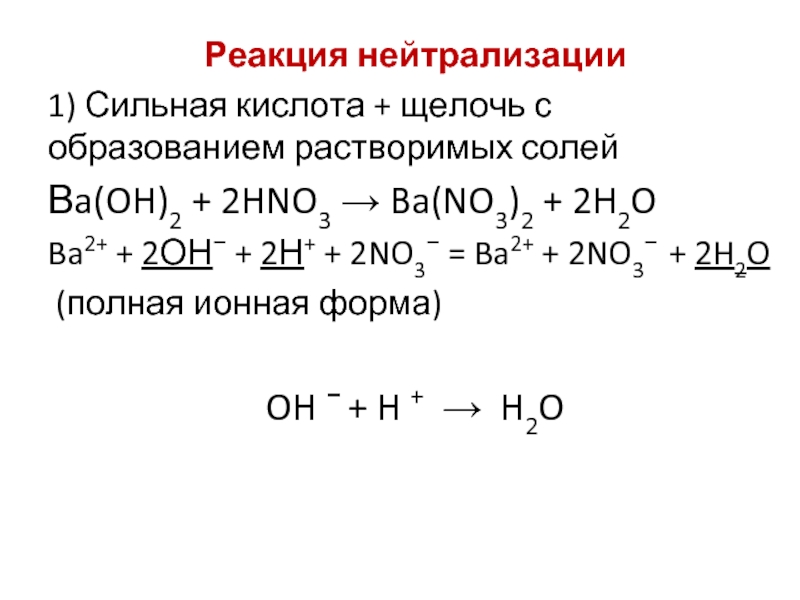
Слайд 16Реакция нейтрализации
1) Сильная кислота + щелочь с образованием растворимых солей
Вa(OH)2 +
Ba2+ + 2ОН− + 2Н+ + 2NO3− = Ba2+ + 2NO3− + 2H2O
(полная ионная форма)
OH − + H + → H2O
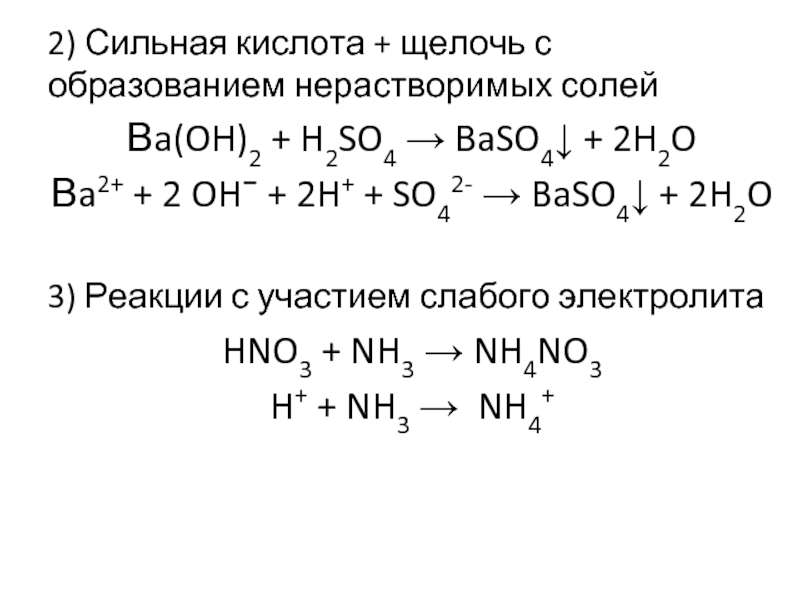
Слайд 172) Сильная кислота + щелочь с образованием нерастворимых солей
Вa(OH)2 + H2SO4
Вa2+ + 2 OH− + 2H+ + SO42- → BaSO4↓ + 2H2O
3) Реакции с участием слабого электролита
HNO3 + NH3 → NH4NO3
H+ + NH3 → NH4+
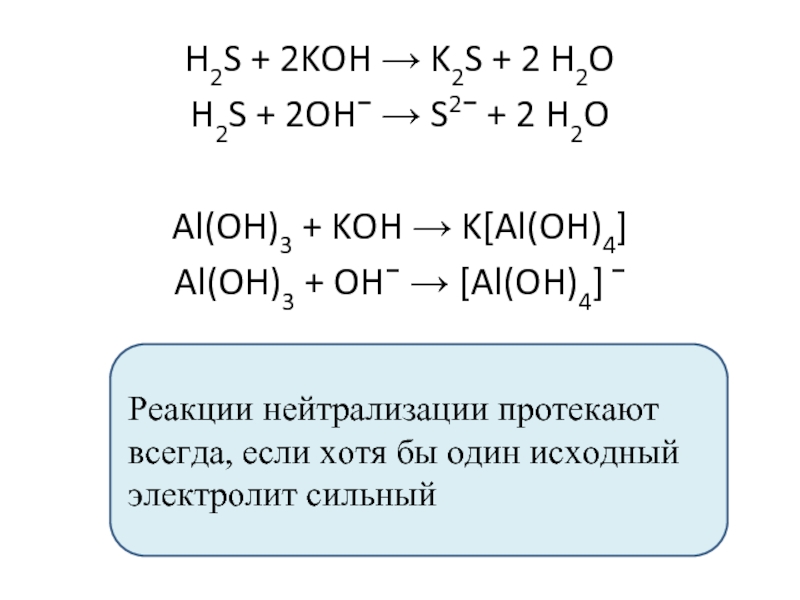
Слайд 18H2S + 2KOH → K2S + 2 H2O
H2S + 2OH− →
Al(OH)3 + KOH → K[Al(OH)4]
Al(OH)3 + OH− → [Al(OH)4] −
Реакции нейтрализации протекают всегда, если хотя бы один исходный электролит сильный
Слайд 194)
H2S + 2NH3 → (NH4)2S
H2S + 2NH3 → 2NH4+ + S2−
Mg(OH)2
ионная форма отсутствует
Al(OH)3 + H2S ≠ – реакция не идет
Реакция нейтрализации между двумя слабыми электролитами возможна, если продукт реакции (соль) существует в присутствии воды
Слайд 205) Неполная нейтрализация
в избытке кислоты:
H2SО4 + KOH → KНSО4 +
2H+ + SО42− + OH- → НSО4− + H2O
в избытке основания:
Fe(OH)3 + 2HCl → Fe(OH)Cl2 + 2 H2O
Fe(OH)3 + 2H+ → Fe(OH)2+ + 2 H2O
Слайд 21Гидролиз солей
Не подвергаются гидролизу соли:
Образованные только сильными электролитами (NaCl, KNO3, RbBr,
Нерастворимые;
Реакция обмена между ионами соли и молекулами воды
Слайд 221) Соль, образованная сильным основанием и слабой кислотой
- гидролиз ПО
K3PO4 – соль, образованная слабой кислотой и сильным основанием.
PO43- + НОН ⇄ НРО42- + ОН-
K3PO4 + Н2О ⇄ К2НРО4 + КОН
ОН- - среда щелочная; рН > 7
Слайд 232) Соль, образованная слабым основанием и сильной кислотой
- гидролиз ПО
CuCl2 – соль, образованная слабым основанием и сильной кислотой.
Cu+2 + НОН ⇄ CuOH+ +H+
CuCl2+H2O ⇄ (CuOH)Cl + HCl
H+ - среда кислая; рН < 7
Слайд 243) Соль, образованная слабым основанием и слабой кислотой
- гидролиз ПО
Гидролизуются соли –
Al2S3,Cr2S3(необратимо)
Al2S3 + H2O → Al(OH)3↓ + H2S↑
NH4F, CH3COONH4(обратимо)
NH4F + H2O ⇄ NH3 · H2O + HF
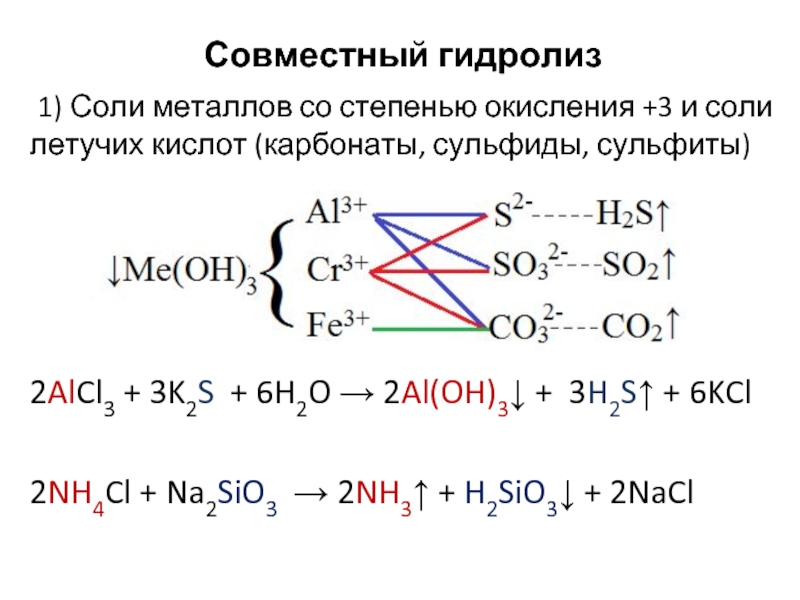
Слайд 25Совместный гидролиз
1) Соли металлов со степенью окисления +3 и соли летучих
2AlCl3 + 3K2S + 6H2O → 2Al(OH)3↓ + 3H2S↑ + 6KCl
2NH4Cl + Na2SiO3 → 2NH3↑ + H2SiO3↓ + 2NaCl
Слайд 262) Соли металлов со степенью окисления +2 (кроме кальция, стронция и
2 CuCl2 + 2Na2CO3 + H2O → (CuOH)2CO3↓ +
+ CO2↑ + 4 NaCl
Слайд 27Гидролиз - эндотермический процесс
KF
Какие факторы усиливают гидролиз?
Нагревание
Добавление воды
Как подавить (ослабить) процесс гидролиза?
Раствор делают максимально концентрированным;
Для смещения равновесия влево добавляют один из продуктов гидролиза – кислоту, если идёт гидролиз по катиону или щёлочь, если идёт гидролиз по аниону.
Пример: Al+3 + HOH ⇄ AlOH +2 + H+








![Диссоциация водыH2O ↔ H+ + OH− [H+]·[OH−] = KW – константа автопротолизаKW = 10-14 при](/img/tmb/3/238572/f5e97d91923494d86c4ab6bc24eacfbc-800x.jpg)
![При [H+]=[OH−] =10-7, рН = – lg10-7 =7 – нейтральная средапри [H+] > 10-7, рН](/img/tmb/3/238572/b4913f450cf4ebad21debb8b937d24ff-800x.jpg)