- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Диены. Сопряженные диены презентация
Содержание
- 1. Диены. Сопряженные диены
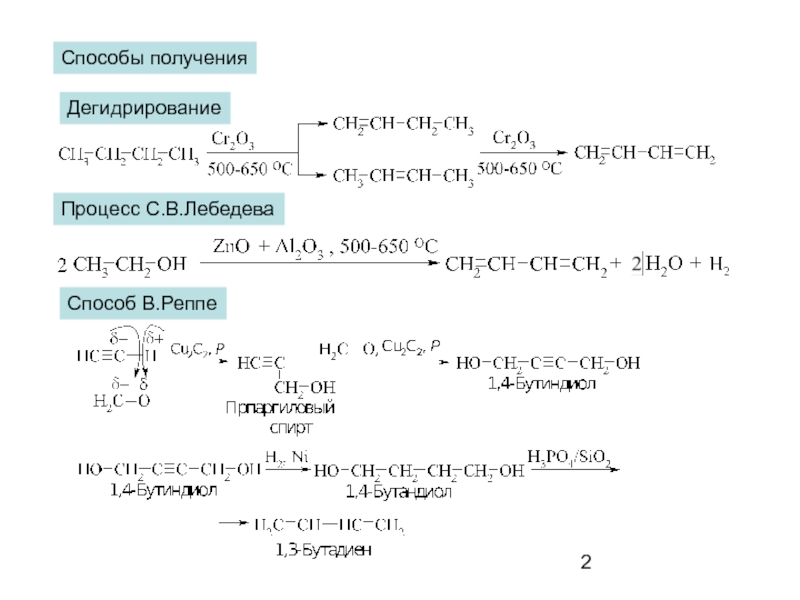
- 2. Способы получения Дегидрирование Процесс С.В.Лебедева Способ В.Реппе
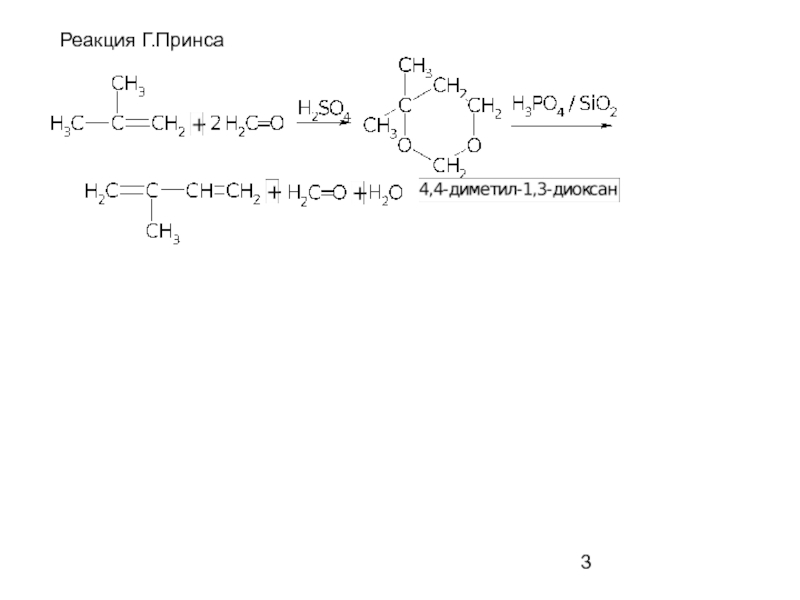
- 3. Реакция Г.Принса
- 4. Теплоты гидрирования алкенов и диенов Строение молекулы
- 5. Гибридизация атомов углерода и длины простых
- 6. Рис. Зависимость порядка связи углерод-углерод
- 7. Химические свойства Галогенирование и гидрогалогенирование Электрофильное присоединение
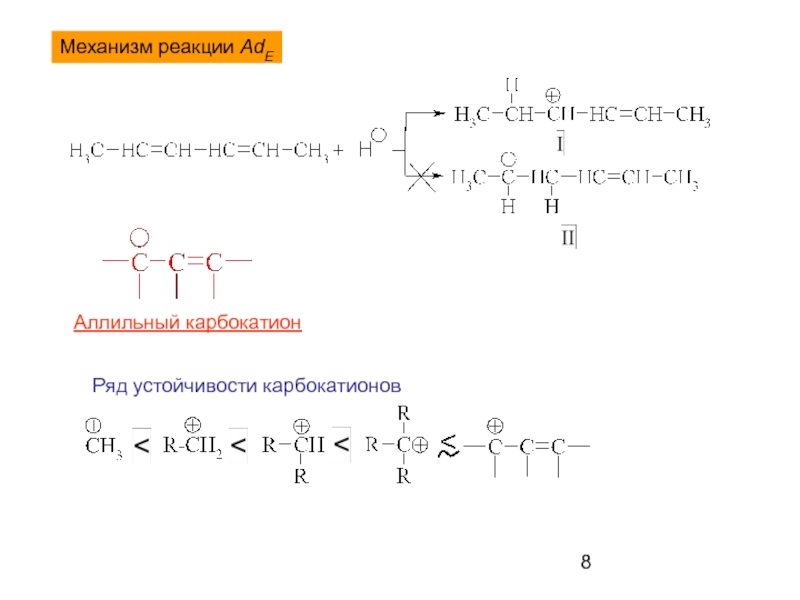
- 8. Механизм реакции AdE Аллильный карбокатион Ряд устойчивости карбокатионов
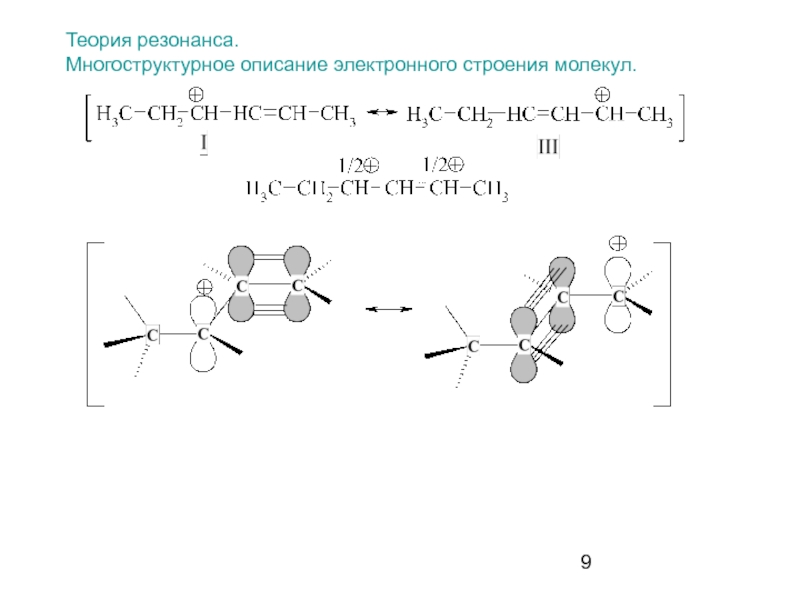
- 9. Теория резонанса. Многоструктурное описание электронного строения молекул.
- 10. Если молекула может быть представлена двумя или
- 11. Энергия реальной молекулы (резонансного гибрида) меньше, чем
- 12. Правила построения граничных структур. 1) Резонансные (граничные
- 13. При перемещении электронов помещайте отрицательный заряд на
- 14. 4) Энергия реальной молекулы ниже, чем энергия
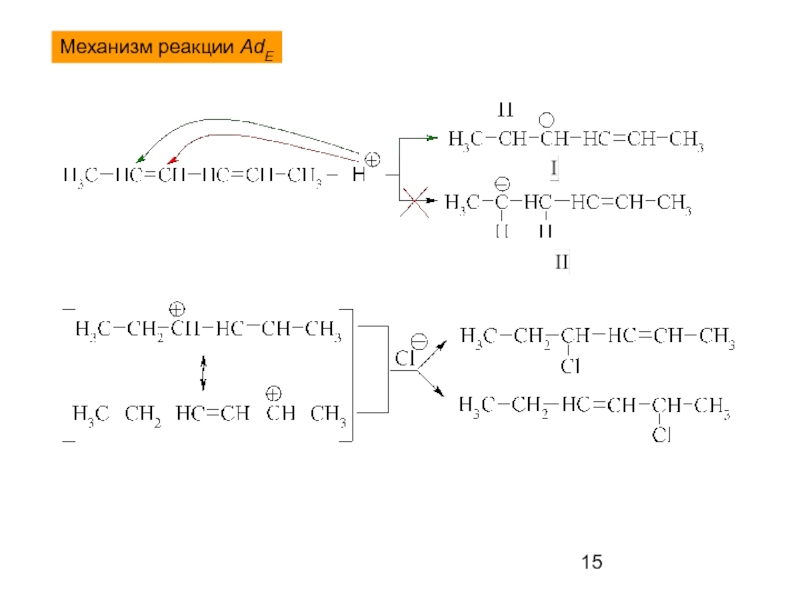
- 15. Механизм реакции AdE
- 16. 1,2- и 1,4-Присоединение. Кинетический контроль, термодинамический контроль.
- 17. при -80 °С образуется кинетически контролируемый продукт
- 18. при 40 °С образуется термодинамически контролируемый
- 19. Образование π-связи. Симметрия орбиталей. Электроциклические реакции.
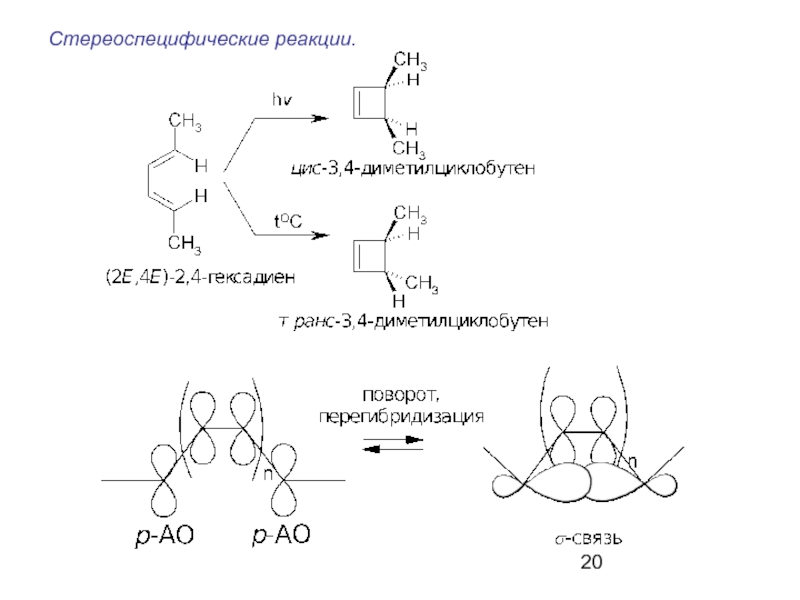
- 20. Стереоспецифические реакции.
- 21. Р.Вудворд, Р.Хофман (1965 г.) Принцип сохранения орбитальной
- 22. ВЗМО* возбужденной под действием УФ облучения молекулы
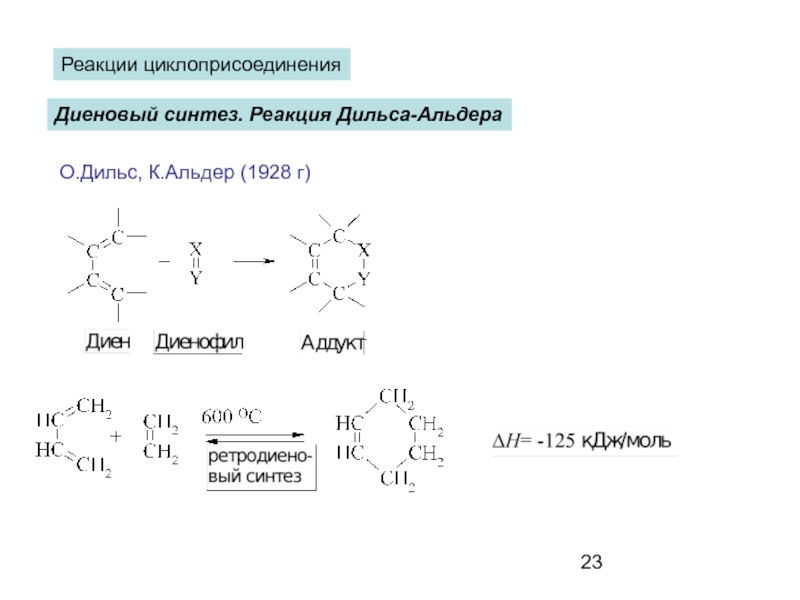
- 23. Диеновый синтез. Реакция Дильса-Альдера Реакции циклоприсоединения О.Дильс, К.Альдер (1928 г)
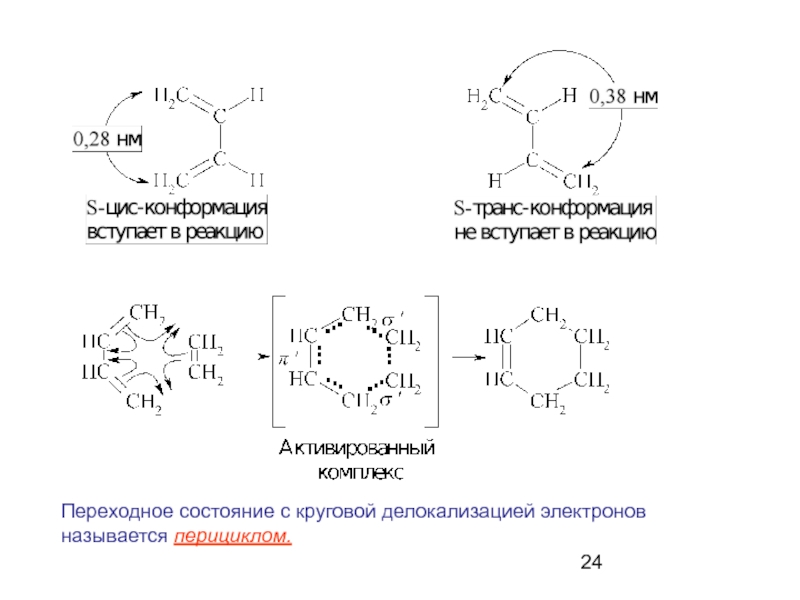
- 24. Переходное состояние с круговой делокализацией электронов называется перициклом.
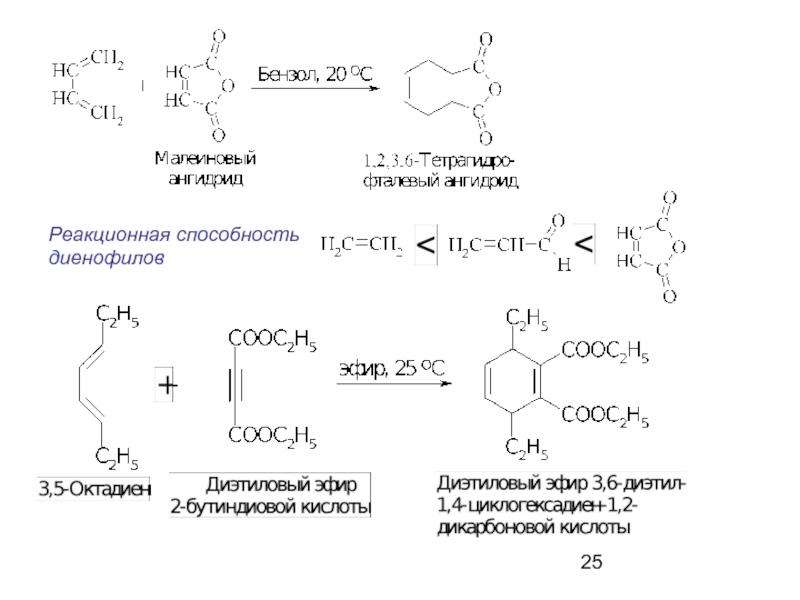
- 25. Реакционная способность диенофилов
- 26. Диен – донор, диенофил – акцептор. Орбитальный
- 27. Полимеризация
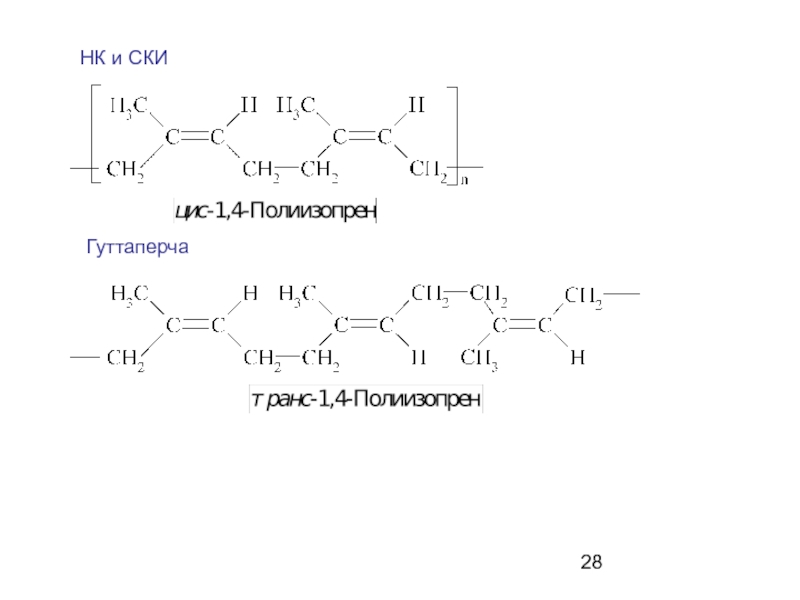
- 28. НК и СКИ Гуттаперча
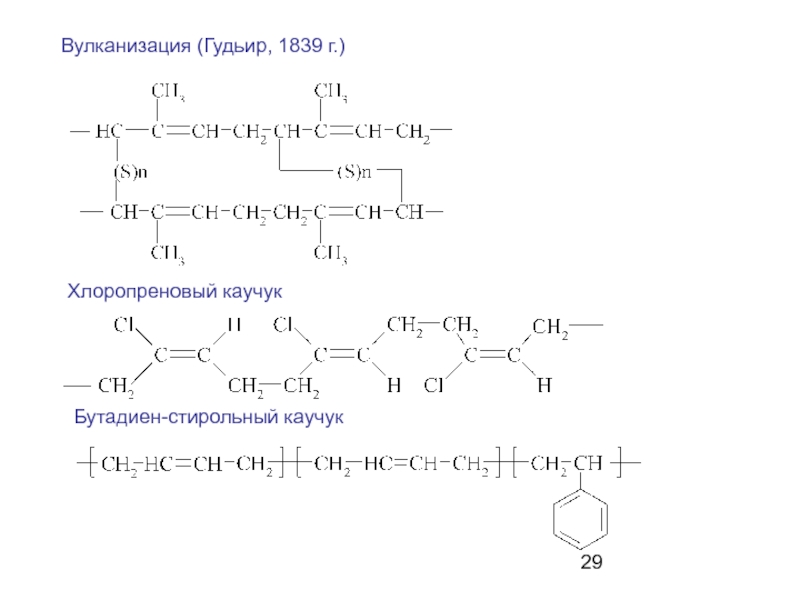
- 29. Вулканизация (Гудьир, 1839 г.) Хлоропреновый каучук Бутадиен-стирольный каучук
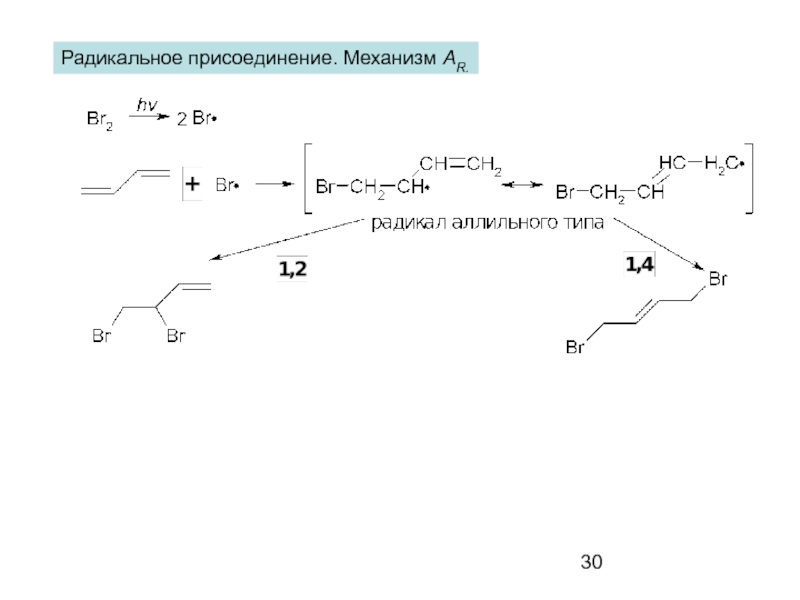
- 30. Радикальное присоединение. Механизм AR.
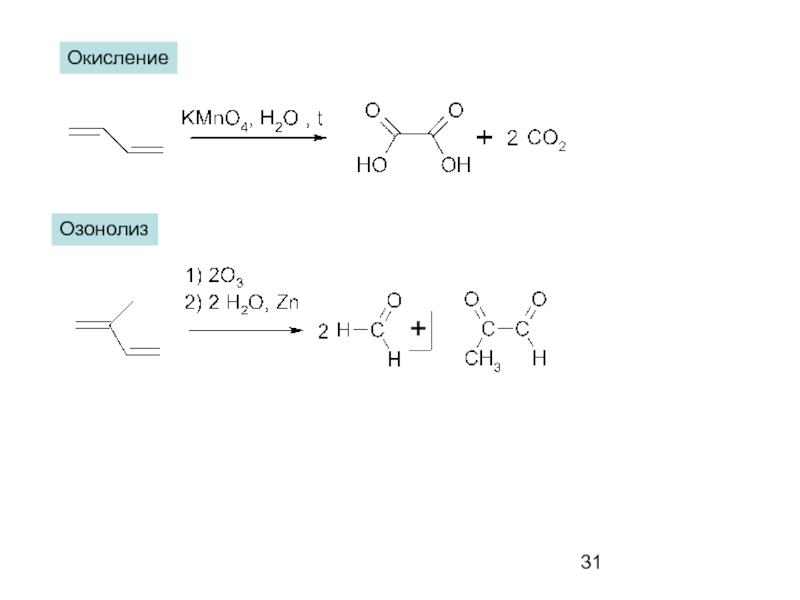
- 31. Окисление Озонолиз
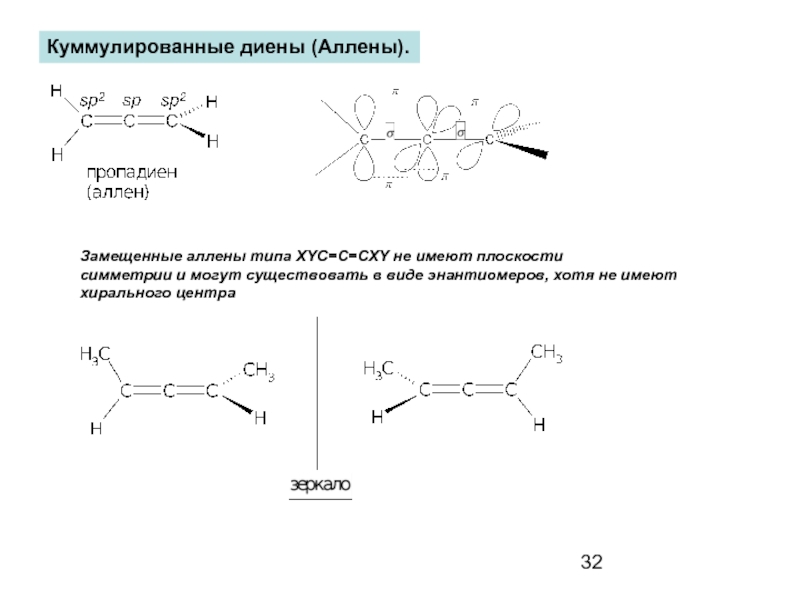
- 32. Куммулированные диены (Аллены). Замещенные аллены типа XYC=C=CXY
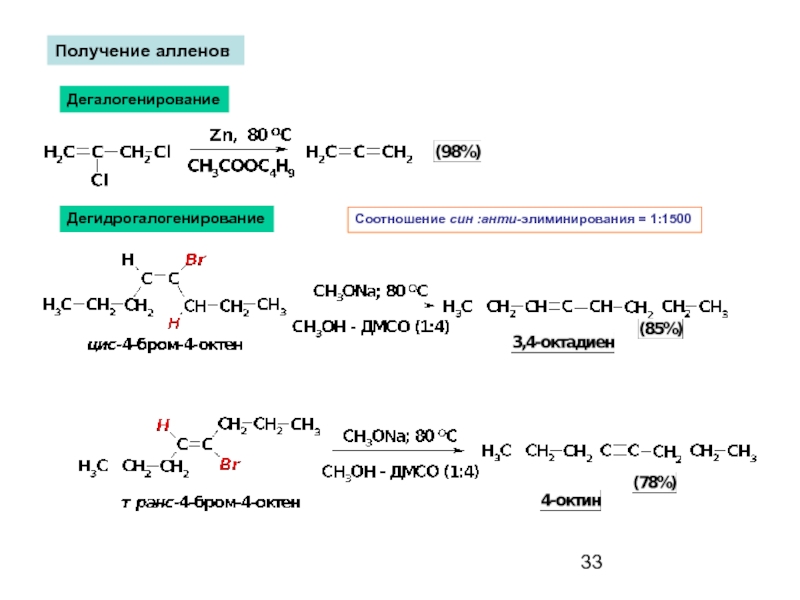
- 33. Получение алленов Дегалогенирование Дегидрогалогенирование Соотношение син :анти-элиминирования = 1:1500
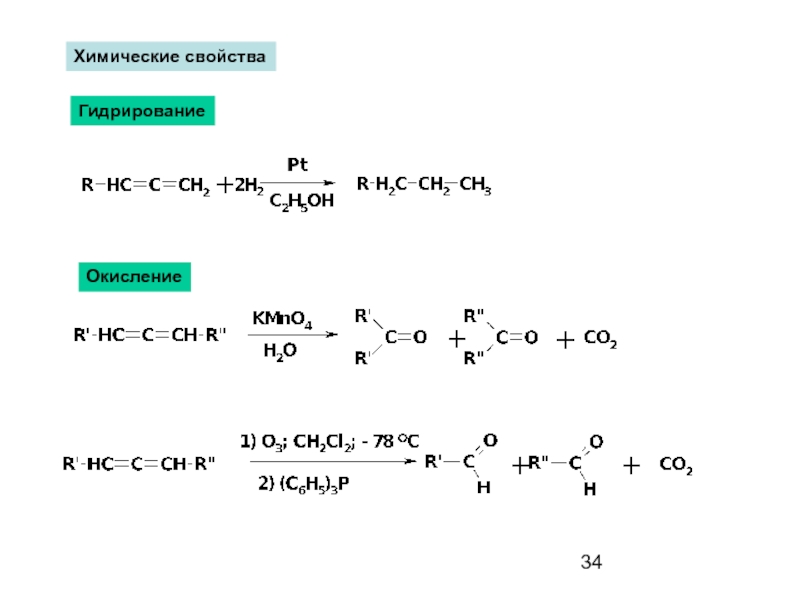
- 34. Химические свойства Гидрирование Окисление
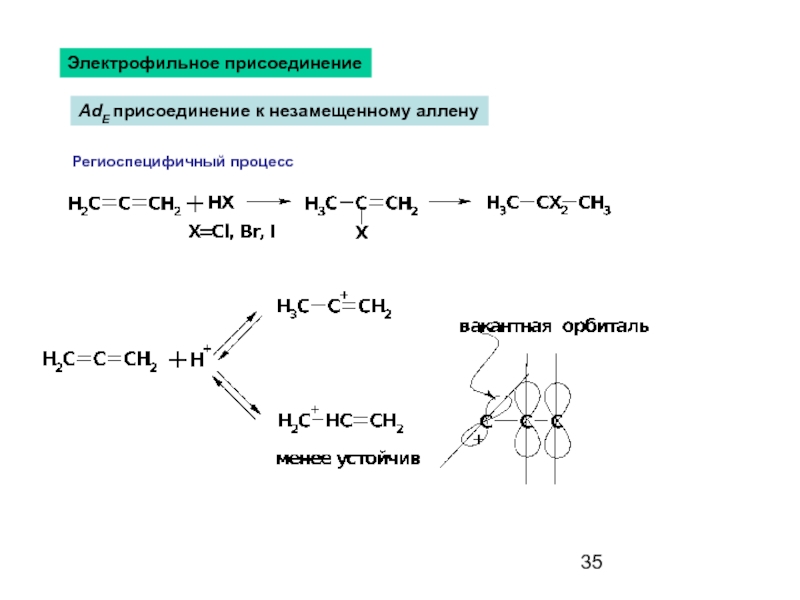
- 35. Электрофильное присоединение AdE присоединение к незамещенному аллену Региоспецифичный процесс
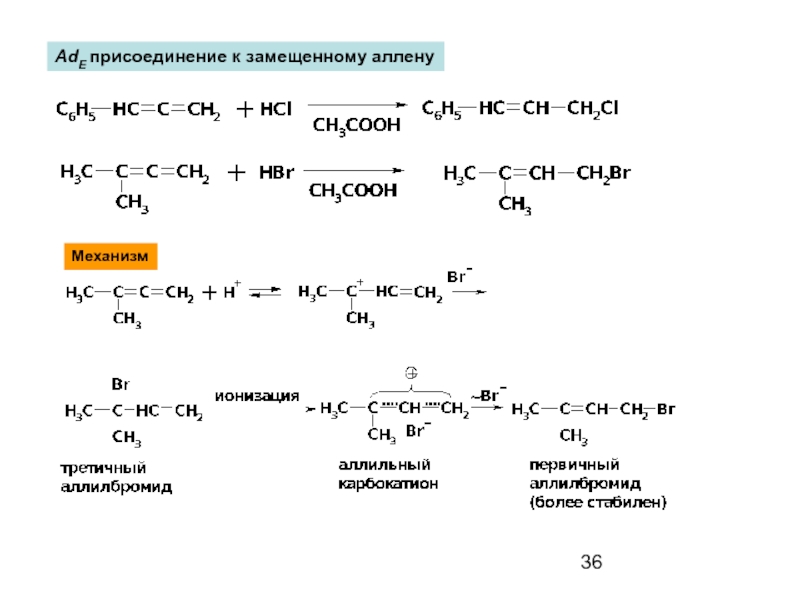
- 36. AdE присоединение к замещенному аллену Механизм
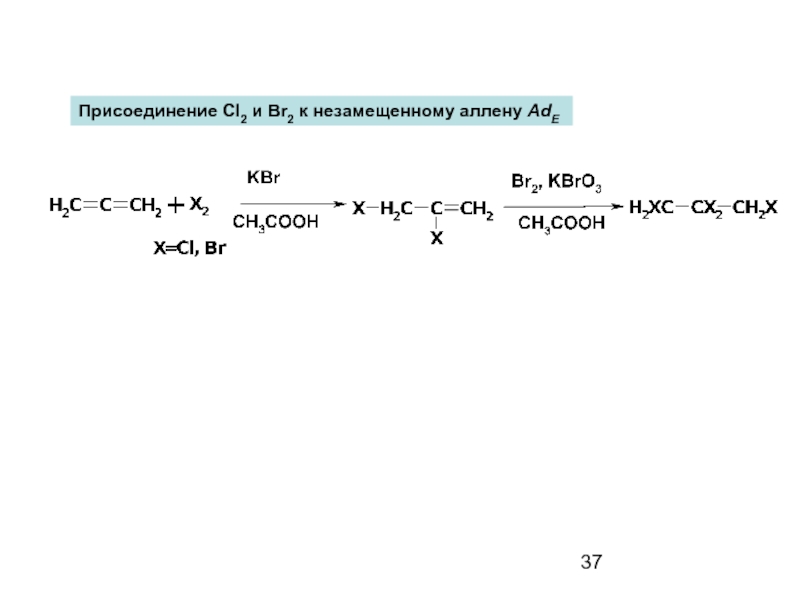
- 37. Присоединение Cl2 и Br2 к незамещенному аллену AdE
Слайд 4Теплоты гидрирования алкенов и диенов
Строение молекулы сопряженных диенов
Рис. Влияние сопряжения
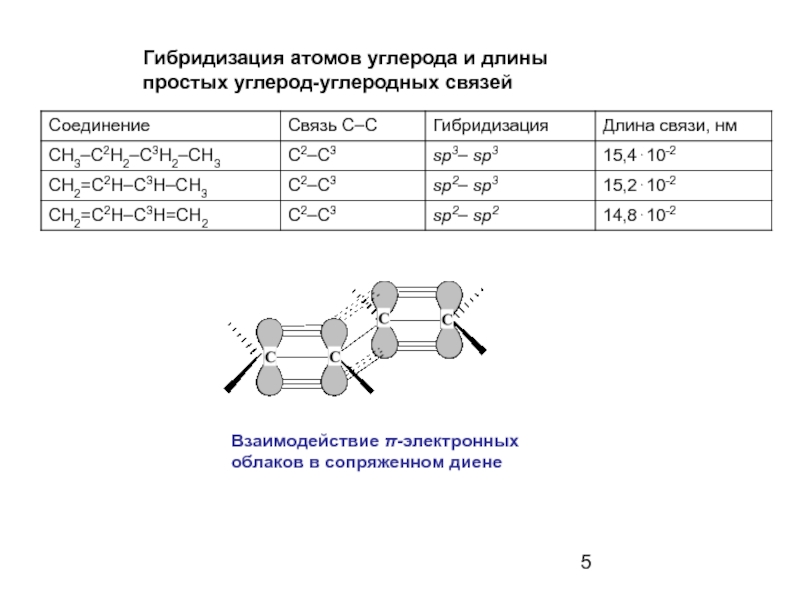
Слайд 5Гибридизация атомов углерода и длины
простых углерод-углеродных связей
Взаимодействие π-электронных
облаков в
Слайд 6
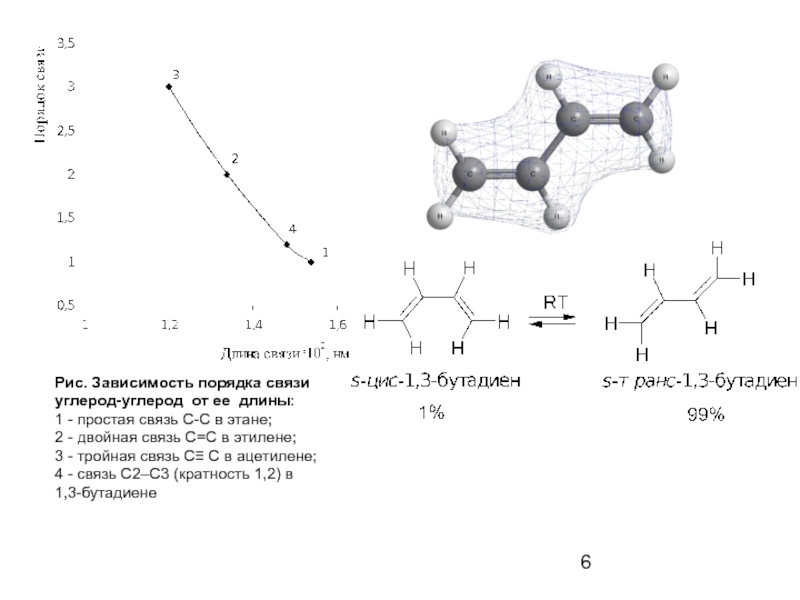
Рис. Зависимость порядка связи
углерод-углерод от ее длины:
1 - простая
2 - двойная связь С=С в этилене;
3 - тройная связь С≡ С в ацетилене;
4 - связь С2–С3 (кратность 1,2) в 1,3-бутадиене
Слайд 10Если молекула может быть представлена двумя или более структурами,
в которых
распределение π-электронов, то реальное распределение π-элекронов
не может быть удовлетворительно представлено ни одной из них.
Реальная молекула представляет собой нечто промежуточное между
ними – резонансный гибрид этих структур.
Такие гипотетические структуры называют граничными (каноническими).
Граничные структуры соединяют знаком ↔.
Основное положение теории резонанса
Граничные структуры должны иметь одинаковое число неспаренных
электронов. Структура (I) не может быть граничной структурой для
аллильного катиона.
Слайд 11Энергия реальной молекулы (резонансного гибрида) меньше, чем
энергия любой из граничных
структур в истинную структуру частицы неодинаков, наиболее
устойчивая структура дает наибольший вклад. Наибольшая
стабилизация достигается в тех случаях, когда структуры, вносящие
вклад в резонансный гибрид, энергетически эквивалентны.
Выигрыш энергии за счет суммирования вкладов всех граничных
структур называют энергией резонанса.
Слайд 12Правила построения граничных структур.
1) Резонансные (граничные или канонические) структуры реально не
2) В граничных структурах можно перемещать только электроны кратных связей (π-электроны) и неподеленные пары электронов (n-электроны).
Порядок связывания атомов должен быть одинаковым во всех граничных структурах (нельзя писать изомеры). Общее число электронов и суммарный заряд в каждой резонансной структуре должны быть одинаковыми.
Все атомы, участвующие в резонансе, лежат в одной плоскости.
Например, структура 3 не может быть граничной структурой для аллильного катиона, потому что при ее написании мы переместили атом водорода.
Слайд 13При перемещении электронов помещайте отрицательный заряд на более электроотрицательный атом.
Структуры с
(дают меньший вклад), чем структура с полными октетами электронов
на каждом атоме.
3) Всем граничным структурам должны соответствовать формулы Льюиса.
Нельзя писать структуры, в которых атомы углерода имеют пять связей. Элементы второго периода периодической системы подчиняются правилу октета. Например, у кислорода восемь электронов, но у углерода десять электронов (пять валентностей), т.е. такую структуру писать нельзя.
Слайд 144) Энергия реальной молекулы ниже, чем энергия любой граничной структуры. Аллильный
Это называется резонансная стабилизация
Слайд 17при -80 °С образуется кинетически контролируемый продукт реакции
Рис. Кинетический и термодинамический
в реакции присоединения НВr к 1,3-бутадиену
Е,
кДж/моль
Слайд 18при 40 °С образуется термодинамически контролируемый
продукт реакции
Термодинамически контролируемый продукт –
Перициклические реакции.
Электроциклические реакции
Реакции циклоприсоединения
Особенности перициклических реакций:
инициируются нагреванием или излучением (мало чувствительны
к катализаторам, типу растворителя);
протекают без образования ионов и радикалов;
стереоспецифические процессы.
Перициклические реакции – это реакции ненасыщенных
молекул, протекающие через циклическое переходное
состояние
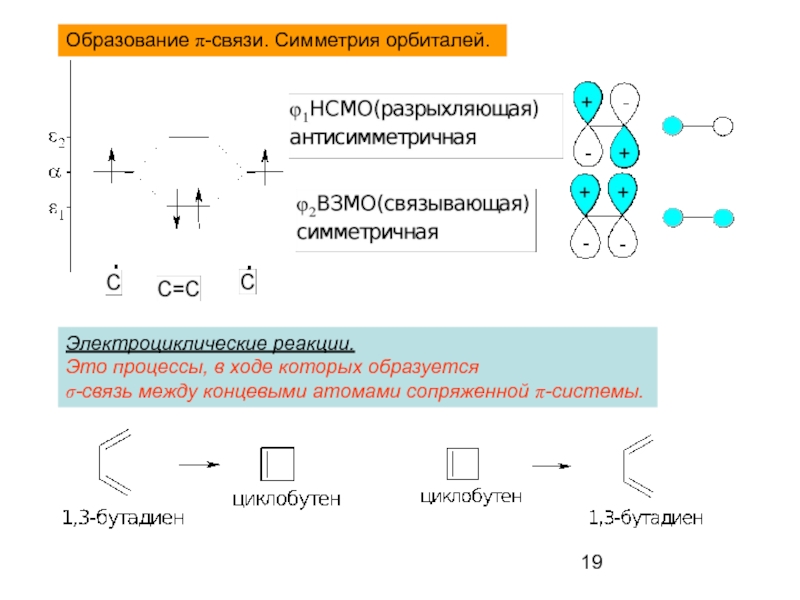
Слайд 19Образование π-связи. Симметрия орбиталей.
Электроциклические реакции.
Это процессы, в ходе которых образуется
σ-связь между концевыми атомами сопряженной π-системы.
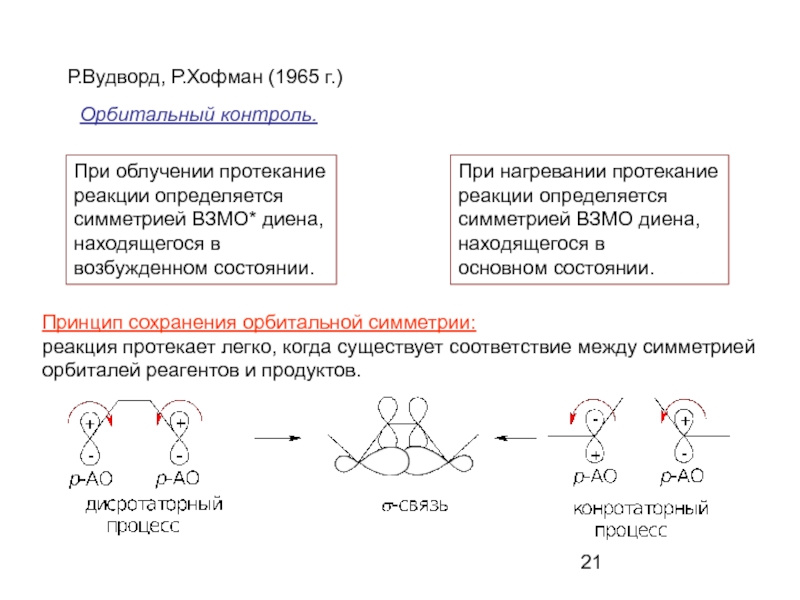
Слайд 21Р.Вудворд, Р.Хофман (1965 г.)
Принцип сохранения орбитальной симметрии:
реакция протекает легко, когда существует
орбиталей реагентов и продуктов.
Орбитальный контроль.
При облучении протекание
реакции определяется
симметрией ВЗМО* диена,
находящегося в
возбужденном состоянии.
При нагревании протекание
реакции определяется
симметрией ВЗМО диена,
находящегося в
основном состоянии.
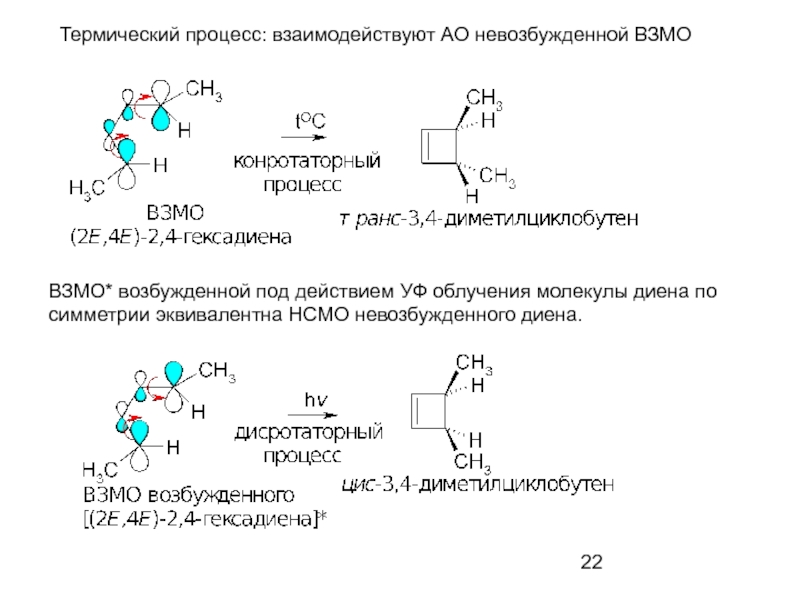
Слайд 22ВЗМО* возбужденной под действием УФ облучения молекулы диена по
симметрии эквивалентна
Термический процесс: взаимодействуют АО невозбужденной ВЗМО
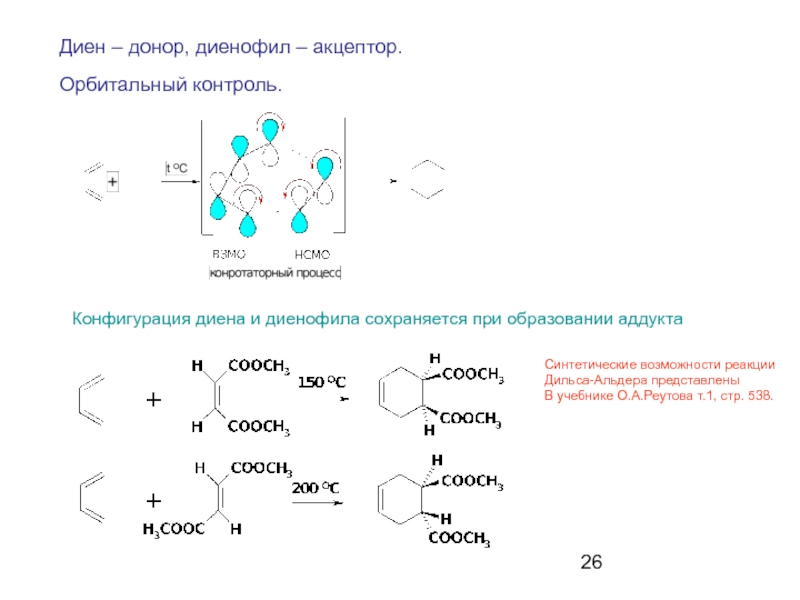
Слайд 26Диен – донор, диенофил – акцептор.
Орбитальный контроль.
Конфигурация диена и диенофила сохраняется
Синтетические возможности реакции
Дильса-Альдера представлены
В учебнике О.А.Реутова т.1, стр. 538.
Слайд 32Куммулированные диены (Аллены).
Замещенные аллены типа XYC=C=CXY не имеют плоскости
симметрии и
хирального центра