- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Патофизиология апоптоза презентация
Содержание
- 1. Патофизиология апоптоза
- 2. Содержание Введение Понятие апоптоза Примеры апоптоза Механизм
- 3. Введение Исследования феномена программируемой клеточной смерти начались
- 4. Понятие апоптоза Апоптоз - форма гибели отдельных
- 6. Примеры апоптоза Запрограммированная гибель клеток —
- 7. Гибель клеток. Клетки, выполнившие свою функцию,
- 8. Дегенерация. При некоторых патологических состояниях наблюдают
- 9. Ликвидации аутоагрессивных Т-клеток: в процессе развития
- 10. Старение Например, путём гормонозависимой инволюции клеток
- 11. Трансфекция. Внедрение в клетку нуклеиновой кислоты вируса
- 12. Повреждение клетки. Воздействие на клетку агентов, повреждающих
- 13. Примеры апоптоза Опухолевый рост (апоптоз выявляется как
- 14. Механизм апоптоза При реализации апоптоза условно можно
- 15. Стадия инициации На этой стадии
- 16. Инициирующие апоптоз стимулы трансмембранные внутриклеточные отрицательные смешанные положительные
- 17. Положительные сигналы генерируют запуск программы апоптоза.
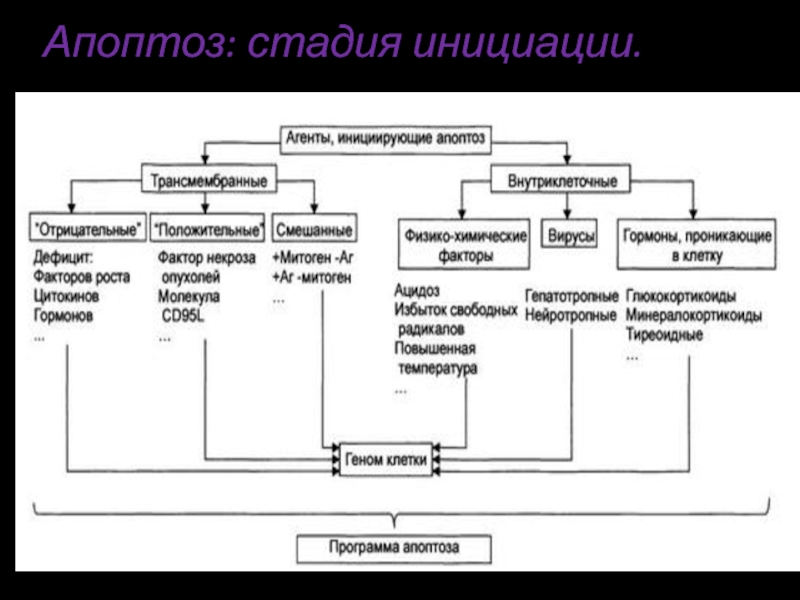
- 18. Апоптоз: стадия инициации.
- 19. Стадия программирования На этой стадии специализированные
- 21. Стадия программирования Выделяют два (не исключающих друг
- 22. Прямая передача сигнала осуществляется через:
- 23. Адапторные белки. В качестве адапторного белка выступает,
- 24. Цитохром С. Выделяясь из митохондрий, цитохром С
- 25. Гранзимы. Эти протеазы выделяют цитотоксические Т-лимфоциты,
- 26. Апоптоз: стадия программирования.
- 27. Опосредованная передача сигнала подразумевает репрессию генов, кодирующих
- 28. Стадия реализации программы Стадия реализации программы
- 29. Стадия реализации программы В результате разрушения белков
- 30. Апоптоз: стадия реализации программы.
- 31. Стадия удаления фрагментов погибших клеток На
- 34. Заключение Апоптоз является генетически запрограммированным защитным механизмом,
- 35. Список использованной литературы Gaspar Banfalvi. Apoptotic chromatin
Слайд 2Содержание
Введение
Понятие апоптоза
Примеры апоптоза
Механизм апоптоза
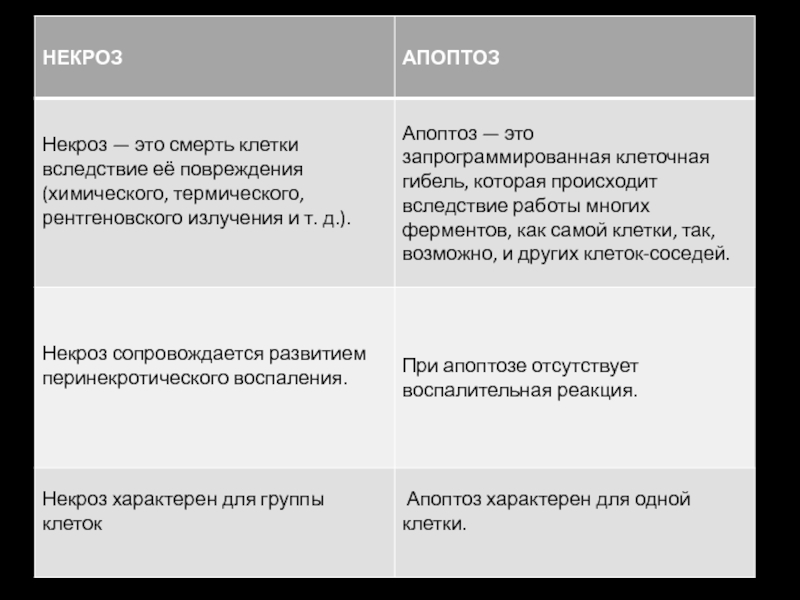
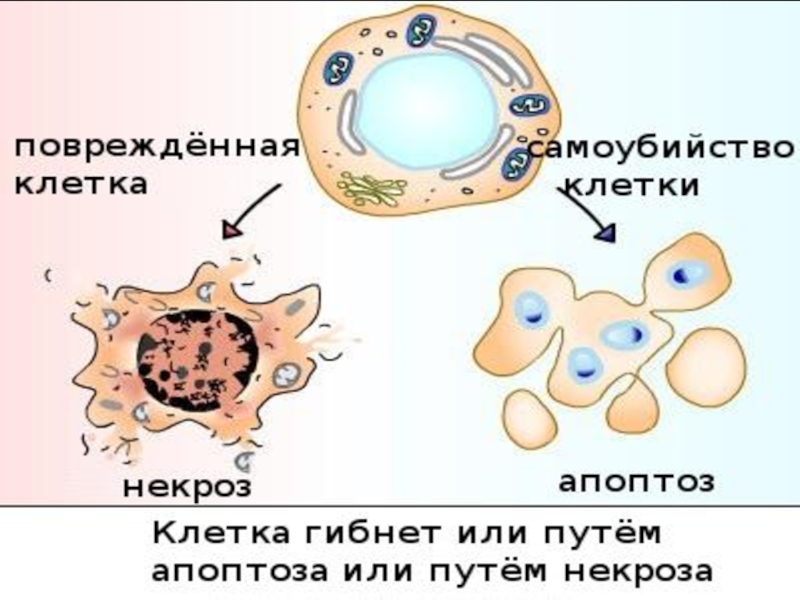
Различия апоптоза и некроза
Заключение
Список использованной литературы
Слайд 3Введение
Исследования феномена программируемой клеточной смерти начались с конца 1960-х годов. Одним
В 1972 году коллектив британских учёных во главе с Дж. Керром впервые предложили использовать термин «апоптоз» для обозначения программируемой клеточной смерти.
14 марта 2000 года Джон Керр был удостоен престижной премии Пауля Эрлиха и Людвига Дармштедтера за свой вклад в исследования апоптоза.
Слайд 4Понятие апоптоза
Апоптоз - форма гибели отдельных клеток, возникающая под действием вне-
Апоптоз — запрограммированная гибель клетки.
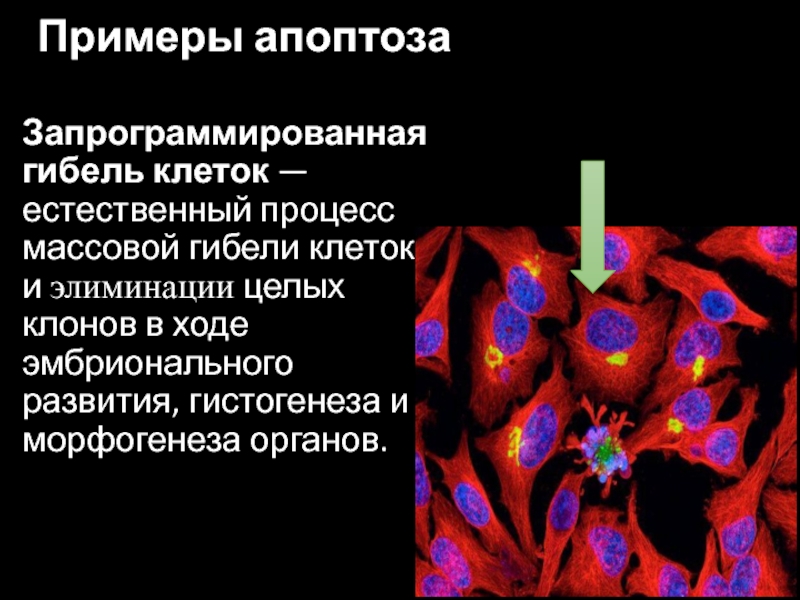
Слайд 6Примеры апоптоза
Запрограммированная гибель клеток — естественный процесс массовой гибели клеток и
Слайд 7Гибель клеток.
Клетки, выполнившие свою функцию, гибнут путём апоптоза. Механизм гибели
Слайд 8Дегенерация.
При некоторых патологических состояниях наблюдают относительно избирательную гибель клеток, например,
Слайд 9Ликвидации аутоагрессивных Т-клеток:
в процессе развития тимуса или удаления лимфоцитов после
устранение клеток тканей, подвергшихся воздействию цитотоксических Т-лимфоцитов или естественных киллеров.
Слайд 10Старение
Например, путём гормонозависимой инволюции клеток эндометрия и атрезии фолликулов яичников
Слайд 11Трансфекция. Внедрение в клетку нуклеиновой кислоты вируса (например, при вирусном гепатите,
Слайд 12Повреждение клетки. Воздействие на клетку агентов, повреждающих её, но не приводящих
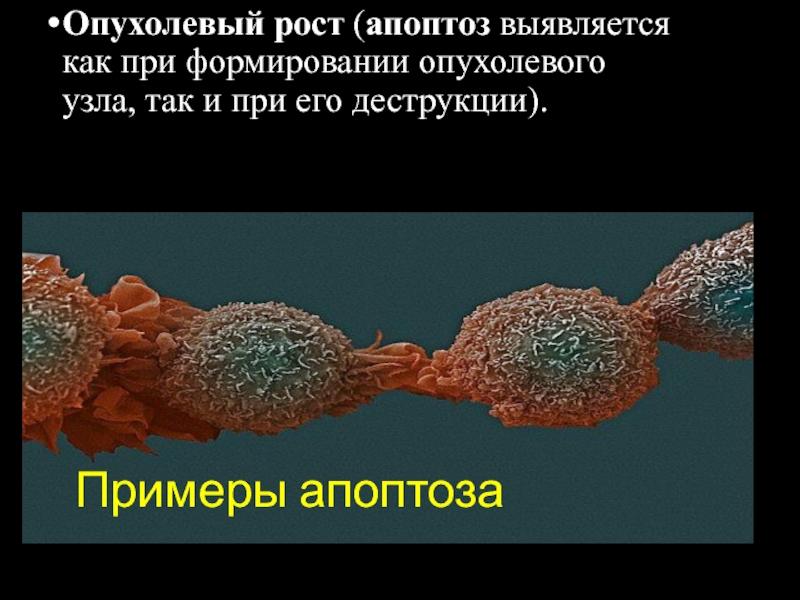
Слайд 13Примеры апоптоза
Опухолевый рост (апоптоз выявляется как при формировании опухолевого узла, так
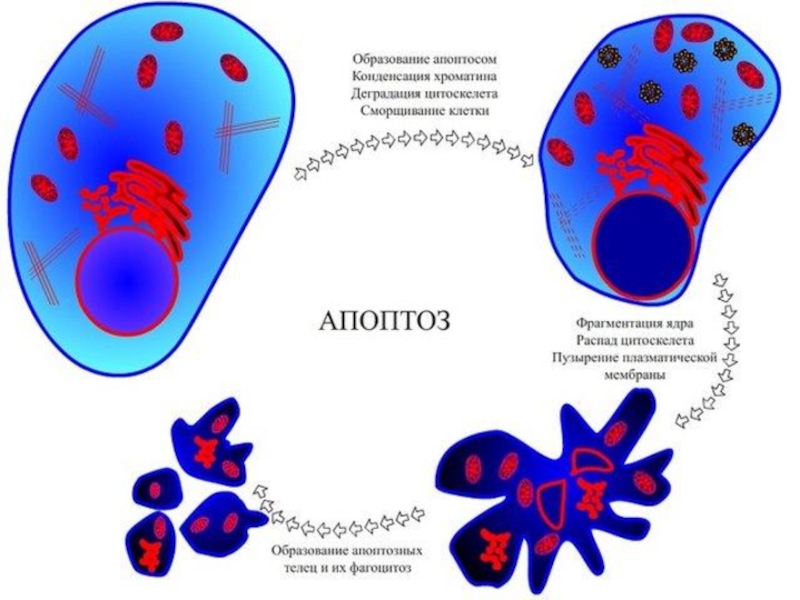
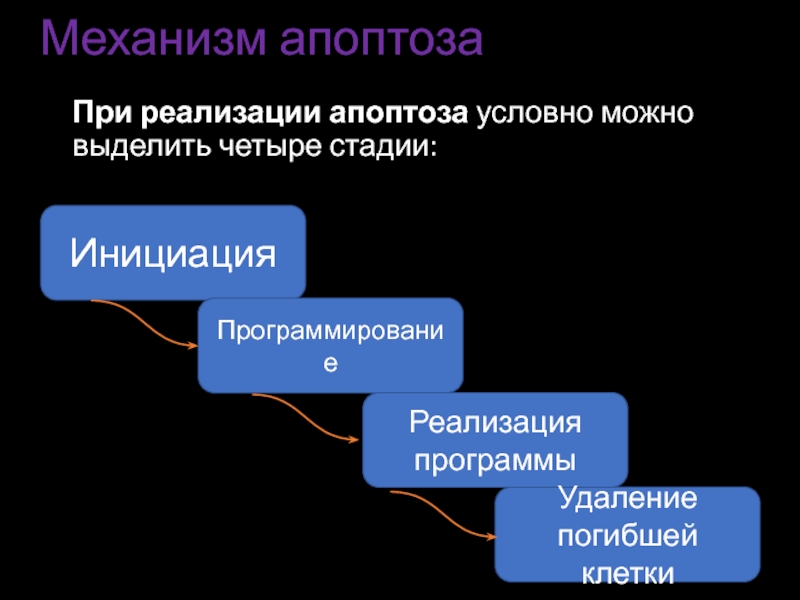
Слайд 14Механизм апоптоза
При реализации апоптоза условно можно выделить четыре стадии:
Инициация
Программирование
Реализация
Удаление погибшей клетки
Слайд 15Стадия инициации
На этой стадии информационные сигналы рецептируются клеткой. Патогенный агент либо
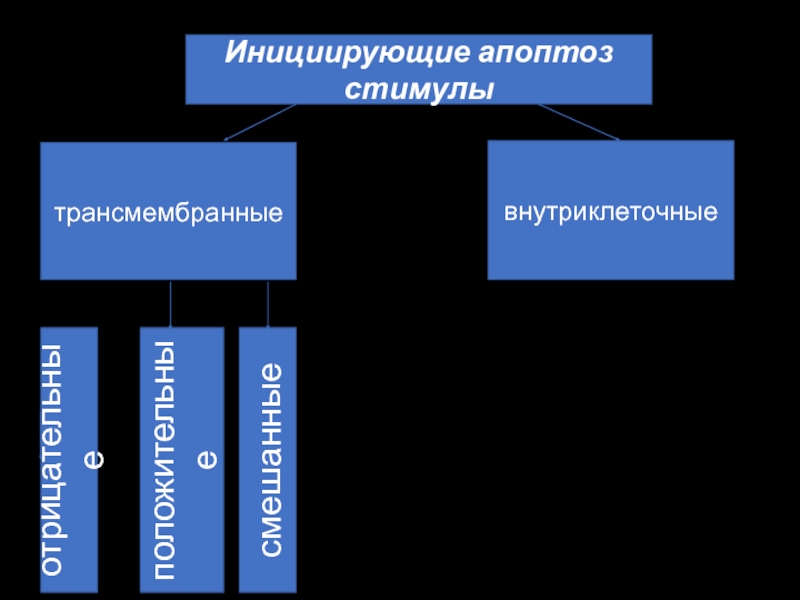
Слайд 16Инициирующие апоптоз стимулы
трансмембранные
внутриклеточные
отрицательные
смешанные
положительные
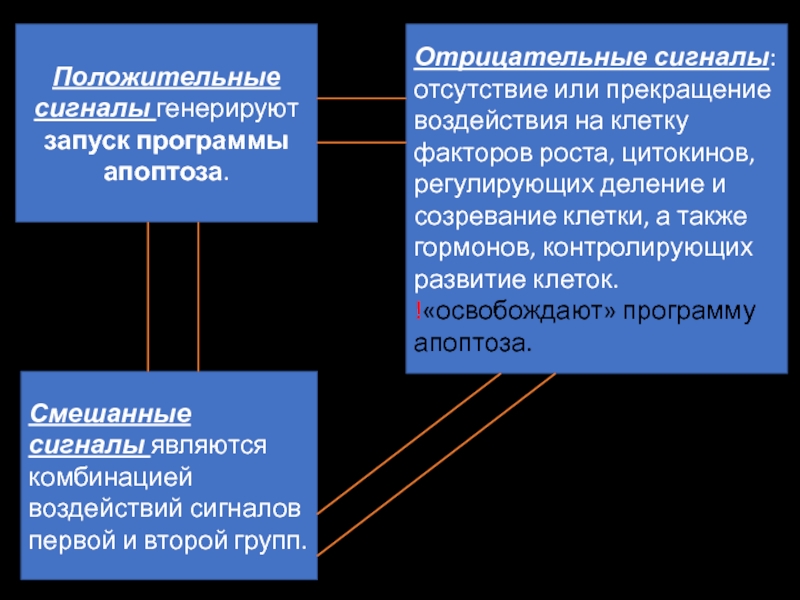
Слайд 17Положительные сигналы генерируют запуск программы апоптоза.
Смешанные сигналы являются комбинацией воздействий
Отрицательные сигналы: отсутствие или прекращение воздействия на клетку факторов роста, цитокинов, регулирующих деление и созревание клетки, а также гормонов, контролирующих развитие клеток.
!«освобождают» программу апоптоза.
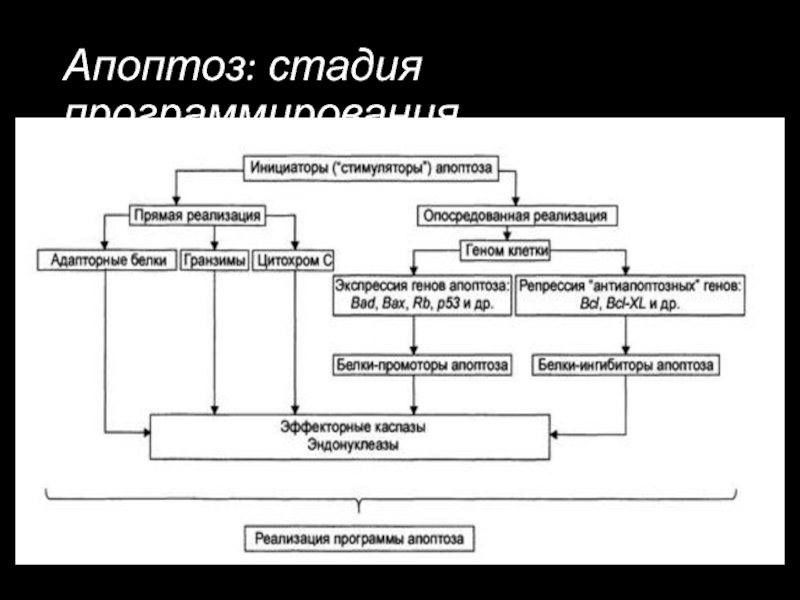
Слайд 19Стадия программирования
На этой стадии специализированные белки либо реализуют сигнал к апоптозу
Слайд 21Стадия программирования
Выделяют два (не исключающих друг друга) варианта реализации стадий программирования:
путём прямой активации эффекторных каспаз и эндонуклеаз (минуя геном клетки);
2) опосредованной через геном передачи сигнала на эффекторные каспазы и эндонуклеазы.
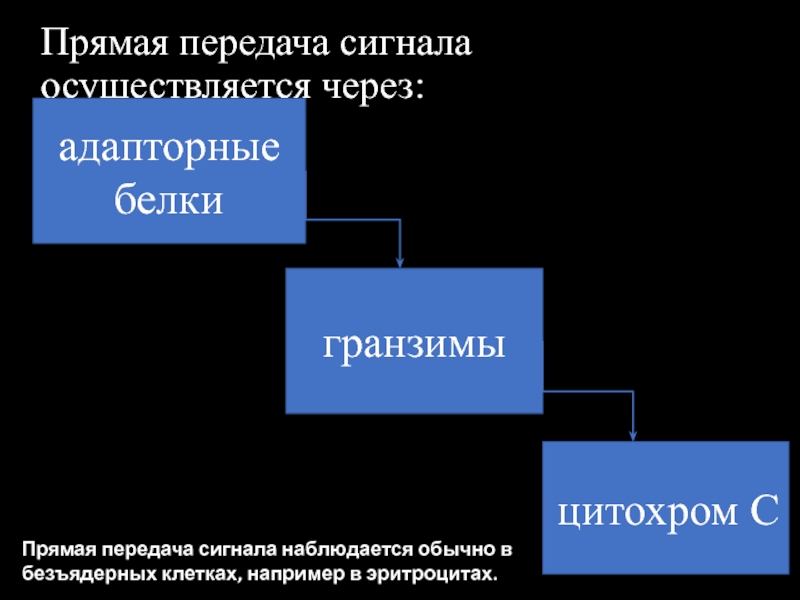
Слайд 22Прямая передача сигнала осуществляется через:
адапторные белки
цитохром С
гранзимы
Прямая передача
Слайд 23Адапторные белки. В качестве адапторного белка выступает, например, каспаза-8. Так реализуют
Слайд 24Цитохром С. Выделяясь из митохондрий, цитохром С вместе с белком Apaf-1
Слайд 25 Гранзимы. Эти протеазы выделяют цитотоксические Т-лимфоциты, протеазы проникают в клетки-мишени
Слайд 27Опосредованная передача сигнала подразумевает репрессию генов, кодирующих ингибиторы апоптоза, и активацию
Белки-ингибиторы апоптоза блокируют апоптоз (например, путём уменьшения проницаемости мембран митохондрий, тем самым уменьшая вероятность выхода в цитозоль одного из пусковых факторов апоптоза — цитохрома С).
Белки-промоторы апоптоза активируют эффекторные каспазы и эндонуклеазы.
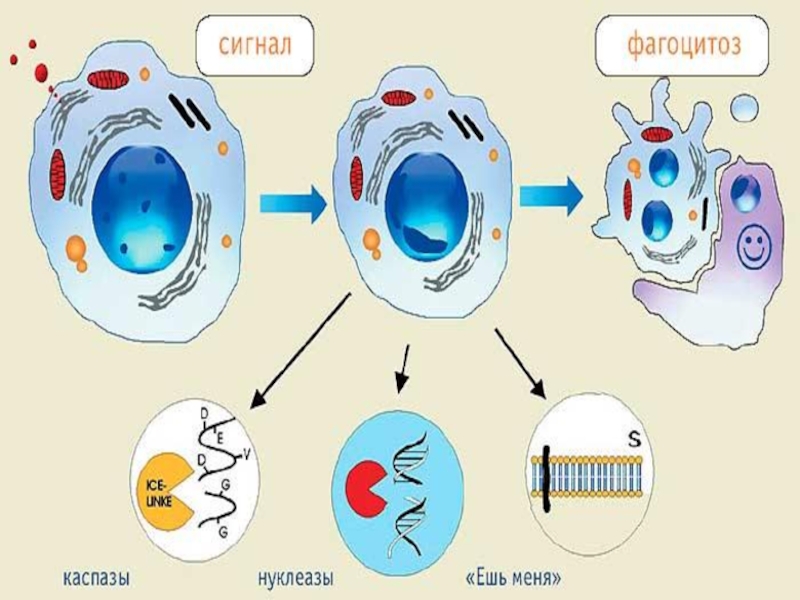
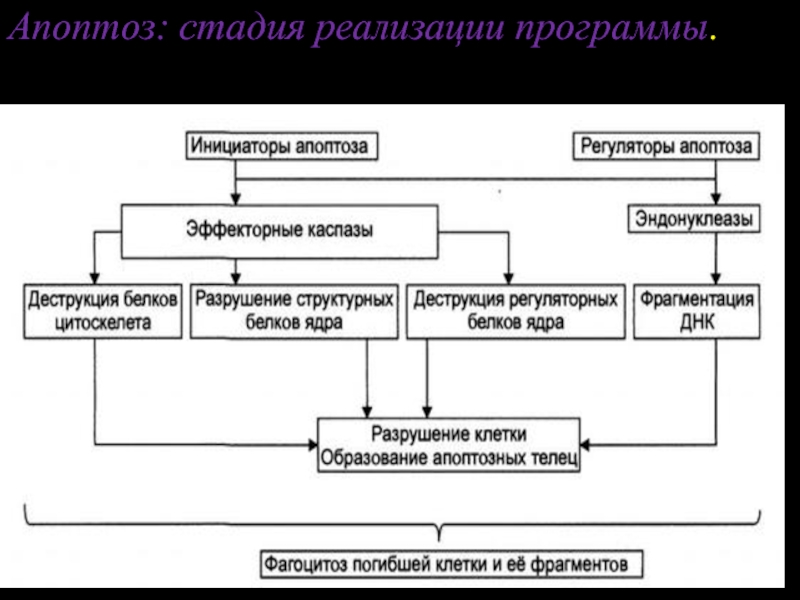
Слайд 28Стадия реализации программы
Стадия реализации программы апоптоза (исполнительная, эффекторная) состоит в собственно
Слайд 29Стадия реализации программы
В результате разрушения белков и хроматина в процессе апоптоза
Непосредственными исполнителями процесса «умертвления» клетки являются Ca2+,Mg2+ -зависимые эндонуклеазы (катализируют распад нуклеиновых кислот) и эффекторные каспазы (подвергают протеолитическому расщеплению различные белки, в том числе белки цитоскелета, ядра, регуляторные белки и ферменты).
Слайд 31Стадия удаления фрагментов погибших клеток
На поверхности апоптозных телец экспрессируются лиганды, с
Слайд 34Заключение
Апоптоз является генетически запрограммированным защитным механизмом, который направлен на запуск самоуничтожения
Как правило, борьба с дефектными клетками не ограничивается только запуском апоптоза, и протекает при активации реакций клеточного и гуморального иммунитета.
Проявлением недостаточности апоптоза служит неконтролируемое деление атипичных клеток, то есть образование и рост опухоли.
В то же время, усиленный апоптоз может приводить к раннему старению, развитию клеточной аплазии и дегенерации.
В настоящее время при разработке современных методов противоопухолевого лечения немало внимания уделяется процессам клеточной регуляции и индукции апоптоза.
Слайд 35Список использованной литературы
Gaspar Banfalvi. Apoptotic chromatin changes. — Springer Science +
Karp G. Cell and Molecular Biology Concepts and Experiments. — 6th edition. — John Wiley & Sons, 2010. — 765 p. — ISBN 978-0-470-48337-4
Анисимов В. Н. Молекулярные и физиологические механизмы старения. — 2-ое, переработанное и дополненное. — СПб.: Наука, 2008. — Т. 1. — 481 с. — ISBN 978-5-02-026356-7