- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Разработка новых лекарственных средств на предприятии ООО Фармтехнология презентация
Содержание
- 1. Разработка новых лекарственных средств на предприятии ООО Фармтехнология
- 2. Предприятие ООО «Фармтехнология» создано в
- 3. Предприятием разработаны и используются технологии производства :
- 4. Участок специализированных пластиковых изделий медицинского назначения,
- 5. Производственная номенклатура составляет более 150 наименований лекарственных
- 6. противомикробные препараты для системного применения
- 7. На предприятии постоянно проводится: повышение уровня
- 8. Основное направление работы – производство качественных генериков
- 9. Обычно генерик допускается в обращение после
- 10. Стратегический приоритет предприятия «Фармтехнология» - обновление и динамичное развитие ассортимента лекарственных средств.
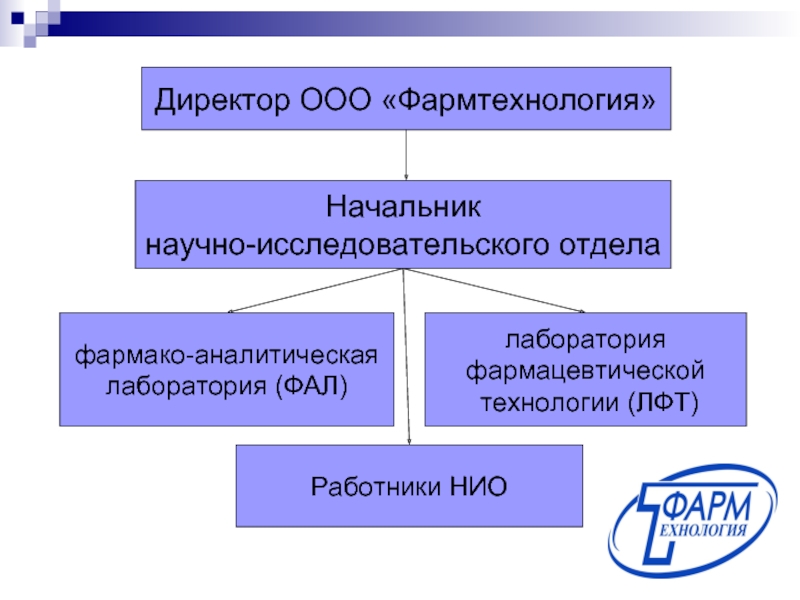
- 11. Директор ООО «Фармтехнология» Начальник научно-исследовательского отдела
- 12. Задачи научно-исследовательского отдела Участие совместно
- 13. Задачи научно-исследовательского отдела Наработка опытных
- 14. Задачи научно-исследовательского отдела Разработка и валидация аналитических
- 15. Задачи научно-исследовательского отдела Закладка на
- 16. Задачи научно-исследовательского отдела Совместно с
- 17. Итоговое регистрационное досье на ЛС рассматривается постоянно
- 18. Задачи научно-исследовательского отдела Техническое обеспечение
- 19. С учетом приведенных положений считаем, что действующая
- 20. «Фармацевтическая промышленность в Беларуси в 2011-2015 годах
- 21. Благодарю за внимание!
Слайд 1ООО "Фармтехнология"
Разработка новых лекарственных средств
на предприятии
ООО «Фармтехнология»
Козлов В.Г.
Слайд 2Предприятие
ООО «Фармтехнология»
создано в 1991 году
Численность сотрудников составляет 375 человек
Контроль
качества - 74 человека
Полный производственный цикл
Производственные площади занимают более 10 тысяч квадратных метров.
Полный производственный цикл
Производственные площади занимают более 10 тысяч квадратных метров.
Слайд 3Предприятием разработаны и используются технологии производства :
твердых лекарственных форм (таблетки, капсулы,
порошки для приготовления растворов и суспензий),
жидких лекарственных форм (назальные капли и спреи, сиропы, суспензии, растворы, эмульсии, настойки, спреи для наружного применения),
мягких лекарственных форм (мази, гели, крема, шампуни и линименты).
жидких лекарственных форм (назальные капли и спреи, сиропы, суспензии, растворы, эмульсии, настойки, спреи для наружного применения),
мягких лекарственных форм (мази, гели, крема, шампуни и линименты).
Слайд 4
Участок специализированных пластиковых изделий медицинского назначения, выпускает более 20 видов различных
медицинских флаконов, бутылок, банок, дозирующих стаканчиков, крышек, пробок, форсунок и других изделий.
Участок по производству очищенной воды, оснащен современным оборудованием в соответствии с международными стандартами.
Участок по производству очищенной воды, оснащен современным оборудованием в соответствии с международными стандартами.
Слайд 5Производственная номенклатура составляет более 150 наименований лекарственных препаратов.
препараты для лечения заболеваний
дыхательных путей,
для профилактики и лечения гриппа и простудных заболеваний,
для лечения заболеваний носа,
дерматологические средства,
для профилактики и лечения гриппа и простудных заболеваний,
для лечения заболеваний носа,
дерматологические средства,
Слайд 6
противомикробные препараты для системного применения в педиатрической практике,
противовоспалительные,
противовирусные,
кардиологические.
Более 40 препаратов входят
в «Перечень основных лекарственных средств»
Слайд 7 На предприятии постоянно проводится:
повышение уровня научного обеспечения производства и разработки
новых лекарственных средств,
переоснащение существующих и создание новых технологических линий, внедрение новых технологий,
повышение уровня знаний работников
переоснащение существующих и создание новых технологических линий, внедрение новых технологий,
повышение уровня знаний работников
Слайд 8Основное направление работы – производство качественных генериков
Это лекарственное средство, обладающее доказанной
терапевтической взаимозаменяемостью с оригинальным препаратом аналогичного состава, выпуск которого осуществляется другим производителем, но не разработчиком лекарства-оригинала
Содержит одно и то же лекарственное вещество в одинаковой дозе и в той же лекарственной форме, что и оригинальное ЛС
Содержит одно и то же лекарственное вещество в одинаковой дозе и в той же лекарственной форме, что и оригинальное ЛС
Слайд 9
Обычно генерик допускается в обращение после истечения срока патента или других
эксклюзивных прав на оригинальный препарат
Обычно регистрация генерика осуществляется на основании регистрационного досье сокращенного объема и данных по биоэквивалентности
Выпуск генерика можно наладить за более короткое время и с наименьшими материальными затратами
Новый генерик позволяет достаточно быстро и сравнительно дешево расширить возможности современного медикаментозного лечения
Обычно регистрация генерика осуществляется на основании регистрационного досье сокращенного объема и данных по биоэквивалентности
Выпуск генерика можно наладить за более короткое время и с наименьшими материальными затратами
Новый генерик позволяет достаточно быстро и сравнительно дешево расширить возможности современного медикаментозного лечения
Слайд 10Стратегический приоритет предприятия «Фармтехнология» - обновление и динамичное развитие ассортимента лекарственных
средств.
Слайд 11Директор ООО «Фармтехнология»
Начальник
научно-исследовательского отдела
фармако-аналитическая
лаборатория (ФАЛ)
лаборатория
фармацевтической
технологии (ЛФТ)
Работники
НИО
Слайд 12Задачи научно-исследовательского отдела
Участие совместно с отделом маркетинга и продаж
предприятия в определении стратегии производства и выпуска новых генерических лекарственных средств (ЛС), согласование ежегодного плана разработки новых препаратов.
Разработка состава и технологии производства новых генерических ЛС, результаты которой отражаются в описании технологического процесса (блок-схема, аппаратурное оформление технологии с пояснительной запиской).
Разработка состава и технологии производства новых генерических ЛС, результаты которой отражаются в описании технологического процесса (блок-схема, аппаратурное оформление технологии с пояснительной запиской).
Слайд 13Задачи научно-исследовательского отдела
Наработка опытных образцов и образцов опытно-промышленных серий
разрабатываемых ЛС.
Проведение исследований по тесту сравнительной кинетики растворения (ТСКР) для опытных образцов (на этапе разработки) и образцов опытно-промышленных серий (на этапе государственной регистрации) новых ЛС, планируемых к производству и выпуску.
Разработка программ (протоколов) исследований по ТСКР, биоэквивалентных испытаний (БЭИ) и (при необходимости) по до – и пострегистрационным клиническим испытаниям (КИ) ЛС.
Проведение исследований по тесту сравнительной кинетики растворения (ТСКР) для опытных образцов (на этапе разработки) и образцов опытно-промышленных серий (на этапе государственной регистрации) новых ЛС, планируемых к производству и выпуску.
Разработка программ (протоколов) исследований по ТСКР, биоэквивалентных испытаний (БЭИ) и (при необходимости) по до – и пострегистрационным клиническим испытаниям (КИ) ЛС.
Слайд 14Задачи научно-исследовательского отдела
Разработка и валидация аналитических методик определения концентрации лекарственных средств
в рамках проведения исследований по ТСКР (модельные среды) и/или их метаболитов в рамках проведения аналитического этапа БЭИ
Слайд 15Задачи научно-исследовательского отдела
Закладка на хранение и изучение стабильности опытных
образцов и образцов опытно-промышленных серий ЛС по физико-химическим показателям с подготовкой итоговых отчетов.
Разработка и валидация методик химического анализа разрабатываемых ЛС с целью подготовки проектов ФСП, пояснительных записок и приложений к ним.
Разработка методик определения сопутствующих примесей готовых лекарственных форм ранее разработанных и поставленных на производство лекарственных средств с целью подготовки их к государственной перерегистации.
Разработка и валидация методик химического анализа разрабатываемых ЛС с целью подготовки проектов ФСП, пояснительных записок и приложений к ним.
Разработка методик определения сопутствующих примесей готовых лекарственных форм ранее разработанных и поставленных на производство лекарственных средств с целью подготовки их к государственной перерегистации.
Слайд 16Задачи научно-исследовательского отдела
Совместно с отделом управления качеством участие в
проведении перспективной валидации технологического процесса производства новых генерических ЛС.
Подготовка проектов инструкций по медицинскому применению и листков-вкладышей на разработанные ЛС, а также литературного обзора об опыте клинического применения препаратов-аналогов, с последующей их передачей вместе с проектами ФСП, пояснительными записками и приложениями к ним, валидационными отчетами, отчетами по стабильности, по ТСКР и БЭИ в ОКК предприятия для проведения работ по формированию итоговых регистрационных досье и их представления на государственную регистрацию.
Подготовка проектов инструкций по медицинскому применению и листков-вкладышей на разработанные ЛС, а также литературного обзора об опыте клинического применения препаратов-аналогов, с последующей их передачей вместе с проектами ФСП, пояснительными записками и приложениями к ним, валидационными отчетами, отчетами по стабильности, по ТСКР и БЭИ в ОКК предприятия для проведения работ по формированию итоговых регистрационных досье и их представления на государственную регистрацию.
Слайд 17Итоговое регистрационное досье на ЛС рассматривается постоянно действующей комиссией по регистрации
лекарственных средств.
В случае положительного решения комиссии, досье передается в
УП «Центр экспертиз и испытаний в здравоохранении».
Слайд 18Задачи научно-исследовательского отдела
Техническое обеспечение и контроль за проведением БЭИ
и КИ ЛС в соответствии с действующими требованиями ТКП 184-2009 (02040) и ГФРБ.
Контроль за проведением исследований в рамках качественной лабораторной практики (GLP) в соответствии с требованиями ТКП 1255-2008 «Надлежащая лабораторная практика».
Контроль за проведением исследований в рамках качественной лабораторной практики (GLP) в соответствии с требованиями ТКП 1255-2008 «Надлежащая лабораторная практика».
Слайд 19С учетом приведенных положений считаем, что действующая на предприятии система разработки
новых лекарственных средств способна обеспечить динамичное развитие производства и решение задач поставленных перед фармацевтической промышленностью Республики Беларусь
Слайд 20«Фармацевтическая промышленность в Беларуси в 2011-2015 годах должна получить приоритетное развитие
и стать одной из стратегических отраслей. За счет качества и эффективности доля отечественных препаратов на внутреннем рынке должна превысить 50% с сегодняшних 25%», заявил Президент Беларуси А.Г.Лукашенко, выступая на четвертом Всебелорусском народном собрании.