- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Lektsia_10_11_Khimia_C_Kh_1 презентация
Содержание
- 1. Lektsia_10_11_Khimia_C_Kh_1
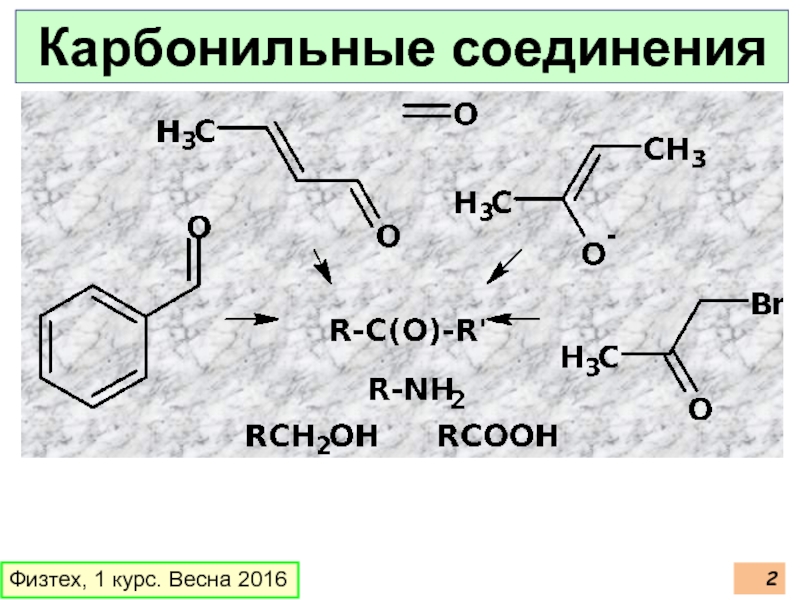
- 2. Физтех, 1 курс. Весна 2016 Карбонильные соединения
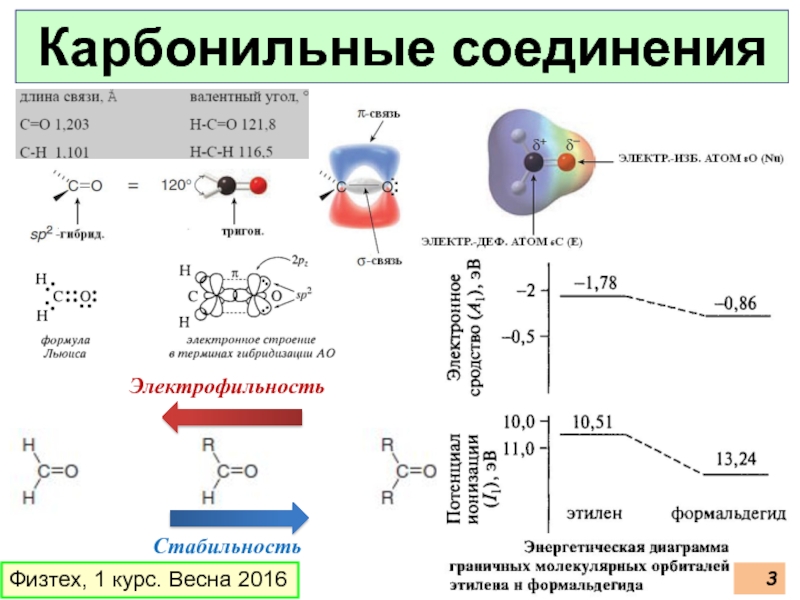
- 3. Электрофильность
- 4. Физтех, 1 курс. Весна 2016 Карбонильные соединения
- 5. Физтех, 1 курс. Весна 2016 Карбонильные соединения
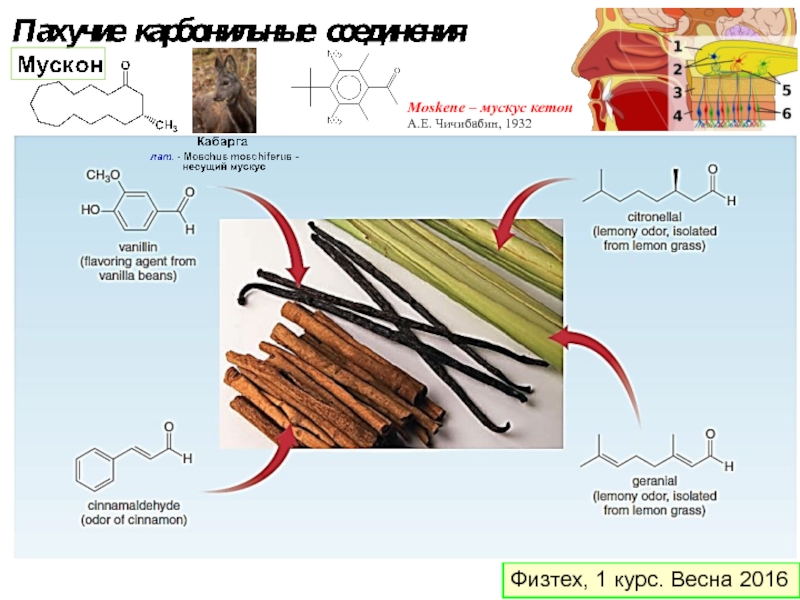
- 6. Физтех, 1 курс. Весна 2016 Moskene – мускус кетон А.Е. Чичибабин, 1932
- 7. Физтех, 1 курс. Весна 2016 Генезис обоняния:
- 8. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 9. Альдегиды – более реакционноспособные соединения чем кетоны
- 10. Физтех, 1 курс. Весна 2016 Карбонильные соединения
- 11. Физтех, 1 курс. Весна 2016 Механизм AdN Bürgi–Dunitz angle Карбонильные соединения
- 12. Физтех, 1 курс. Весна 2016 AdN реакции
- 13. Физтех, 1 курс. Весна 2016 Карбонильные соединения
- 14. Физтех, 1 курс. Весна 2016 Карбонильные соединения
- 15. Физтех, 1 курс. Весна 2016 Карбонильные соединения, ХС 6) Реакция Виттига
- 16. Физтех, 1 курс. Весна 2016 Карбонильные соединения
- 17. Lewis Hastings Sarett
- 18. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 19. Физтех, 1 курс. Весна 2016 Карбонильные соединения ПЛ Реакции гидроборирования, окисления Реакция Кучерова
- 20. Физтех, 1 курс. Весна 2016 Карбонильные соединения
- 21. Физтех, 1 курс. Весна 2016 Карбонильные соединения ,ПЛ Синтез через 1,3-дитиан пиролиз солей карбоновых кислот
- 22. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 23. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 24. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 25. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 26. Физтех, 1 курс. Весна 2016 Карбонильные соединения, ХС или НNO3 Окисление кетонов
- 27. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 28. Физтех, 1 курс. Весна 2016 Функциональные производные
- 29. Физтех, 1 курс. Весна 2016 Карбонильные соединения
- 30. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 31. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 33. Физтех, 1 курс. Весна 2016 Карбонильные соединения
- 35. Физтех, 1 курс. Весна 2016 Карбонильные соединения, ХС Рацемизация. Дейтерообмен
- 36. Физтех, 1 курс. Весна 2016 Карбонильные соединения, ХС Галогенирование карбонильных соединений
- 37. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 38. Физтех, 1 курс. Весна 2016 Карбонильные соединения, ХС Механизм, катализ АКК основанием
- 39. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 40. Физтех, 1 курс. Весна 2016 Карбонильные соединения,
- 41. Физтех, 1 курс. Весна 2016 Карбонильные соединения Направленные конденсации
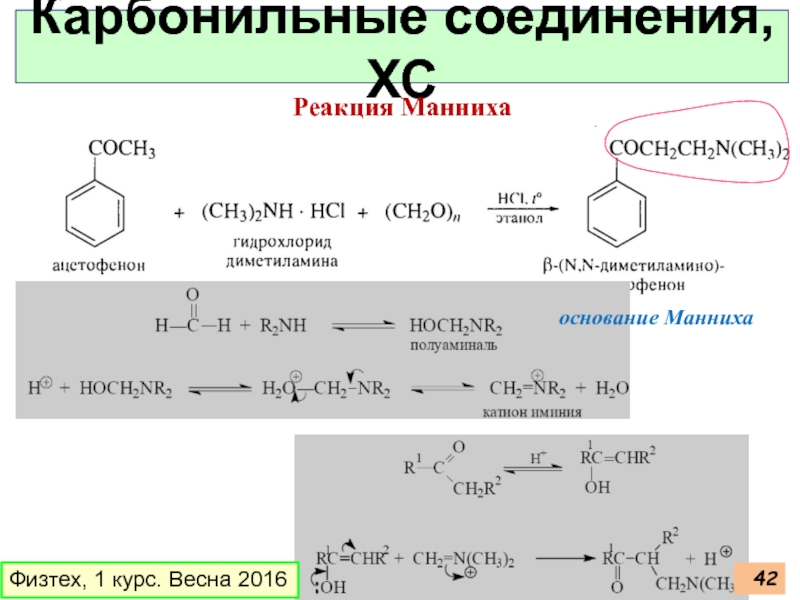
- 42. Физтех, 1 курс. Весна 2016 Карбонильные соединения, ХС Реакция Манниха основание Манниха
- 43. Физтех, 1 курс. Весна 2016 Карбонильные соединения, ХС Реакция Кневенагеля Реакция Перкина Бензоиновая конденсация
- 44. Физтех, 1 курс. Весна 2016 Функциональные производные
- 45. Физтех, 1 курс. Весна 2016 Нн Карбонильные соединения, ПЛ Строение α,β-непредельных альдегидов и кетонов
- 46. Физтех, 1 курс. Весна 2016 Нн Карбонильные
- 47. Физтех, 1 курс. Весна 2016 Нн Карбонильные
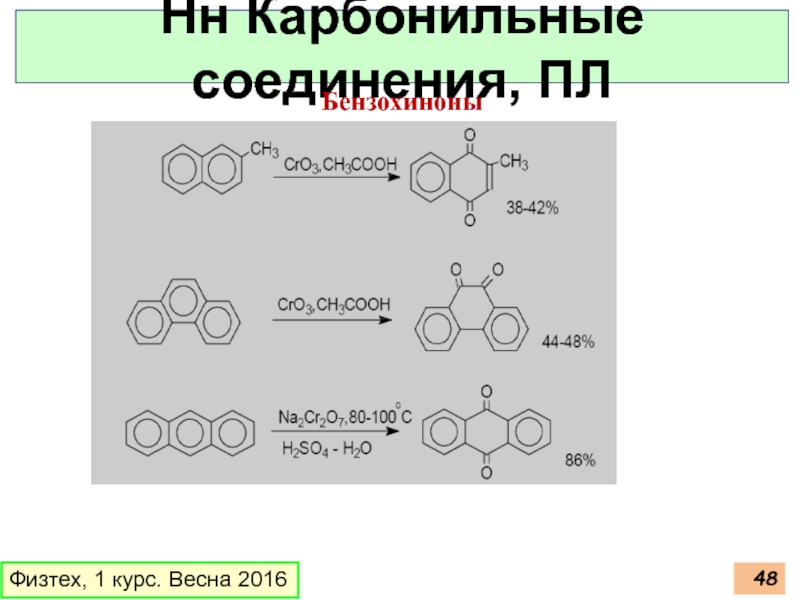
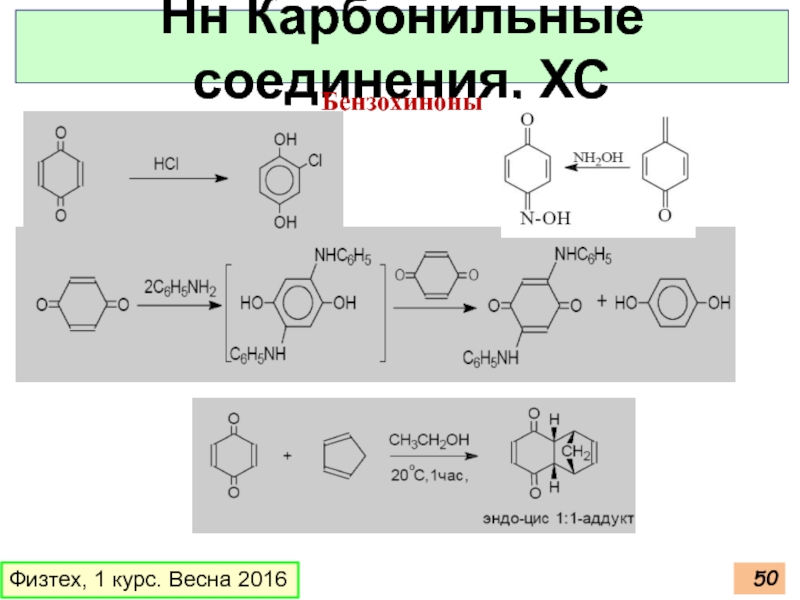
- 48. Физтех, 1 курс. Весна 2016 Нн Карбонильные соединения, ПЛ Бензохиноны
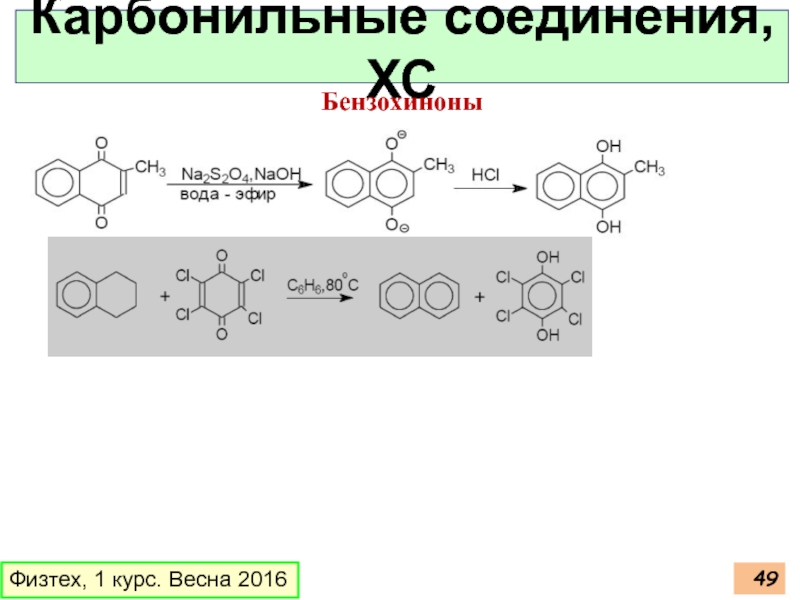
- 49. Физтех, 1 курс. Весна 2016 Карбонильные соединения, ХС Бензохиноны
- 50. Физтех, 1 курс. Весна 2016 Нн Карбонильные соединения, ХС Бензохиноны
- 51. Физтех, 1 курс. Весна 2016 Нн Карбонильные соединения, ХС
- 52. Физтех, 1 курс. Весна 2016 Нн Карбонильные
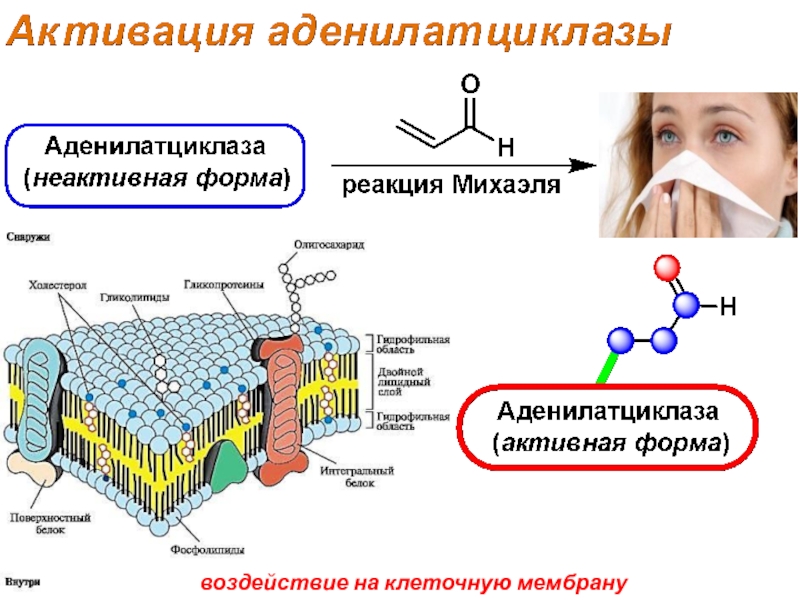
- 55. воздействие на клеточную мембрану
- 57. Нн Карбонильные соединения, ХС Аннелирование по Робинсону
- 58. Физтех, 1 курс. Весна 2016 Нн Карбонильные
- 59. Физтех, 1 курс. Весна 2016 Нн Карбонильные
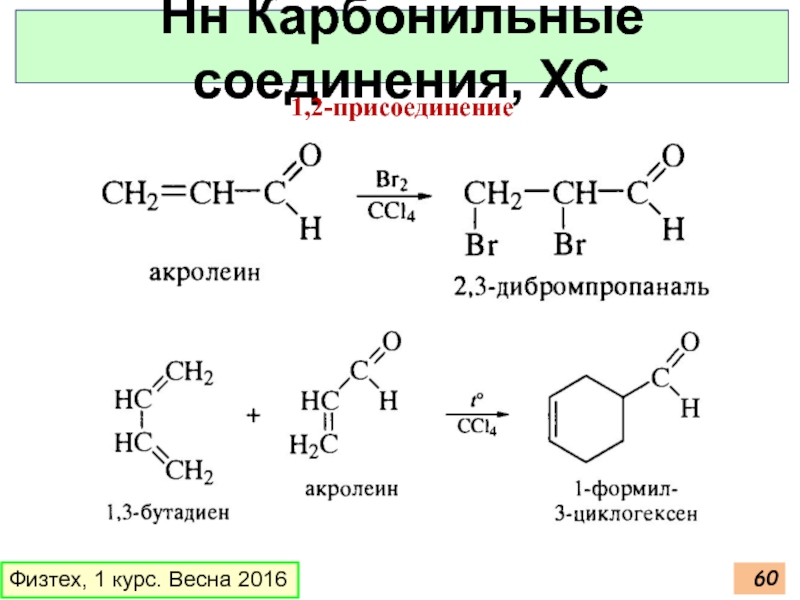
- 60. Физтех, 1 курс. Весна 2016 Нн Карбонильные соединения, ХС 1,2-присоединение
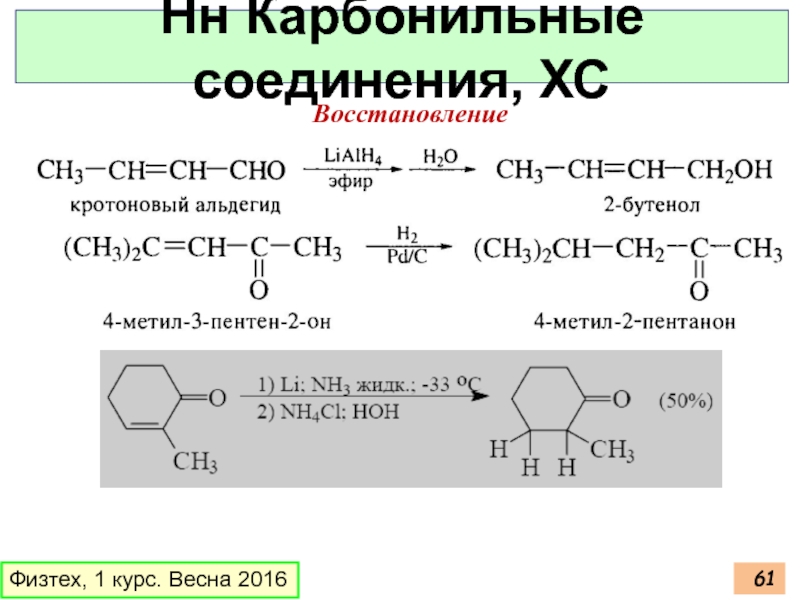
- 61. Физтех, 1 курс. Весна 2016 Нн Карбонильные соединения, ХС Восстановление
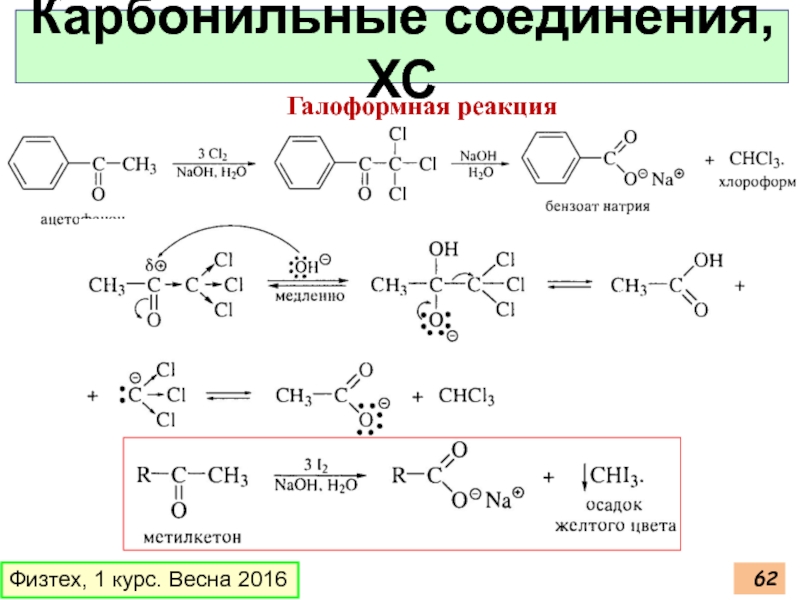
- 62. Физтех, 1 курс. Весна 2016 Карбонильные соединения, ХС Галоформная реакция
- 63. Коротко о главном Кетоны и альдегиды кислородсодержащий
- 64. Основные понятия Для реакции карбонильной группы основной
- 65. Физтех, 1 курс. Весна 2016 Функциональные производные
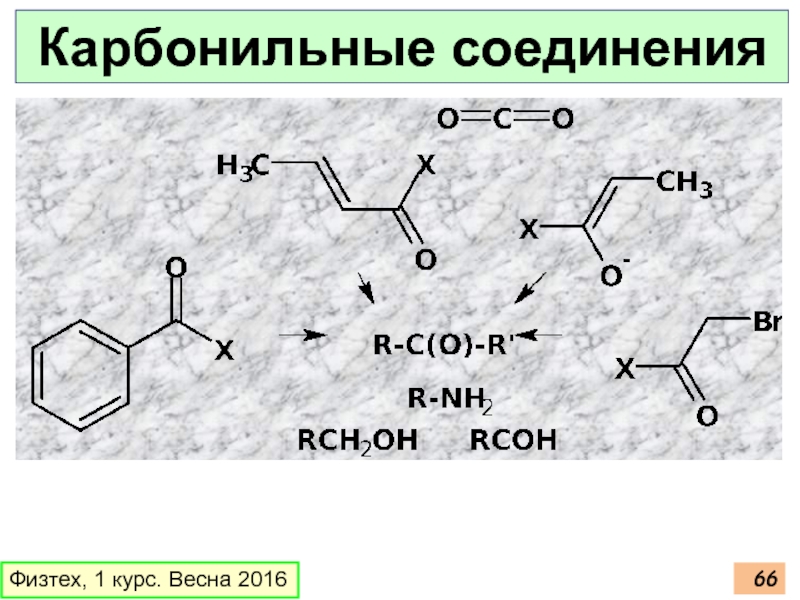
- 66. Физтех, 1 курс. Весна 2016 Карбонильные соединения
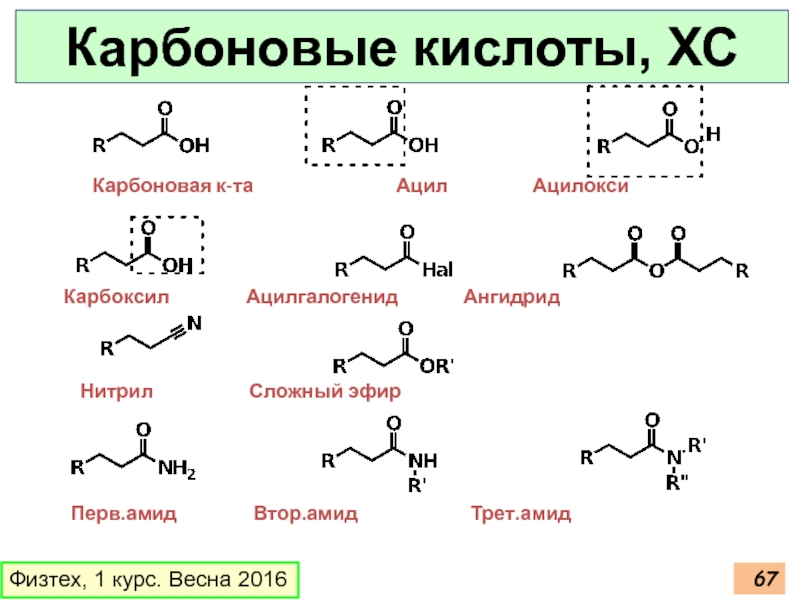
- 67. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
- 68. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
- 69. Электрофильность
- 70. Карбоновые кислоты, ФС Физтех, 1 курс. Весна 2016
- 72. Физтех, 1 курс. Весна 2016 Карбонильные соединения
- 73. Физтех, 1 курс. Весна 2016 Карбонильные соединения
- 74. Карбоновые кислоты, ФС Физтех, 1 курс. Весна
- 75. Карбоновые кислоты, ПЛ Физтех, 1 курс. Весна 2016
- 76. Карбоновые кислоты, ПЛ Физтех, 1 курс. Весна
- 77. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
- 78. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
- 79. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016
- 80. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Восстановление, селективность
- 81. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Восстановление, селективность
- 82. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
- 84. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
- 85. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016
- 86. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Декарбоксилирование радикальное: Бородин - Хунсдиккер
- 87. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Декарбоксилирование радикальное: Кочи (1965)
- 88. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Декарбоксилирование металл-катализируемое
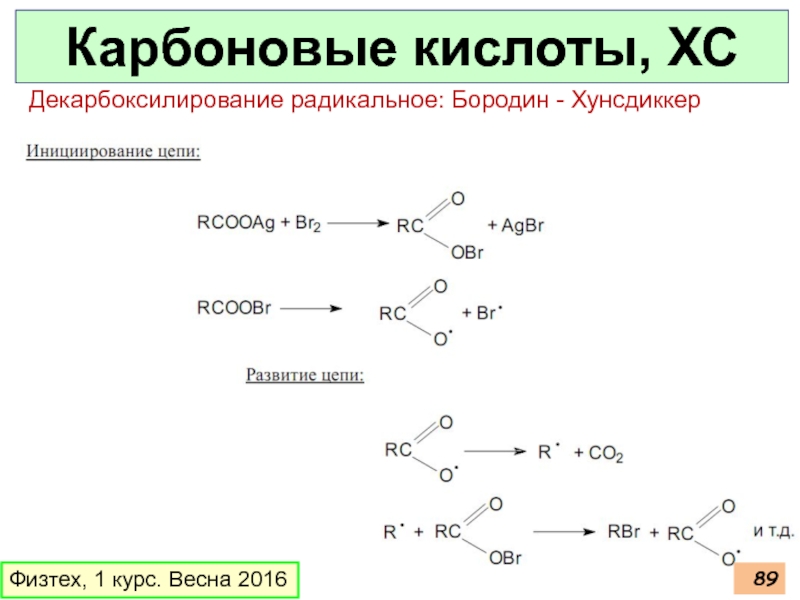
- 89. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Декарбоксилирование радикальное: Бородин - Хунсдиккер
- 90. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
- 91. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
- 92. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Реакция Гелль (1881) -Фольгарда-Зелинского
- 93. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Нуклеофильное замещение – главная реакция
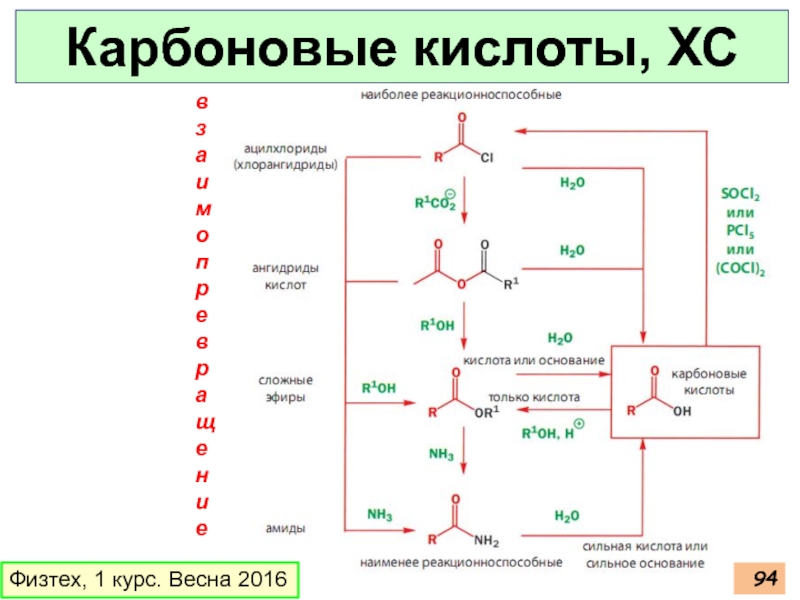
- 94. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 взаимопревращение
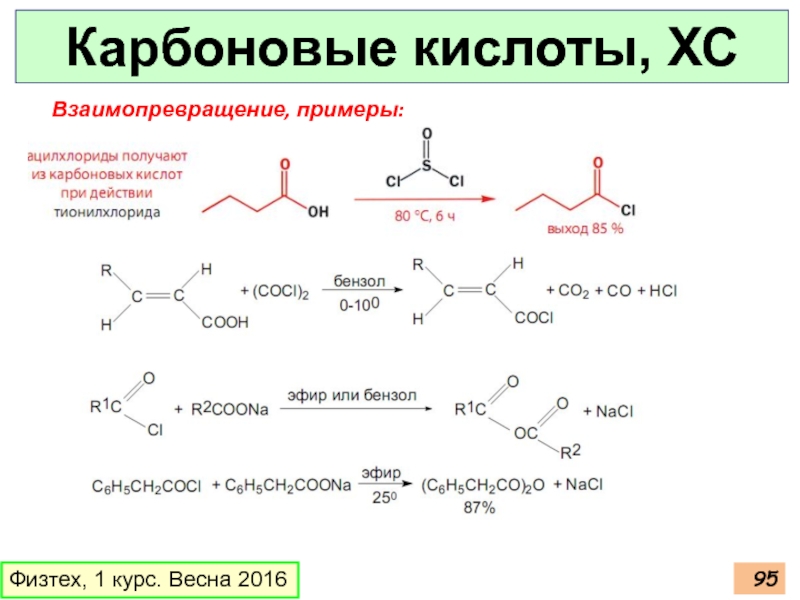
- 95. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Взаимопревращение, примеры:
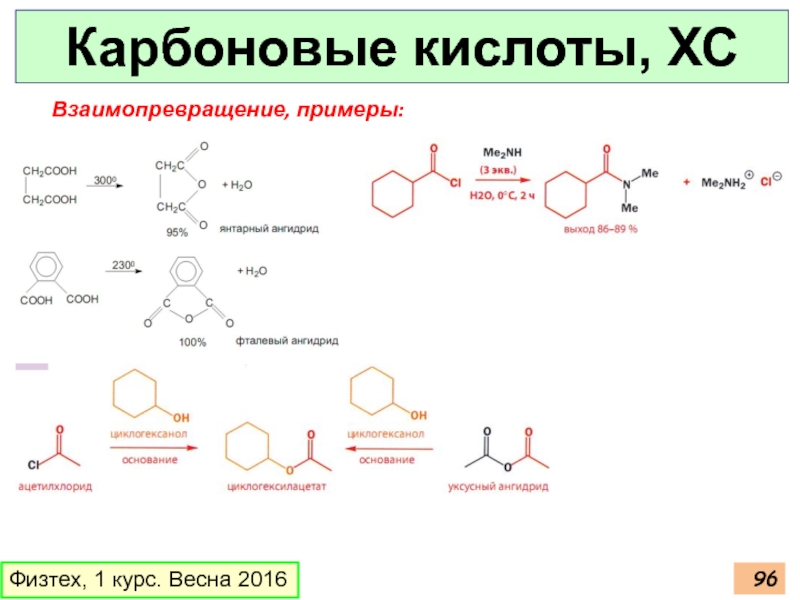
- 96. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Взаимопревращение, примеры:
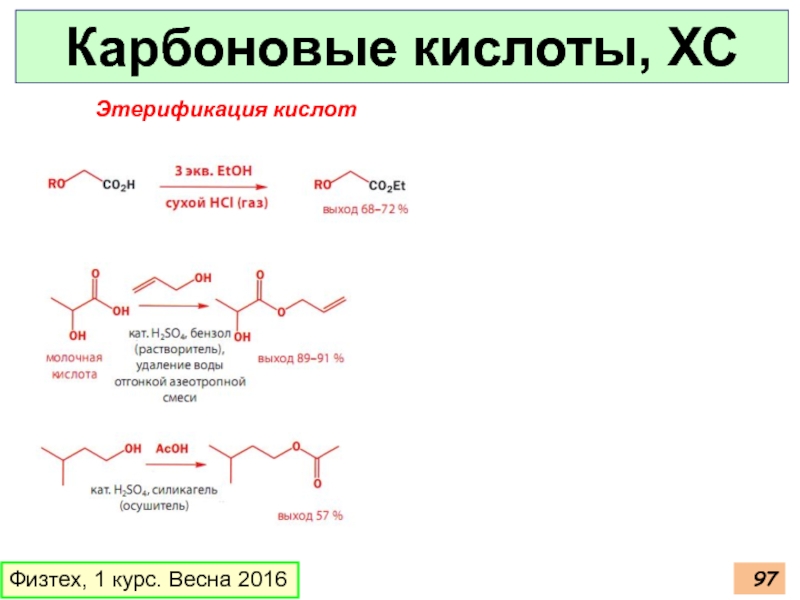
- 97. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Этерификация кислот
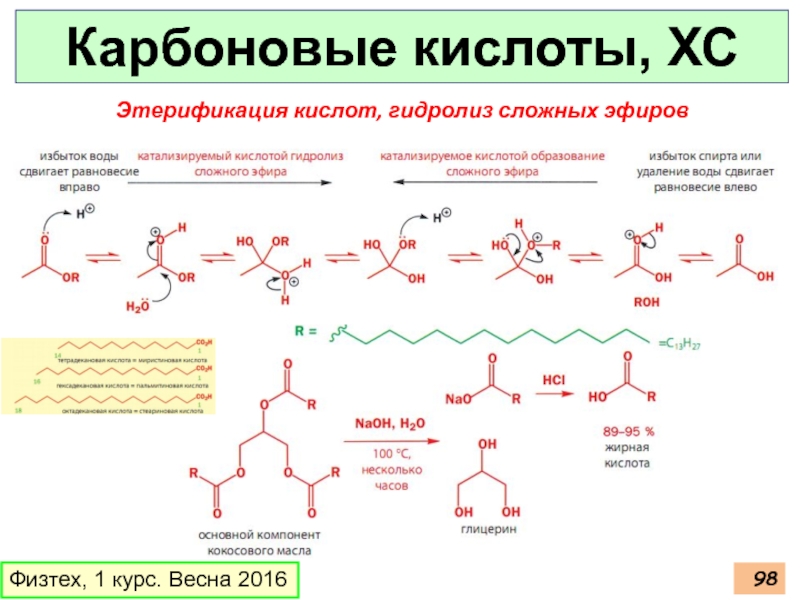
- 98. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Этерификация кислот, гидролиз сложных эфиров
- 99. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
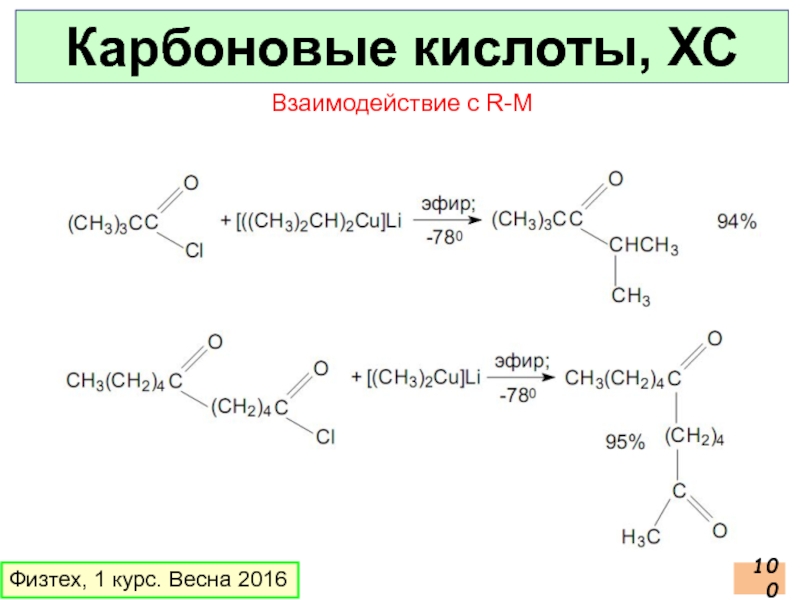
- 100. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Взаимодействие с R-M
- 101. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
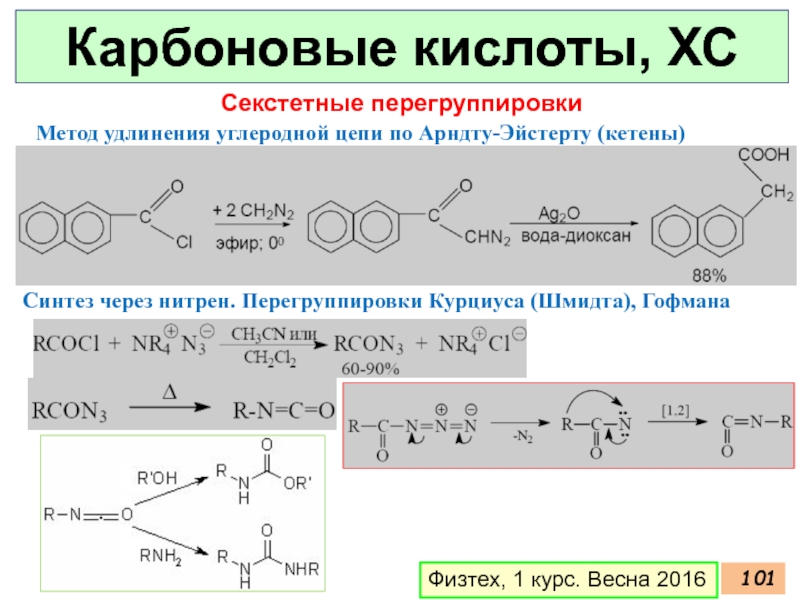
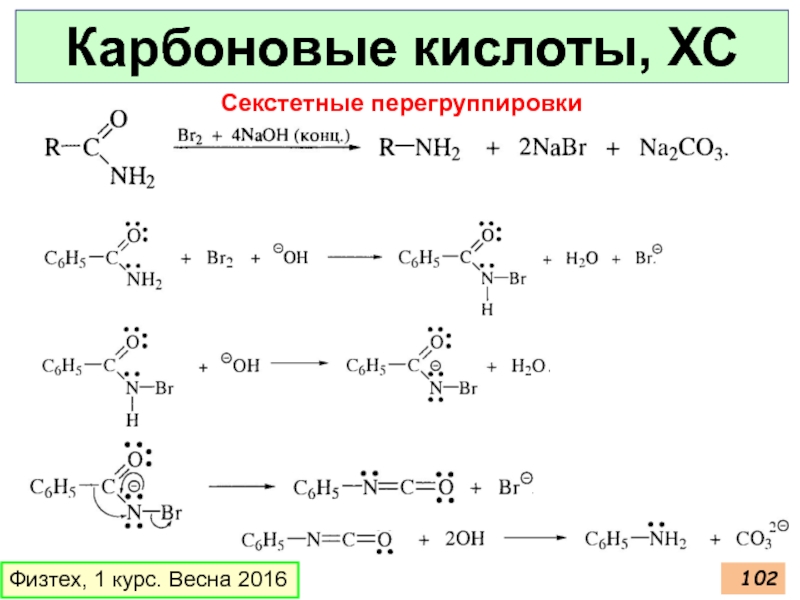
- 102. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Секстетные перегруппировки
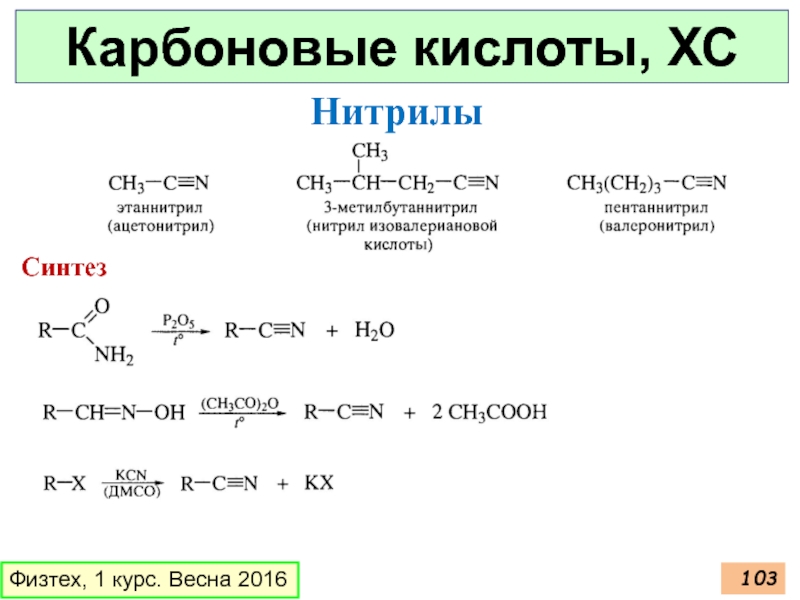
- 103. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Нитрилы Синтез
- 104. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Реакция Риттера Гидролиз Восстановление Нитрилы
- 105. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
- 106. Оксокарбоновые кислоты, ПЛ Физтех, 1 курс. Весна 2016 Оксокислоты Сложноэфирная конденсация Кляйзена
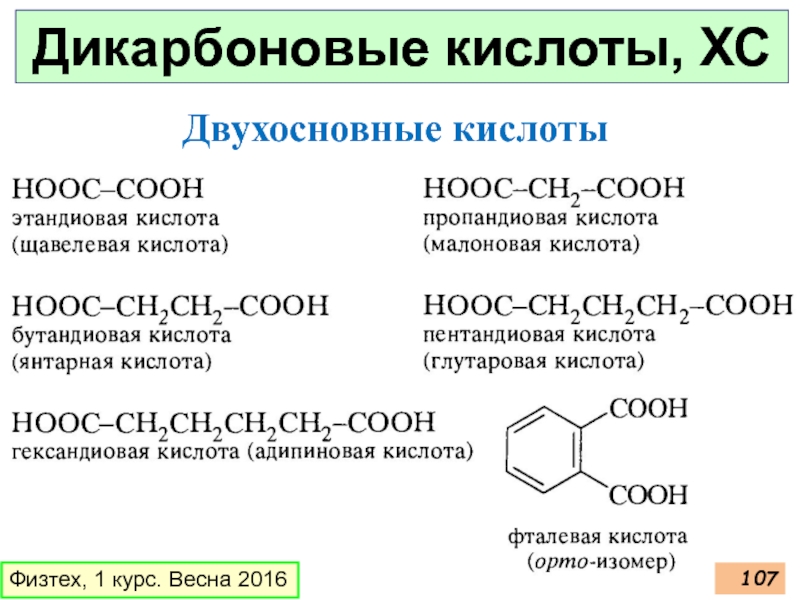
- 107. Дикарбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Двухосновные кислоты
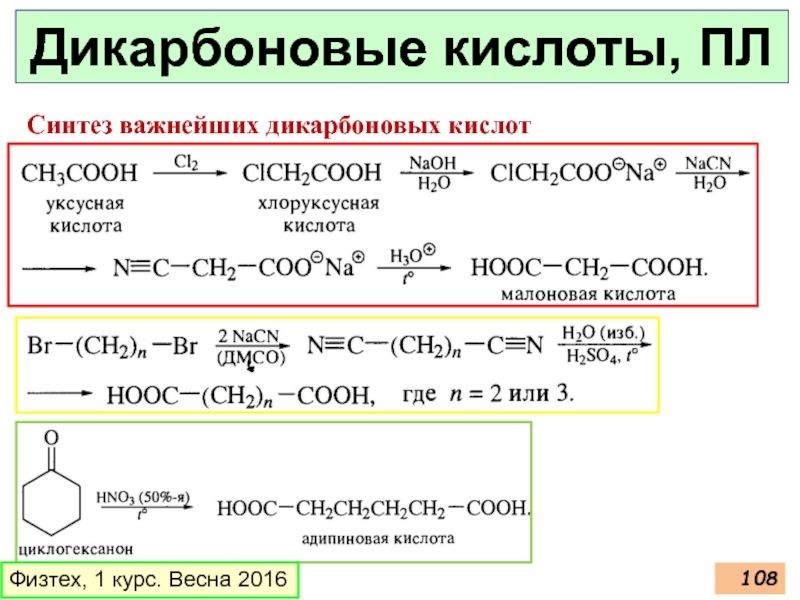
- 108. Дикарбоновые кислоты, ПЛ Физтех, 1 курс. Весна 2016 Синтез важнейших дикарбоновых кислот
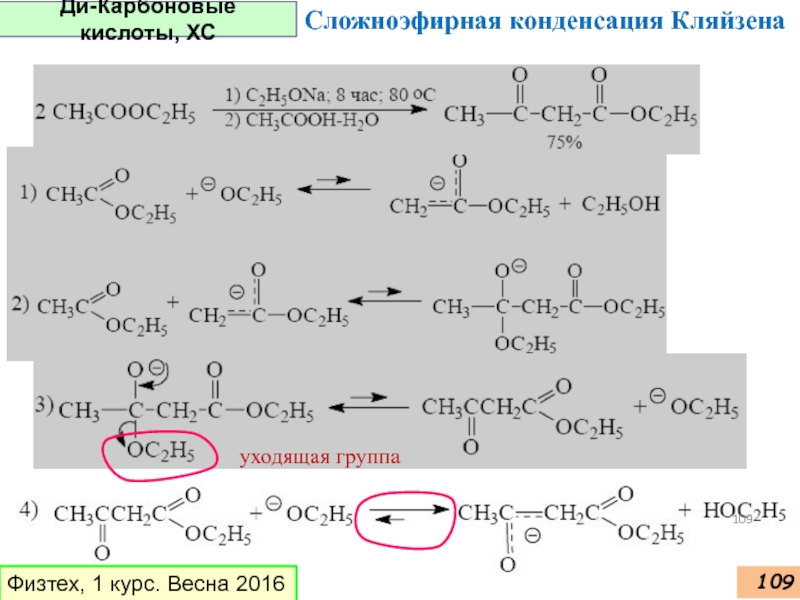
- 109. Ди-Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Сложноэфирная конденсация Кляйзена уходящая группа
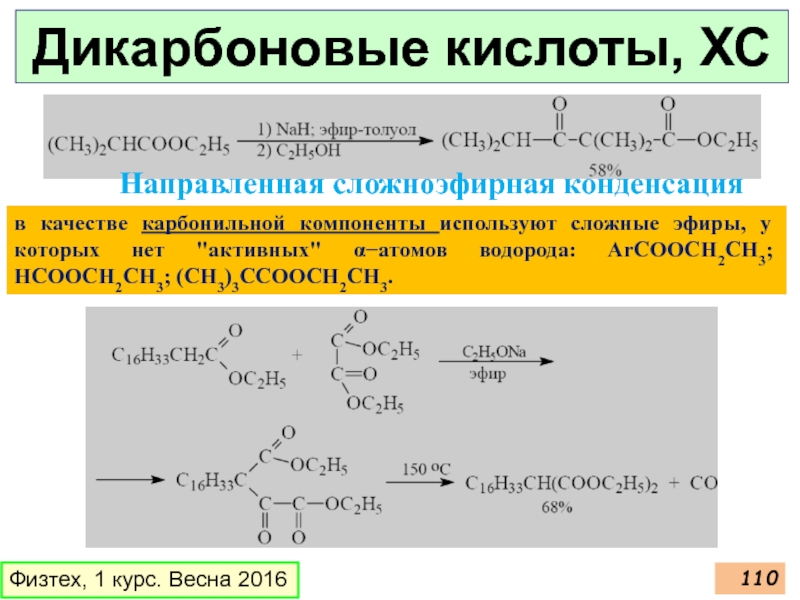
- 110. Дикарбоновые кислоты, ХС Физтех, 1 курс. Весна
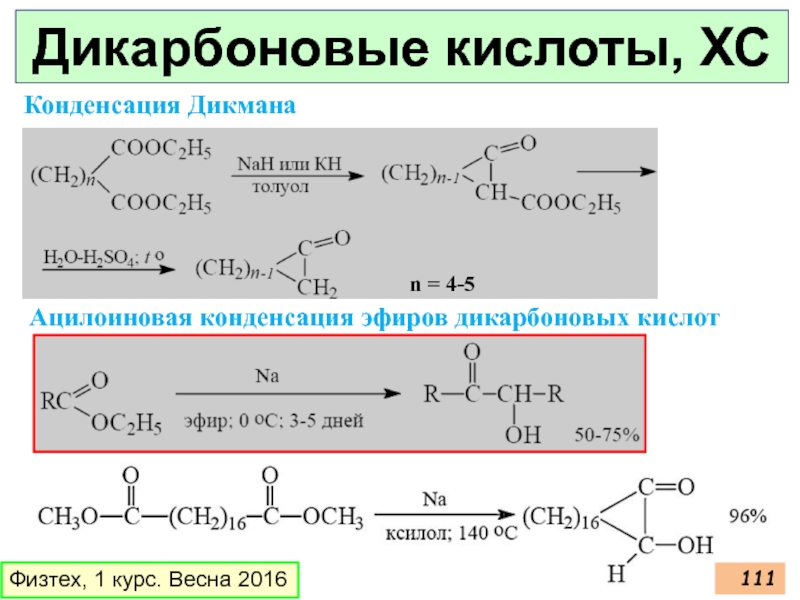
- 111. Дикарбоновые кислоты, ХС Физтех, 1 курс. Весна
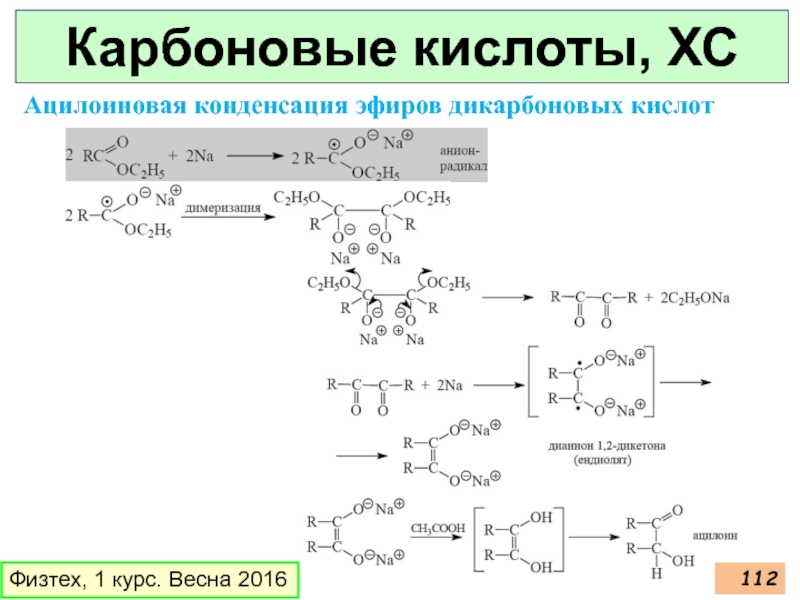
- 112. Карбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Ацилоиновая конденсация эфиров дикарбоновых кислот
- 113. Карбоновые кислоты, ХС Физтех, 1 курс. Весна
- 114. Оксокарбоновые кислоты, ХС Физтех, 1 курс. Весна
- 115. Оксокарбоновые кислоты, ХС Физтех, 1 курс. Весна 2016
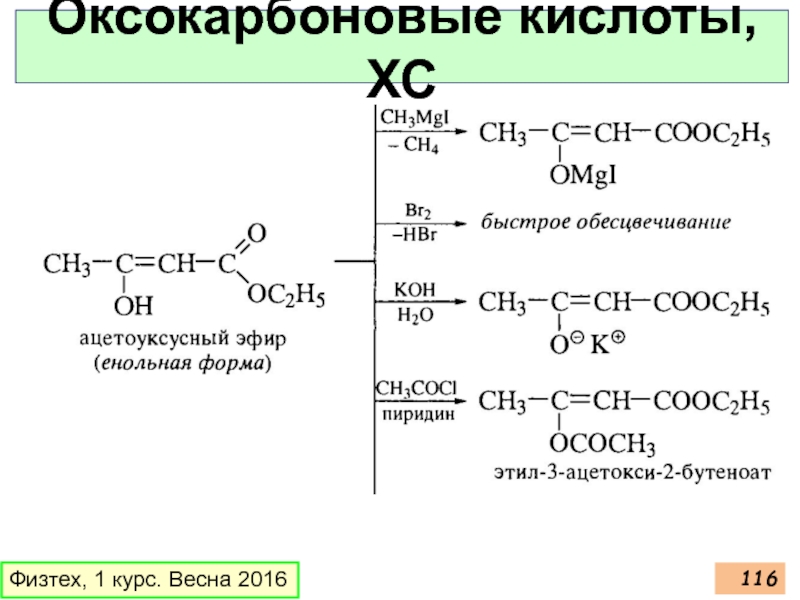
- 116. Оксокарбоновые кислоты, ХС Физтех, 1 курс. Весна 2016
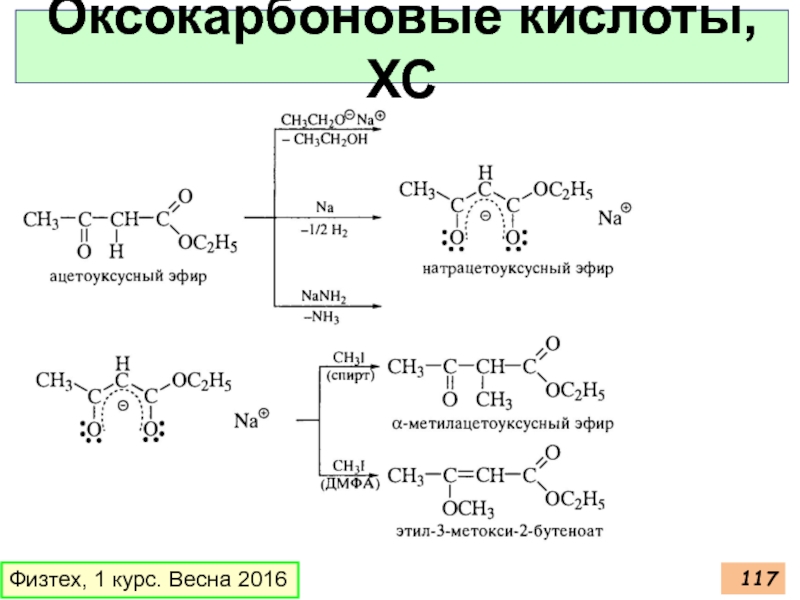
- 117. Оксокарбоновые кислоты, ХС Физтех, 1 курс. Весна 2016
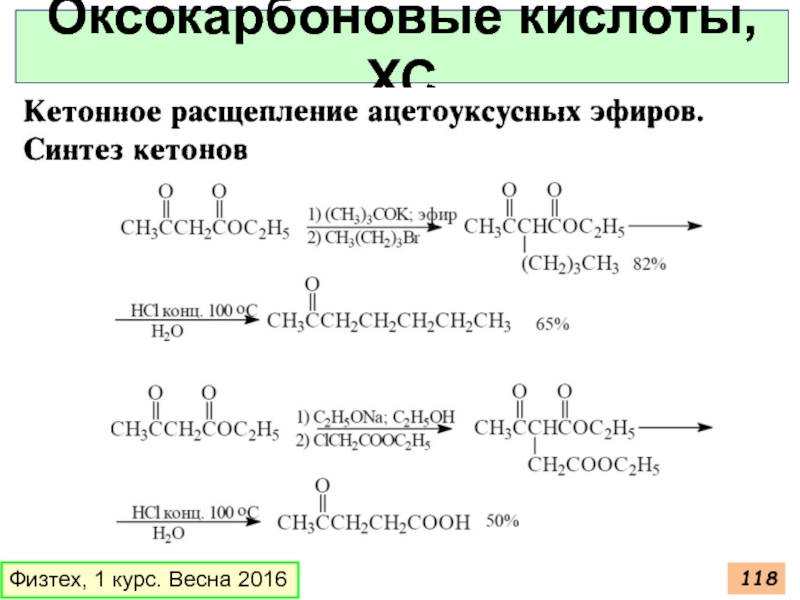
- 118. Оксокарбоновые кислоты, ХС Физтех, 1 курс. Весна 2016
- 119. Оксокарбоновые кислоты, ХС Физтех, 1 курс. Весна 2016
- 120. Дикарбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Синтезы с использованием малонового эфира
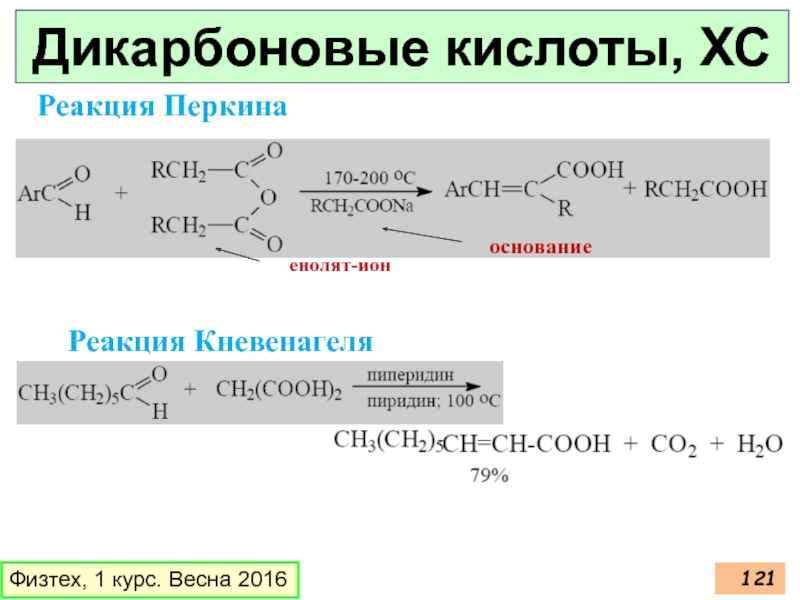
- 121. Дикарбоновые кислоты, ХС Физтех, 1 курс. Весна 2016 Реакция Кневенагеля Реакция Перкина основание енолят-ион
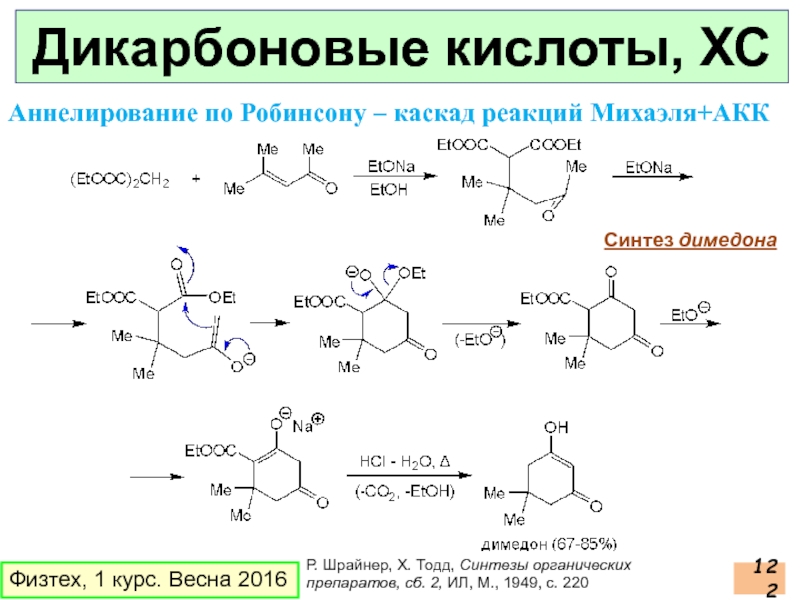
- 122. Физтех, 1 курс. Весна 2016 Дикарбоновые кислоты,
- 123. Коротко о главном Производные карбоновых кислот –
- 124. Основные понятия Для реакции карбоксильной группы основной
Слайд 1Физтех, 1 курс. Весна 2016
Функциональные производные с кратной связью C=“Э”
Часть 1
Карбонильные
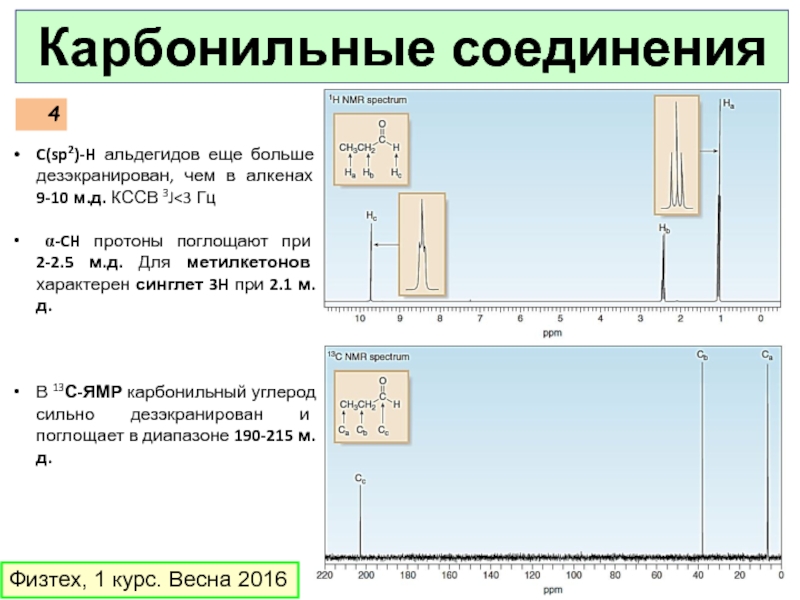
Слайд 4Физтех, 1 курс. Весна 2016
Карбонильные соединения
C(sp2)-H альдегидов еще больше дезэкранирован, чем
α-CH протоны поглощают при 2-2.5 м.д. Для метилкетонов характерен синглет 3H при 2.1 м.д.
В 13С-ЯМР карбонильный углерод сильно дезэкранирован и поглощает в диапазоне 190-215 м.д.
Слайд 7Физтех, 1 курс. Весна 2016
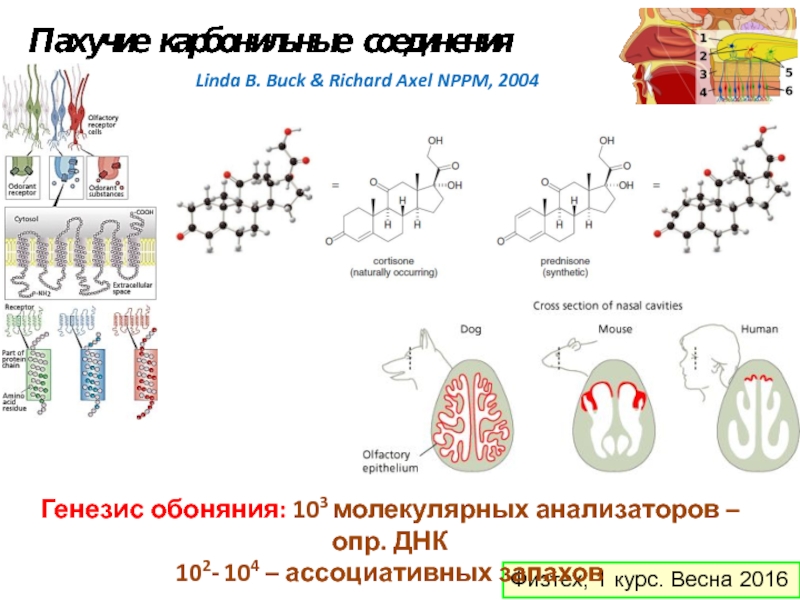
Генезис обоняния: 103 молекулярных анализаторов – опр.
102- 104 – ассоциативных запахов
Linda B. Buck & Richard Axel NPPM, 2004
Слайд 8Физтех, 1 курс. Весна 2016
Карбонильные соединения, ФС
Основность
Кислотность α-С-Н связей
Енол является на
Слайд 9Альдегиды – более реакционноспособные соединения чем кетоны в реакциях нуклеофильного присоединения
Более
а) отсутствием стерических препятствий для атаки нуклеофильного агента
б) более высокой термодинамической стабильностью кетонов по сравнению с альдегидами
1) гиперконъюгация σ-связи С-Н-α-углеродного атома и частично пустой p-орбитали карбонильного углерода приводит к делокализации заряда
2) (+I)-эффект алкильной группы при карбонильном атоме углерода также приводит к делокализации положительного заряда по цепи углеродных связей
Карбонильные соединения, ФС
Физтех, 1 курс. Весна 2016
Слайд 10Физтех, 1 курс. Весна 2016
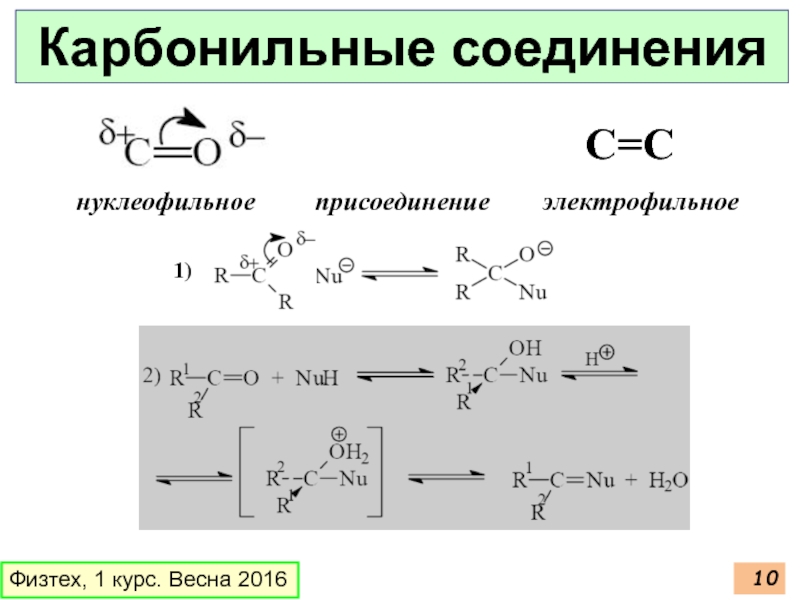
Карбонильные соединения
С=С
нуклеофильное
1)
Слайд 12Физтех, 1 курс. Весна 2016
AdN реакции КС (примеры)
Карбонильные соединения
1) Гидратация (O-нуклеофилы)
2)
обрат. р-я:
Слайд 13Физтех, 1 курс. Весна 2016
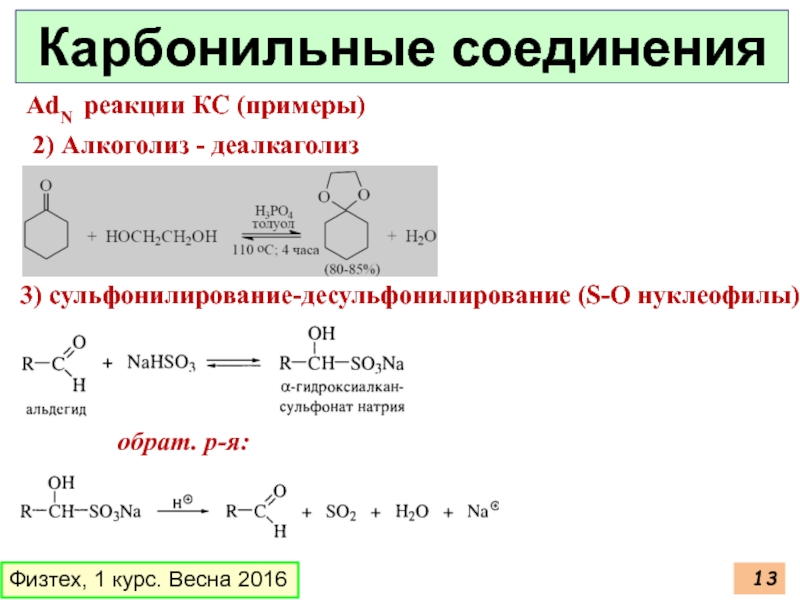
Карбонильные соединения
AdN реакции КС (примеры)
2) Алкоголиз -
3) сульфонилирование-десульфонилирование (S-O нуклеофилы)
обрат. р-я:
Слайд 14Физтех, 1 курс. Весна 2016
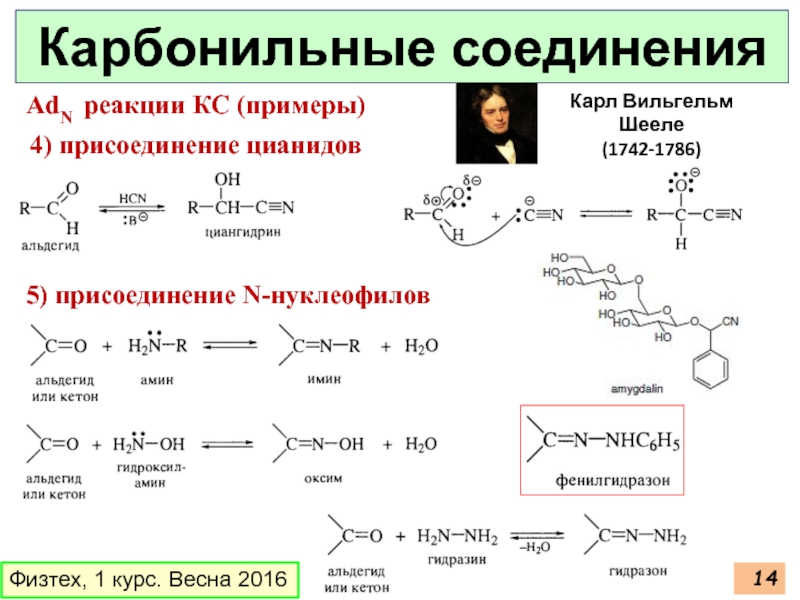
Карбонильные соединения
4) присоединение цианидов
AdN реакции КС (примеры)
5)
Карл Вильгельм Шееле
(1742-1786)
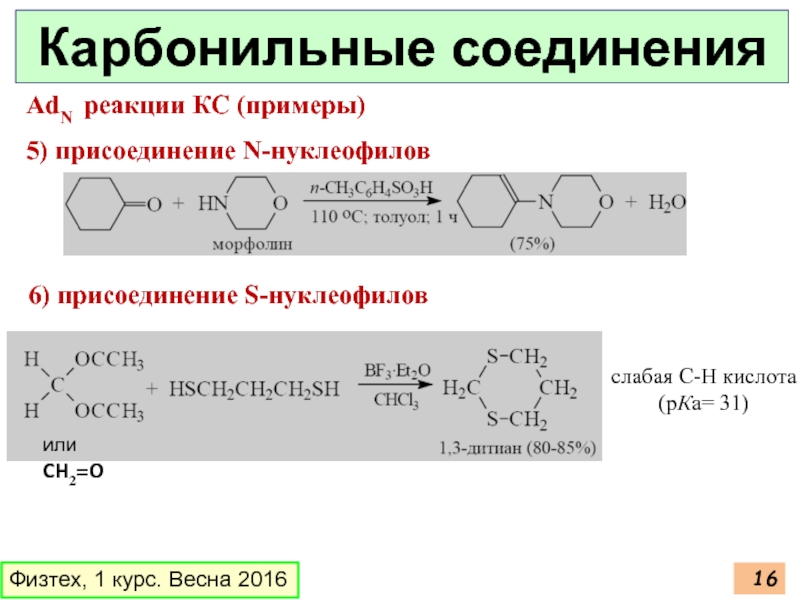
Слайд 16Физтех, 1 курс. Весна 2016
Карбонильные соединения
AdN реакции КС (примеры)
5) присоединение N-нуклеофилов
6)
слабая С-Н кислота (рКа= 31)
или CH2=O
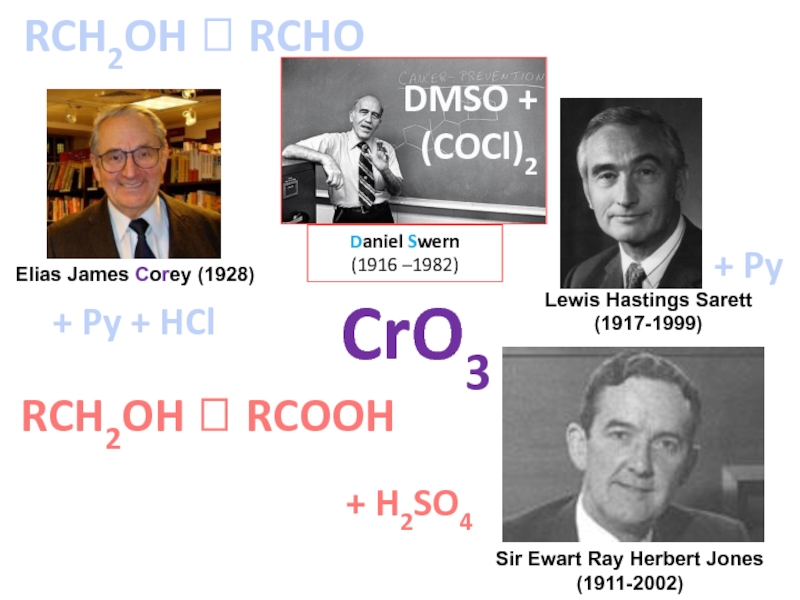
Слайд 17
Lewis Hastings Sarett
(1917-1999)
Sir Ewart Ray Herbert Jones
(1911-2002)
Elias James Corey (1928)
Daniel
(1916 –1982)
CrO3
+ Py + HCl
+ Py
+ H2SO4
DMSO + (COCl)2
RCH2OH ? RCHO
RCH2OH ? RCOOH
Слайд 18Физтех, 1 курс. Весна 2016
Карбонильные соединения, ПЛ
реагент Кори, пиридинийхлорхромат
Реагенты: Сверна, Кори,
окисление спиртов
озонолиз алкенов
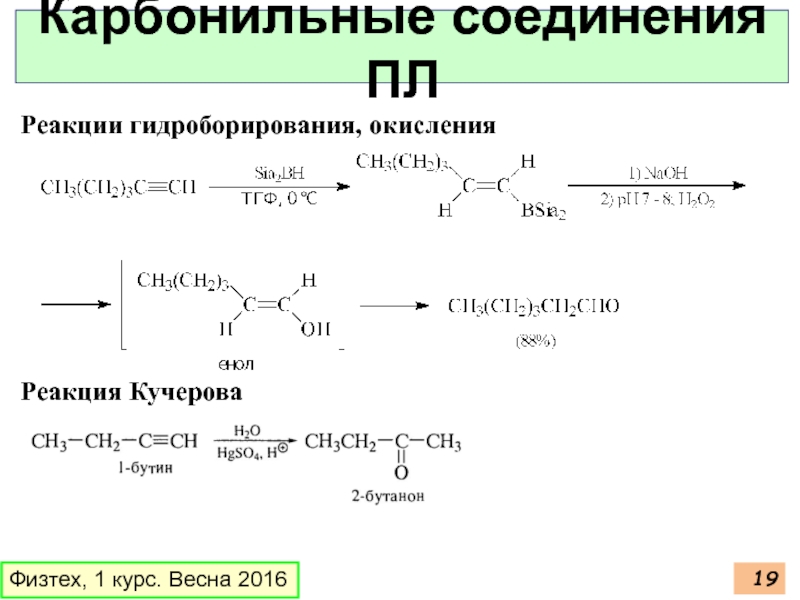
Слайд 19Физтех, 1 курс. Весна 2016
Карбонильные соединения ПЛ
Реакции гидроборирования, окисления
Реакция Кучерова
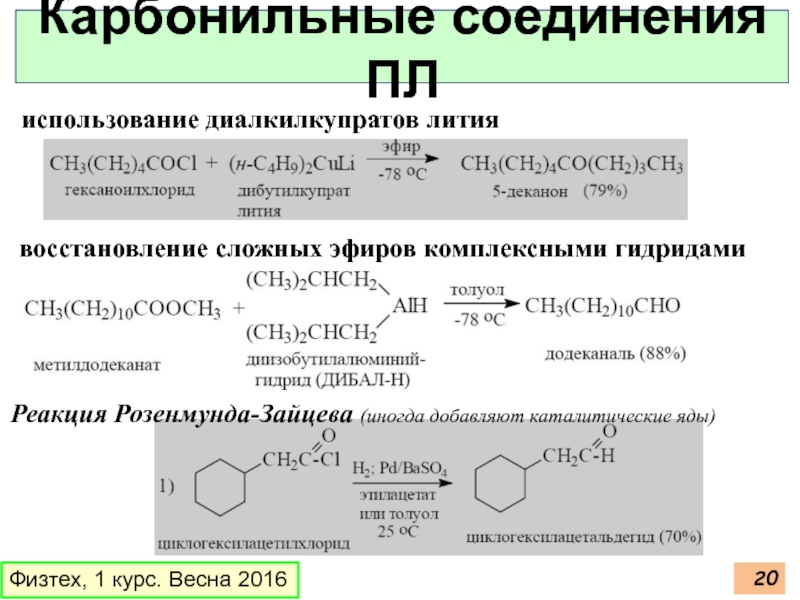
Слайд 20Физтех, 1 курс. Весна 2016
Карбонильные соединения ПЛ
использование диалкилкупратов лития
восстановление сложных эфиров
Реакция Розенмунда-Зайцева (иногда добавляют каталитические яды)
Слайд 21Физтех, 1 курс. Весна 2016
Карбонильные соединения ,ПЛ
Синтез через 1,3-дитиан
пиролиз солей карбоновых
Слайд 22Физтех, 1 курс. Весна 2016
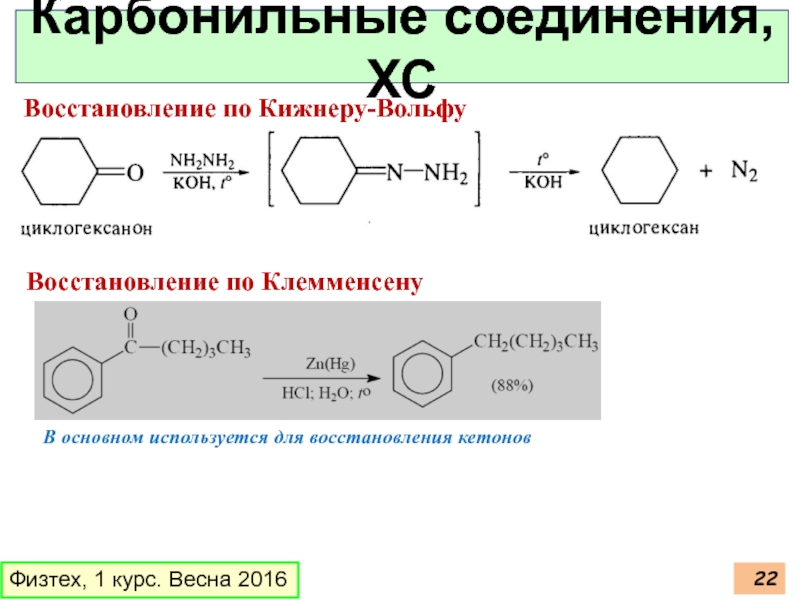
Карбонильные соединения, ХС
Восстановление по Кижнеру-Вольфу
Восстановление по Клемменсену
В
Слайд 23Физтех, 1 курс. Весна 2016
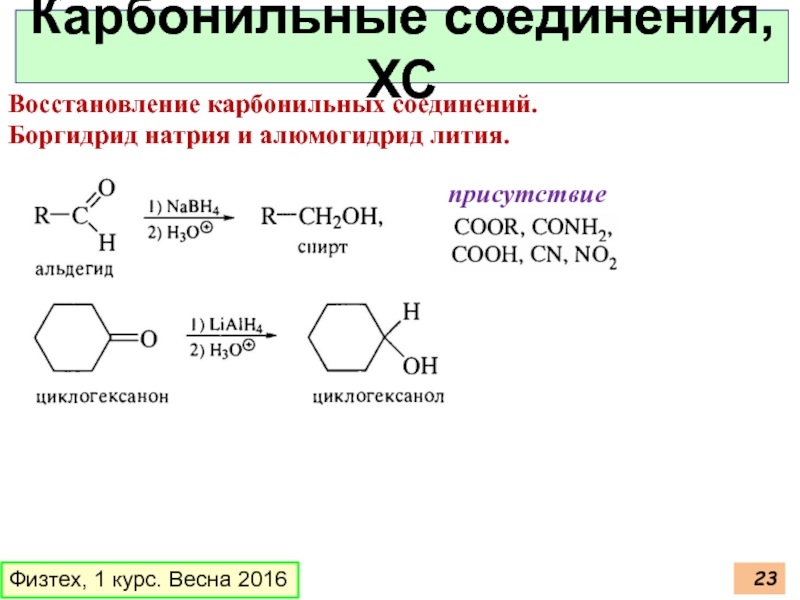
Карбонильные соединения, ХС
Восстановление карбонильных соединений.
Боргидрид натрия и
присутствие
Слайд 24Физтех, 1 курс. Весна 2016
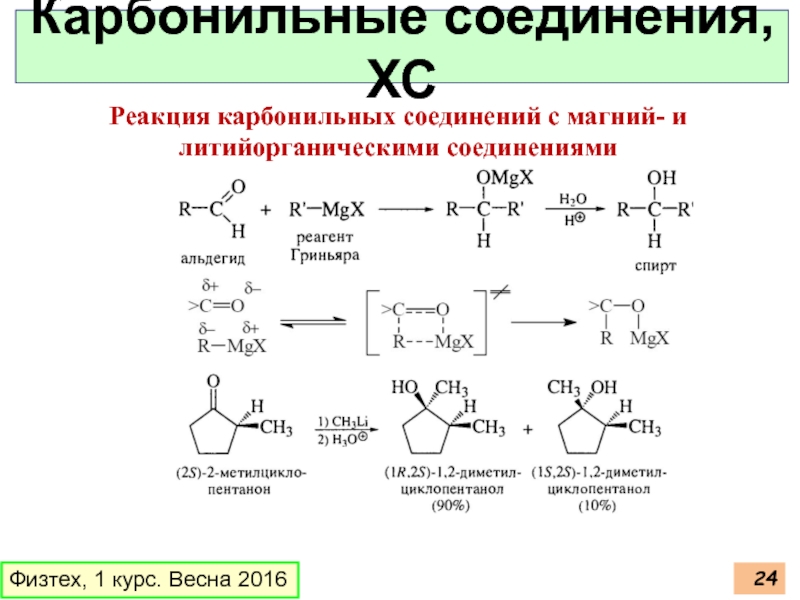
Карбонильные соединения, ХС
Реакция карбонильных соединений с магний-
Слайд 25Физтех, 1 курс. Весна 2016
Карбонильные соединения, ХС
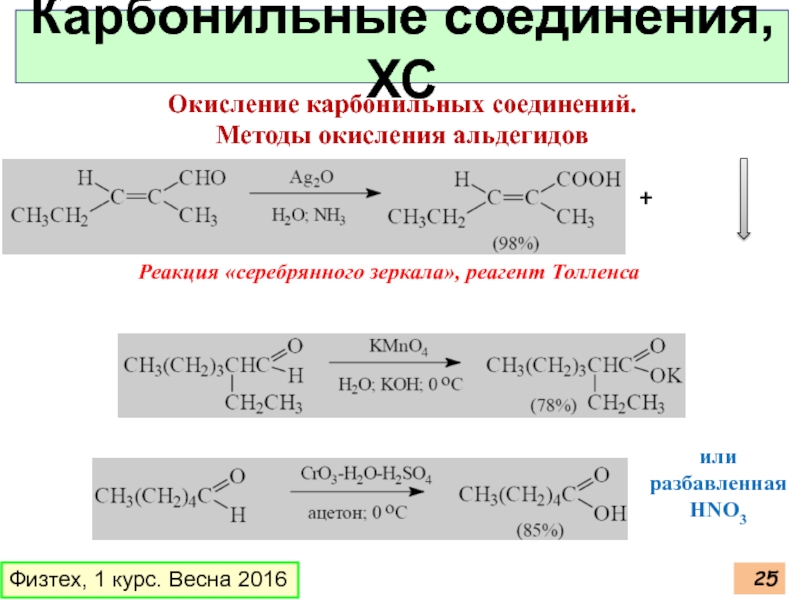
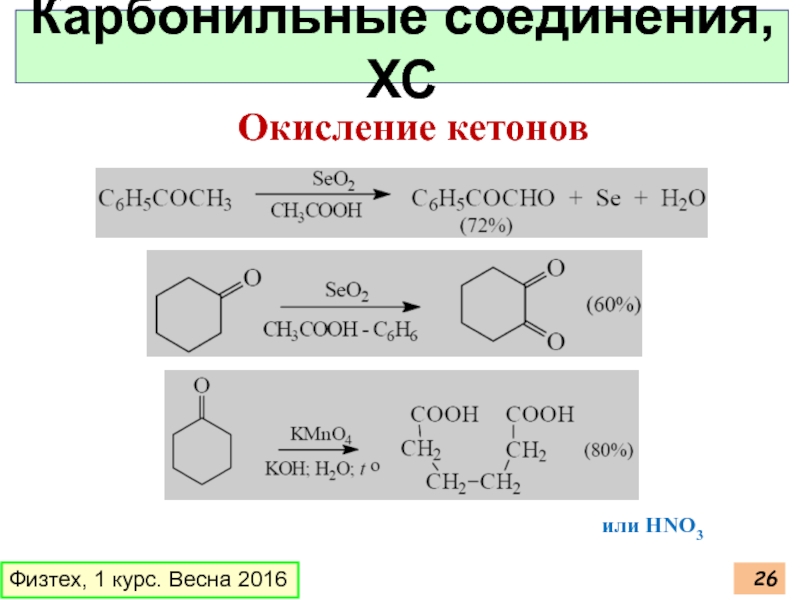
Окисление карбонильных соединений.
Методы окисления
или разбавленная НNO3
Реакция «серебрянного зеркала», реагент Толленса
+ Ag
Слайд 27Физтех, 1 курс. Весна 2016
Карбонильные соединения, ХС
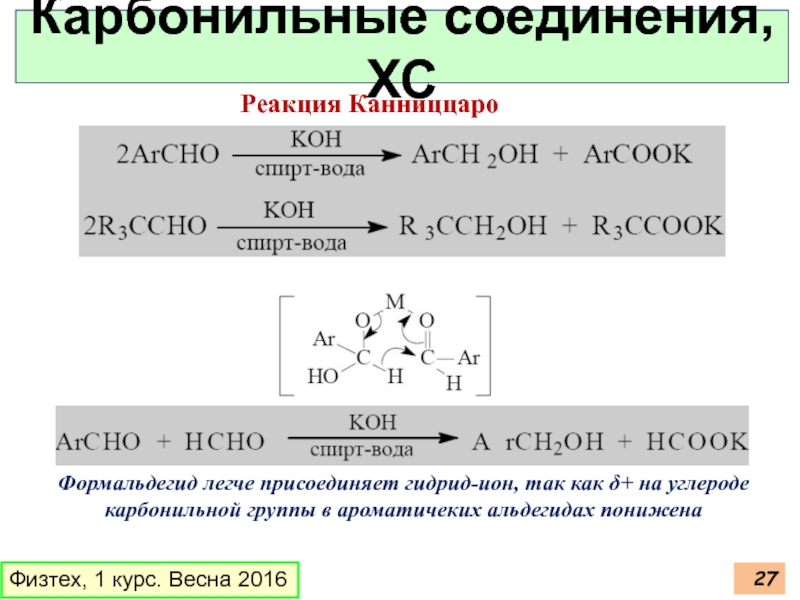
Реакция Канниццаро
Формальдегид легче присоединяет гидрид-ион,
Слайд 28Физтех, 1 курс. Весна 2016
Функциональные производные с кратной связью C=“Э”
Часть 2
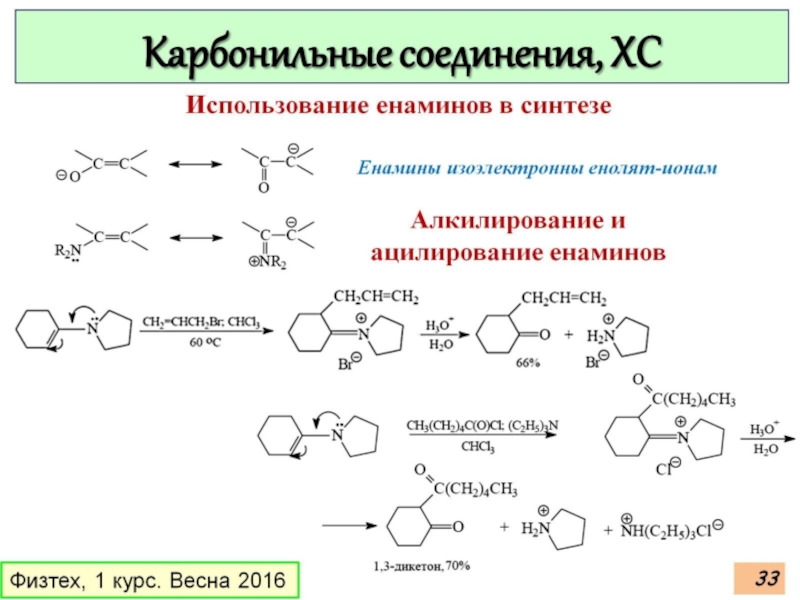
Химические
и енолят-ионов
Слайд 29Физтех, 1 курс. Весна 2016
Карбонильные соединения
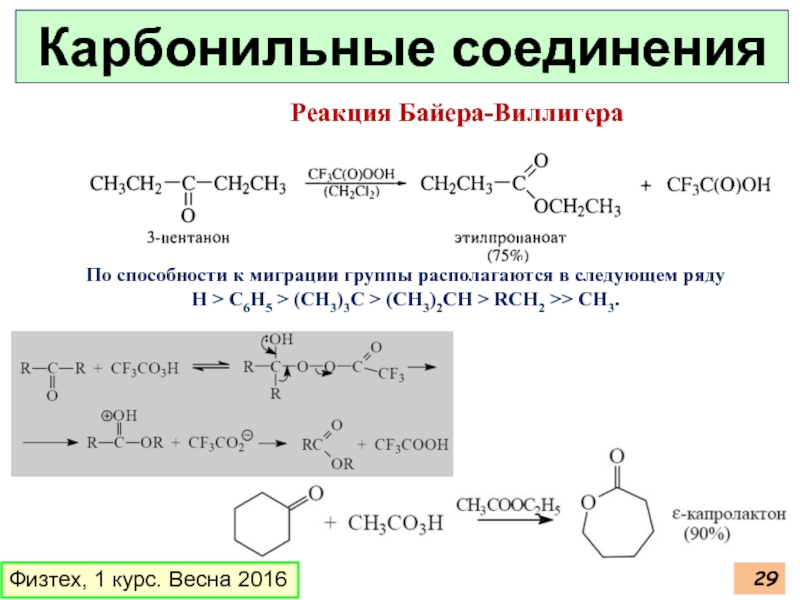
Реакция Байера-Виллигера
По способности к миграции группы
Н > С6Н5 > (СН3)3С > (СН3)2СН > RCH2 >> СН3.
Слайд 30Физтех, 1 курс. Весна 2016
Карбонильные соединения, ХС
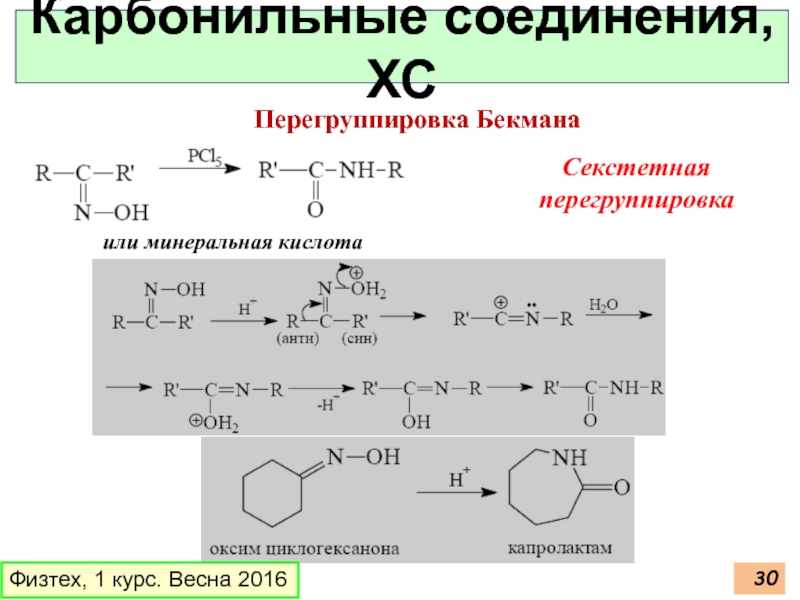
или минеральная кислота
Секстетная перегруппировка
Перегруппировка Бекмана
Слайд 31Физтех, 1 курс. Весна 2016
Карбонильные соединения, ХС
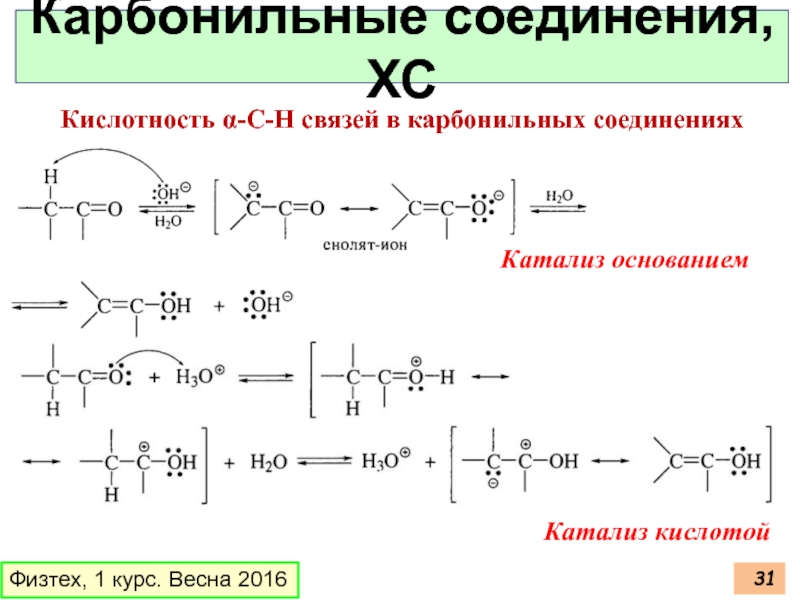
Кислотность α-С-Н связей в карбонильных
Катализ основанием
Катализ кислотой
Слайд 33Физтех, 1 курс. Весна 2016
Карбонильные соединения , ХС
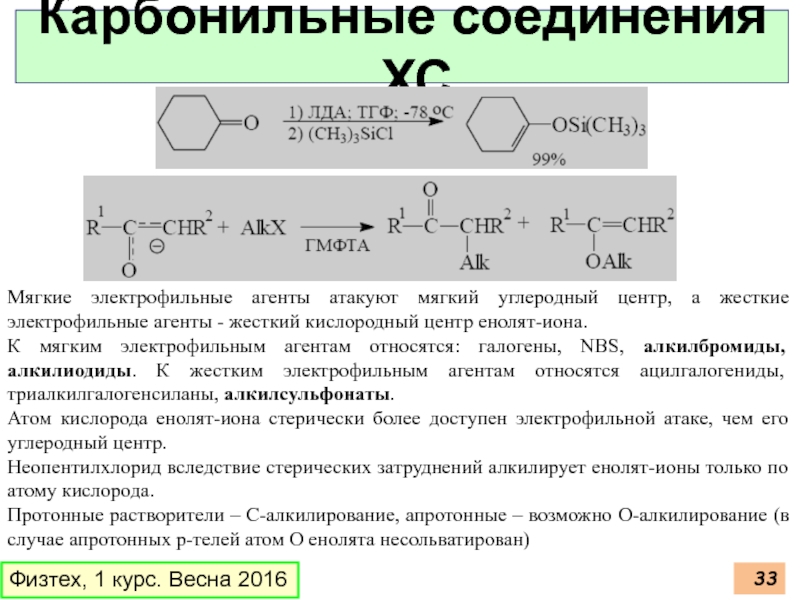
Мягкие электрофильные агенты атакуют
К мягким электрофильным агентам относятся: галогены, NBS, алкилбромиды, алкилиодиды. К жестким электрофильным агентам относятся ацилгалогениды, триалкилгалoгeнсиланы, алкилсульфонаты.
Атом кислорода енолят-иона стерически более доступен электрофильной атаке, чем его углеродный центр.
Неопентилхлорид вследствие стерических затруднений алкилирует енолят-ионы только по атому кислорода.
Протонные растворители – С-алкилирование, апротонные – возможно О-алкилирование (в случае апротонных р-телей атом О енолята несольватирован)
Слайд 36Физтех, 1 курс. Весна 2016
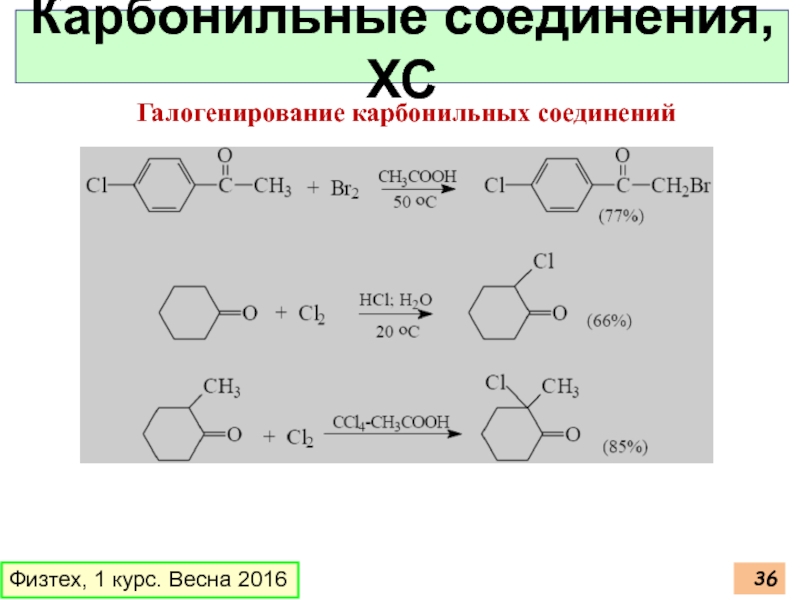
Карбонильные соединения, ХС
Галогенирование карбонильных соединений
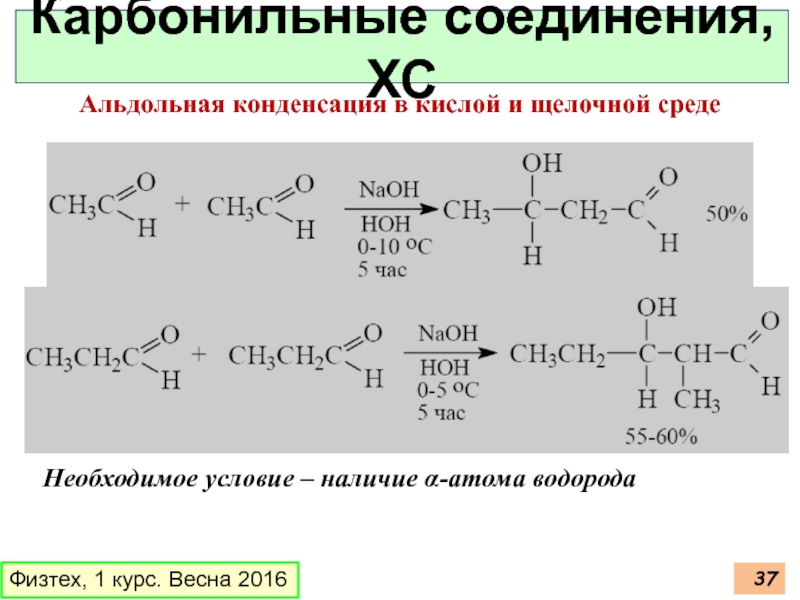
Слайд 37Физтех, 1 курс. Весна 2016
Карбонильные соединения, ХС
Альдольная конденсация в кислой и
Необходимое условие – наличие α-атома водорода
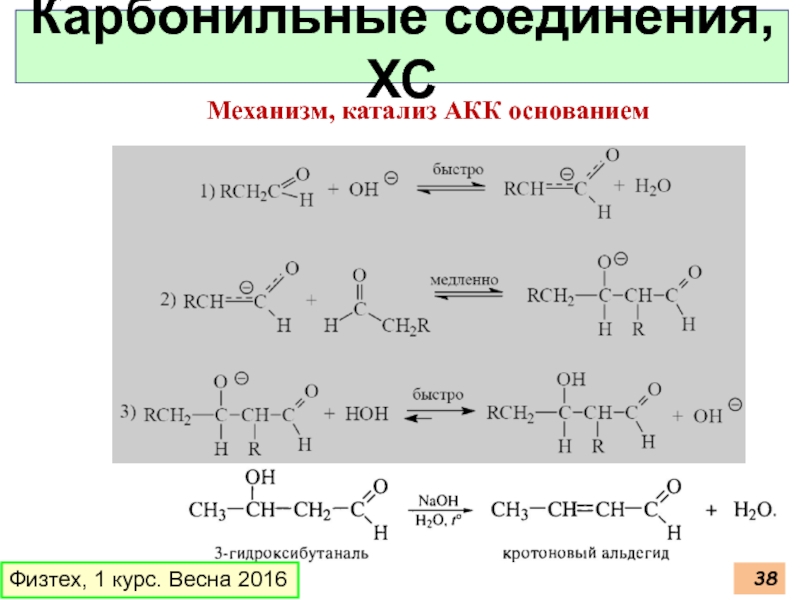
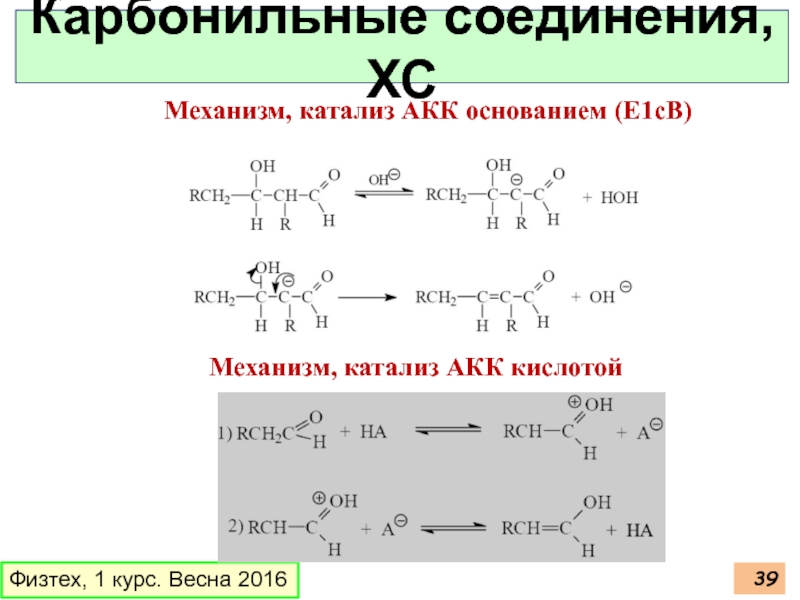
Слайд 39Физтех, 1 курс. Весна 2016
Карбонильные соединения, ХС
Механизм, катализ АКК основанием (E1cB)
Механизм,
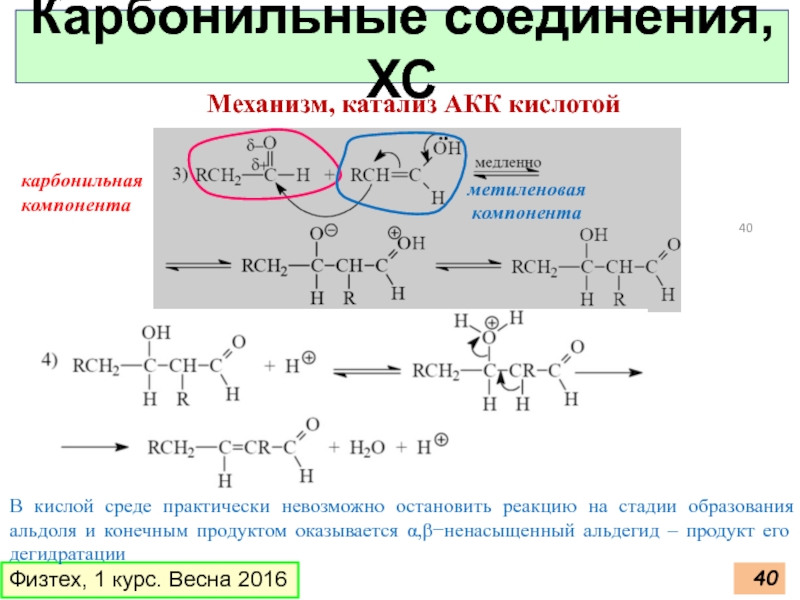
Слайд 40Физтех, 1 курс. Весна 2016
Карбонильные соединения, ХС
Механизм, катализ АКК кислотой
карбонильная компонента
метиленовая
В кислой среде практически невозможно остановить реакцию на стадии образования альдоля и конечным продуктом оказывается α,β−ненасыщенный альдегид – продукт его дегидратации
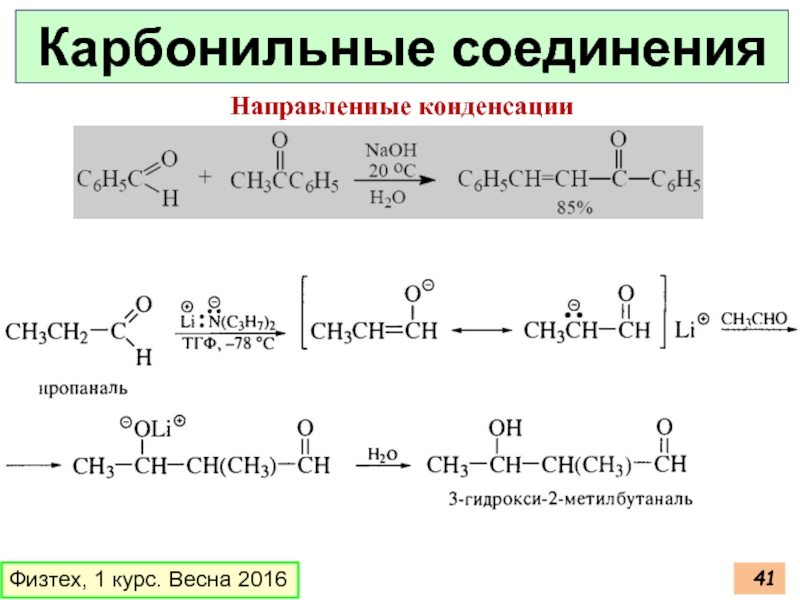
Слайд 43Физтех, 1 курс. Весна 2016
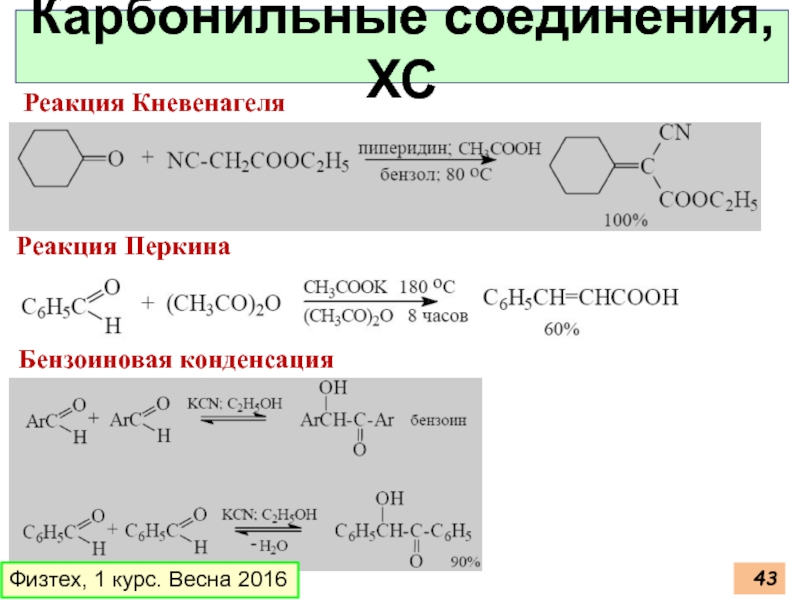
Карбонильные соединения, ХС
Реакция Кневенагеля
Реакция Перкина
Бензоиновая конденсация
Слайд 44Физтех, 1 курс. Весна 2016
Функциональные производные с кратной связью C=“Э”
Часть 3
Сопряженные
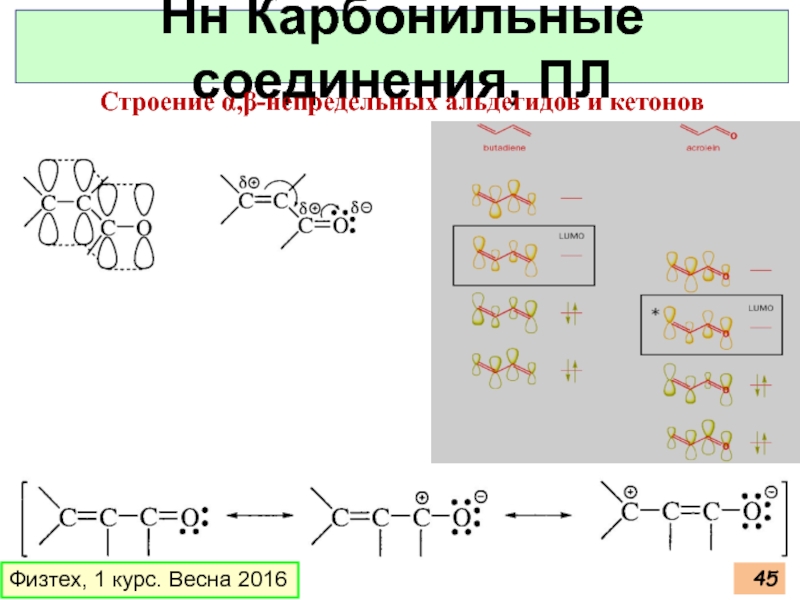
Слайд 45Физтех, 1 курс. Весна 2016
Нн Карбонильные соединения, ПЛ
Строение α,β-непредельных альдегидов и
Слайд 46Физтех, 1 курс. Весна 2016
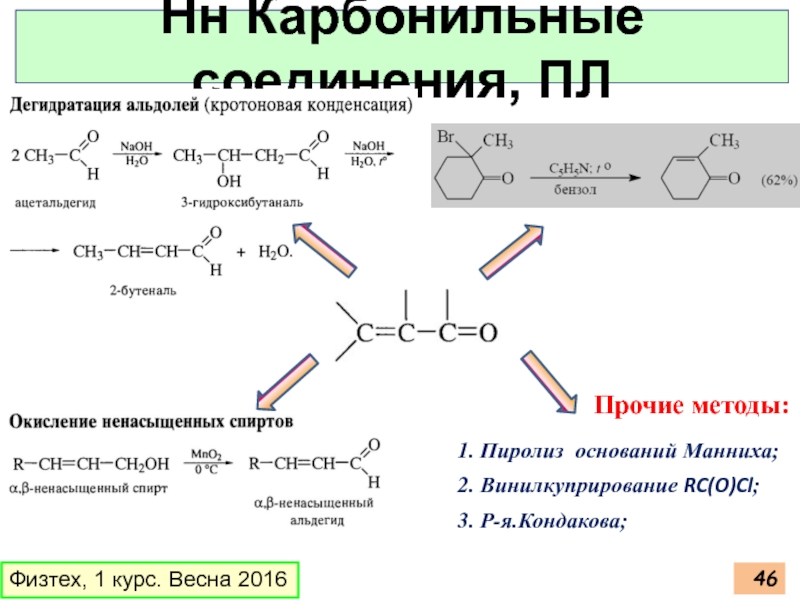
Нн Карбонильные соединения, ПЛ
Прочие методы:
1. Пиролиз оснований
2. Винилкуприрование RC(O)Cl;
3. Р-я.Кондакова;
Слайд 47Физтех, 1 курс. Весна 2016
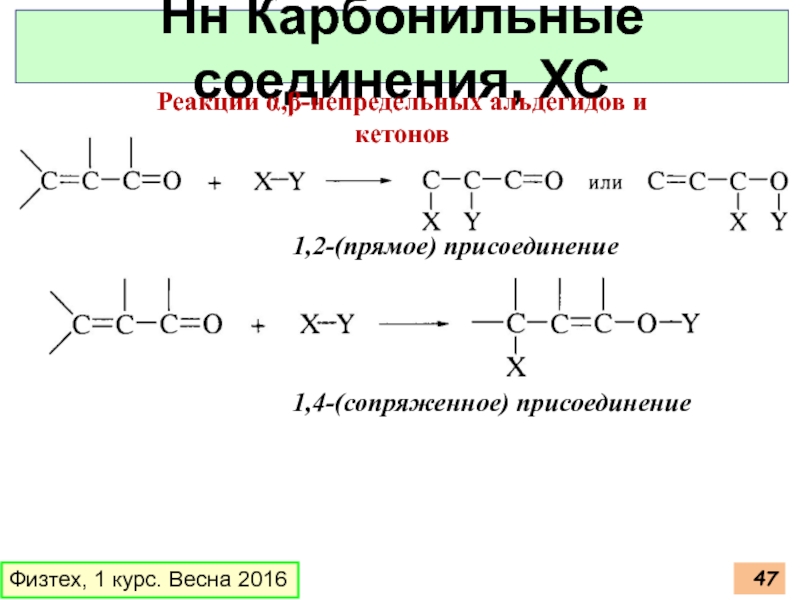
Нн Карбонильные соединения, ХС
Реакции α,β-непредельных альдегидов и
кетонов
1,2-(прямое) присоединение
1,4-(сопряженное) присоединение
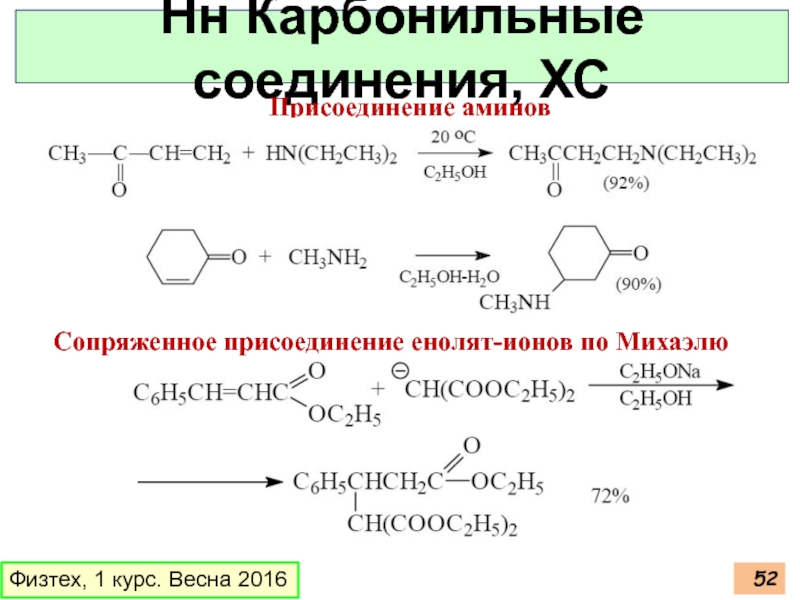
Слайд 52Физтех, 1 курс. Весна 2016
Нн Карбонильные соединения, ХС
Присоединение аминов
Сопряженное присоединение енолят-ионов
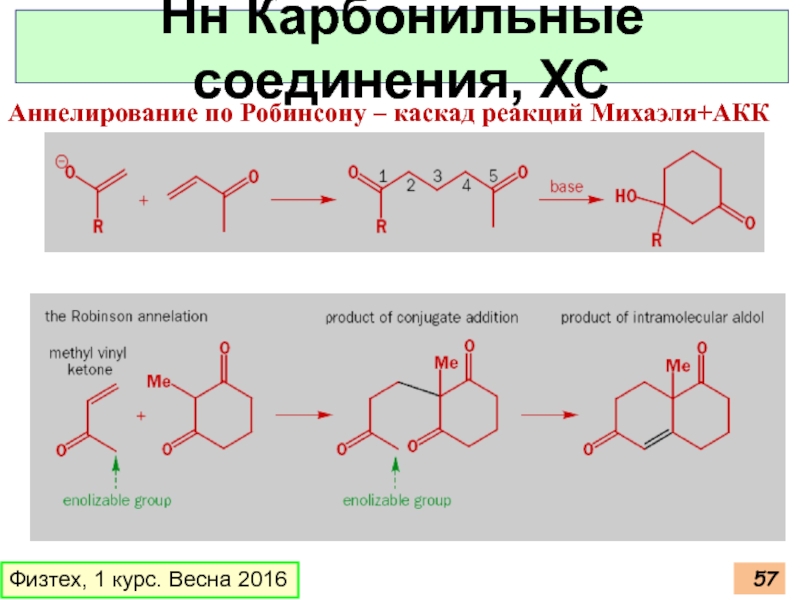
Слайд 57Нн Карбонильные соединения, ХС
Аннелирование по Робинсону – каскад реакций Михаэля+АКК
Физтех, 1
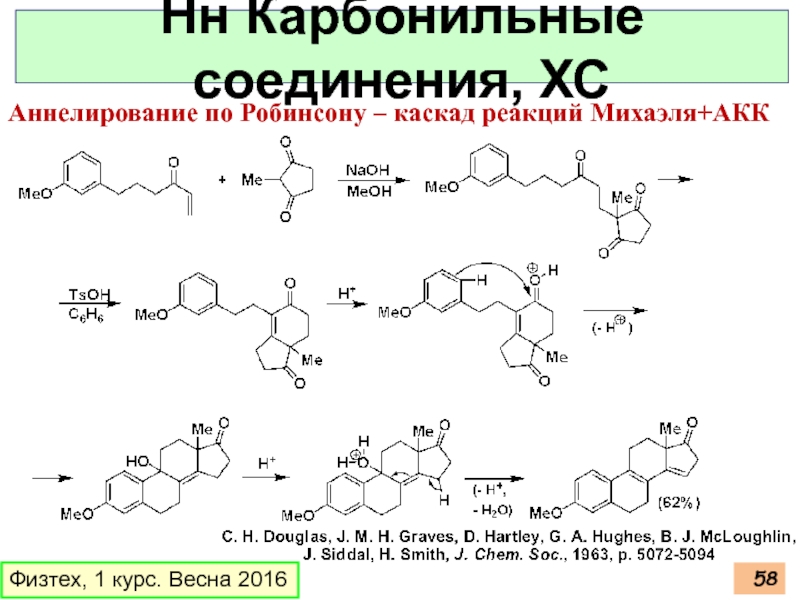
Слайд 58Физтех, 1 курс. Весна 2016
Нн Карбонильные соединения, ХС
Аннелирование по Робинсону –
Слайд 59Физтех, 1 курс. Весна 2016
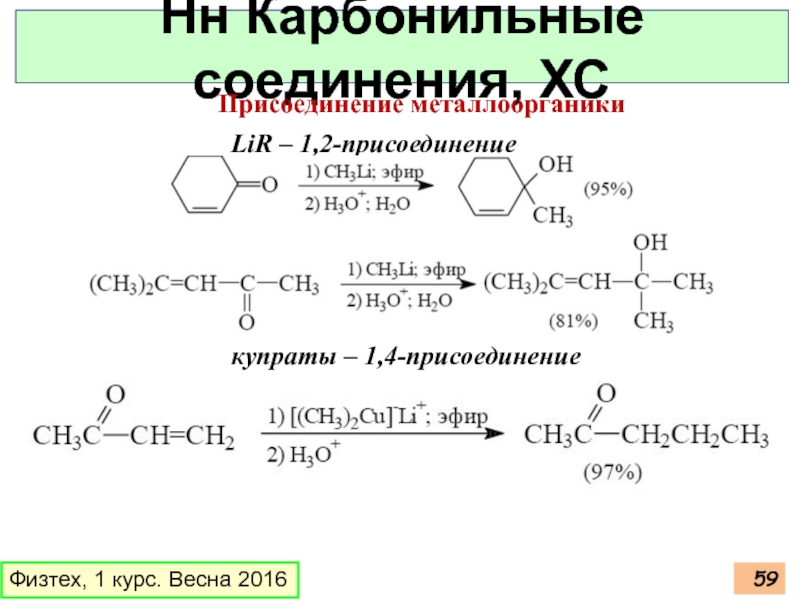
Нн Карбонильные соединения, ХС
Присоединение металлоорганики
LiR – 1,2-присоединение
купраты
Слайд 63Коротко о главном
Кетоны и альдегиды кислородсодержащий промежуточный класс (между спиртами и
Для карбонильной функции характерны реакции протекающие по механизмам AdN, SE
Широкий спектр превращений для КС (в том числе «автореакций») составляют реакции конденсации и диспропорционирования.
Для оксимов и кетонов используют (две) реакции перехода к карбокси-производным (амидам и сл.эфирам) через перегруппировки Бекмана и Байера-Виллигера.
α,β-Непредельные КС - основные продукты АК-конденсаций исходные для создания алициклических полифункциональных КС через каскад реакций аннелирования
Физтех, 1 курс. Весна 2016
Слайд 64Основные понятия
Для реакции карбонильной группы основной путь лежит через «тетраэдрический интермедиат».
Относительная
AdN – атака внешнего нуклеофила зависит от природы субстрата и конкурирует с термодинамически-выгодным процессом - депротонирование – автоконденсация (АКК).
Амбидентная природа енолята и α,β- енонов согласуется с общими принципами теории ЖМКО
Физтех, 1 курс. Весна 2016
Слайд 65Физтех, 1 курс. Весна 2016
Функциональные производные с кратной связью C=“Э”
Часть 4
Производные
Слайд 67Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Карбоновая к-та
Карбоксил Ацилгалогенид Ангидрид
Нитрил Сложный эфир
Перв.амид Втор.амид Трет.амид
Слайд 68Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Карбоновая к-та Гидроксамовая к-та Гидразид
Тиоэфир
Тиоамид Азид
Иминоэфир Амидоксим Амидразон
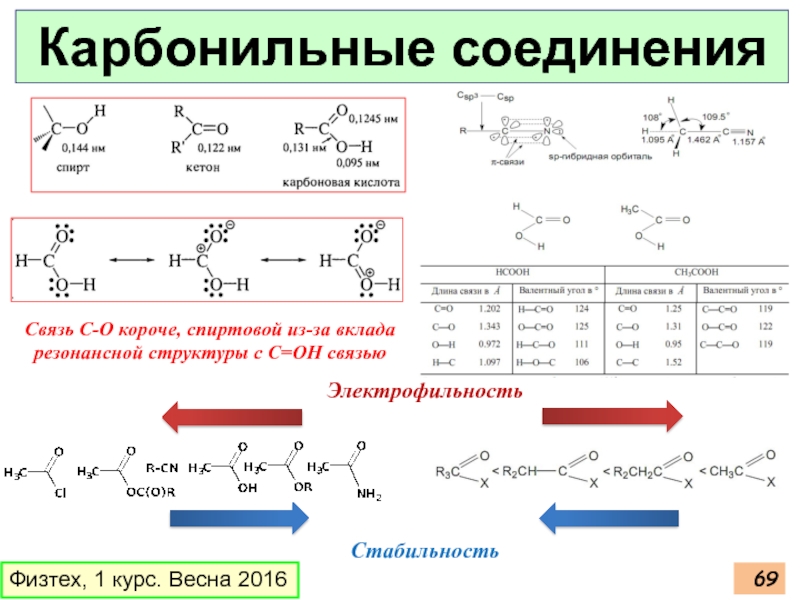
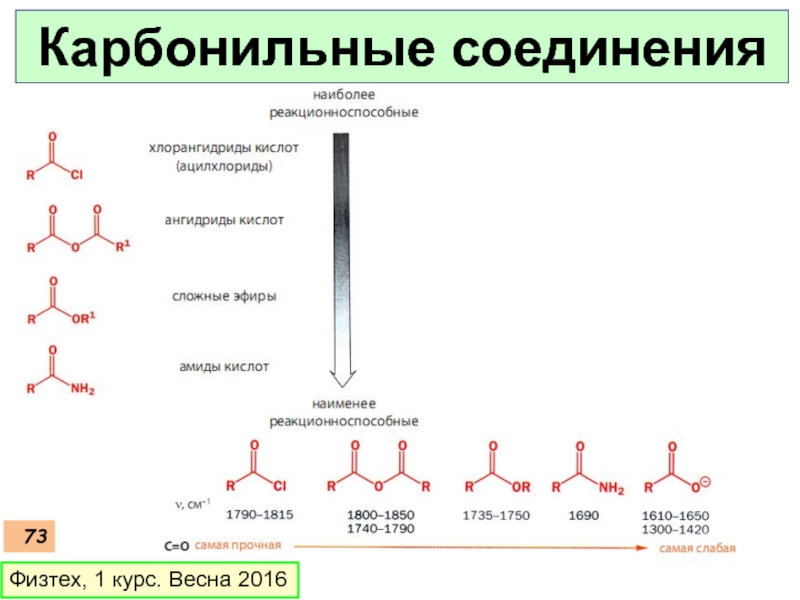
Слайд 69Электрофильность
Стабильность
Физтех, 1 курс. Весна 2016
Карбонильные
Связь С-О короче, спиртовой из-за вклада резонансной структуры с С=ОН связью
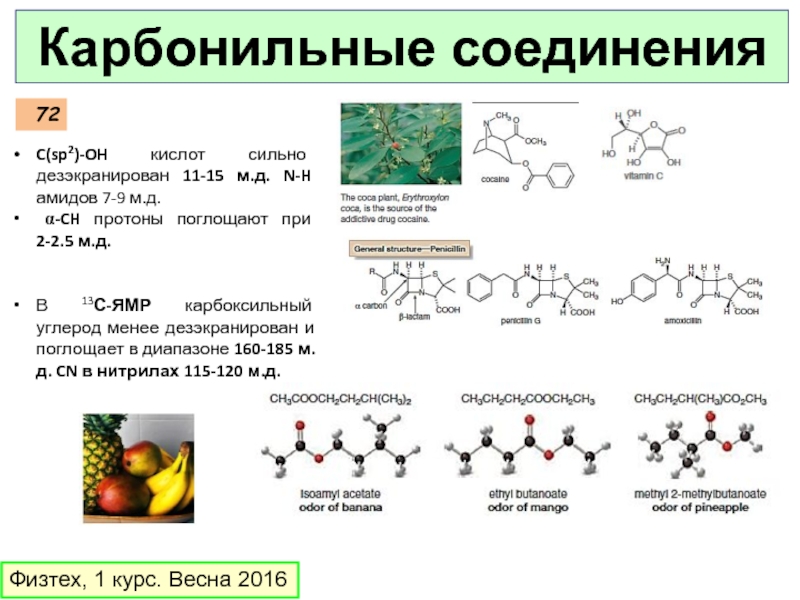
Слайд 72Физтех, 1 курс. Весна 2016
Карбонильные соединения
C(sp2)-OH кислот сильно дезэкранирован 11-15 м.д.
α-CH протоны поглощают при 2-2.5 м.д.
В 13С-ЯМР карбоксильный углерод менее дезэкранирован и поглощает в диапазоне 160-185 м.д. CN в нитрилах 115-120 м.д.
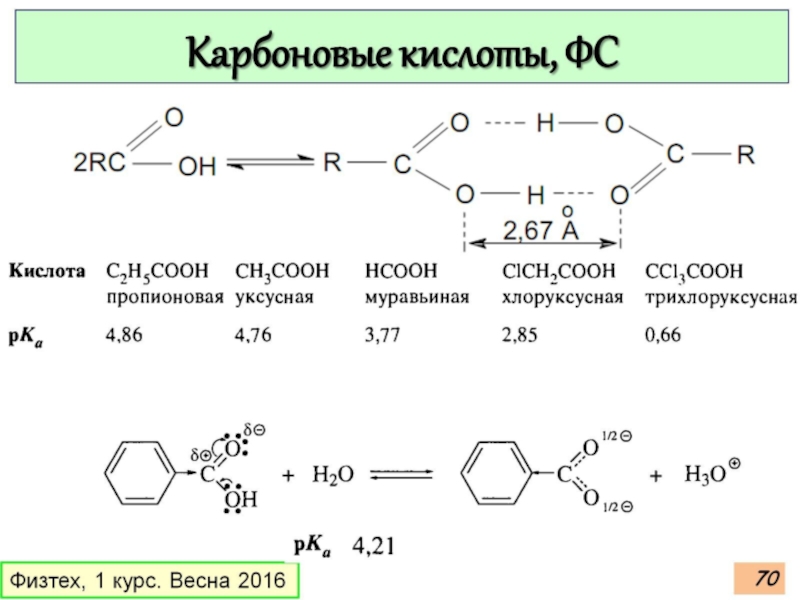
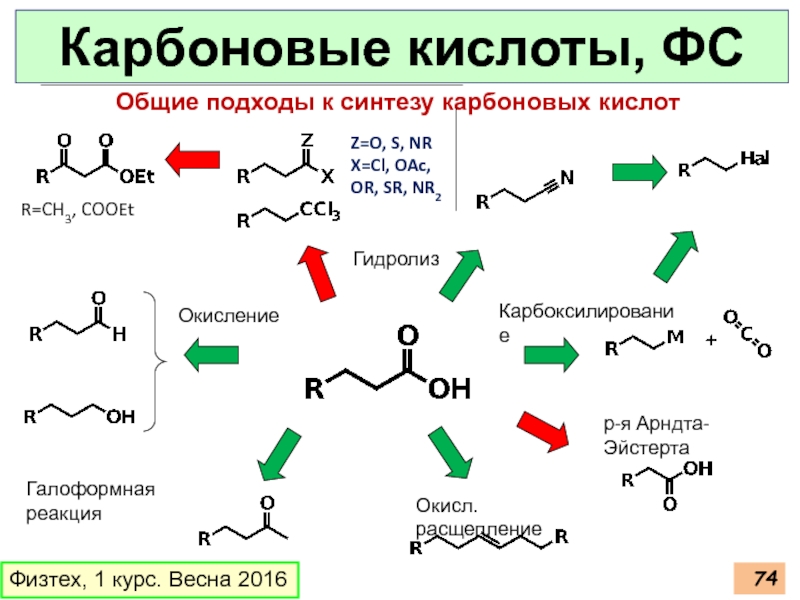
Слайд 74Карбоновые кислоты, ФС
Физтех, 1 курс. Весна 2016
Общие подходы к синтезу карбоновых
R=CH3, COOEt
Гидролиз
Карбоксилирование
Окисл. расщепление
Галоформная реакция
Окисление
р-я Арндта-Эйстерта
Z=O, S, NR
X=Cl, OAc, OR, SR, NR2
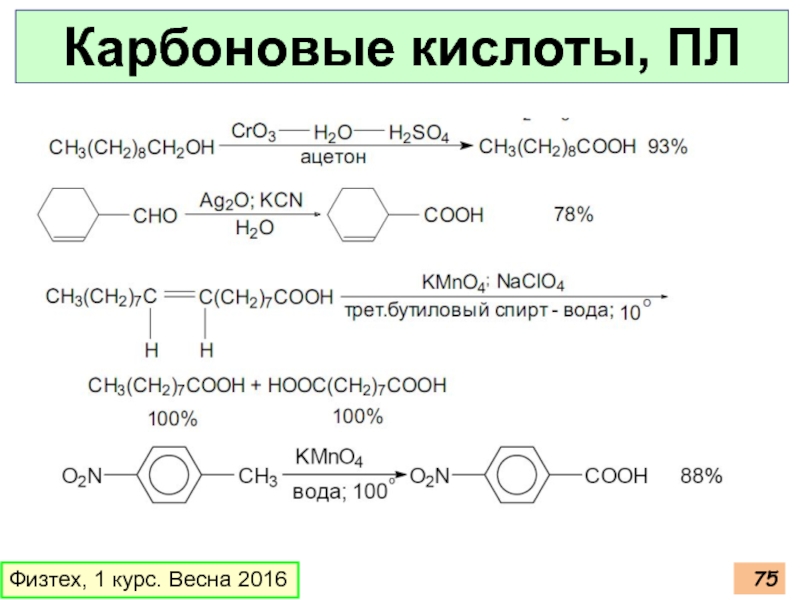
Слайд 76Карбоновые кислоты, ПЛ
Физтех, 1 курс. Весна 2016
Все производные карбоновых кислот при
среде образуют карбоновые кислоты.
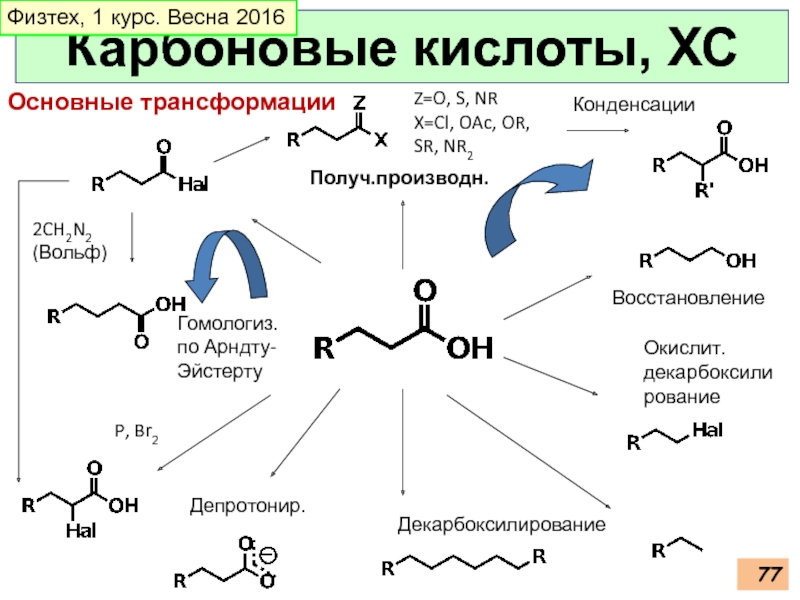
Слайд 77Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Депротонир.
Восстановление
Декарбоксилирование
P, Br2
Окислит. декарбоксилирование
Z=O, S, NR
X=Cl,
Получ.производн.
Гомологиз.
по Арндту-
Эйстерту
2CH2N2
(Вольф)
Конденсации
Основные трансформации
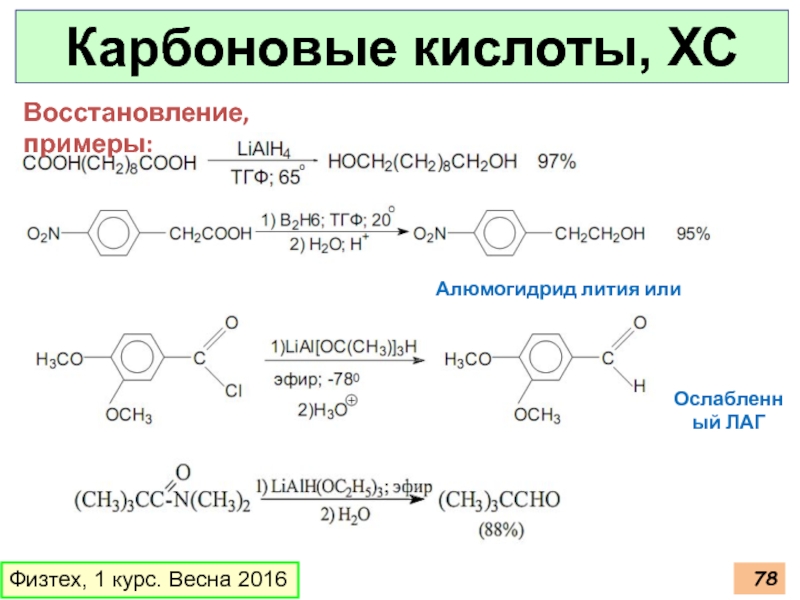
Слайд 78Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Восстановление, примеры:
Алюмогидрид лития или диборан
Ослабленный
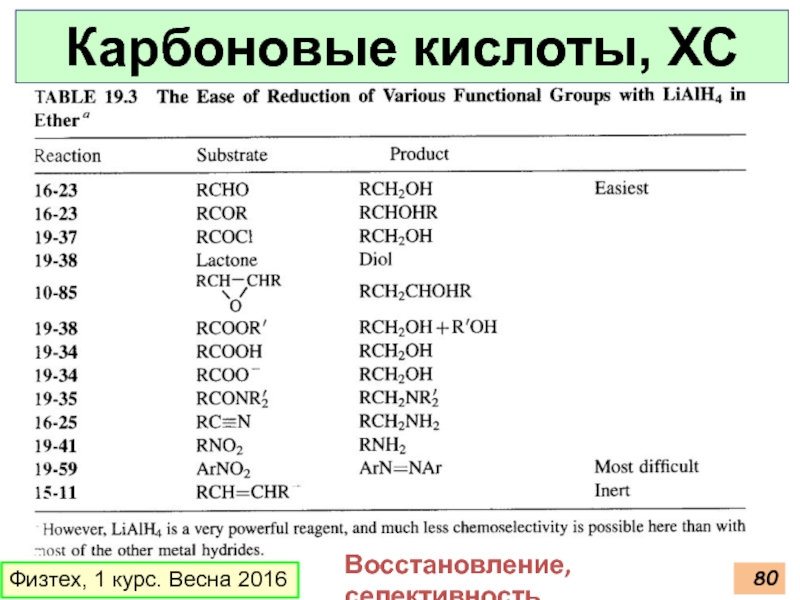
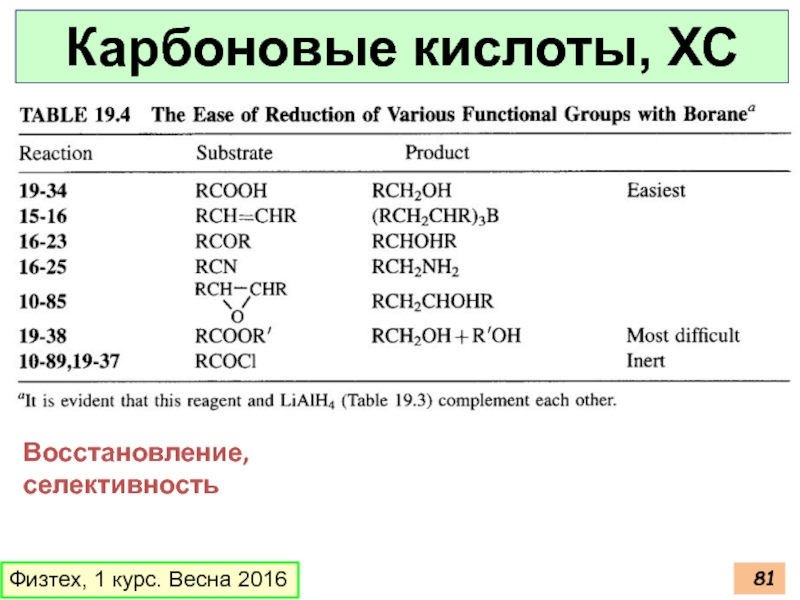
Слайд 82Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Гидрируются
в жёстких условиях
Восстановление, селективность
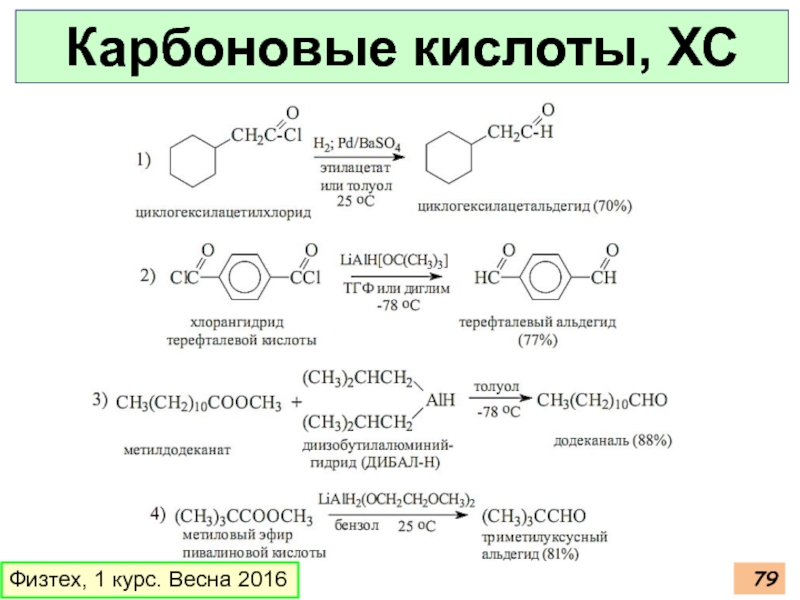
Слайд 84Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
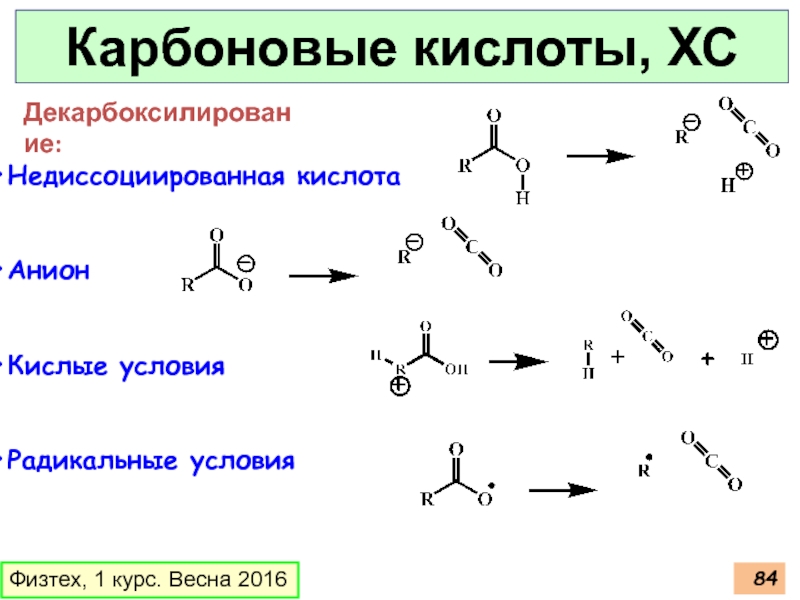
Декарбоксилирование:
Недиссоциированная кислота
Анион
Кислые условия
Радикальные условия
Слайд 86Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
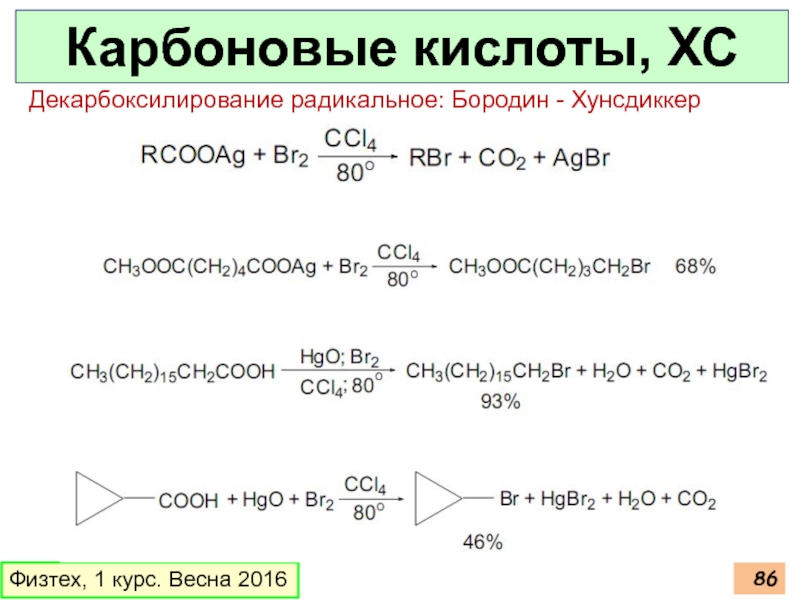
Декарбоксилирование радикальное: Бородин - Хунсдиккер
Слайд 87Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
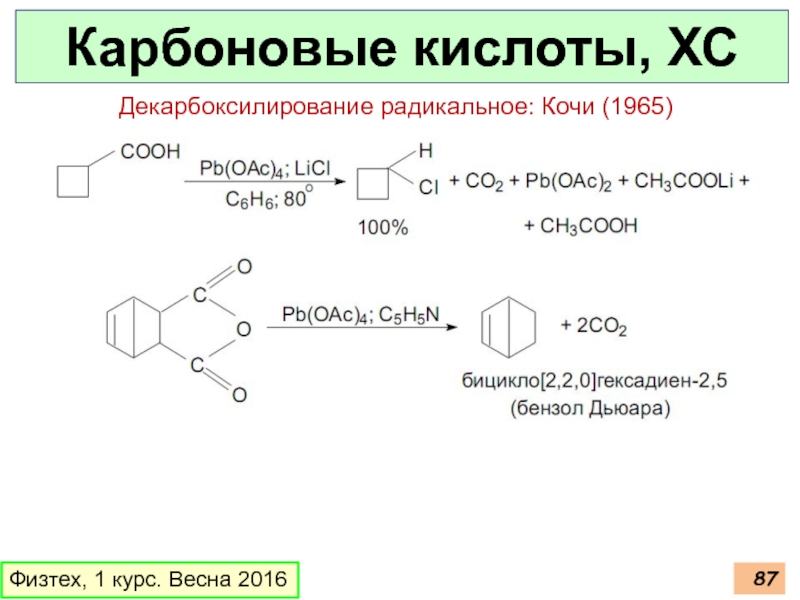
Декарбоксилирование радикальное: Кочи (1965)
Слайд 89Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Декарбоксилирование радикальное: Бородин - Хунсдиккер
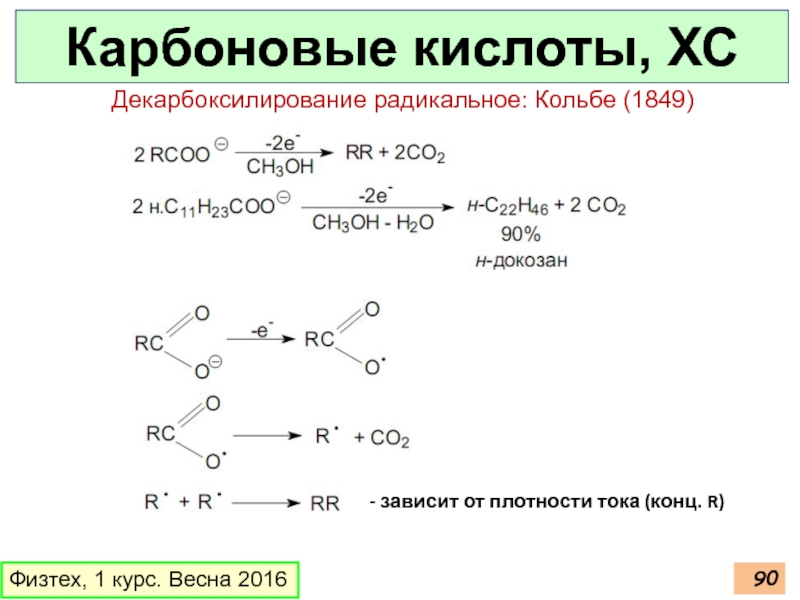
Слайд 90Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Декарбоксилирование радикальное: Кольбе (1849)
- зависит
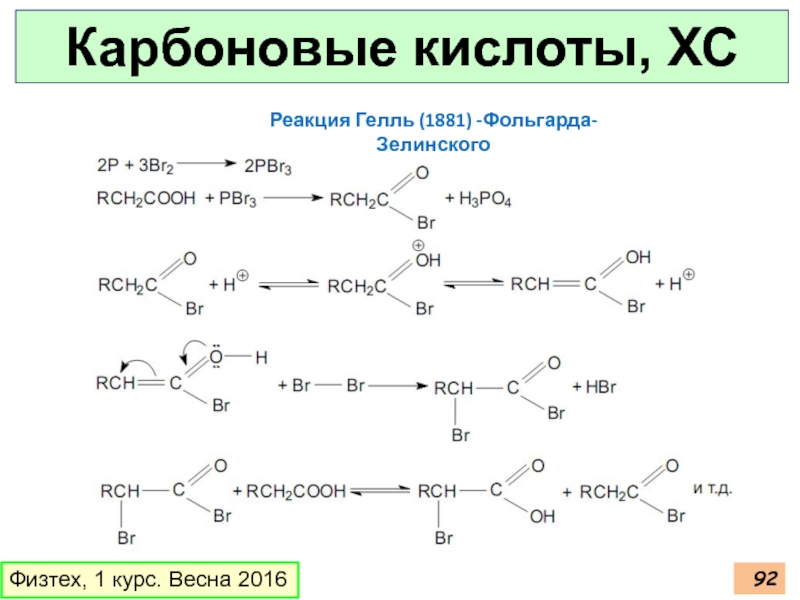
Слайд 91Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Галогенирование в альфа-положение
Реакция Гелль (1881)
Что будет при радикальном галогенировании?
Слайд 98Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Этерификация кислот, гидролиз сложных эфиров
Слайд 99Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Взаимодействие с R-M
Решение проблемы –
(Zn, Cu, Fe, Cd, Hg)
Слайд 101Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Секстетные перегруппировки
Метод удлинения углеродной
Синтез через нитрен. Перегруппировки Курциуса (Шмидта), Гофмана
Слайд 104Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
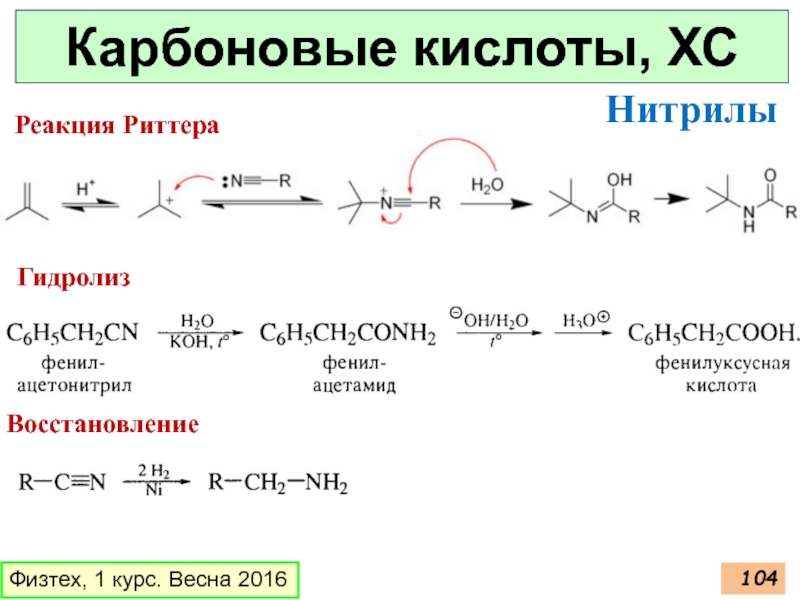
Реакция Риттера
Гидролиз
Восстановление
Нитрилы
Слайд 105Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
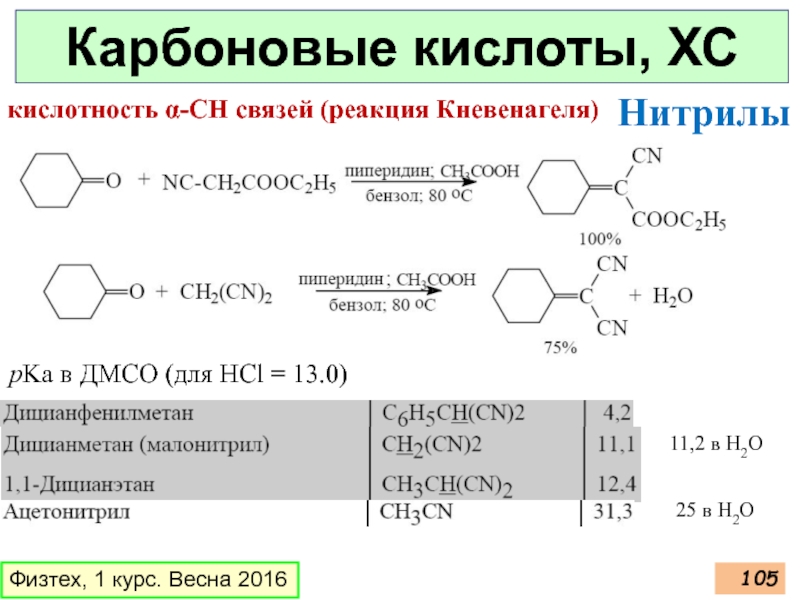
кислотность α-СН связей (реакция Кневенагеля)
Нитрилы
pKa
11,2 в Н2О
25 в Н2О
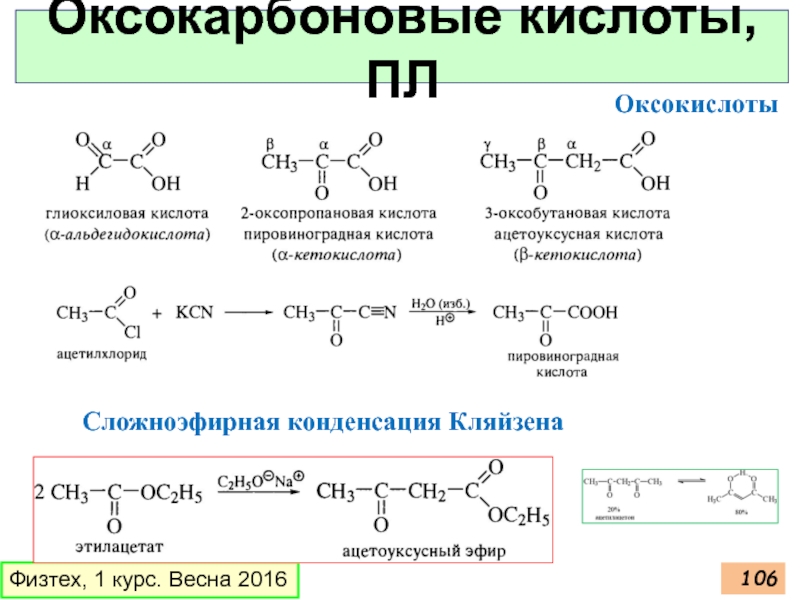
Слайд 106Оксокарбоновые кислоты, ПЛ
Физтех, 1 курс. Весна 2016
Оксокислоты
Сложноэфирная конденсация Кляйзена
Слайд 109Ди-Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Сложноэфирная конденсация Кляйзена
уходящая группа
Слайд 110Дикарбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Направленная сложноэфирная конденсация
в качестве карбонильной
Слайд 111Дикарбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Конденсация Дикмана
n = 4-5
Ацилоиновая конденсация
Слайд 112Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Ацилоиновая конденсация эфиров дикарбоновых кислот
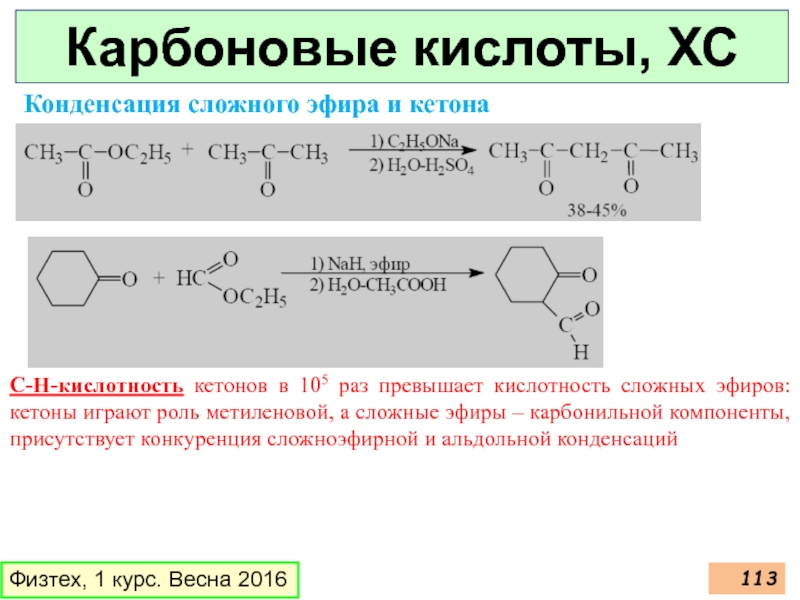
Слайд 113Карбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Конденсация сложного эфира и кетона
С-Н-кислотность
Слайд 114Оксокарбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Свойства ацетоуксусного эфира (АУЭ)
в воде
в
Слайд 120Дикарбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Синтезы с использованием малонового эфира
Слайд 121Дикарбоновые кислоты, ХС
Физтех, 1 курс. Весна 2016
Реакция Кневенагеля
Реакция Перкина
основание
енолят-ион
Слайд 122Физтех, 1 курс. Весна 2016
Дикарбоновые кислоты, ХС
Аннелирование по Робинсону – каскад
Р. Шрайнер, Х. Тодд, Синтезы органических препаратов, сб. 2, ИЛ, М., 1949, с. 220
Синтез димедона
Слайд 123Коротко о главном
Производные карбоновых кислот – максимально устойчивые окисленные формы производных
Для карбоксильной функции характерны реакции протекающие по механизмам AdN, в меньшей мере SE
Широкий спектр превращений для карбоновых составляют реакции конденсации (Кляйзена (Дикмана), Кневенагеля, Перкина и ацилоиновая конденсации)
Для нестабильных ацильных форм протекают перегруппировки в кетены и изоцианаты – предшественники кислот и аминов
Большинство производных кислот можно получить из младших представителей эфиров оксокислот – АУЭ и дикислот: щавелевой и малоновой кислот.
Физтех, 1 курс. Весна 2016
Слайд 124Основные понятия
Для реакции карбоксильной группы основной путь лежит через «тетраэдрический интермедиат».
Еще
AdN – атака внешнего нуклеофила зависит от его силы и от природы субстрата, поэтому производные КК можно превратить друг в друга
Величина pKa позволяет точно определить природу реагента в сложных конденсациях и каскадных процессах.
Физтех, 1 курс. Весна 2016