- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Электронная природа химических связей в органических соединениях. презентация
Содержание
- 1. Электронная природа химических связей в органических соединениях.
- 2. Основные положения теории строения атома: Атом
- 3. Нельзя проследить траекторию движения электрона. Область, в
- 4. Виды орбиталей (по форме): s-орбиталь р-орбиталь d-орбиталь f-орбиталь
- 5. Сначала заполняются орбитали с самой низкой энергией
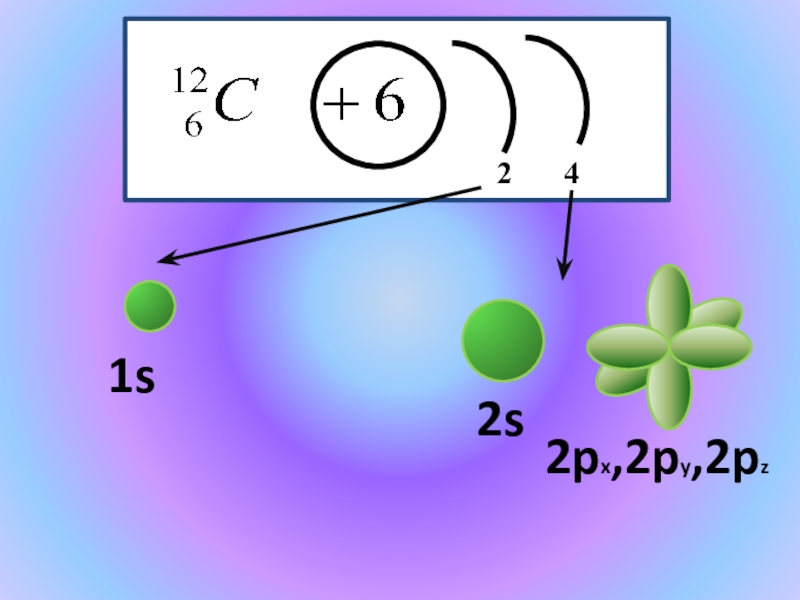
- 6. 1s 2px,2py,2pz 2s
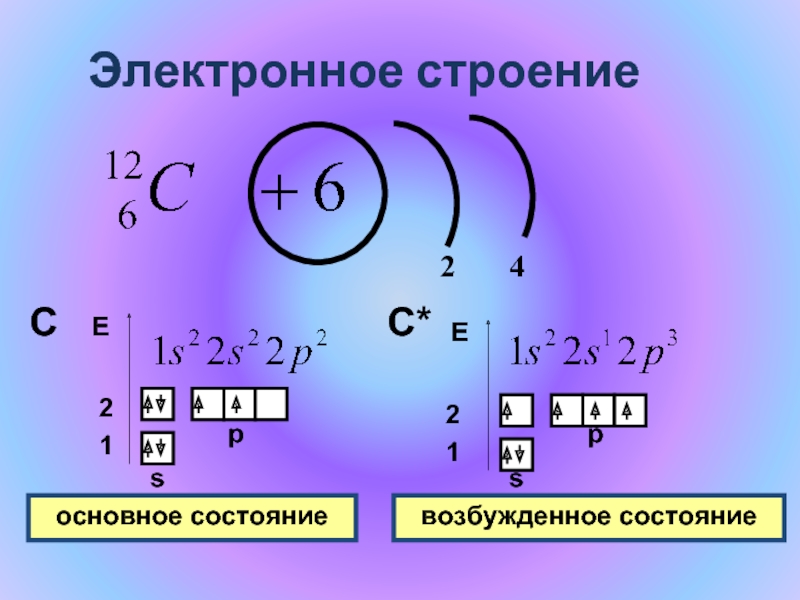
- 7. Электронное строение 2 4 1
- 8. Строение молекулы метана СН4 (метан) Изобразите электронную
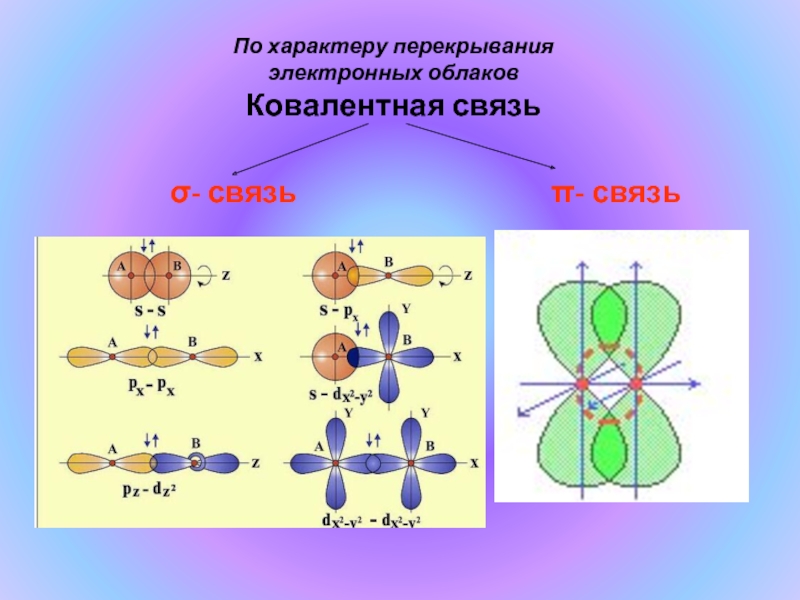
- 9. По характеру перекрывания электронных облаков Ковалентная связь σ- связь π- связь
- 10. Химические связи, образующиеся в результате перекрывания орбиталей
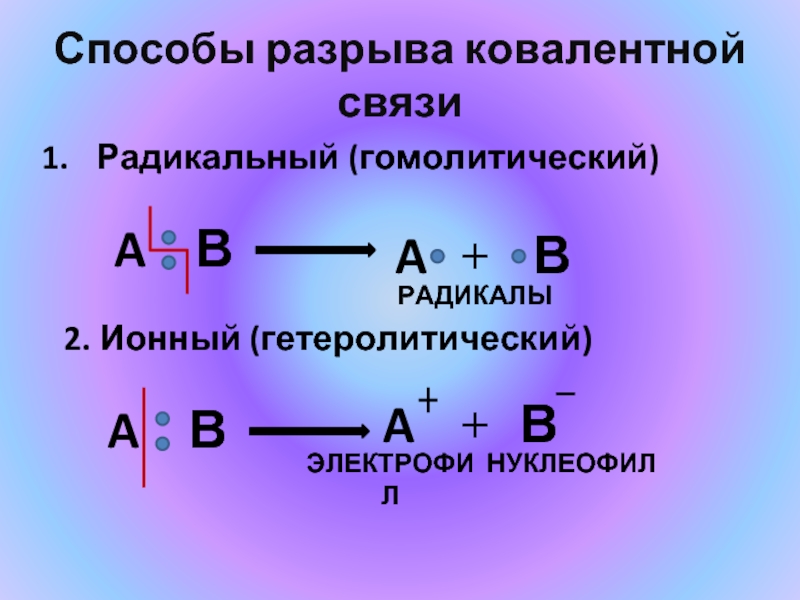
- 11. Способы разрыва ковалентной связи Радикальный (гомолитический) A
Слайд 2
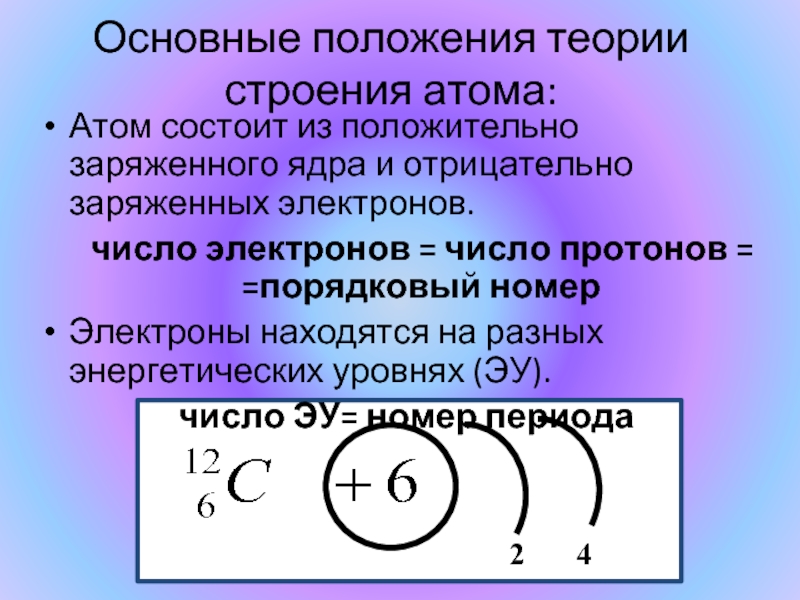
Основные положения теории строения атома:
Атом состоит из положительно заряженного ядра и
число электронов = число протонов = =порядковый номер
Электроны находятся на разных энергетических уровнях (ЭУ).
число ЭУ= номер периода
Слайд 3Нельзя проследить траекторию движения электрона. Область, в которой нахождение электрона наиболее
Орбитали различаются по форме, размерам и энергии.
На одной орбитали – не более 2-х электронов!
Основные положения теории строения атома:
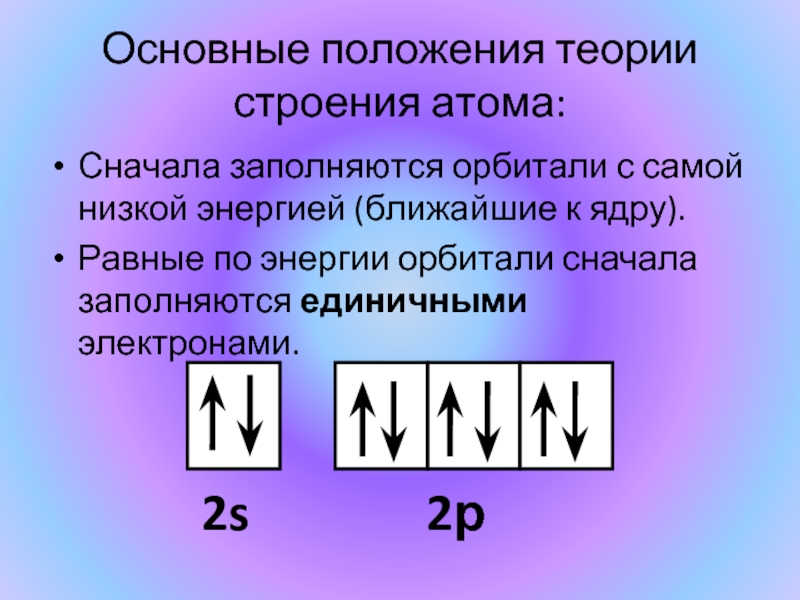
Слайд 5Сначала заполняются орбитали с самой низкой энергией (ближайшие к ядру).
Равные по
Основные положения теории строения атома:
2s
2р
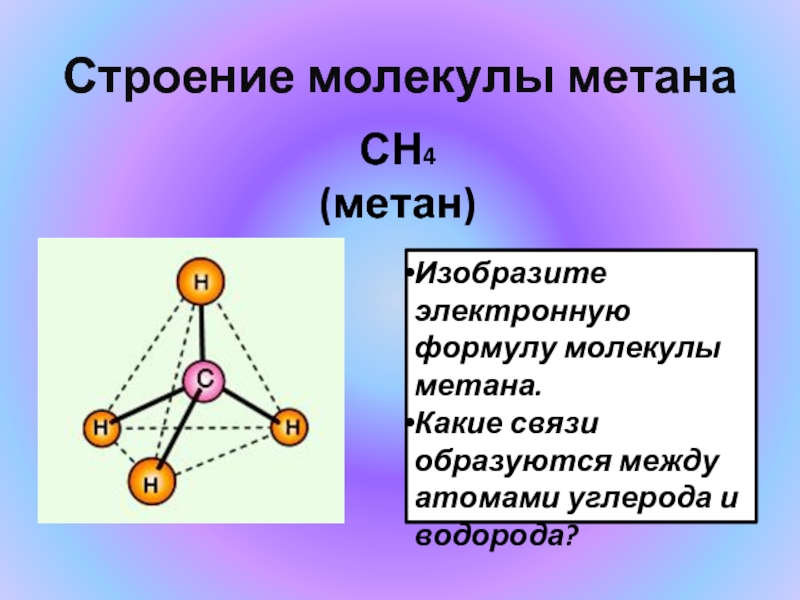
Слайд 8Строение молекулы метана
СН4 (метан)
Изобразите электронную формулу молекулы метана.
Какие связи образуются между
Слайд 10Химические связи, образующиеся в результате перекрывания орбиталей вдоль линии, соединяющей центры
Химические связи, образующиеся в результате перекрывания орбиталей в двух областях, называют π-связями.