- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Автор: учитель биологии Егоров Сергей Владимирович (Еласовская средняя общеобразовательная школа Горномарийского района республики Марий Эл). презентация
Содержание
- 1. Автор: учитель биологии Егоров Сергей Владимирович (Еласовская средняя общеобразовательная школа Горномарийского района республики Марий Эл).
- 2. биополимеры Нуклеиновые кислоты белки углеводы липиды Всё!
- 3. белки строение структура функции аминокислоты классификация белков В начало
- 4. Строение белков
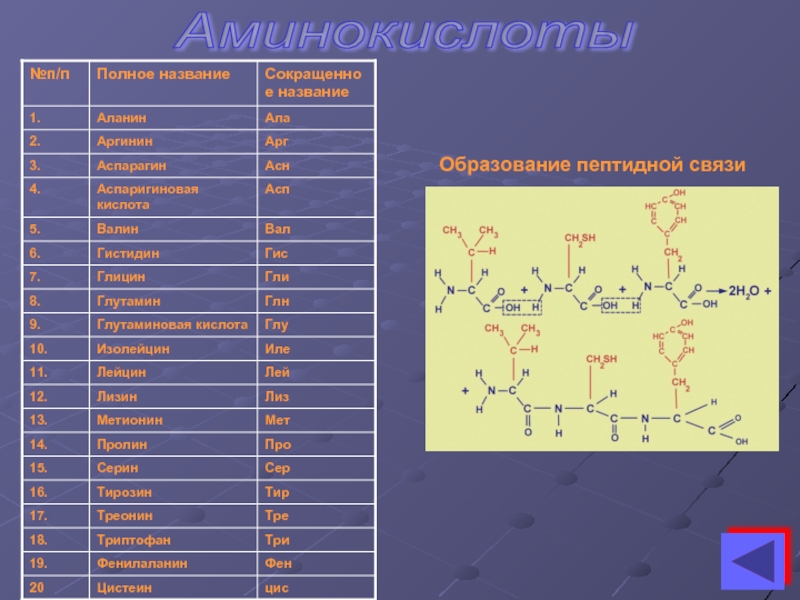
- 5. Аминокислоты Образование пептидной связи
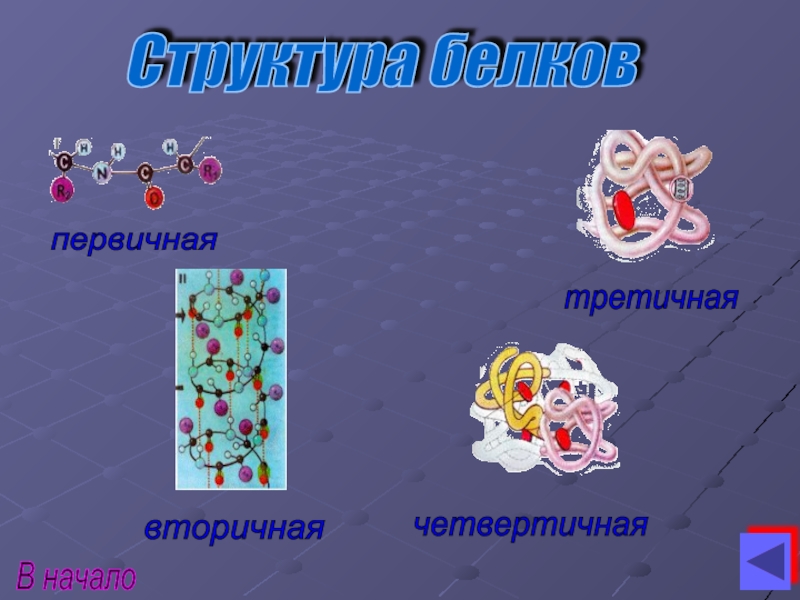
- 6. первичная вторичная третичная четвертичная Структура белков В начало
- 7. первичная стуртура белков Последовательное
- 8. вторичная стуктура белков
- 9. третичная стуктура белков
- 10. четвертичная структура белков
- 11. Функции белков
- 12. классификация белков I. По химическому составу
- 13. Нуклеиновые кислоты ДНК РНК В начало
- 14. Д Н К Структура Функции Строение
- 15. Нуклеиновые кислоты
- 16. Структура ДНК первичная вторичная третичная четвертичная
- 17. Происходит последовательное расположение нуклеотидов в
- 18. Происходит определенное пространственное
- 19. Происходит
- 20. Происходит общее пространственное расположение
- 21. Значение ДНК (как РНК)
- 22. Р Н К виды строение
- 23. Строение РНК
- 24. р – РНК (рибосомная) Виды
- 25. Т – РНК (транспортная)
- 26. и – РНК (информационная, матричная)
- 27. р – РНК (рибосомная)
- 28. углеводы виды функции В начало
- 29. Виды углеводов моносахариды дисахариды
- 30. Функции углеводов
- 31. липиды Липиды присутствуют
Слайд 1Автор: учитель биологии Егоров Сергей Владимирович (Еласовская средняя общеобразовательная школа Горномарийского
Слайд 4Строение белков
Белки – это высокомолекулярные
Слайд 7первичная стуртура белков
Последовательное расположение аминокислотных остатков в полипептидной цепи.
Первичная структура белков может быть использована для систематической номенклатуры белков.
Слайд 8вторичная стуктура белков
Происходит пространственное расположение полипептидной цепи.
Слайд 9третичная стуктура белков
Происходит общее пространственное расположение
Слайд 10четвертичная структура белков
Четвертичную структуру имеют только
Слайд 11Функции белков
1) Пластическая (строительная) функция. Белки
Слайд 12классификация белков
I. По химическому составу выделяют белки:
1) Простые (протеины), состоящие только
II. По растворимости в различных растворителях:
1) Альбумины – растворяются в насыщенных растворах минеральных солей;
2) глобулины - растворяются в полунасыщенных растворах минеральных солей;
3) проламины – растворяются в 60%-80% этаноле;
4) глютаимины – растворяются в щелочных растворах и др.
III. По характеру добавочных групп:
1) Металлопротеиды
2) Неметаллопротеиды.
Слайд 15 Нуклеиновые кислоты – высокомолекулярные соединения, характеризующиеся
Строение ДНК
Слайд 17 Происходит последовательное расположение нуклеотидов в полинуклеотидной цепи.
Первичная структура ДНК
(Ген – участок молекулы ДНК, содержащий информацию о первичной структуре одного определенного белка.)
Слайд 18 Происходит определенное пространственное расположение полинуклеотидной цепи.
Вторичная структура Д Н К
Выделяют несколько форм вторичной структуры ДНК:
1) В – форма. Расположение АГЦО перпендикулярно к оси молекулы.
В шаг спирали входят 16 пар нуклеотидов. Эта форма более стабильная.
2) А – форма. Расположение АГЦО происходит под углом 70 градусов
к оси. В шаг спирали входят 11 пар нуклеотидов. Эта форма образуется
в ходе репликации и транскрипции.
3) Z – форма. Характеризуется левой закруткой спирали. В шаг спирали
входит 12 пар нуклеотидов.
Слайд 19
Происходит общее пространственное расположение молекулы ДНК.
Третичная структура Д Н К
В результате всей упаковки молекула ДНК уменьшается в 100 000 раз.
Слайд 20 Происходит общее пространственное расположение отдельных молекул ДНК в
Четвертичная структура Д Н К
Слайд 21 Значение ДНК (как РНК) в клетке очень велико.
Функции Д Н К
Слайд 23Строение РНК
РНК, как и ДНК представляет собой
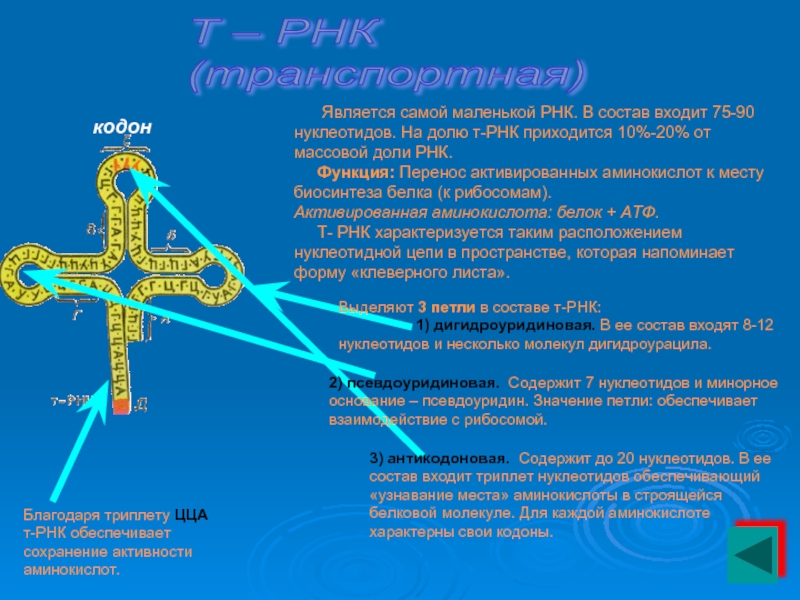
Слайд 25Т – РНК
(транспортная)
Является самой маленькой РНК.
кодон
Выделяют 3 петли в составе т-РНК:
1) дигидроуридиновая. В ее состав входят 8-12 нуклеотидов и несколько молекул дигидроурацила.
2) псевдоуридиновая. Содержит 7 нуклеотидов и минорное основание – псевдоуридин. Значение петли: обеспечивает взаимодействие с рибосомой.
3) антикодоновая. Содержит до 20 нуклеотидов. В ее состав входит триплет нуклеотидов обеспечивающий «узнавание места» аминокислоты в строящейся белковой молекуле. Для каждой аминокислоте характерны свои кодоны.
Благодаря триплету ЦЦА
т-РНК обеспечивает сохранение активности аминокислот.
Слайд 26и – РНК
(информационная, матричная)
И - РНК
Слайд 27р – РНК
(рибосомная)
Являются основным структурным компонентом
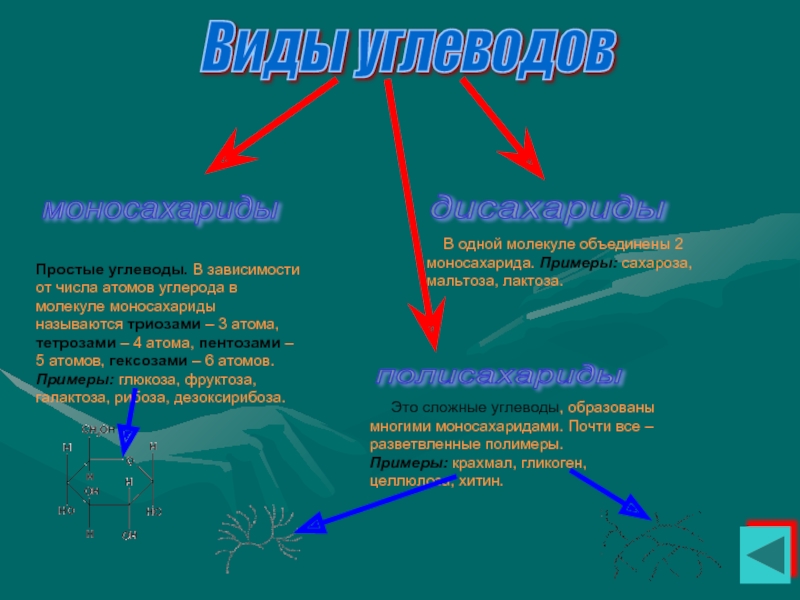
Слайд 29Виды углеводов
моносахариды
дисахариды
полисахариды
Простые углеводы. В зависимости от числа
В одной молекуле объединены 2 моносахарида. Примеры: сахароза, мальтоза, лактоза.
Это сложные углеводы, образованы многими моносахаридами. Почти все – разветвленные полимеры.
Примеры: крахмал, гликоген, целлюлоза, хитин.
Слайд 30Функции углеводов
1) Основная функция – энергетическая.
Слайд 31липиды
Липиды присутствуют во всех без исключения клетках,
В начало