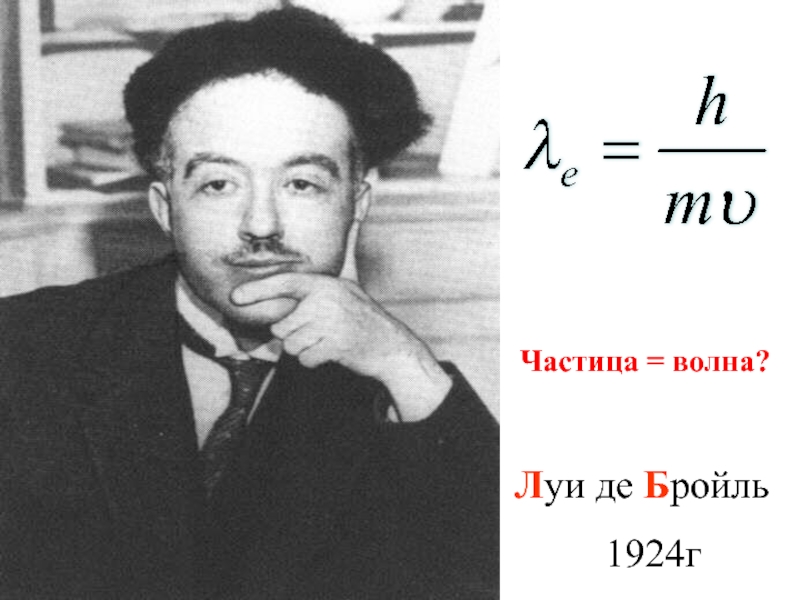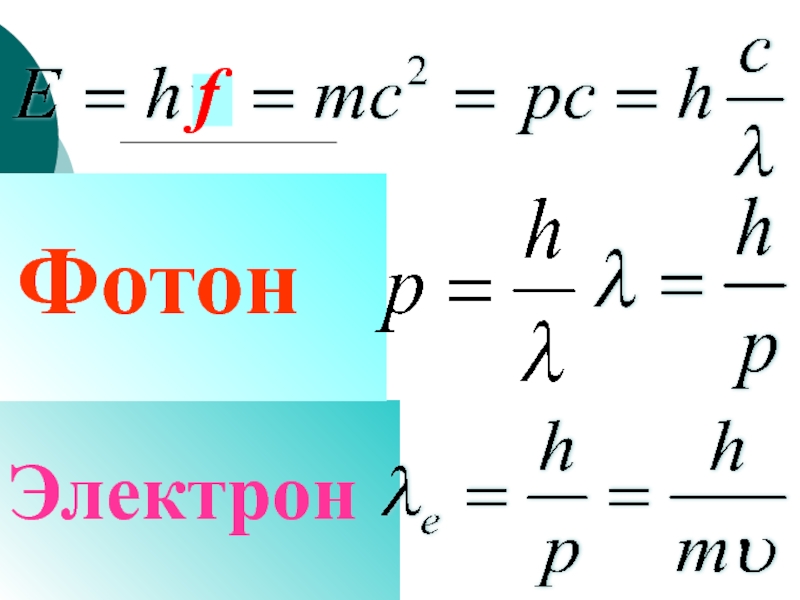- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Атом. Молекула. Кристалл. презентация
Содержание
- 1. Атом. Молекула. Кристалл.
- 2. Микро и макро Микромир Макромир
- 3. Модель атома Томсона Джосеф Джон Томсон 19 век
- 4. Опыт Резерфорда Вывод: планетарная модель атома !!!
- 5. Электрон может двигаться по произвольной орбите
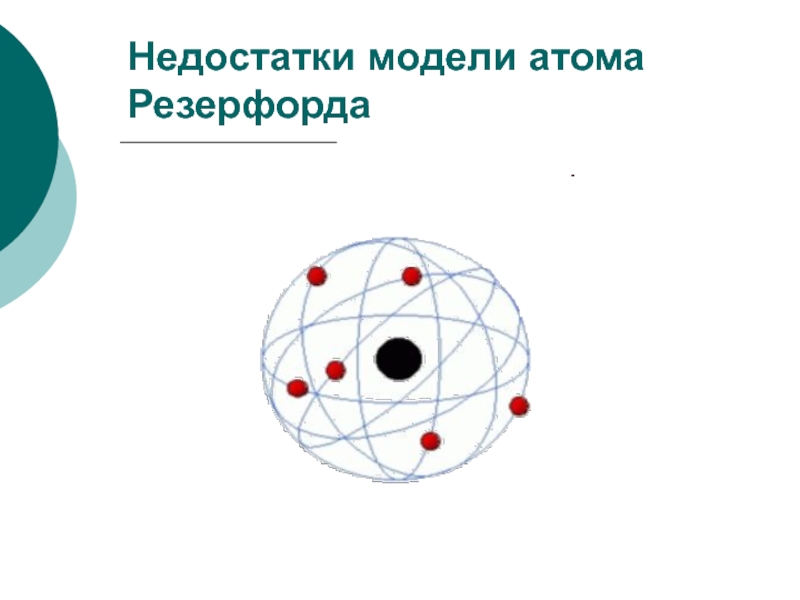
- 6. Недостатки модели атома Резерфорда
- 7. Время жизни атома 10 с -9
- 8. В мире микрочастиц, в мире атомов действуют
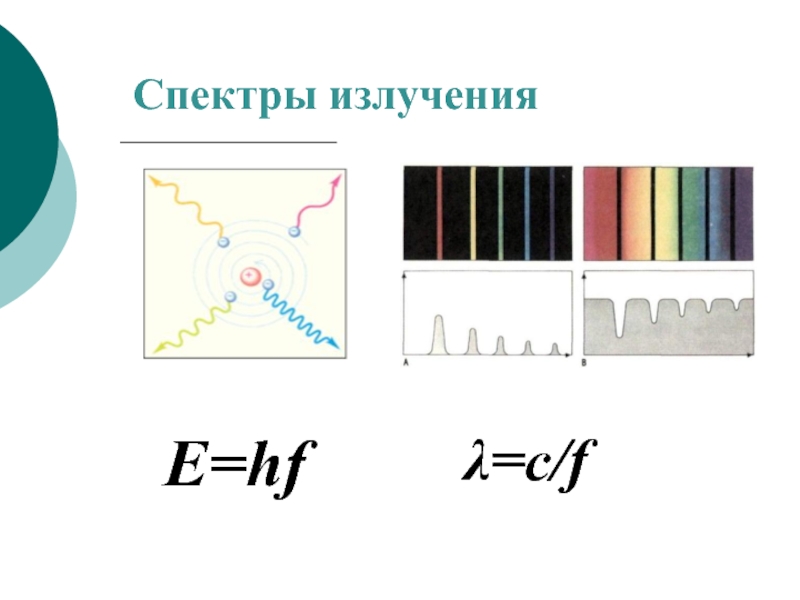
- 9. Спектры излучения E=hf λ=c/f
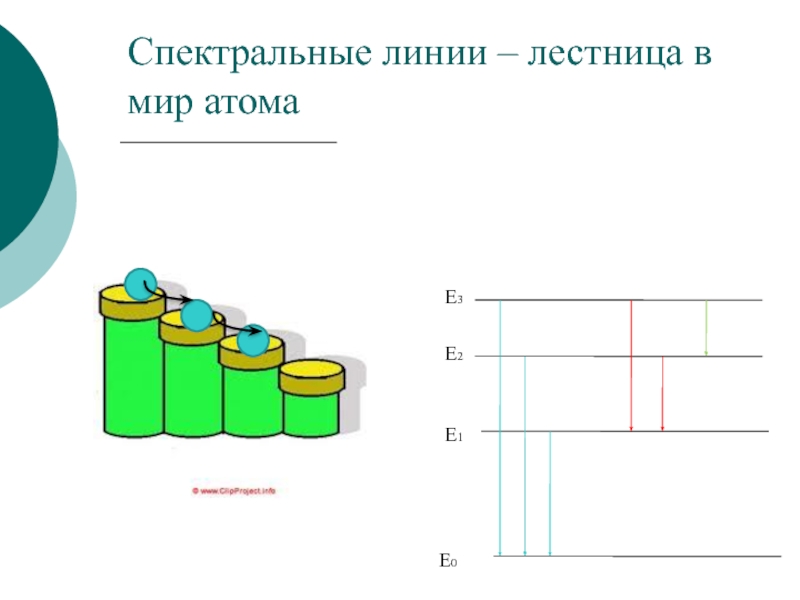
- 10. Cпектральные линии – лестница в мир атома E0 E1 E3 E2
- 11. Нильс Бор 1885 – 1962 г.г.
- 12. Первый постулат Бора (постулат стационарных состояний)
- 13. Второй постулат Бора (правило частот)
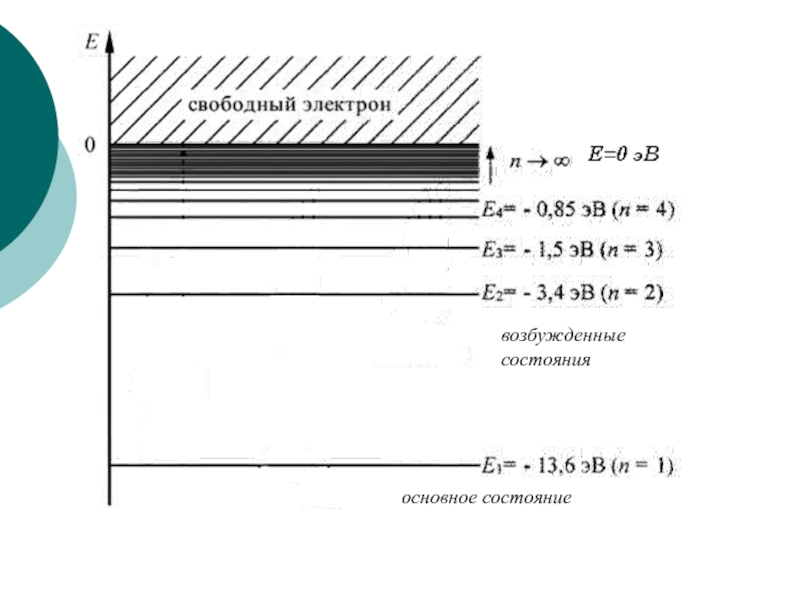
- 14. основное состояние возбужденные состояния
- 15. Спектральный анализ и теория Бора R= 1,0974*107 м-1 Постоянная Ридберга Формула Бальмера
- 16. Трудности теории Бора В теории Бора сохранились
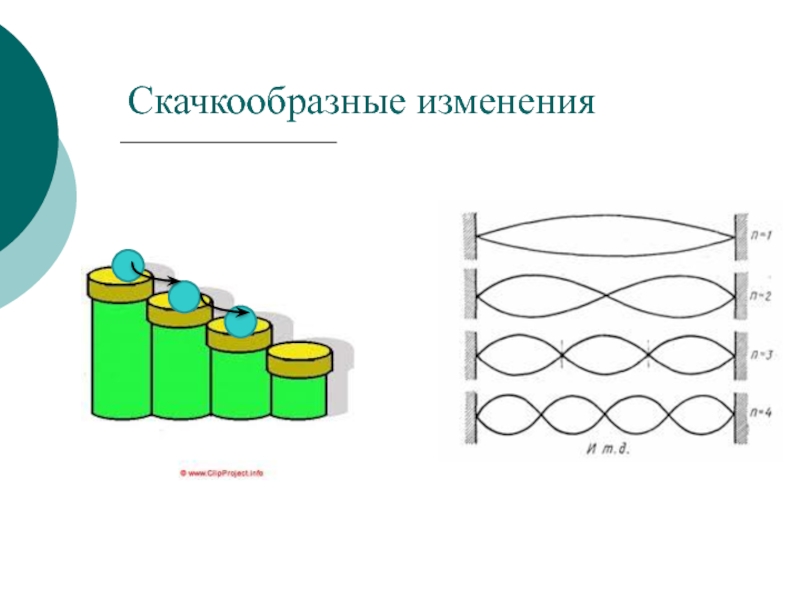
- 17. Скачкообразные изменения
- 18. Луи де Бройль 1924г Частица = волна?
- 19. Электронные волны 1927 год
- 20. Электроннвые влны – волны вероятности Макс Борн
- 21. Электрон Фотон f
- 22. Стр.26 задачи
- 23. В стационарном квантовом состоянии атома водорода на
- 24. Экспериментальное подтверждение гипотезы де Бройля. 1927 г. - американские
- 25. Дифракция электронов Картина дифракции электронов на поликристаллическом
- 26. Волны вероятности Подлетая к экрану со щелями,
- 27. Опыты Фабриканта, Бибермана, Сушкина Опыт Дж. Томсона был
- 28. Волновые свойства макроскопических тел. Впоследствии дифракционные явления
- 29. Квантовая механика Гипотеза де Бройля основывалась на соображениях
- 30. ДОМА: Стр.26-27 задачи
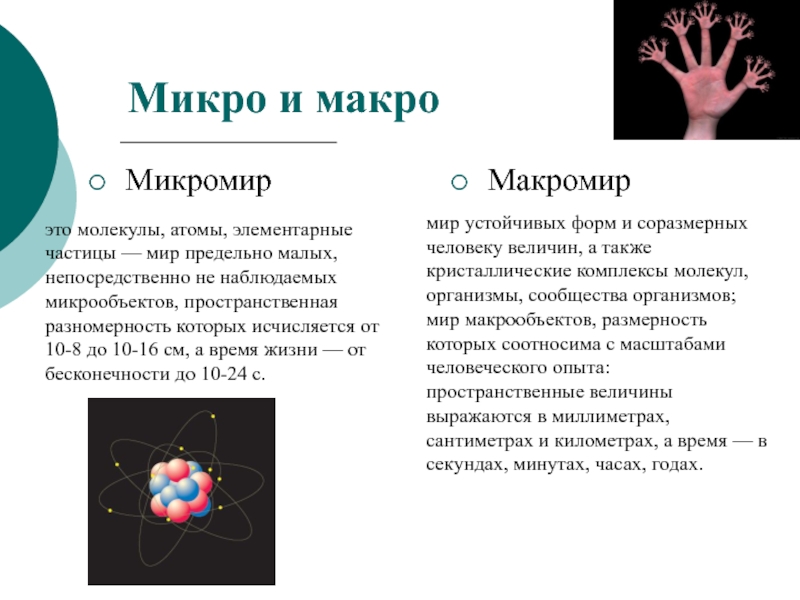
Слайд 2Микро и макро
Микромир
Макромир
это молекулы, атомы, элементарные частицы — мир
мир устойчивых форм и соразмерных человеку величин, а также кристаллические комплексы молекул, организмы, сообщества организмов; мир макрообъектов, размерность которых соотносима с масштабами человеческого опыта: пространственные величины выражаются в миллиметрах, сантиметрах и километрах, а время — в секундах, минутах, часах, годах.
Слайд 8В мире микрочастиц, в мире атомов действуют какие-то новые закономерности, которые
Слайд 16Трудности теории Бора
В теории Бора сохранились представления об орбитальном движении электронов
Классическая ядерная модель атома Резерфорда была дополнена в теории Бора идеей о квантовании электронных орбит.
Поэтому теорию Бора иногда называют полуклассической.
Слайд 20Электроннвые влны – волны вероятности
Макс Борн
Волновая функция ψ(x,y,z,t)
ψ² - вероятность нахождения
Слайд 23В стационарном квантовом состоянии атома водорода на длине орбиты должно укладываться
nλn = 2πrn.
Объяснение правила квантования
Иллюстрация идеи де Бройля о возникновении стоячих волн на стационарной орбите для случая n = 4.
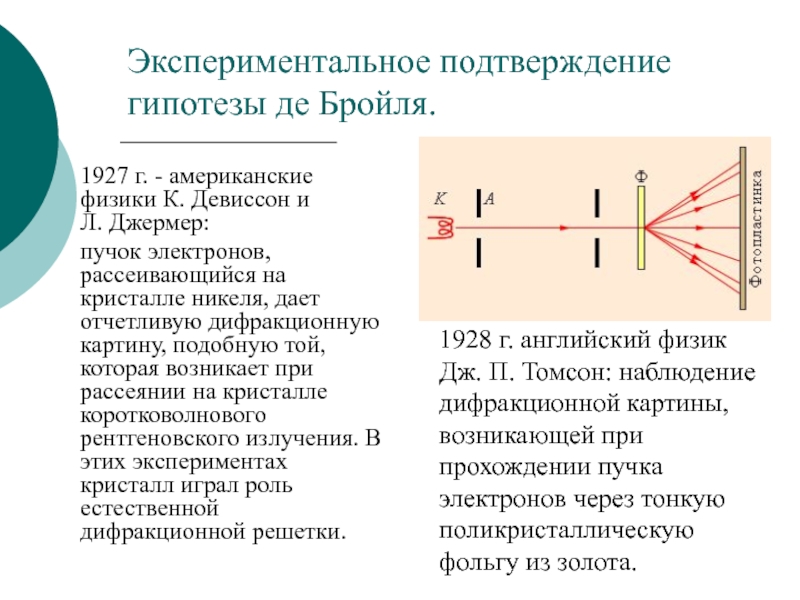
Слайд 24Экспериментальное подтверждение гипотезы де Бройля.
1927 г. - американские физики К. Девиссон и Л. Джермер:
пучок
1928 г. английский физик Дж. П. Томсон: наблюдение дифракционной картины, возникающей при прохождении пучка электронов через тонкую поликристаллическую фольгу из золота.
Слайд 25Дифракция электронов
Картина дифракции электронов на поликристаллическом образце при длительной экспозиции (a) и
Слайд 26Волны вероятности
Подлетая к экрану со щелями, частицы взаимодействуют с ним как
Поведение частиц в пространстве между экраном со щелями и фотопластинкой описывается в квантовой физике с помощью Ψ(x,y,z,t)-функций.
Квадрат модуля пси-функции определяет вероятность обнаружения частицы в том или ином месте. Таким образом, попадание частиц в различные точки фотопластинки есть вероятностный процесс.
Волны вероятности – электрнные волны.
Слайд 27Опыты Фабриканта, Бибермана, Сушкина
Опыт Дж. Томсона был многократно повторен с неизменным результатом,
Слайд 28Волновые свойства макроскопических тел.
Впоследствии дифракционные явления были обнаружены также для нейтронов,
Экспериментальное доказательство наличия волновых свойств микрочастиц привело к выводу о том, что это универсальное явление природы, общее свойство материи.
Следовательно, волновые свойства должны быть присущи и макроскопическим телам. Однако вследствие большой массы макроскопических тел их волновые свойства не могут быть обнаружены экспериментально.
Например, пылинке массой 10–9 г, движущийся со скоростью 0,5 м/с соответствует волна де Бройля с длиной волны порядка 10-21 м, т. е. приблизительно на 11 порядков меньше размеров атомов. Такая длина волны лежит за пределами доступной наблюдению области.