- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
9 кл. Алкины, Ацетиленовые углеводороды презентация
Содержание
- 1. 9 кл. Алкины, Ацетиленовые углеводороды
- 2. 1. Определение Алкины – непредельные углеводороды, молекулы которых содержат одну тройную связь. CH≡CH CH3-C≡CH
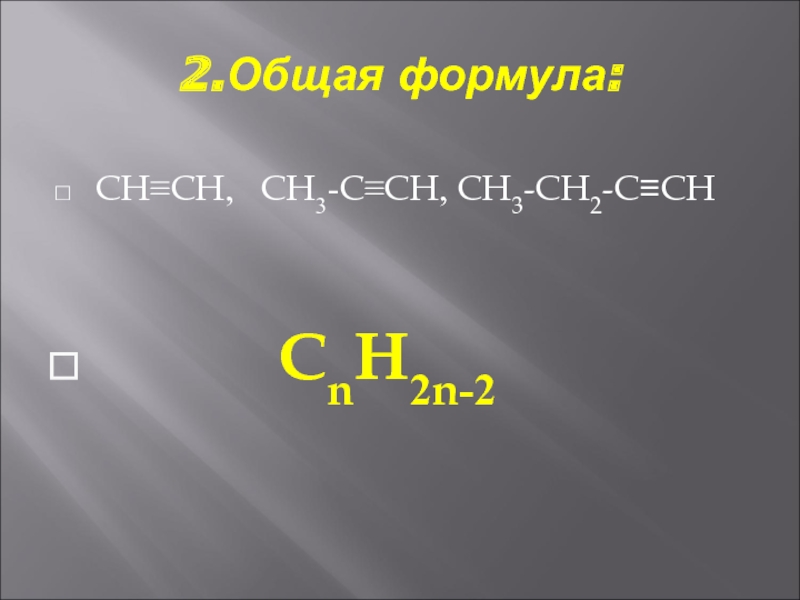
- 3. 2.Общая формула: CH≡CH, CH3-C≡CH, CH3-CH2-C≡CH
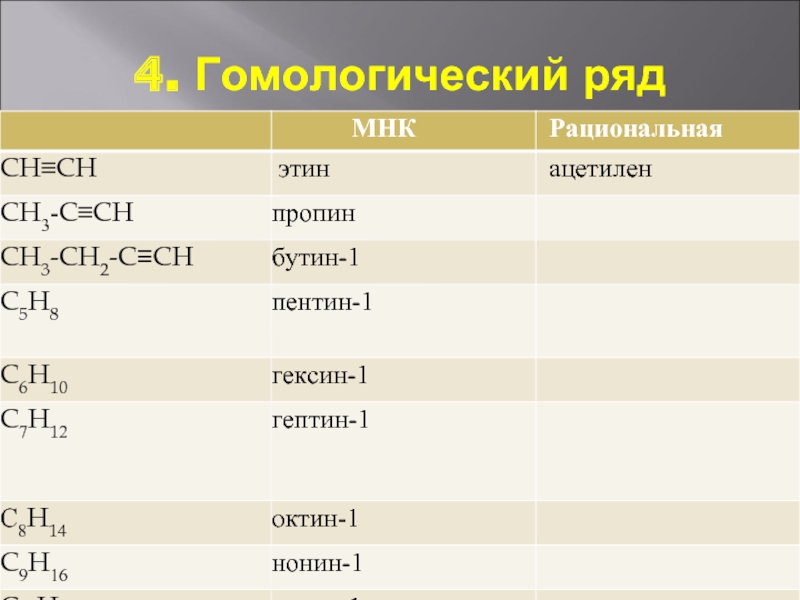
- 4. 4. Гомологический ряд
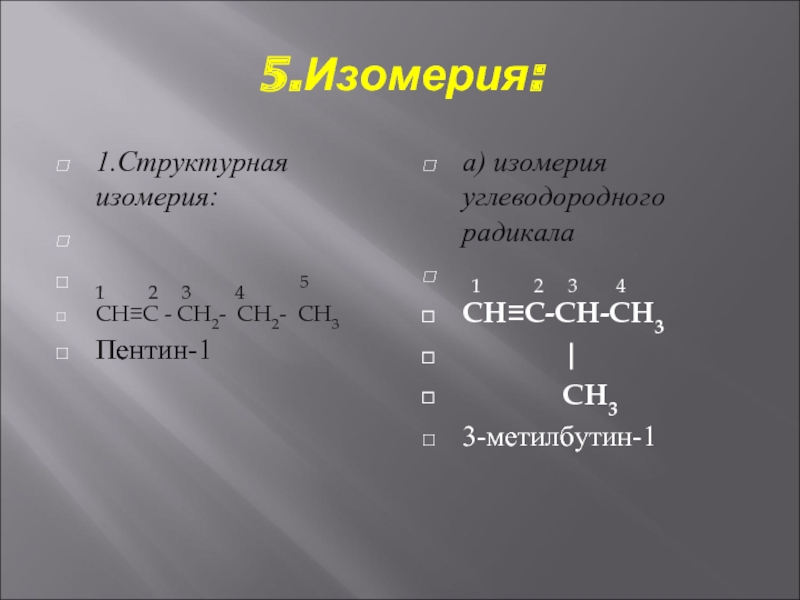
- 5. 5.Изомерия: 1.Структурная изомерия: 1
- 6. б) изомерия положения тройной связи 1
- 7. 6.Номенклатура 1
- 8. 7.Физические свойства : Температуры плавления кипения увеличиваются
- 9. 8.Способы получения: 1.Дегидрогалогенирования
- 10. 9.Химические свойства: Характерные реакции- присоединения, окисления,
- 11. А.Реакции присоединения 1. Галогенирования
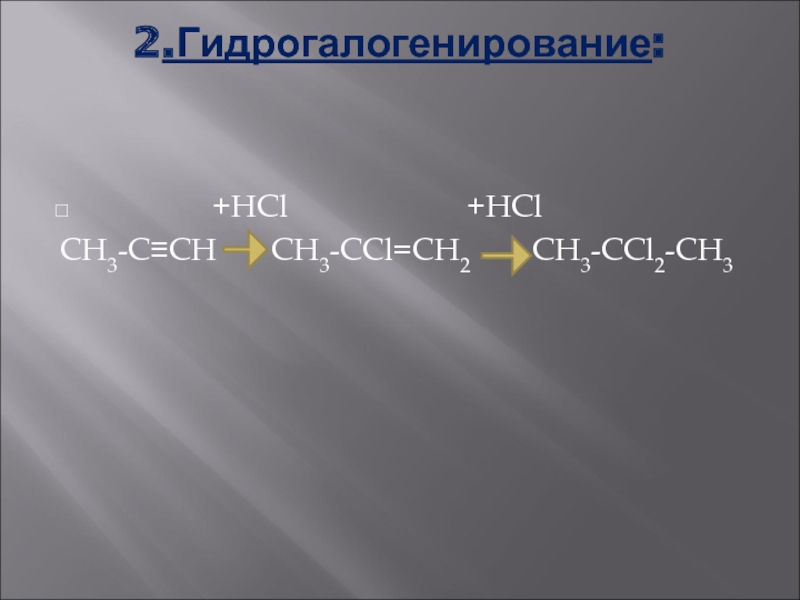
- 12. 2.Гидрогалогенирование:
- 13. 3.Гидротация (реакция Кучерова) протекает в две стадии.
- 14. 4.Гидрогенизации или гидрирования: ( катализатор-Ni)
- 15. Реакции окисления 5) мягкое окисление Обесцвечивается
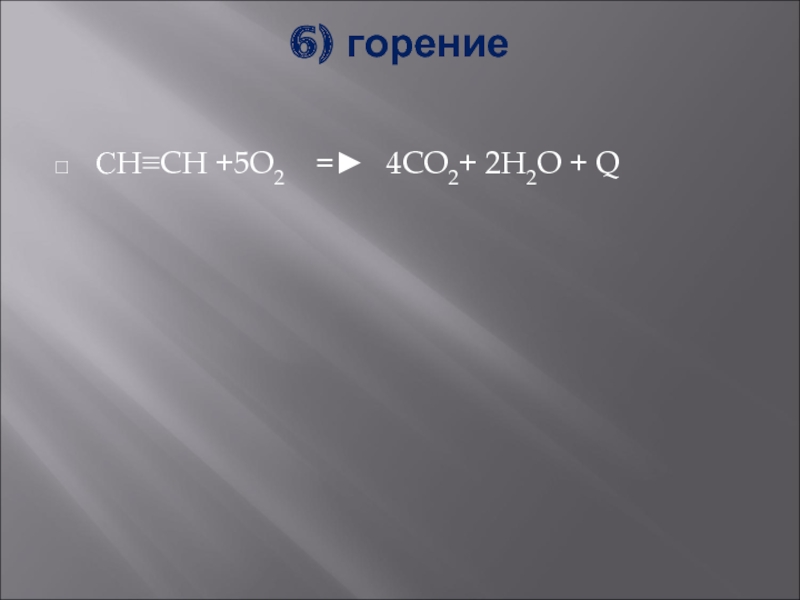
- 16. 6) горение СH≡CH +5O2 =► 4CO2+ 2H2O + Q
- 17. 10. Отдельные представители Этин или ацетилен CH≡CH простейший алкин
- 18. а) физические свойства - бесцветный газ без
- 19. б) получение : 1.термический крекинг метана
- 20. в) химические свойства ацетилена
- 21. г)применение: Ацетилен в больших количествах применяется
- 22. Д/З $34упр.3, 5,6
Слайд 21. Определение
Алкины – непредельные углеводороды, молекулы которых содержат одну тройную связь.
CH≡CH
CH3-C≡CH
Слайд 55.Изомерия:
1.Структурная изомерия:
1 2
3 4 5
CH≡C - CH2- CH2- CH3
Пентин-1
CH≡C - CH2- CH2- CH3
Пентин-1
а) изомерия углеводородного радикала
1 2 3 4
CH≡C-CH-CH3
|
CH3
3-метилбутин-1
Слайд 76.Номенклатура
1 2
3 4 5 6 7 8
CH3- C≡C- CH - CH – CH2 -CH2-CH3
| |
CH2 CH3
|
CH3
5-метил-4-этилоктин -2
CH3- C≡C- CH - CH – CH2 -CH2-CH3
| |
CH2 CH3
|
CH3
5-метил-4-этилоктин -2
Слайд 87.Физические свойства :
Температуры плавления кипения увеличиваются с ростом молекулярной массы.
При обычных
условиях
C2H2 - C4H6 –газы,
C5H 8 - C16H30 -жидкости,
начиная с C18H34-твердые вещества.
Температуры кипения алкинов выше, чем у соответствующих алкенов и алканов.
C2H2 - C4H6 –газы,
C5H 8 - C16H30 -жидкости,
начиная с C18H34-твердые вещества.
Температуры кипения алкинов выше, чем у соответствующих алкенов и алканов.
Слайд 98.Способы получения:
1.Дегидрогалогенирования
Br
| спирт
а) CH3-CH2- C-CH3 + 2KOH = CH3-CH2 -C≡CH + 2KBr +2H2O
|
Br
спирт
б) CH3-CH-CH-CH3 + 2KOH = CH3-C≡C-CH3+ 2KBr + 2H2O
| |
Br Br
Слайд 109.Химические свойства:
Характерные реакции- присоединения, окисления, полимеризации.
Реакции присоединения протекают медленнее, чем у
алкенов. Продукты определяются правилом Марковникова.
Слайд 11А.Реакции присоединения
1. Галогенирования
+Br2
+Br2
CH≡CH CHBr=CHBr CHBr2-CHBr2
Этин 1,2-дибромэтен 1,1,2,2-тетрабромэтан
Алкины обесцвечивают бромную воду- это качественная реакция на алкины и алкены.
CH≡CH CHBr=CHBr CHBr2-CHBr2
Этин 1,2-дибромэтен 1,1,2,2-тетрабромэтан
Алкины обесцвечивают бромную воду- это качественная реакция на алкины и алкены.
Слайд 133.Гидротация (реакция Кучерова) протекает в две стадии.
Hg2+,H+
СH≡CH +H2O =► CH2=CH =► CH3-C-H
| \\
OH O
уксусный альдегид
(этаналь)
На первой стадии образуется неустойчивый непредельный спирт, который затем изомеризуется в альдегид.
СH≡CH +H2O =► CH2=CH =► CH3-C-H
| \\
OH O
уксусный альдегид
(этаналь)
На первой стадии образуется неустойчивый непредельный спирт, который затем изомеризуется в альдегид.
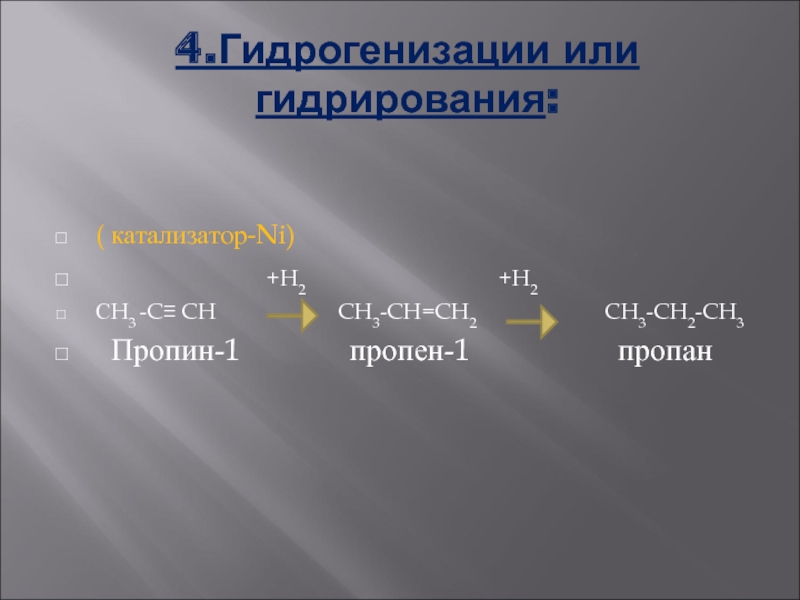
Слайд 144.Гидрогенизации или
гидрирования:
( катализатор-Ni)
+H2 +H2
СH3 -C≡ CH CH3-CH=CH2 CH3-CH2-CH3
Пропин-1 пропен-1 пропан
СH3 -C≡ CH CH3-CH=CH2 CH3-CH2-CH3
Пропин-1 пропен-1 пропан
Слайд 15Реакции окисления
5) мягкое окисление
Обесцвечивается раствор марганцовки, это качественная реакция на
алкины.
KMnO4
CH≡CH + [O]+H2O =► O=C-C=O
/ \
HO OH
щавеливая кислота
Обесцвечивается раствор марганцовки, это качественная реакция на алкины.
KMnO4
CH≡CH + [O]+H2O =► O=C-C=O
/ \
HO OH
щавеливая кислота
Обесцвечивается раствор марганцовки, это качественная реакция на алкины.
Слайд 18а) физические свойства
- бесцветный газ без запаха, мало растворим в воде,
горит ярким,
сильно коптящим пламенем ,tкип=-83,60С, Смеси с воздухом взрывоопасны. Ацетилен обладает наркотическими свойствами.
сильно коптящим пламенем ,tкип=-83,60С, Смеси с воздухом взрывоопасны. Ацетилен обладает наркотическими свойствами.
Слайд 19б) получение :
1.термический крекинг метана
15000C
2CH4 => C2H2+3H2
2.гидролиз карбида кальция
CaC2+ H2O => Ca(OH)2 +C2H2
2CH4 => C2H2+3H2
2.гидролиз карбида кальция
CaC2+ H2O => Ca(OH)2 +C2H2
Слайд 20
в) химические свойства ацетилена
1. тримеризация ( реакция Зелинского)
Cакт,6000C
3СН≡СH => C6H6
ацетилен бензол
3СН≡СH => C6H6
ацетилен бензол
Слайд 21г)применение:
Ацетилен в больших количествах применяется для автогенной сварки и резки
металлов,
т.к. температура пламени -31500С. Применяется этин очень широко при органическом синтезе.
т.к. температура пламени -31500С. Применяется этин очень широко при органическом синтезе.