- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Средства, применяемые при нейродегенеративных заболеваниях. Противопаркинсонические средства презентация
Содержание
- 1. Средства, применяемые при нейродегенеративных заболеваниях. Противопаркинсонические средства
- 2. Нейродегенеративными заболеваниями (греческий νέυρο-, нейро-, «нервы-» и
- 3. Клинические проявления НДЗ характеризуются существенным полиморфизмом за
- 4. Класс-я НДЗ Спорадические НДЗ: • Прогрессирующий
- 5. Болезнь Альцгеймера (G30) Хроническое прогрессирующее дегенеративное заболевание
- 6. Деме́нция приобретённое слабоумие, стойкое снижение познавательной деятельности
- 7. Генетически детерменированное заболевание Патогенез – нарушение
- 8. Бета амилоид обладает нейротоксическими свойствами, активирует тканевые
- 9. Лечение направлено на остановку прогрессирования заболевания (нейропротективная терапия) и уменьшение выраженности имеющихся симптомов.
- 10. Уменьшение выраженности симптомов Оптимизация синаптической передачи
- 11. Ингибиторы ацетилхолинэстеразы антихолинэстеразные средства Донепезил Ривастигмин Галантамин
- 12. Антиглутаматные препараты антагонисты NMDA-рецепторов - Мемантин неконкурентный
- 13. Способствует нормализации психической активности, улучшает память,
- 14. В настоящее время разрабатываются лекарственные препараты, которые
- 15. IV. ПРОТИВОПАРКИНСОНИЧЕСКИЕ СРЕДСТВА. А) Вещества, активирующие дофаминергические
- 16. Противопаркинсонические средства — средства, применяемые для лечения
- 17. Первичный (идиопатический) паркинсонизм (болезнь Паркинсона) встречается в
- 18. Основные клинические проявления болезни: брадикинезия (скованность
- 19. Формы паркинсонизма: 1. Дрожательный (↑ АХ,
- 20. Возможной причиной заболевания - образование свободных кислородных
- 21. При болезни Паркинсона число дофаминергических нейронов уменьшается,
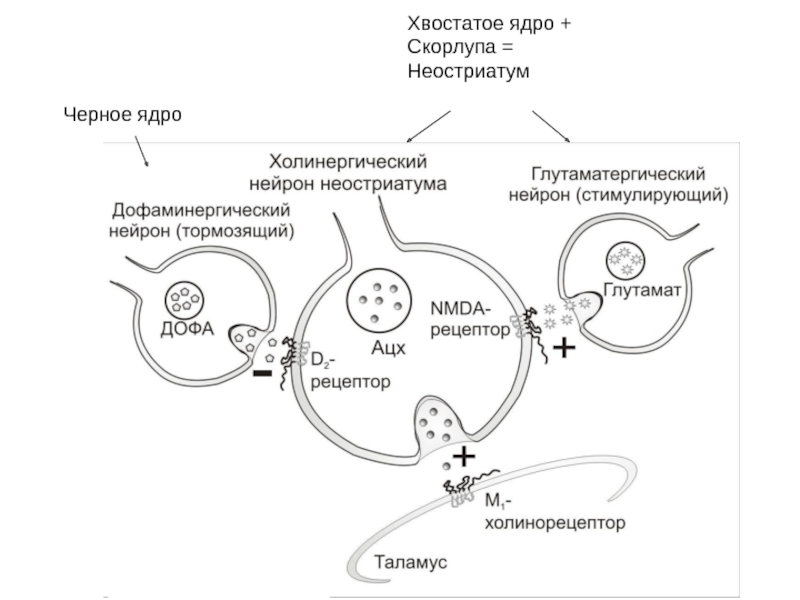
- 22. Хвостатое ядро + Скорлупа = Неостриатум Черное ядро
- 23. I. Дофаминергические препараты Предш.дофамина: Леводопа*(по 100-250 мг,
- 24. В настоящее время при лечении болезни Паркинсона
- 25. Леводопа (100-250 мг) – непосредственный предшественник дофамина,
- 26. ФАРМАКОКИНЕТИКА - всасывается из ЖКТ за счет
- 27. Средства, стимулирующие дофаминергическую передачу Леводопа - (L-ДОФА),
- 28. Леводопа ФК- всасывается из кишечника путем активного
- 29. Для предотвращения декарбоксилирования леводопы в периферических тканях
- 30. Леводопа выпускается в комбинации с блокаторами периферической
- 31. Показаниями к назначению препаратов, содержащих леводопу, являются
- 32. Для предупреждения тошноты и рвоты назначают блокатор
- 33. При длительном (более 5 лет) приеме леводопы
- 34. Кроме того, для повышения эффективности проводимого лечения
- 35. Селегилин (5 мг) - селективный ингибитор МАО-В
- 36. Селегилин назначают в сочетании с леводопой.
- 37. Амантадин усиливает высвобождение дофамина из неповрежденных
- 38. Агонисты дофаминовых рецепторов - непосредственно возбуждают дофаминовые
- 39. Бромокриптин (2,5 мг) - селективный агонист D2-дофаминовых
- 40. Средства, угнетающие холинергическую передачу Тригексифенидил -
- 41. Средства, угнетающие холинергическую передачу Побочные эффекты,
- 42. Тригексифенидил (циклодол, - 2,5 мг). Оказывает
Слайд 1Средства, применяемые при нейродегенеративных заболеваниях. Противопаркинсонические средства.
Слайд 2Нейродегенеративными заболеваниями (греческий νέυρο-, нейро-, «нервы-» и латинский dēgenerāre, «вырождаться») обозначается
Общим для этих заболеваний является прогрессирующая гибель нервных клеток (нейродегенерация), ведущая к различным неврологическим симптомам — прежде всего, к деменции и нарушению движений.
Слайд 3Клинические проявления НДЗ характеризуются существенным полиморфизмом за счет различных сочетаний пяти
экстрапирамидного,
пирамидного,
мозжечкового,
вегетативной недостаточности и
деменции
Слайд 4Класс-я НДЗ
Спорадические НДЗ:
• Прогрессирующий надъядерный паралич (болезнь Стила —Ричардсона — Ольшевского).
•
• Деменция с тельцами Леви.
• Паркинсоническая деменция (синдром Гуам).
• Кортикобазальная дегенерация.
• Болезнь Альцгеймера.
Ирритативные НДЗ:
• Болезнь Гентингтона.
• Болезнь Галлервордена—Шпатца.
• Болезнь Вильсона—Коновалова.
• Болезнь Фара.
• Болезнь Бессена — Корнцвейга.
Слайд 5Болезнь Альцгеймера (G30)
Хроническое прогрессирующее дегенеративное заболевание головного мозга, проявляющееся нарушениями памяти
Самое распространенное НДЗ
Самая частая причина деменций – вызывает не менее 35-40% деменций
Фактор риска развития – пожилой возраст
Слайд 6Деме́нция
приобретённое слабоумие, стойкое снижение познавательной деятельности с утратой в той или
Слайд 7Генетически детерменированное заболевание
Патогенез –
нарушение метаболизма предшественника амилоидного белка, который расщепляется
один из фрагментов является нерастворимым и поэтому откладывается в паренхиме головного мозга и стенках церебральных сосудов.
Далее происходит агрегация этого фрагмента в патологический белок – бета амилоид.
Локальные скопления бета амилоида – сенильные бляшки
Слайд 8Бета амилоид обладает нейротоксическими свойствами, активирует тканевые медиаторы воспаления, что приводит
атрофия нейронов коры и подкорковых структур мозга, в том числе подкорковых холинергических нейронов. При этом отмечается снижение концентрации ацетилхолина в тканях мозга
Слайд 9Лечение направлено на остановку прогрессирования заболевания (нейропротективная терапия) и уменьшение выраженности
Слайд 10Уменьшение выраженности симптомов
Оптимизация синаптической передачи
(при б.А. снижение активности холинергических нейронов):
Ингибиторы
Антиглутаматные препараты
Слайд 11Ингибиторы ацетилхолинэстеразы
антихолинэстеразные средства
Донепезил
Ривастигмин
Галантамин
в меньшей степени ингибируют ацетилхолинэстеразу периферических тканей (скелетных мышц,
третичные амины - хорошо проникают через ГЭБ
Слайд 12Антиглутаматные препараты
антагонисты NMDA-рецепторов - Мемантин
неконкурентный антагонист глутаматных N-метил-D-аспартат (NMDA)-рецепторов,
тормозит глутаматергическую нейротрансмиссию
оказывает нейромодулирующее действие.
Слайд 13
Способствует нормализации психической активности, улучшает память, повышает способность к концентрации внимания,
Действие:
нейропротективное,
антиспастическое,
противопаркинсоническое
Слайд 14В настоящее время разрабатываются лекарственные препараты, которые позволят непосредственно влиять на
Речь идет о так называемой антиамилоидной терапии.
Антиамилоидная терапия основана на введении антител, препятствующих синтезу амилоида или же приводящих к его разрушению.
Это могут быть как антитела непосредственно к амилоиду, так и антитела к ферментам, участвующим в его синтезе.
Слайд 15IV. ПРОТИВОПАРКИНСОНИЧЕСКИЕ СРЕДСТВА.
А) Вещества, активирующие дофаминергические влияния (леводопа*, карбидопа*, мадопар, бромокриптин*,
Б) Вещества, угнетающие глутаматергические влияния (мидантан*);
В) Вещества, угнетающие холинергические влияния (циклодол*, амизил, тропацин).
Слайд 16Противопаркинсонические средства — средства, применяемые для лечения болезни Паркинсона, синдрома паркинсонизма,
Слайд 17Первичный (идиопатический) паркинсонизм (болезнь Паркинсона) встречается в большинстве случаев.
Вторичный, симптоматический паркинсонизм:
лекарственный паркинсонизм
васкулярный - острый при инсультах
токсический и гипоксический
метаболический
постэнцефалический
опухолевый и паранеопластический
травматический
Паркинсонизм с дополнительными неврологическими или нейропсихологическими дефицитами (паркинсонизм-плюс):
в рамках других нейродегенеративных заболеваний
Слайд 18Основные клинические проявления болезни:
брадикинезия (скованность движений),
ригидность (повышенный тонус скелетных
постуральная неустойчивость (неудерживание равновесия, трудность при ходьбе) и
тремор (дрожание) рук, головы.
Клинические проявления болезни возникают при гибели 70-80% дофаминергических нейронов головного мозга.
Встречается у 0,3% населения в разных странах 1% - старше 60 лет.
Болезнь Паркинсона (дрожательный паралич) - хроническое нейродегенеративное заболевание, основой которого является поражение пигментсодержащих дофаминергических нейронов плотной части черной субстанции головного мозга.
Слайд 19Формы паркинсонизма:
1. Дрожательный (↑ АХ, легкий) – постоянный тремор рук, головы
2. Ригидно-брадикинетический (↓ дофамина, тяжелый) - повышение тонуса мышц, скованность произвольных движений вплоть до полной обездвиженности.
3. Дрожательно-ригидный (смешанный) – тремор (4-8 Гц), усиливающийся при волнении, практически исчезающий во сне. К тремору постепенно присоединяется скованность.
Слайд 20Возможной причиной заболевания - образование свободных кислородных радикалов в процессе окислительного
Имеются данные о том, что существует генетическая предрасположенность к болезни Паркинсона.
Причиной синдрома паркинсонизма, также проявляющегося дрожательным параличом, могут быть инфекционные заболевания нервной системы (вирусный энцефалит), сосудистые заболевания головного мозга, травмы черепа, интоксикации (оксидом углерода, марганцем, этанолом), сифилитические поражения мозга.
Лекарственный паркинсонизм - форма синдрома паркинсонизма, развивающаяся при длительном применении некоторых лекарственных средств, например, типичных нейролептиков (фенотиазины, бутирофеноны).
Слайд 21При болезни Паркинсона число дофаминергических нейронов уменьшается, и в связи с
Для снятия этих симптомов необходимо восстановить нарушенный баланс между указанными системами в неостриатуме, что может быть достигнуто:
повышением дофаминергических влияний,
снижением влияния глутаматергических нейронов,
уменьшением влияния холинергических нейронов.
Слайд 23I. Дофаминергические препараты
Предш.дофамина: Леводопа*(по 100-250 мг, 3-4 р./день после еды)
Комбинированные
Наком, Синемет (+Карбидопа), Мадопар (+Бенсеразид)
Стимуляторы выделения дофамина:
Амантадин (Мидантан)
Ингибиторы МАО В: Селегилин (Депренил)
Стимуляторы дофаминовых рецепторов:
Бромокриптин (Парлодел)
II. Антихолинергические препараты
Тригексифенидил* (Циклодол, таб. 2,5 мг 3-4 р.д.)
Дифенилтропин, Бипериден (Акинетон) - ~
III. Ингибиторы КОМТ
Энтакапон
КЛАССИФИКАЦИЯ
Слайд 24В настоящее время при лечении болезни Паркинсона в основном используются следующие
Средства, стимулирующие дофаминергическую передачу
Предшественник дофамина - Леводопа
Ингибиторы моноаминоксидазы В - Селегилин (Депренил, Элдеприл, Юмекс)
Средства, повышающие выделение дофамина - Амантадин (Мидантан)
Средства, стимулирующие дофаминовые рецепторы (агонисты дофаминовых рецепторов) - Бромокриптин (Парлодел), перголид (Пермакс), прамипексол
(Мирапекс), ропинирол (Реквип)
Средства, угнетающие холинергическую передачу
Центральные холиноблокаторы: Тригексифенидил (Циклодол), бипериден (Акинетон).
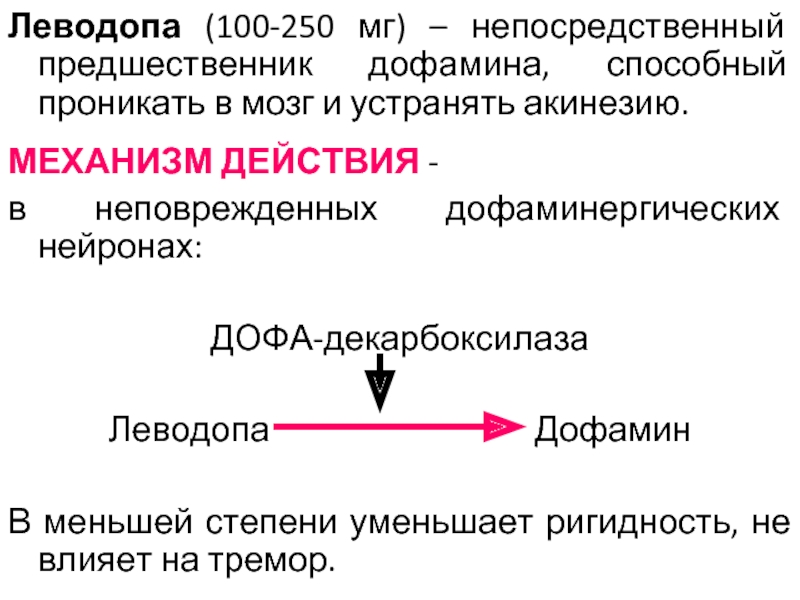
Слайд 25Леводопа (100-250 мг) – непосредственный предшественник дофамина, способный проникать в мозг
МЕХАНИЗМ ДЕЙСТВИЯ -
в неповрежденных дофаминергических нейронах:
ДОФА-декарбоксилаза
Леводопа Дофамин
В меньшей степени уменьшает ригидность, не влияет на тремор.
Слайд 26ФАРМАКОКИНЕТИКА - всасывается из ЖКТ за счет активного транспорта, в той
В стенке кишечника и в печени Леводопа подвергается интенсивному метаболизму декарбоксилазой ароматических аминокислот, что приводит к превращению в дофамин более 90% введенного препарата.
Образовавшийся в периферических тканях дофамин не проникает в мозг и вызывает ряд побочных эффектов.
Слайд 27Средства, стимулирующие дофаминергическую передачу
Леводопа - (L-ДОФА), непосредственный предшественник дофамина.
Дофамин не
Леводопа проникает через ГЭБ путем активного транспорта
(с помощью транспортной системы, которая переносит через мембраны ароматические аминокислоты).
В неповрежденных дофаминергических нейронах леводопа под влиянием ДОФА-декарбоксилазы превращается в дофамин, который выделяется из окончаний дофаминергических волокон и стимулирует D2-рецепторы на холинергических нейронах неостриатума.
В результате активность этих нейронов снижается, что приводит к устранению симптомов паркинсонизма.
Леводопа относится к наиболее эффективным ППС: уменьшает брадикинезию, мышечную ригидность и в меньшей степени тремор.
Слайд 28Леводопа ФК- всасывается из кишечника путем активного транспорта, используя систему трансмембранного
В стенке кишечника и в печени леводопа подвергается интенсивному метаболизму под действием ДОФА-декарбоксилазы, что приводит к превращению в дофамин более 90% введенного препарата. Образовавшийся в периферических тканях дофамин не проникает в мозг и вызывает ряд побочных эффектов.
Часть леводопы метаболизируется также МАО и КОМТ, в результате только 1—3% леводопы поступает в ЦНС.
Слайд 29Для предотвращения декарбоксилирования леводопы в периферических тканях используют ингибиторы ДОФА-декарбоксилазы, не
При этом большее количество леводопы (около 10%) поступает в ткани мозга и достигает места своего действия.
Это позволяет снизить назначаемую дозу леводопы и уменьшаются периферические побочные эффекты леводопы.
Слайд 30Леводопа выпускается в комбинации с блокаторами периферической ДОФА-декарбоксилазы и входит в
Наком, Синемет, Дуэллин (леводопа+карбидопа) и Мадопар (леводопа+бенсеразид).
Слайд 31Показаниями к назначению препаратов, содержащих леводопу, являются болезнь Паркинсона и паркинсонизм
Действие развивается медленно (через 1 нед) и достигает максимума через 1 мес. Лечение - длительно.
ПД:
ортостатическая гипотензия, тахикардия, сердечные аритмии, которые связаны с образованием дофамина в периферических тканях и действием дофамина на сосуды и сердце.
Частый побочными эффектами являются тошнота и рвота, которые возникают вследствие стимуляции дофамином D2-рецепторов пусковой зоны рвотного центра.
Слайд 32Для предупреждения тошноты и рвоты назначают блокатор дофаминовых рецепторов домперидон, который
При этом домперидон не блокирует дофаминовые рецепторы в неостриатуме и поэтому не снижает эффективность леводопы.
Такие побочные эффекты, как психозы, галлюцинации, бессонница, тревожность, депрессия, нарушение координации движений связаны с действием дофамина в ЦНС.
Для устранения психозов применяют блокатор дофаминовых рецепторов центрального действия клозапин (атипичный нейролептик), который в большей степени блокирует D4-, чем D2-рецепторы в ЦНС и поэтому в меньшей степени, чем типичные нейролептики влияет на эффективность леводопы.
Слайд 33При длительном (более 5 лет) приеме леводопы эффективность снижается, что связано
Для повышения эффективности леводопы, кроме ингибиторов ДОФА-декарбоксилазы, одновременно с леводопой назначают ингибиторы КОМТ.
Одним из таких препаратов - энтакапон (Комтан). Препарат не проникает через гематоэнцефалический барьер и задерживает метаболизм леводопы в периферических тканях, при этом повышается количество леводопы, поступающей в ЦНС, что позволяет снизить дозу леводопы.
Слайд 34Кроме того, для повышения эффективности проводимого лечения леводопу обычно сочетают с
селегилин (ингибитор МАО-В),
амантадин (препарат, высвобождающий дофамин из пресинаптических окончаний) и
агонисты дофаминовых рецепторов.
Слайд 35Селегилин (5 мг) - селективный ингибитор МАО-В в ткани мозга. Этот
Селегилин, уменьшает разрушение дофамина в нейронах черной субстанции, что позволяет уменьшить дозу Леводопы в среднем на 30%.
Показания: тяжелые формы болезни и синдрома Паркинсона (за исключением лекарственного паркинсонизма).
Побочные эффекты: тошнота, гипотония, нарушение способности к концентрации внимания и спутанность сознания.
Слайд 36Селегилин назначают в сочетании с леводопой.
В качестве монотерапии препарат используют
Полагают, что селегилин обладает нейропротекторным действием, задерживая разрушение дофаминергических нейронов мозга.
Побочные эффекты: тошнота, рвота, артериальная гипотензия, нарушение концентрации внимания и спутанность сознания.
Слайд 37Амантадин
усиливает высвобождение дофамина из неповрежденных нейронов в синаптическую щель и
Повышение концентрации дофамина в ЦНС приводит к ослаблению симптомов болезни Паркинсона.
+Противовирусное действие связано, возможно, со способностью амантадина блокировать проникновение вируса А в клетки – профилактика и лечение гриппа
Слайд 38Агонисты дофаминовых рецепторов - непосредственно возбуждают дофаминовые рецепторы в неостриатуме.
Бромокриптин,
Перголид и бромокриптин относятся к производным алкалоидов спорыньи.
Слайд 39Бромокриптин (2,5 мг) - селективный агонист D2-дофаминовых рецепторов.
ФАРМАКОКИНЕТИКА - хорошо
Т1/2 - 2-8 ч (50-70 ч для метаболитов).
Выведение - через печень, около 6% - через почки.
Показания: тяжелые формы болезни и синдрома Паркинсона, в том числе – лекарственный паркинсонизм.
Слайд 40Средства, угнетающие холинергическую передачу
Тригексифенидил - центральный холиноблокатор, блокируя М,-холинорецепторы неостриатума, уменьшает
Умеренное противопаркинсоническое действие.
Преимущественно уменьшает тремор и мышечную ригидность, мало влияя на брадикинезию.
Бипериден — центральный холиноблокатор, близкий по свойствам тригексифенидилу.
Показания к назначению центральных холиноблокаторов: начальные стадии болезни Паркинсона и паркинсонизм.
Слайд 41Средства, угнетающие холинергическую передачу
Побочные эффекты, связанные с блокадой периферических М-холинорецепторов: нарушение
Побочные эффекты, связанные с блокадой центральных М-холинорецепторов - нарушение памяти и концентрации внимания, особенно у пожилых пациентов.
Слайд 42Тригексифенидил (циклодол, - 2,5 мг).
Оказывает центральное холиноблокирующее действие. Преимущественно уменьшает
Дифенилтропин, Бипериден – близкие по свойствам с тригексифенидилом.
Побочные эффекты –
периферические - нарушения зрения, обострение глаукомы, сухость во рту, сердцебиение, задержка мочеиспускания
центральные - нарушения памяти и концентрации внимания, особенно у пожилых пациентов