- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Современные представления о гемокоагуляции презентация
Содержание
- 1. Современные представления о гемокоагуляции
- 2. Quo vadis – эволюция гемостаза Появление замкнутой
- 3. Quo vadis – эволюция гемостаза Вопрос о
- 4. Quo vadis – эволюция гемостаза Беспозвоночные –
- 5. Является ли система гемостаза функциональной системой? «Функциональная
- 6. Два типа функциональных систем: Системы первого типа:
- 7. Richard Langton Gregory (1923-2010) В случаях, когда
- 8. Walter Bradford Cannon (1871-1945)
- 9. Реакция системы гемостаза на острый стресс:
- 10. Влияние острого стресса на систему гемокоагуляции: СТРЕСС
- 11. Гемоконцентрация vs гемодилюция: «физиологический парадокс»? Гемоконцентрация
- 12. Влияние дилюции плазмы здорового донора 0,9% раствором
- 13. Артериальная гиетензия vs артериальная гипотензия: «физиологический парадокс»?
- 14. Регуляция гемокоагуляции эндокринной системой: Гемокоагуляция НЕЙРОГИПОФИЗ
- 15. Взаимосвязь коагуляции и воспалительной реакции: Система
- 16. «Белки острой фазы воспаления» «Активаторы» С3
- 17. Какой эффект является «физиологически полезным» с точки
- 18. Для того, что бы понять функциональную структуру
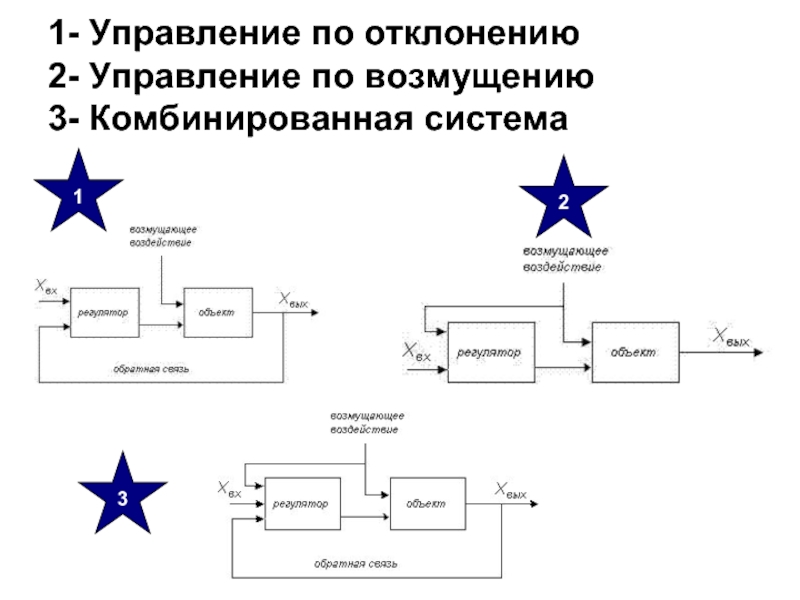
- 19. 1- Управление по отклонению 2- Управление по возмущению 3- Комбинированная система 1 2 3
- 20. Иван Иванович Ползунов (1728-1766) James Watt (1736-1819) Принцип регуляции по отклонению – принцип Ползунова-Уатта
- 21. Jean-Victor Poncelet (1788-1867) Братья Сименсы Принцип регуляции по возмущению – принцип Понселе -Сименсов
- 22. Задачи, стоящие перед системой гемокоагуляции, настолько сложны
- 23. А зачем нам все это нужно? «Классическая»
- 24. Большинство приобретенных коагулопатий, с которыми мы сталкиваемся
- 25. УПРАВЛЕНИЕ ПО ВОЗМУЩЕНИЮ А. Положительные обратные связи
- 26. УПРАВЛЕНИЕ ПО ОТКЛОНЕНИЮ А. Положительные обратные связи
- 27. Система гемостаза функциональная система организма, состоящая из
- 28. Система гемостаза («анатомо-гистологические» субсистемы) Сосуды, эндотелий Тромбоциты Гуморальные факторы
- 29. Система гемостаза (функциональные субсистемы) Свертывающая система
- 30. Современные представления о системе гемокоагуляции
- 31. «Классическая» или «Y-образная» схема гемостаза предполагает существование
- 33. Внутренний путь: XIIa+XIa Внешний путь: VIIa+III Теназа:
- 34. Недостатки «классической» схемы гемостаза: Не отражает прогрессии
- 35. Внутренний путь: XIIa+XIa Внешний путь: VIIa+III Теназа:
- 36. Чем плоха «схема водопада»?
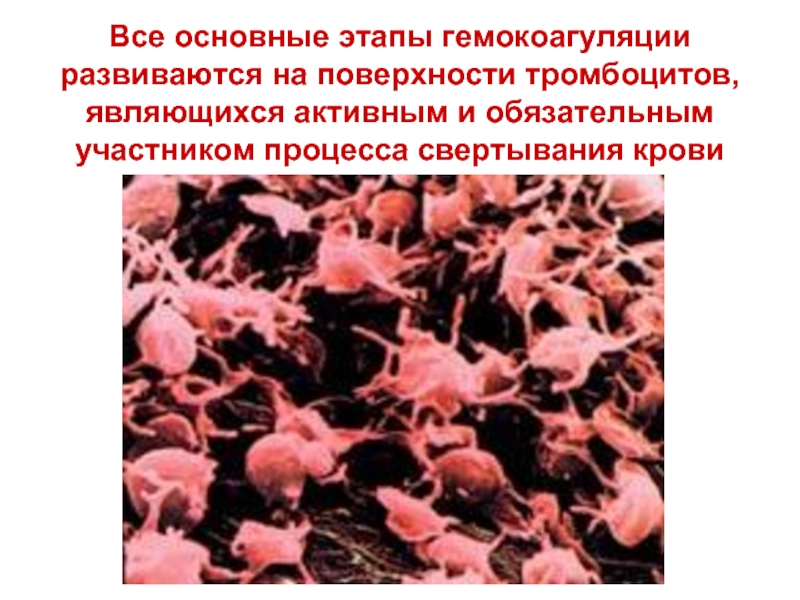
- 37. Все основные этапы гемокоагуляции развиваются на поверхности
- 38. Процесс свертывания крови – это процесс активации
- 40. На 1000 молекул фибриногена у здорового человека:
- 42. Не все факторы свертывания крови являются «нерасходуемыми»
- 43. Потребляемые факторы: Фибриноген (I) (остается в свертке
- 44. Факторы – проферменты: Протромбин (II) Проконвертин (VII)
- 45. В процессе свертывания крови можно выделить четыре
- 46. Повреждение сосуда приводит к выходу крови во
- 48. Небольшое («пусковое») количество тромбина активирует тромбоциты. Начинается
- 50. Основные физиологические антикоагулянты: Xa + Va
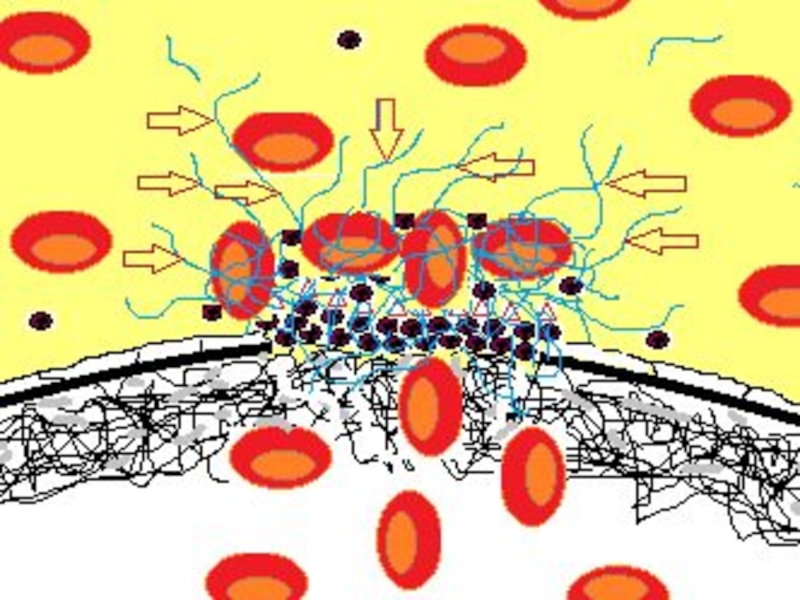
- 51. Первые тромбоциты, контактирующие с субэндотелиальными структурами, максимально
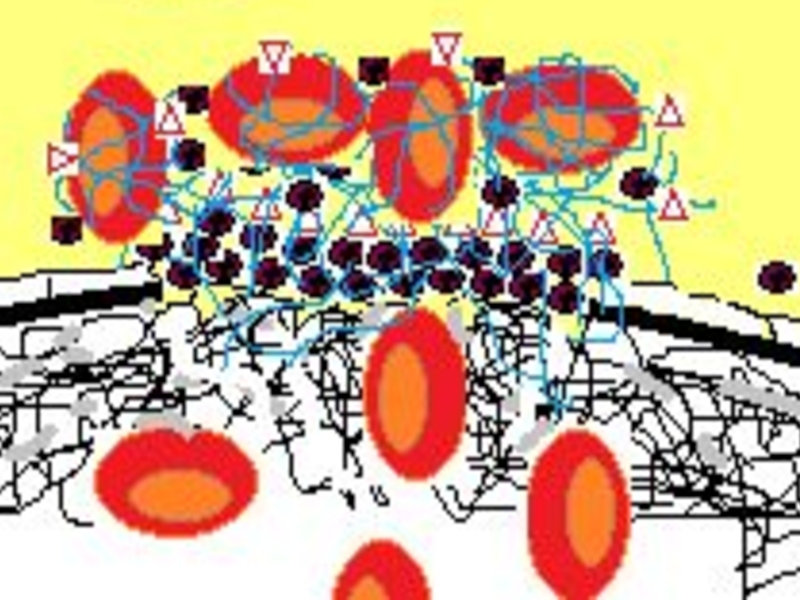
- 53. Тромбин (красные треугольники на схеме), фиксированный на
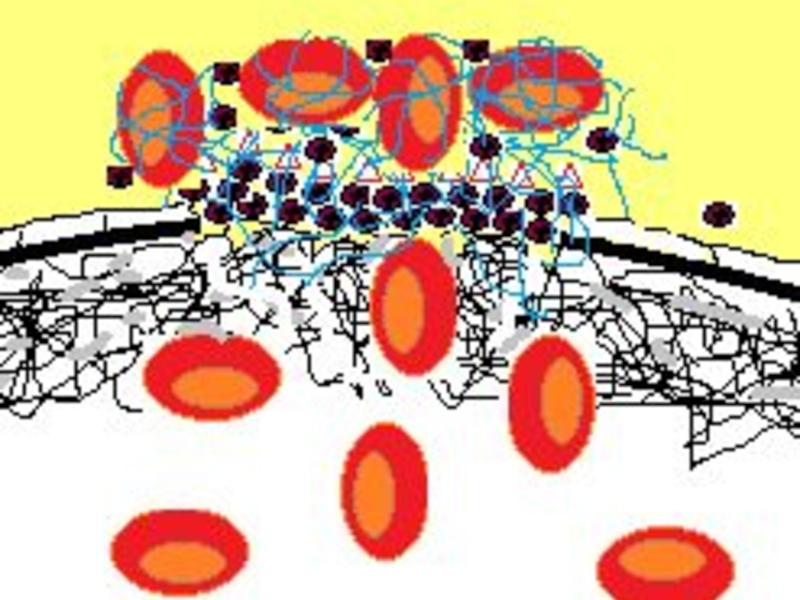
- 55. Значительное количество тромбина, образовавшегося на поверхности активированных
- 57. В посткоагуляционную стадию начинается процесс ретракции кровяного
- 59. В то же время, одновременно с процессом
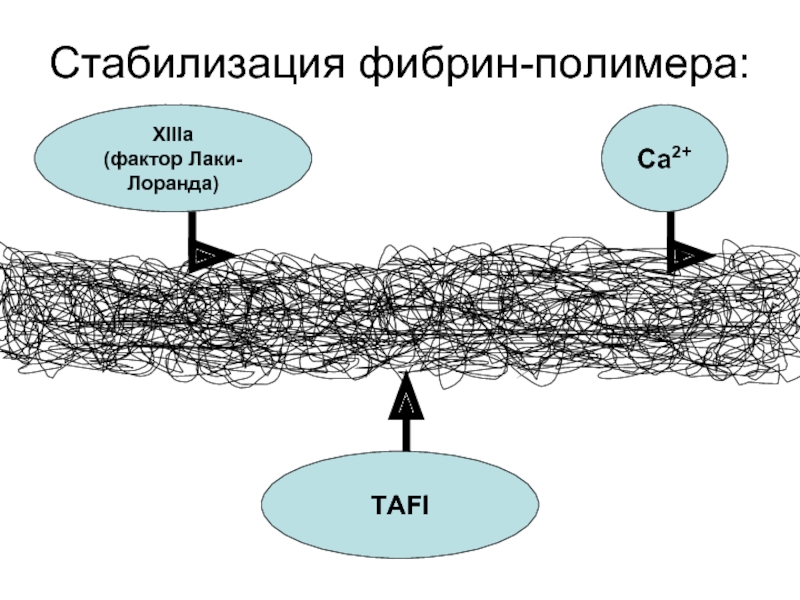
- 61. Стабилизация фибрин-полимера: XIIIa (фактор Лаки-Лоранда) TAFI Ca2+
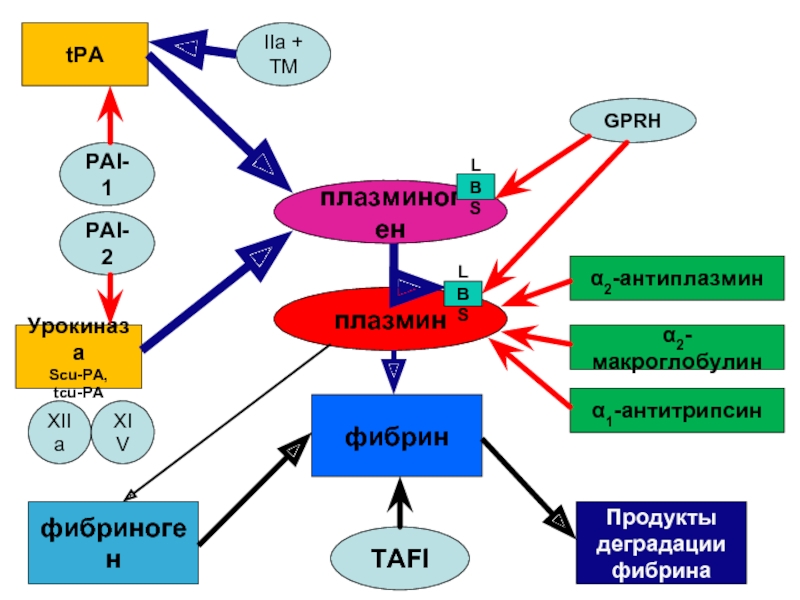
- 62. плазминоген плазмин фибрин фибриноген Продукты деградации фибрина
Слайд 2Quo vadis – эволюция гемостаза
Появление замкнутой полости у живых существ ставит
Два основных врага всего живущего на планете – это травма и инфекция
Область агрессии должна быть локализована и восстановлена
Слайд 3Quo vadis – эволюция гемостаза
Вопрос о первичности клеточного и гуморального звеньев
Система гемостаза и система иммунитета скорее всего имеют общее происхождение
Только тесное и скоординированное взаимодействие клеточного ми гуморального звеньев обеспечивают адекватный гемостаз
Слайд 4Quo vadis – эволюция гемостаза
Беспозвоночные – протеолитические ферменты и гемолимфоциты
Насекомые
Рыбы – малые лимфоциты обладают гемостатической функцией. Система относительно низкого перфузионного давления крови позволяет обойтись без значительных усилителей процесса
Земноводные и пресмыкающиеся – появление системы высокого давления (2 круга кровообращения) потребовали появления развитого клеточного звена
Птицы – смена оперения невозможна без микрососудистого гемостаза (тромбоциты)
Ныряющие животные – необходимость восстановления кровообращения в периферических тканях потребовала развития системы фибринолиза
Плацентарное размножение – необходима система амплификации для обеспечения практически мгновенного гемостаза
Слайд 5Является ли система гемостаза функциональной системой?
«Функциональная система — это система различных
Петр Кузьмич Анохин
ГЛАВНАЯ ПРОБЛЕМА СОСТОИТ В ТОМ, ЧТО ПЕРЕД СИСТЕМОЙ
СТОЯТ ДВЕ КЛЮЧЕВЫЕ, КАК БУДТО-БЫ ВЗАИМОИСКЛЮЧАЮЩИЕ
ЗАДАЧИ!
Слайд 6Два типа функциональных систем:
Системы первого типа: обеспечение гомеостаза за счет внутренних
Системы второго типа: поддержание гомеостаза за счет поведенческих реакций (с использованием ресурсов внешней среды)
Слайд 7Richard Langton Gregory
(1923-2010)
В случаях, когда мы имеем дело с простыми системами,
выпадение одного из элементов системы ведет к утрате
одной из функций. В случае сложной системы, имеющей
множественные обратные связи (петли), выпадение одного
из элементов приводит к перестройке всей системы.
В сущности, с этого момента мы имеем дело уже с новой
системой.
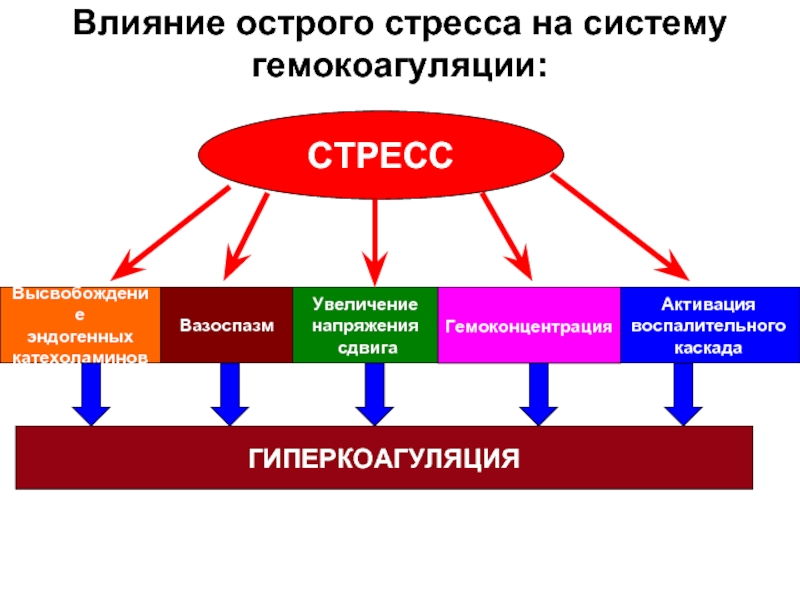
Слайд 10Влияние острого стресса на систему гемокоагуляции:
СТРЕСС
Высвобождение
эндогенных
катехоламинов
Вазоспазм
Увеличение
напряжения
сдвига
Активация
воспалительного
каскада
Гемоконцентрация
ГИПЕРКОАГУЛЯЦИЯ
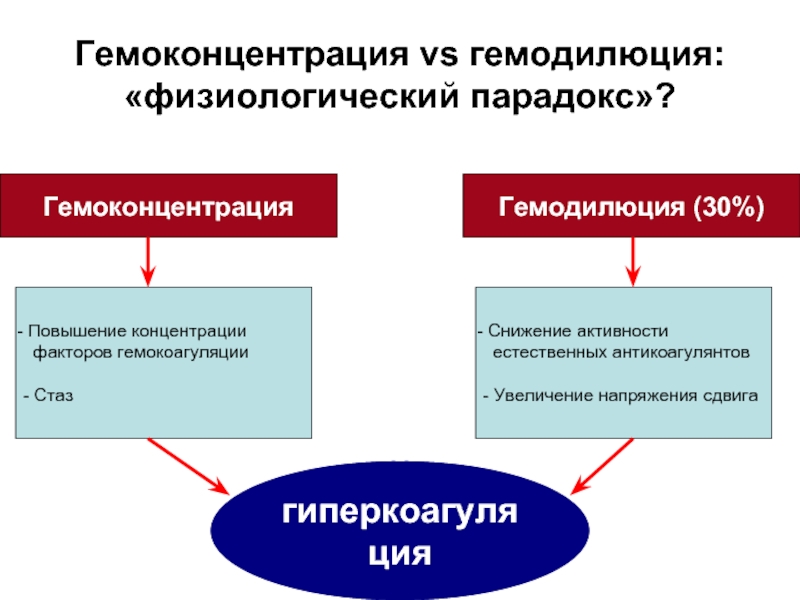
Слайд 11Гемоконцентрация vs гемодилюция: «физиологический парадокс»?
Гемоконцентрация
Гемодилюция (30%)
гиперкоагуляция
Повышение концентрации
факторов
- Стаз
Снижение активности
естественных антикоагулянтов
- Увеличение напряжения сдвига
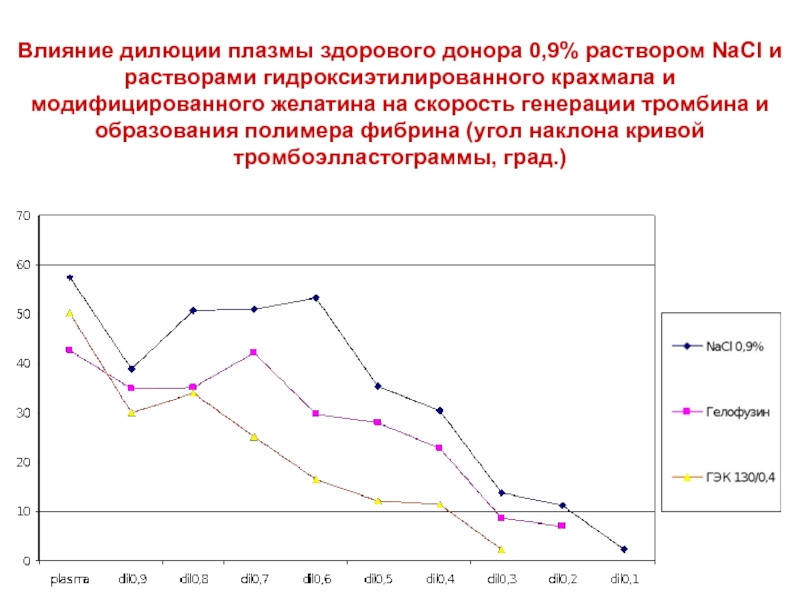
Слайд 12Влияние дилюции плазмы здорового донора 0,9% раствором NaCl и растворами гидроксиэтилированного
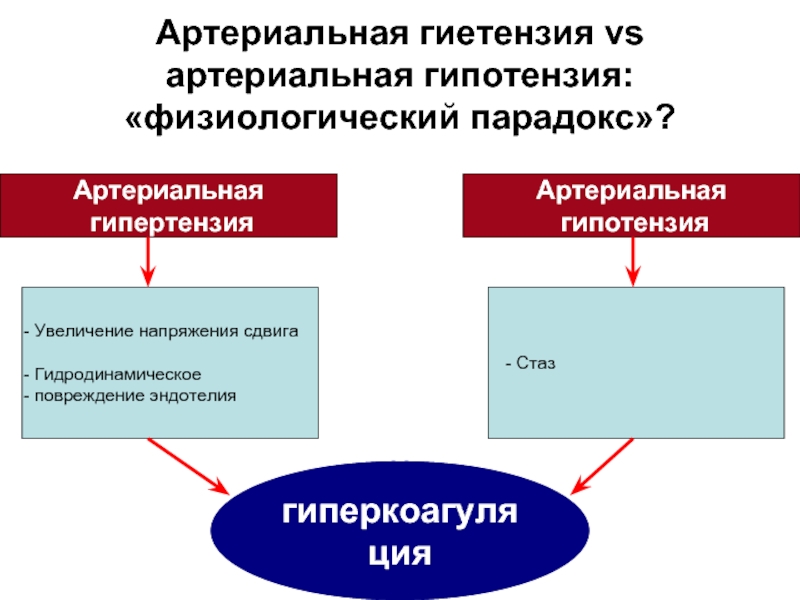
Слайд 13Артериальная гиетензия vs артериальная гипотензия: «физиологический парадокс»?
Артериальная
гипертензия
Артериальная
гипотензия
гиперкоагуляция
-
Увеличение напряжения сдвига
Гидродинамическое
повреждение эндотелия
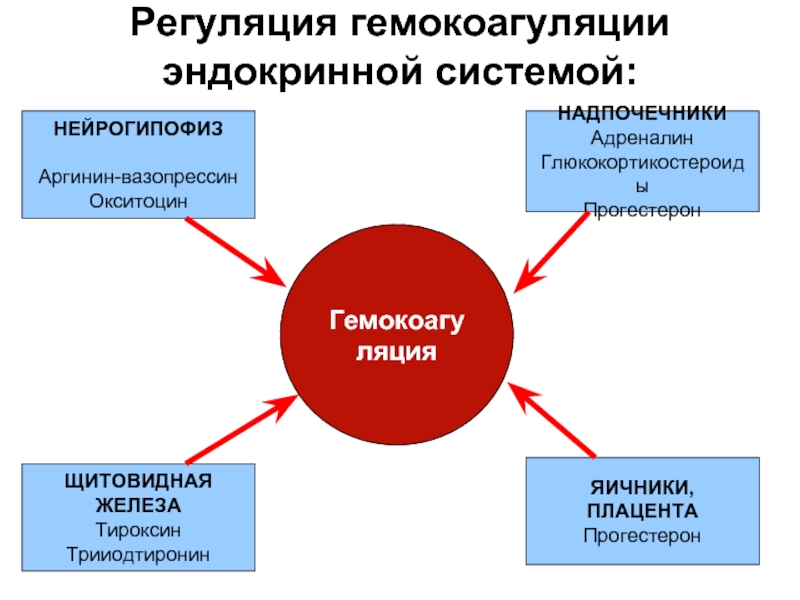
Слайд 14Регуляция гемокоагуляции эндокринной системой:
Гемокоагуляция
НЕЙРОГИПОФИЗ
Аргинин-вазопрессин
Окситоцин
НАДПОЧЕЧНИКИ
Адреналин
Глюкокортикостероиды
Прогестерон
ЩИТОВИДНАЯ
ЖЕЛЕЗА
Тироксин
Трииодтиронин
ЯИЧНИКИ,
ПЛАЦЕНТА
Прогестерон
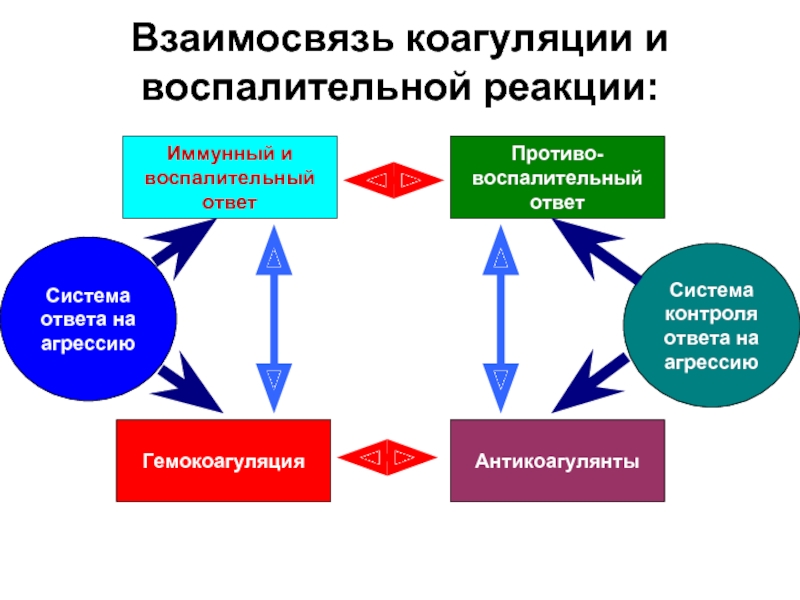
Слайд 15Взаимосвязь коагуляции и воспалительной реакции:
Система
ответа на
агрессию
Иммунный и
воспалительный
ответ
Гемокоагуляция
Система
контроля
ответа на
агрессию
Антикоагулянты
Противо-
воспалительный
ответ
Слайд 16«Белки острой фазы воспаления»
«Активаторы»
С3 С4 С9
С1 ингибитор
Фактор В
С4в связывающий протеин
MBL
Фибриноген
Плазминоген
t-PA
Урокиназа
Протеин S
Витронектин
PAI-1
α-1
Церулоплазмин
Гаптоглобулин
Гемопексин
Фосфолипаза А2
Липополисахарид-связывающий протеин
Антагонист рецептора ИЛ-1
G-CSF
С-реактивный белок
Плазменный амилоидный протеин А
Фибронектин
Ферритин
Ангиотензиноген
«Ингибиторы»
Альбумин
Трансферрин
Транстиретин
α-2 HS гликопротеин
α- фетопротеин
Тироксин-связывающий белок
Инсулинополобный фактор роста-1
Фактор 12
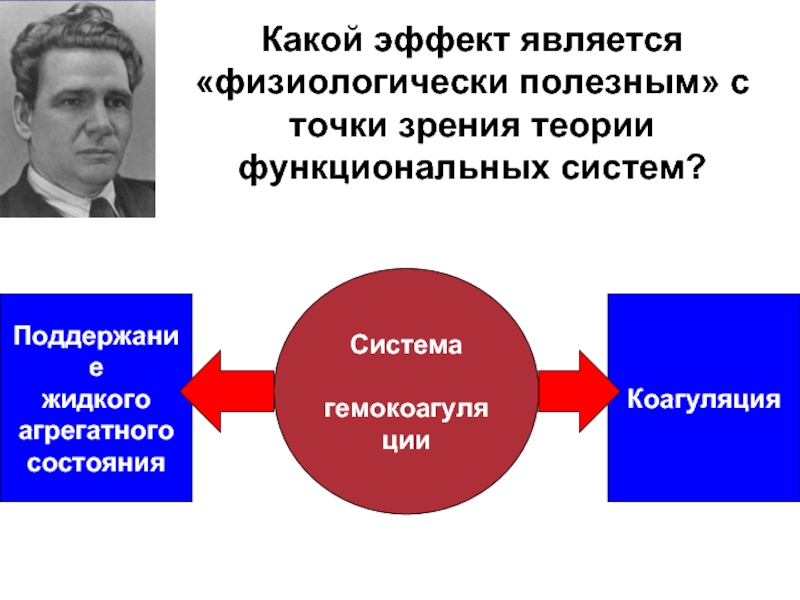
Слайд 17Какой эффект является «физиологически полезным» с точки зрения теории функциональных систем?
Система
Поддержание
жидкого
агрегатного
состояния
Коагуляция
Слайд 18Для того, что бы понять функциональную структуру системы гемокоагуляции, представляется рациональным
Слайд 20Иван Иванович Ползунов (1728-1766)
James Watt (1736-1819)
Принцип регуляции по отклонению –
принцип
Слайд 21Jean-Victor Poncelet (1788-1867)
Братья Сименсы
Принцип регуляции по возмущению –
принцип Понселе -Сименсов
Слайд 22Задачи, стоящие перед системой гемокоагуляции, настолько сложны и противоречивы, что регуляция
Слайд 23А зачем нам все это нужно?
«Классическая» или «Y-образная» схема гемостаза (Robert
Схема «водопада» («Waterfall hypothesis», Earl Davie and Oscar Ratnoff, 1962) не отражает реального положения дел.
Слайд 24Большинство приобретенных коагулопатий, с которыми мы сталкиваемся в хирургической практике, клинически
1
2
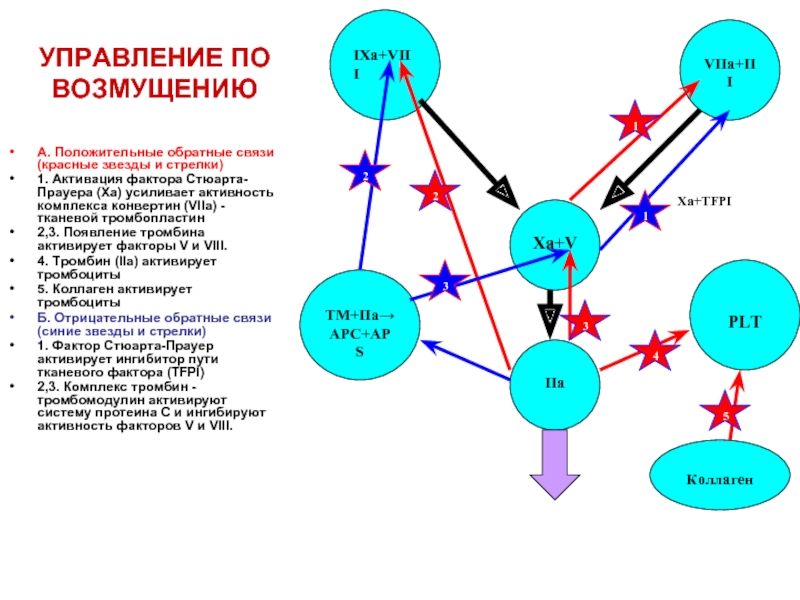
Слайд 25УПРАВЛЕНИЕ ПО ВОЗМУЩЕНИЮ
А. Положительные обратные связи (красные звезды и стрелки)
1. Активация
2,3. Появление тромбина активирует факторы V и VIII.
4. Тромбин (IIa) активирует тромбоциты
5. Коллаген активирует тромбоциты
Б. Отрицательные обратные связи (синие звезды и стрелки)
1. Фактор Стюарта-Прауер активирует ингибитор пути тканевого фактора (TFPI)
2,3. Комплекс тромбин - тромбомодулин активируют систему протеина С и ингибируют активность факторов V и VIII.
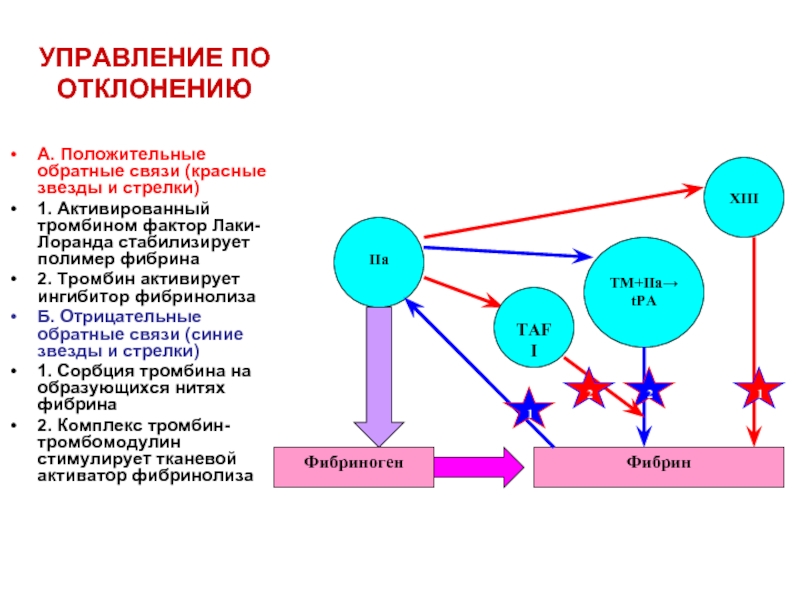
Слайд 26УПРАВЛЕНИЕ ПО ОТКЛОНЕНИЮ
А. Положительные обратные связи (красные звезды и стрелки)
1. Активированный
2. Тромбин активирует ингибитор фибринолиза
Б. Отрицательные обратные связи (синие звезды и стрелки)
1. Сорбция тромбина на образующихся нитях фибрина
2. Комплекс тромбин-тромбомодулин стимулирует тканевой активатор фибринолиза
Слайд 27Система гемостаза
функциональная система организма, состоящая из нескольких взаимодействующих между собой субсистем,
Слайд 28Система гемостаза
(«анатомо-гистологические» субсистемы)
Сосуды, эндотелий
Тромбоциты
Гуморальные факторы
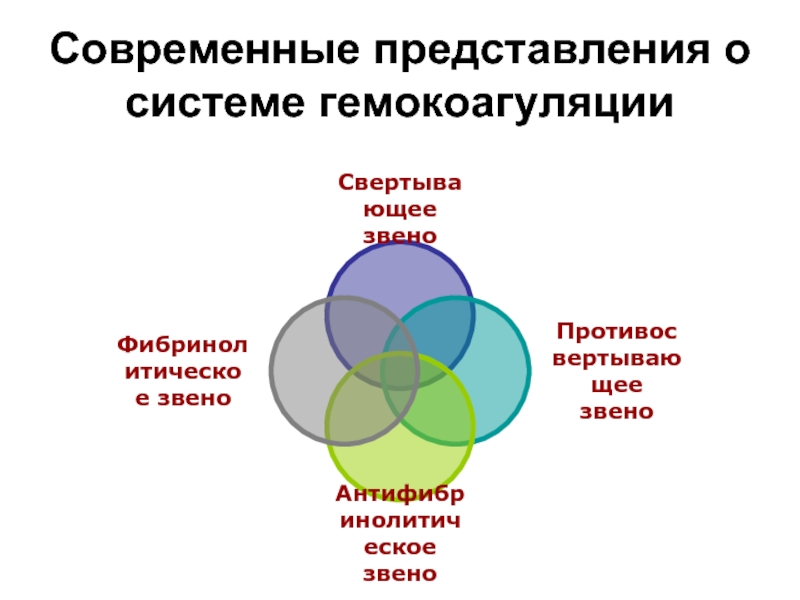
Слайд 29Система гемостаза (функциональные субсистемы)
Свертывающая система
Противосвертывающая система
Фибринолитическая система
Антифибринолитическая система
Слайд 31«Классическая» или «Y-образная» схема гемостаза предполагает существование двух независимых путей его
Oscar Ratnoff
Robert Gwin Macfarlane
1962
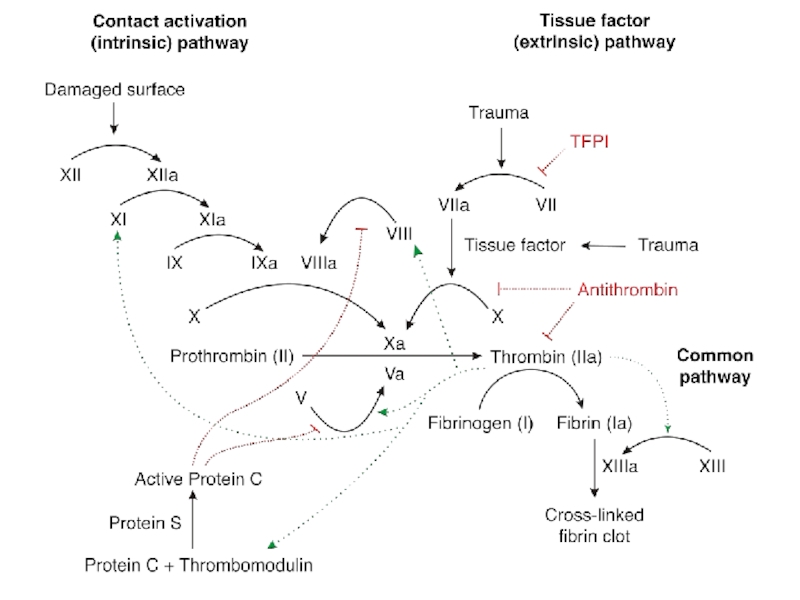
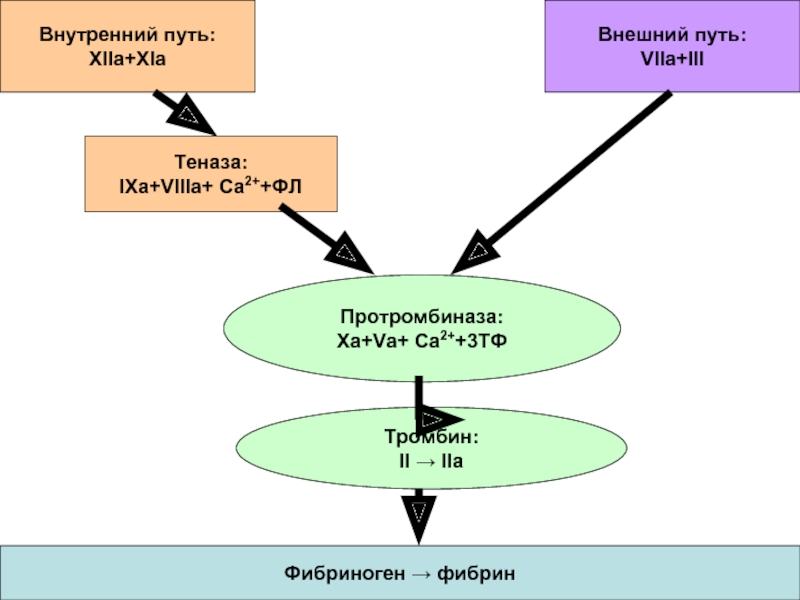
Слайд 33Внутренний путь:
XIIa+XIa
Внешний путь:
VIIa+III
Теназа:
IXa+VIIIa+ Ca2++ФЛ
Протромбиназа:
Xa+Va+ Ca2++3ТФ
Тромбин:
II → IIa
Фибриноген → фибрин
Слайд 34Недостатки «классической» схемы гемостаза:
Не отражает прогрессии генерации активных факторов
Противопоставляет «внутренний» и
Не учитывает активную роль тромбоцитарного и эндотелиального звеньев гемостаза
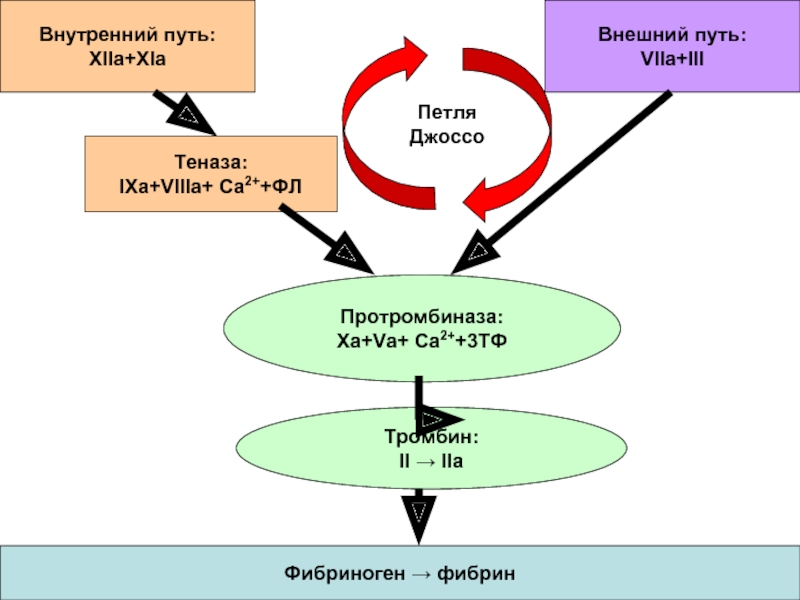
Слайд 35Внутренний путь:
XIIa+XIa
Внешний путь:
VIIa+III
Теназа:
IXa+VIIIa+ Ca2++ФЛ
Протромбиназа:
Xa+Va+ Ca2++3ТФ
Тромбин:
II → IIa
Фибриноген → фибрин
Петля Джоссо
Слайд 37Все основные этапы гемокоагуляции развиваются на поверхности тромбоцитов, являющихся активным и
Слайд 38Процесс свертывания крови – это процесс активации одних ферментов другими ферментами
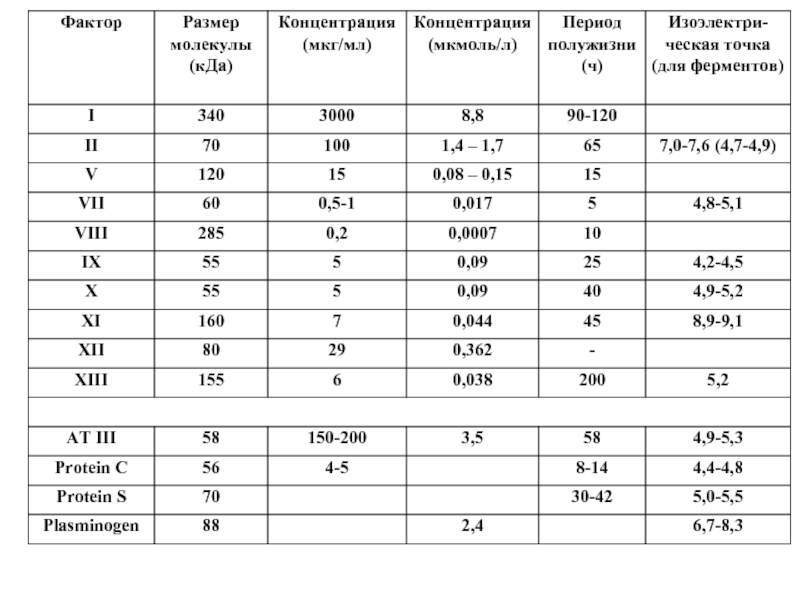
Слайд 40На 1000 молекул фибриногена у здорового человека:
Протромбина (II) – 140 молекул
Проакцелерина
Проконвертина (VII) – 1 молекула
Стюарта-Прауера (X) – 20 молекул
Антигемофильного А (VIII) – 0,03 молекулы
Антигемофильного В (IX) – 10 молекул
Антитромбина III (ПАТ) – 400 молекул
Слайд 42Не все факторы свертывания крови являются «нерасходуемыми» катализаторами. Ряд факторов необратимо
Слайд 43Потребляемые факторы:
Фибриноген (I) (остается в свертке в виде фибрина)
Протромбин (II) (сорбируется
Проакцелерин (V) (является расходуемым кофактором фактора Xa)
Антигемофильный А (VIII) (является расходуемым кофактором фактора IXa)
Тромбоциты (остается в образовавшемся свертке, претерпевая необратимые изменения)
Слайд 44Факторы – проферменты:
Протромбин (II)
Проконвертин (VII)
Антигемофильный В (IX)
Стюарта-Прауера (X)
Розенталя (XI)
Хагемана (XII)
Фибринстабилизирующий (XIII)
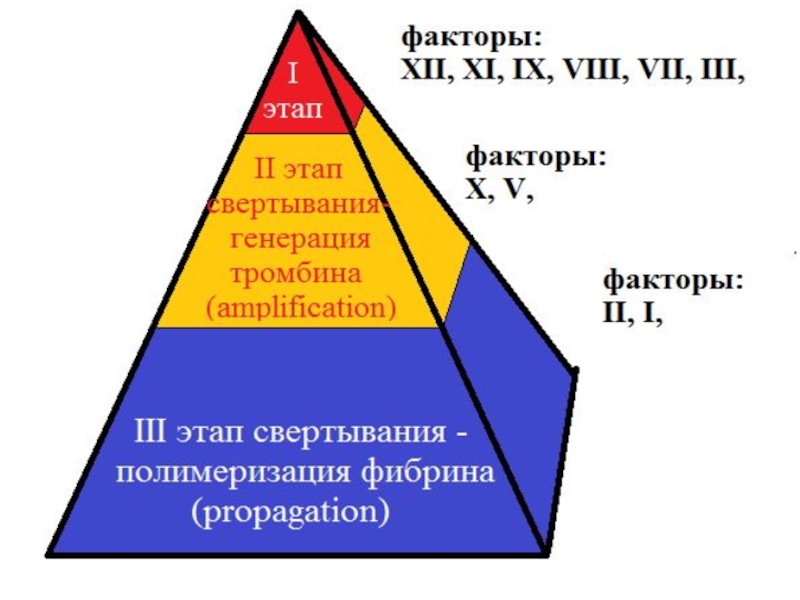
Слайд 45В процессе свертывания крови можно выделить четыре основных периода:
1. Инициирование (initiation
2. Усиление (amplification phase)
3. Распространение (propagation phase)
4. Посткоагуляционная фаза
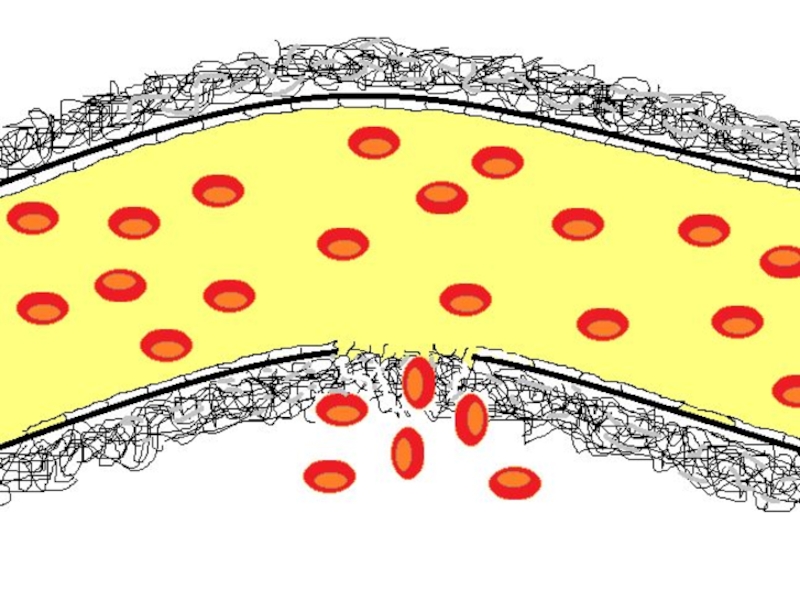
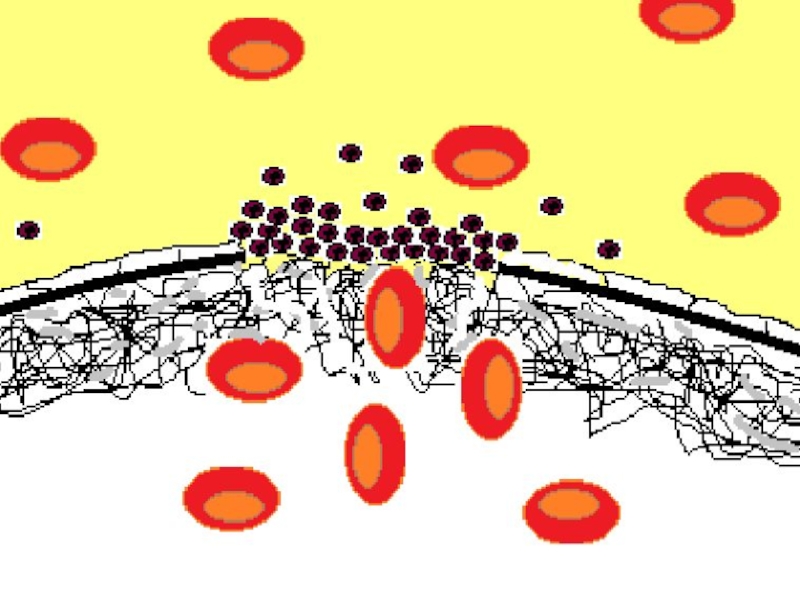
Слайд 46Повреждение сосуда приводит к выходу крови во внесосудистое пространство. Одновременно происходит
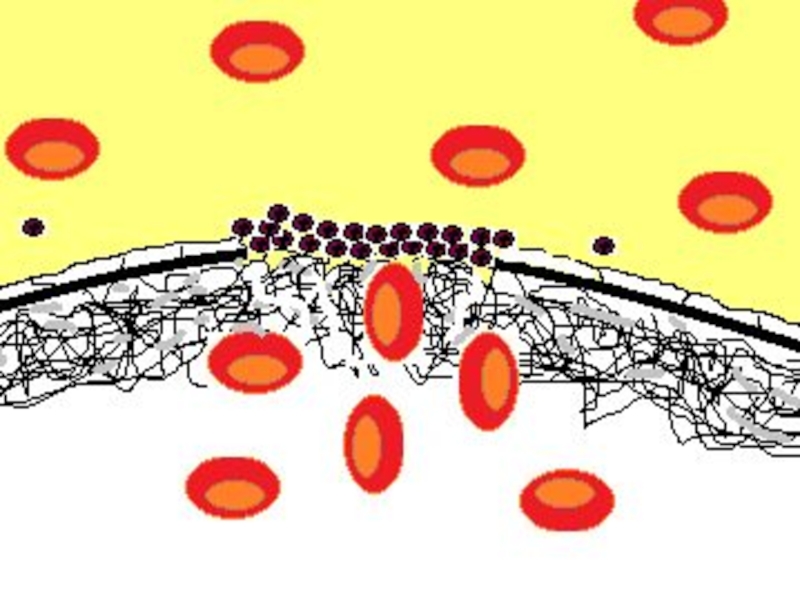
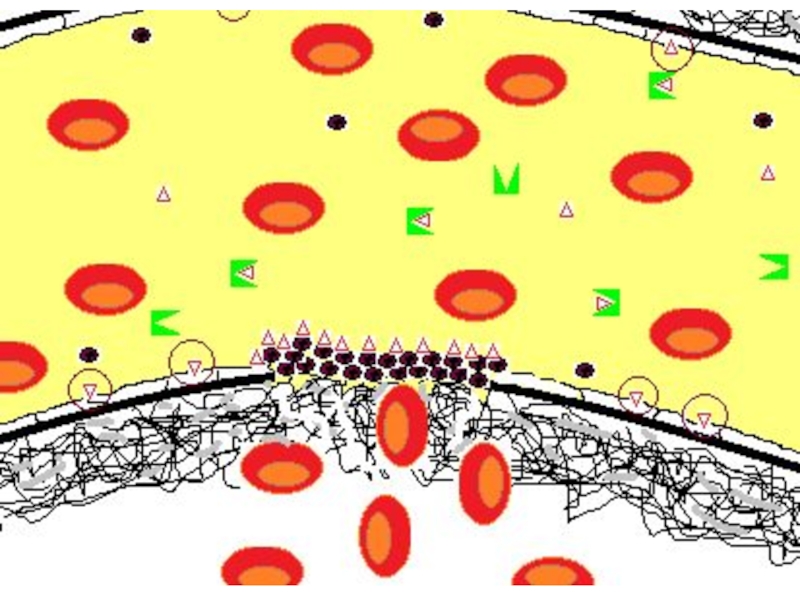
Слайд 48Небольшое («пусковое») количество тромбина активирует тромбоциты. Начинается процесс их адгезии и
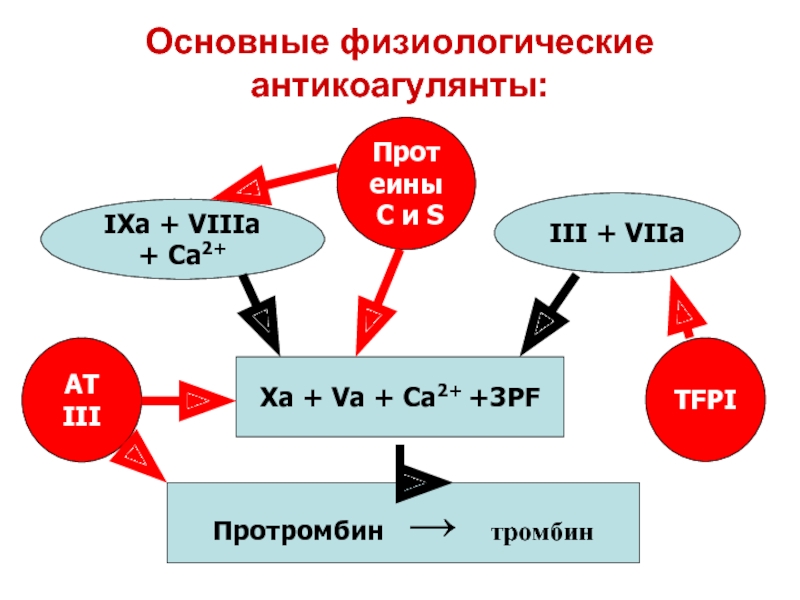
Слайд 50Основные физиологические антикоагулянты:
Xa + Va + Ca2+ +3PF
Протромбин →
IXa + VIIIa + Ca2+
III + VIIa
АТ III
TFPI
Протеины
C и S