- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Разработка метода клинического исследования фармацевтических препаратов с использованием тканевого инжиниринга презентация
Содержание
- 1. Разработка метода клинического исследования фармацевтических препаратов с использованием тканевого инжиниринга
- 2. Цель: разработать метод клинического исследования фармацевтических препаратов с использованием тканевого инжиниринга.
- 3. Задачи:
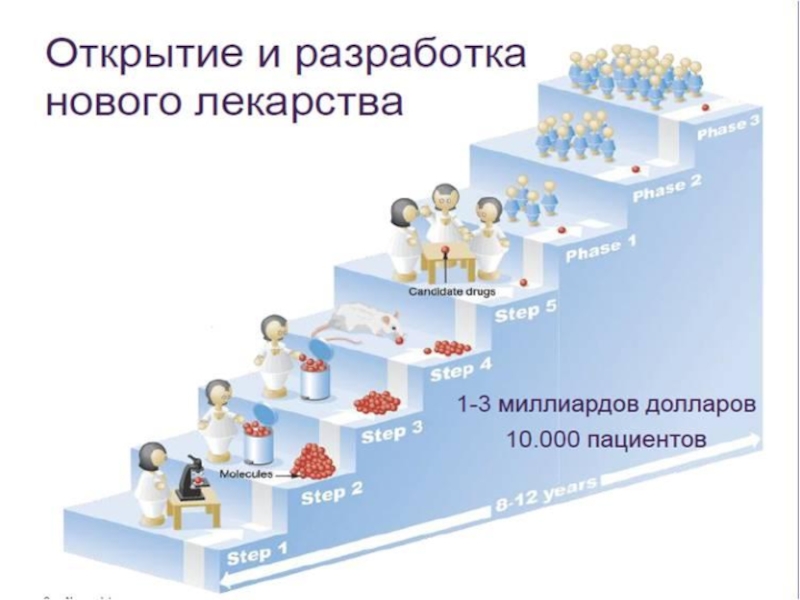
- 4. Разработка лекарственных средств включает в себя
- 5. Этапы создания лекарственного средства:
- 6. Slide Title Product A Feature 1 Feature
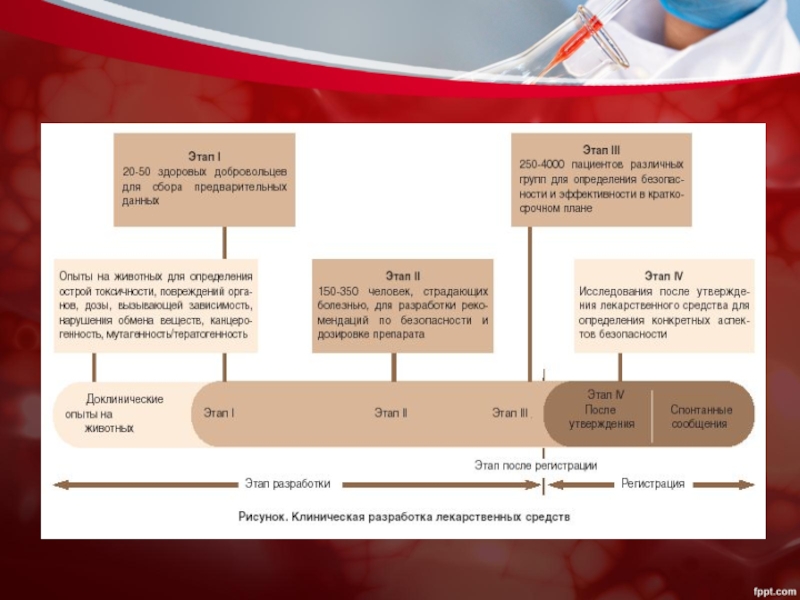
- 7. Клиническое исследование (испытание) любое систематическое исследование
- 9. Фаза І ИССЛЕДОВАНИЯ: Первичные испытания средств на
- 10. Фаза ІI ИССЛЕДОВАНИЯ: Испытания на больших группах
- 11. Фаза ІII ИССЛЕДОВАНИЯ: Крупномасштабные клинические исследования на
- 12. Фаза ІV ИССЛЕДОВАНИЯ: Постмаркетинговые. ЦЕЛЬ: 1.Выявление
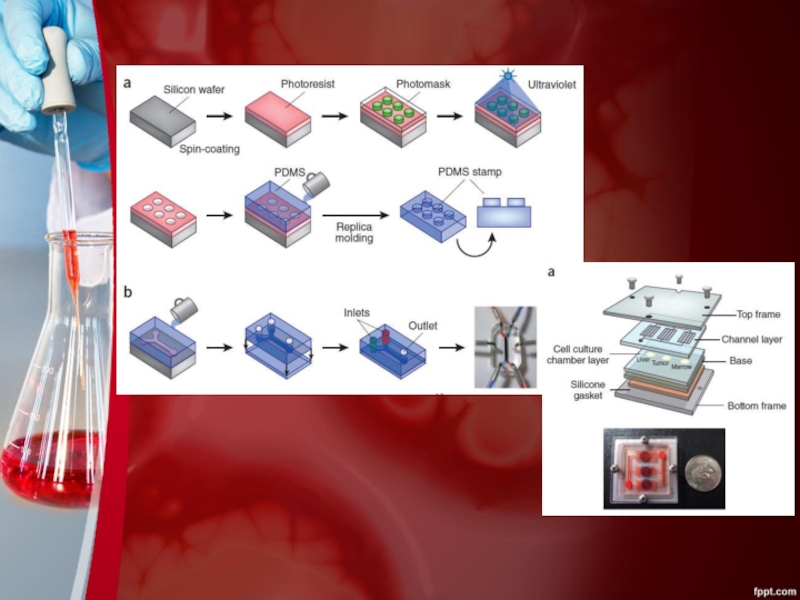
- 13. Суть предлагаемой методики Органы-на-чипах являются микрожидкостными приборами
- 15. Перспективы методики: Обеспечение точной альтернативы традиционным испытаниям
- 16. Преимущества: Достижение высокого разрешения в микроскопических системах
- 17. Недостатки: Невозможно полностью смоделировать все функции органа;
- 18. Вывод Предложенная методика воспроизведения живых органов на
- 19. СПАСИБО ЗА ВНИМАНИЕ!
Слайд 2Цель:
разработать метод клинического исследования фармацевтических препаратов с использованием тканевого инжиниринга.
Слайд 4Разработка лекарственных средств
включает в себя поиск новых фармакологически активных веществ, последующее
изучение их лекарственных свойств, доклинические исследования, разработку технологий производства фармацевтических субстанций, разработку составов и технологий производства лекарственных препаратов.
Слайд 7Клиническое исследование (испытание)
любое систематическое исследование медицинского продукта с участием людей в
качестве субъектов (пациентов или здоровых добровольцев) с целью оценки его фармакокинетики, эффективности и безопасности.
Слайд 9Фаза І
ИССЛЕДОВАНИЯ:
Первичные испытания средств на людях, обычно здоровых добровольцах.
ЦЕЛЬ:
1.Обеспечить необходимый уровень
безопасности лекарственного средства;
2.Установить фармокинетический профиль лекарственного средства.
2.Установить фармокинетический профиль лекарственного средства.
Слайд 10Фаза ІI
ИССЛЕДОВАНИЯ:
Испытания на больших группах людей,страдающих определенным заболеванием.
ЦЕЛЬ:
1.Установить эффективность лекарственного средства
у пациентов с исследуемым заболеванием или синдромом;
2.Оценить краткосрочную безопасность лекарственного средства;
3.Определить терапевтическую дозировку.
2.Оценить краткосрочную безопасность лекарственного средства;
3.Определить терапевтическую дозировку.
Слайд 11Фаза ІII
ИССЛЕДОВАНИЯ:
Крупномасштабные клинические исследования на более крупных группах больных разного возраста,
с разными сопутствующими заболеваниями.
ЦЕЛЬ:
Получение данных о безопасности и эффективности лекарственного средства с целью оценки показателя «риск/польза».
ЦЕЛЬ:
Получение данных о безопасности и эффективности лекарственного средства с целью оценки показателя «риск/польза».
Слайд 12Фаза ІV
ИССЛЕДОВАНИЯ:
Постмаркетинговые.
ЦЕЛЬ:
1.Выявление отличий нового лекарственного препарата от других в данной фармгруппе;
2.Сравнение
его эффективности с аналогами;
3.Демонстрация экономичности препарата.
3.Демонстрация экономичности препарата.
Слайд 13Суть предлагаемой методики
Органы-на-чипах являются микрожидкостными приборами для культивирования живых клеток в
постоянно кровоснабжающихся камерах для моделирования физиологических функций тканей и органов.
Цель данной разработки не в том, чтобы построить целый живой орган, а скорее, чтобы синтезировать минимальные функциональные единицы, которые отображают тканевой и органный уровень функции.
Цель данной разработки не в том, чтобы построить целый живой орган, а скорее, чтобы синтезировать минимальные функциональные единицы, которые отображают тканевой и органный уровень функции.
Слайд 15Перспективы методики:
Обеспечение точной альтернативы традиционным испытаниям на животных, которые часто не
в состоянии предсказать человеческие ответы;
Исследования эффектов новых лекарств-кандидатов для безопасности и эффективности препарата в тканях человека;
Проверка безопасности косметики;
Тест на токсичность химических веществ;
Разработка вакцин и препаратов для противодействия угрозам биотерроризма.
Исследования эффектов новых лекарств-кандидатов для безопасности и эффективности препарата в тканях человека;
Проверка безопасности косметики;
Тест на токсичность химических веществ;
Разработка вакцин и препаратов для противодействия угрозам биотерроризма.
Слайд 16Преимущества:
Достижение высокого разрешения в микроскопических системах для визуализации процессов;
Отображение в реальном
времени событий молекулярного уровня;
Облегчение вычислительного моделирования жидких динамических взаимодействий среди различных газов, метаболитов и клеток, которые неизменно воздействуют на жизнеспособность клетки и ее функцию;
Способность управлять средой клетки, что позволяет усилить ее дифференцировку и выживаемость.
Облегчение вычислительного моделирования жидких динамических взаимодействий среди различных газов, метаболитов и клеток, которые неизменно воздействуют на жизнеспособность клетки и ее функцию;
Способность управлять средой клетки, что позволяет усилить ее дифференцировку и выживаемость.
Слайд 17Недостатки:
Невозможно полностью смоделировать все функции органа;
Сложность в воспроизведении пространственной неоднородности ткани;
Технические
проблемы.
Слайд 18Вывод
Предложенная методика воспроизведения живых органов на микрожидкостных чипах является наиболее перспективной
и оптимальной для клинического исследования фармпрепаратов.
Но все же стоит отметить, что данная методика имеет и существенные недостатки, которые не позволяют внедрить ее в использование и гарантировать полную замену клинических испытаний на людях.
Итак, полная замена клинических исследований фармпрепаратов на эксперименты на животных тканях НЕВОЗМОЖНА, поскольку такие эксперименты являются острыми .
Но все же стоит отметить, что данная методика имеет и существенные недостатки, которые не позволяют внедрить ее в использование и гарантировать полную замену клинических испытаний на людях.
Итак, полная замена клинических исследований фармпрепаратов на эксперименты на животных тканях НЕВОЗМОЖНА, поскольку такие эксперименты являются острыми .