- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Патофизиология клетки презентация
Содержание
- 1. Патофизиология клетки
- 2. Клетка – один из гистоло-гических элементов
- 3. Для своего роста, дифференци-ровки
- 4. Клетка является элементар-ной частицей живых систем
- 5. Первая научная теория о
- 6. В настоящее время, несмо-тря на
- 7. В последнее время, благо-даря стремительному раз-витию
- 8. Прояснились многие вопросы о слож-ных сигнальных
- 9. Любая клетка
- 10. Гомеостаз (от греч. homos –
- 11. Понятие «гомеостаз клетки» вклю-чает в
- 12. Внутриклеточная концентрация ио-нов Са2+ (практически нет
- 13. Факторы, влияющие на константы гомеостаза клетки
- 14. Факторы, влияющие на константы гомеостаза клетки
- 15. При взаимодействии клетки
- 16. Причины развития адаптивных (приспособительных) реакций
- 17. Адаптация клетки Несмотря на
- 18. Различные патогенные факторы,
- 19. Причины повреждения клеток
- 20. Причины повреждения клеток
- 21. Причины повреждения клеток
- 22. Причины повреждения клеток
- 23. Причины повреждения клеток
- 24. Варианты действия патогенных факторов на клетку
- 25. Примеры опосредованного действия на клетку
- 26. Опосредованные повреждения реализуются через: систему
- 27. Повреждение клетки может быть
- 28. Типы (виды) повреждения клетки В
- 29. Типы (виды) повреждения клетки В зависимости
- 30. Типы (виды) повреждения клетки В зависимости
- 31. Типы (виды) повреждения клетки Неспецифические повреждения
- 32. Выявление конкретного спектра специфических
- 33. Патогенетические варианты повреждения клеток
- 34. Патогенетические варианты повреждения клеток
- 35. Механизмы клеточных повреждений при
- 36. Основные механизмы повреждения клеток Расстройства энергетического
- 37. Механизмы нарушения энергообеспечения в повреждённой клетке
- 38. Нарушения ресинтеза АТФ Дефицит кислорода и/или
- 39. Транспорт энергии АТФ в клетке Митохондрии,
- 40. Нарушение транспорта энергии АТФ в клетке
- 41. Нарушение использования энергии АТФ
- 42. Повреждение клеточных мембран и ферментов Компоненты
- 43. Механизмы повреждения мембран клетки Действие патогенных
- 44. Свободные радикалы-окислители В процессе
- 45. Свободнорадикальные процессы и реакции
- 46. Свободнорадикальное перекисное окисление липидов (СПОЛ) Регуляция
- 47. Чрезмерная активация свободнорадикальных и перекисных
- 48. Чрезмерной активации сво-боднорадикальных и
- 49. Значительная активация гидролаз
- 50. Патогенный фактор Активация гидролаз ↑ Активности
- 51. Внедрение амфифильных соединений в мембрану
- 52. Расстройства реакций обновления мембран Действие повреждающего
- 53. Нарушения конформации макромолекул Нарушение энергообеспечения клеток
- 54. Перерастяжение и разрыв клеточных мембран Расстройства
- 55. Дисбаланс ионов и воды в клетке
- 56. Направление градиентов и содержание отдельных ионов
- 57. Дисбаланс ионов и воды в клетке
- 58. Последствия ионного дисбаланса Ионный дисбаланс Гипергидратация
- 59. Генетические нарушения
- 60. Генетические нарушения в клетке
- 61. Генетические нарушения в клетке Действие патогенных
- 62. Расстройства регуляции функций клеток Нарушения
- 63. Расстройства регуляции функций клеток
- 64. Межклеточные информационные сигналы Сигналы
- 65. Межклеточные информационные сигналы Сигналы
- 66. Рецепторы Схематическое представление клеточной мембраны:
- 67. Расстройства взаимодействия БАВ с рецепторами
- 68. Механизмы нарушения взаимодействия БАВ с рецепторами
- 69. Вторые посредники Внутриклеточные сигнальные
- 70. Расстройства регуляции функции на уровне вторых
- 71. Ответы клеток-мишеней Функции клеток
- 72. Расстройства регуляции функции на уровне ответа
- 73. Типовые формы патологии клетки Дистрофии
- 74. Дистрофии клеток Клеточные дистрофии
- 75. Механизмы дистрофии клеток Синтез аномальных, в
- 76. Виды дистрофий в зависимости от преимущественно
- 77. Дисплазии клеток Дисплазии –
- 78. Дисплазии клеток Дифференцировка клеток
- 79. Примеры дисплазии Образование мегалоблас-тов
- 80. Примеры метаплазии Фиброзно-кистозная бо-лезнь
- 81. Гибель клетки Развитие организма,
- 82. Формы клеточной гибели Некроз Апоптоз
- 83. Некроз Некроз (от греч.
- 84. Некроз
- 85. Значение некроза Значение
- 86. Значение некроза Клинические проявления некроза
- 87. Апоптоз Апоптоз (от греч.
- 88. Апоптоз: программу апоптоза запускает ин-формационный сигнал,
- 89. Апоптоз
- 90. Апоптоз Некроз
- 91. Значение апоптоза Поддержание нормальных про-цессов морфогенеза.
- 92. Значение апоптоза Поддержание клеточного гомео-стаза. Клетки,
- 93. Значение апоптоза Дегенерация. При некоторых пато-логических
- 94. Значение апоптоза Селекция разновидностей клеток внутри
- 95. Значение апоптоза Старение Гормонозависимая инволюция
- 96. Значение апоптоза Повреждение клетки. Воздействие на
- 97. Патология, связанная с нарушением апоптоза
- 98. Патология, связанная с нарушением апоптоза
- 99. Механизмы адаптации клеток к повреждению Внутриклеточные
- 100. Механизмы адаптации клеток к повреждению Внутриклеточные
- 101. Механизмы адаптации клеток к повреждению Межклеточные
- 102. СПАСИБО ЗА ВНИМАНИЕ!
Слайд 1
ДОНЕЦКИЙ НАЦИОНАЛЬНЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
Кафедра физиологии и патологической физиологии
ПАТОФИЗИОЛОГИЯ
КЛЕТКИ
Лектор:
зав. кафедрой
проф. С.В.
Слайд 2
Клетка – один из гистоло-гических элементов орга-
низма.
Человеческий организм
стоит из 107 клонов кле-
ток, включающих около
60 триллионов единиц.
Выполнение работы того или иного органа в конечном счёте определяет-ся структурно-функциональным со-стоянием данных элементарных обра-зований.
Слайд 3
Для своего роста, дифференци-ровки (специализации), функци-онирования, приспособления и выживания
поддерживает собственный гомеостаз,
осуществляет обмен веществ и энергии,
реализует генетическую информацию и передает её потомству,
синтезирует компоненты межклеточно-го вещества,
прямо или опосредованно (через другие гистологические элементы) участвует в вы-полнении всех функций организма.
Слайд 4
Клетка является элементар-ной частицей живых систем любого уровня, но и сама
Поэтому повреждение клетки или группы клеток, нарушая естественную их интеграцию и кооперацию в органе и ор-ганизме, служит материаль-ной основой развивающейся патологии.
Слайд 5
Первая научная теория о роли клеточных наруше-ний в патологии
Слайд 6
В настоящее время, несмо-тря на то, что клеточные повреждения являются,
Слайд 7
В последнее время, благо-даря стремительному раз-витию молекулярной био-логии, цитологии, биофи-зики, биохимии
Появилась реальная воз-можность введения генов в клетку для исправления поврежденных наследст-венных механизмов.
Слайд 8
Прояснились многие вопросы о слож-ных сигнальных системах и взаимодей-ствиях, регулирующих рост,
Все эти достижения позволили переос-мыслить возникновение, развитие и ис-ходы многих заболеваний на качествен-но новом уровне – клеточно-молекуляр-ном.
Слайд 9
Любая клетка
либо функционирует
в
(гомеостаз),
либо приспосаблива-
ется к жизнедеятель-
ности в экстремальных условиях (адаптация),
либо гибнет при превышении её адаптивных возможностей (нек-роз) или воздействии соответст-вующего сигнала (апоптоз).
Слайд 10
Гомеостаз (от греч. homos – один и тот же, одинаковый
Гомеостаз – оптимальный метаболи-ческий уровень нормальной клетки, соответствующий условиям (требова-ниям) среды.
Слайд 11
Понятие «гомеостаз клетки» вклю-чает в себя ряд показателей (констант): внутриклеточное
Наиболее критичны для клеточного гомеостаза:
Внутриклеточная концентрация ионов
Na+ (существенно меньше, чем вне клетки).
Внутриклеточная концентрация ионов
К+ (больше, чем в межклеточном пространстве).
Слайд 12
Внутриклеточная концентрация ио-нов Са2+ (практически нет в цитоплазме, от-куда Са2+ постоянно
Внутриклеточная концентрация ио-нов Н+ (рН около 7,2).
Внеклеточная концентрация ионов Na+ (существенно больше, чем в клетке).
Внеклеточная концентрация ионов К+ (меньше, чем в клетке).
рО2.
Наиболее критичны для клеточного гомеостаза:
Слайд 13
Факторы, влияющие на константы гомеостаза клетки
Структурно-функциональное со-стояние различных мембран клетки
Это своеобразная «метаболическая составляющая гомеостаза», которая определяется работой исполнитель-ного аппарата клетки.
Слайд 14
Факторы, влияющие на константы гомеостаза клетки
Информационные процессы. «Правильность» изменения констант
Это «информационная составляющая гомеостаза».
Исполнительный аппарат клетки выполня-ет лишь «полученные указания».
Слайд 15
При взаимодействии клетки с различ-ными физиологическими стимулами происходит переход
Параметры гомеостаза не выходят за пределы максимально допустимых значений, а метабо-лическая активность и функциональные воз-можности клетки могут значительно повыша-ться. Такой ответ называется адаптацией клетки.
Адаптация (от лат. adaptatio – приспособле-ние) – перестройка жизнедеятельности и структур клетки в ответ на измене-ния условий существования.
Слайд 16
Причины развития адаптивных (приспособительных)
реакций клеток
Однократное воздействие поврежда-ющего фактора.
Влияние постоянно и/или
Воздействие информационных сигна-лов на клетку (или отсутствия таких сигналов).
Слайд 17
Адаптация клетки
Несмотря на существование мно-жества разных типов клеток, адаптивные
набухания клеток и клеточных струк-тур,
гипо- или гиперфункции клеток и клеточных структур,
атрофии или гипертрофии,
гиперплазии,
метаплазии.
Слайд 18
Различные патогенные факторы, дей-ствующие на клетку, могут обусловить её
Повреждение клетки – типический патологический процесс, основу кото-рого составляют нарушения внутри-клеточного гомеостаза, приводящие к нарушению структурной целостности клетки и её функциональных способно-стей.
Слайд 19
Причины повреждения клеток
Классификация по природе патогенных факторов:
Физические факторы
Механические воздействия.
Термические воздействия.
Изменения осмотического давления в клетках.
Действие ионизирующей и ультрафиолетовой радиации.
Слайд 20
Причины повреждения клеток
Классификация по природе патогенных факторов:
Химические факторы
Органические и неорганические кислоты и щёлочи.
Соли тяжёлых металлов.
Цитотоксические соединения и лекарственные средства.
Слайд 21
Причины повреждения клеток
Классификация по природе патогенных факторов:
Биологические факторы
Инфекционные агенты как сами по себе, так и в виде продуктов их жизнедеятельности или деграда-ции.
Цитотоксические факторы системы иммунобиологического надзора.
Чрезмерно высокая или низкая функциональная нагрузка.
Слайд 22
Причины повреждения клеток
Классификация в зависимости от происхождения патогенных
Экзогенные факторы повреждения клетки
Физические воздействия.
Химические агенты.
Биологические факторы.
Эндогенные факторы повреждения клетки
Агенты физической природы.
Химические факторы.
Агенты биологической природы.
Слайд 23
Причины повреждения клеток
Классификация в зависимости от происхождения патогенных
Инфекционно-паразитарные факто-ры:
Эндо- и экзотоксины микроорганиз-мов.
Многоклеточные и одноклеточные паразиты.
Факторы неинфекционного генеза: агенты физической, химической или биологической (но не инфекционной) природы.
Слайд 24
Варианты действия патогенных факторов на клетку
Прямое (непосредственное, первичное) – возникает в
Опосредованное (косвенное, вторич-ное) – возникает как следствие первич-ных нарушений постоянства внутренней среды организма.
В условиях целостного организма первичное дей-ствие повреждающего фактора на клетки-мишени сопровождается изменениями и в других клетках. Эти изменения обусловлены нарушением функци-онирования клеток-мишеней.
Слайд 25
Примеры опосредованного действия на клетку патогенных факторов:
Изменения нервных или эндокринных
Нарушения системного кровообращения (при СН).
Отклонения физико-химических параметров (при состояниях, сопровождающихся ацидозом, алкалозом, образованием СР, продуктов СПОЛ, дисбалансом ионов и воды).
Развитие иммунных и аллергических реак-ций.
Образование избытка или недостаток БАВ (факторов системы комплемента, гистамина, кининов, Пг, циклических нуклеотидов).
Слайд 26
Опосредованные повреждения реализуются через:
систему медиаторов,
нарушения циркуляции оксигениро-ванной крови в малом
нарушения нейрогуморальной регуля-ции,
изменения иммунного статуса,
изменения параметров жёстких кон-стант гомеостаза.
Слайд 27
Повреждение клетки может быть резу-льтатом действия не только патоген-ных
Пример: гибель эпидер-
миса, эпителия кишечни-
ка, эритроцитов и других
клеток в результате про-
цесса их старения.
К механизмам старения и смерти клетки относят постепенное необратимое изменение структуры мембран, ферментов, нуклеиновых кислот, истоще-ние субстратов метаболических реакций, снижение устойчивости клеток к патогенным воздействиям.
Слайд 28
Типы (виды) повреждения клетки
В зависимости от скорости разви-тия основных проявлений
Острое повреждение. Развивается быст-ро, и, как правило, в результате однократ-ного, но интенсивного повреждающего воздействия.
Хроническое повреждение протекает медленно и является следствием много-кратного влияния, но менее интенсивного по силе повреждения агента.
Слайд 29
Типы (виды) повреждения клетки
В зависимости от жизненного цикла клетки:
Митотические повреждения.
Интерфазные повреждения.
В зависимости от степени (глубины) нарушения клеточного гомеостаза:
Обратимые повреждения.
Необратимые повреждения
В зависимости от характера взаимодей-ствия повреждающего фактора с клеткой:
Прямые повреждения.
Опосредованные повреждения.
Слайд 30
Типы (виды) повреждения клетки
В зависимости от характера поврежде-ний вызванных определенным пато-генным
Специфические повреждения – это на-рушения, вызванные определенным пато-генным фактором конкретных структурно-молекулярных компонентов клетки или ме-ханизмов её информационного обеспечения.
Для механического причинного фактора специ-фическое повреждение – нарушение целостности структур клеток.
Холерный экзотоксин активирует образование циклического аденозинмонофосфата (цАМФ) в эпителии тонкого кишечника.
Слайд 31
Типы (виды) повреждения клетки
Неспецифические повреждения – это стандартные, стереотипные изменения в
повышение проницаемости мембран клеток;
активация свободно-радикальных и пере-кисных реакций;
внутриклеточный ацидоз;
денатурация молекул белков;
дисбаланс ионов и воды;
увеличение объёма (набухание) клеток;
снижение мембранного потенциала.
Слайд 32
Выявление конкретного спектра специфических и неспецифических измене-ний в клетках
Слайд 33
Патогенетические варианты повреждения клеток
Насильственное повреждение развивается при действии на
Слайд 34
Патогенетические варианты повреждения клеток
Цитопатический вариант возни-кает в результате первичного
Факторами, запускающими патогенетические механизмы повреждения, являются естест-венные для данной клетки возмущающие стимулы, которые в этих условиях стано-вятся повреждающими.
К цитопатическому варианту относятся все виды по-вреждения клетки, вызываемые отсутствием каких-либо необходимых ей компонентов (при гипоксии, го-лодании, гипо- и авитаминозах, антиоксидантной недоста-точности, генетических дефектах, нервно-трофическое повреждение и др.).
Слайд 35
Механизмы клеточных повреждений при дейст-вии различных этиологи-ческих факторов тесно
Любой причинный фактор обусловливает, как правило, несколько механизмов по-вреждения.
Вот почему изолированное выделение отдельных пато-генетических механизмов оправдано лишь с точки зре-ния удобства их рассмотре-ния и понимания.
Слайд 36
Основные механизмы повреждения клеток
Расстройства энергетического обеспечения клетки
Повреждение мембран и ферментов
Дисбаланс ионов и воды в клетке
Нарушения в геноме и/или механизмов экспрессии генов
Расстройства регуляции функций клеток
Слайд 37
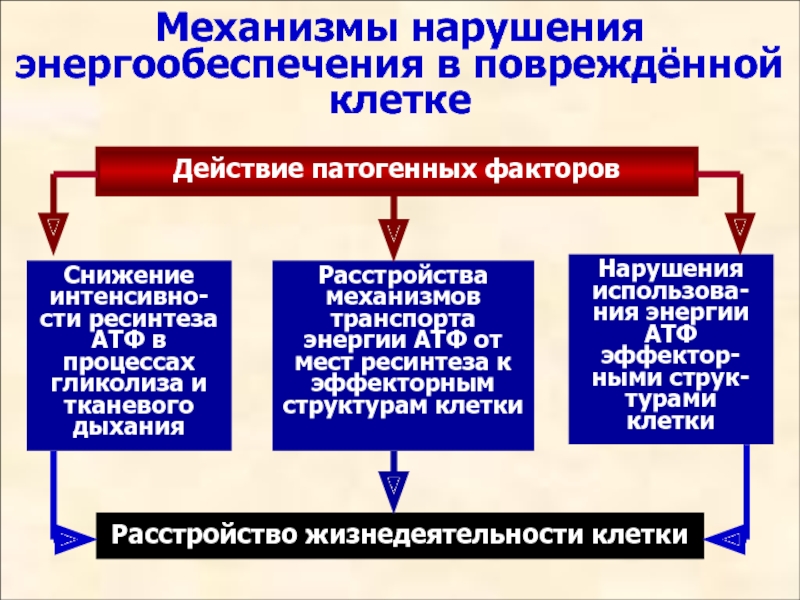
Механизмы нарушения энергообеспечения в повреждённой клетке
Действие патогенных факторов
Снижение интенсивно-сти ресинтеза АТФ
Расстройства механизмов транспорта энергии АТФ от мест ресинтеза к эффекторным структурам клетки
Нарушения использова-ния энергии АТФ эффектор-ными струк-турами
клетки
Расстройство жизнедеятельности клетки
Слайд 38
Нарушения ресинтеза АТФ
Дефицит кислорода и/или субстратов метаболизма
Снижение активности ферментов тканевого дыхания
Повреждение и разрушение митохон-дрий (в которых осуществляются реакции цикла Кребса и перенос электронов к мо-лекулярному кислороду, сопряжённый с фосфорилированием АДФ).
Слайд 39
Транспорт энергии АТФ в клетке
Митохондрии, цитозоль
Ресинтез АТФ
Эффекторные структуры:
миофибриллы, мембранные ионные насосы
АТФ
Креатинфосфокиназа (КФК)
Адениннуклеотидил-
трансфераза
Слайд 40
Нарушение транспорта энергии АТФ в клетке
Системы транспорта энергии могут быть поврежде-ны
Слайд 41
Нарушение использования энергии АТФ
Нарушения энергообеспечения клеток и расстройства их
АТФазы миозина,
Na+,К+-АТФазы плазмолеммы,
протонной и калиевой АТФазы,
Са2+-АТФазы [Са2+-насос] и др.
Следовательно, расстройство жизнедеятель-ности клеток может развиваться даже в ус-ловиях нормального или повышенного со-держания в клетке АТФ.
Слайд 42
Повреждение клеточных мембран и ферментов
Компоненты клеточной мембраны
Повреждение клеточных мембран и ферментов
Слайд 43
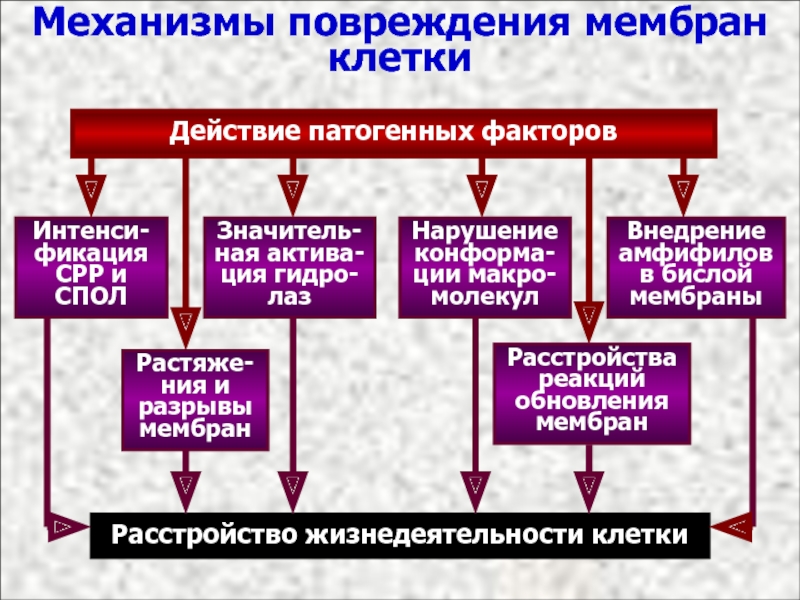
Механизмы повреждения мембран
клетки
Действие патогенных факторов
Значитель-ная актива-ция гидро-лаз
Нарушение конформа-ции макро-молекул
Растяже-ния и разрывы
Интенси-фикация СРР и СПОЛ
Расстройства реакций обновления мембран
Расстройство жизнедеятельности клетки
Внедрение амфифилов в бислой мембраны
Слайд 44
Свободные радикалы-окислители
В процессе нормальной жизнедеятель-ности организма постоянно образуют-ся активные
Радикалы имеют нечетное количество элект-ронов (свободная валентность) и легко вступа-ют в различные химические реакции.
Отнимая электроны у различных органических мо-лекул, они тем самым, изменяют их свойства.
Слайд 45
Свободнорадикальные процессы и реакции СПОЛ – необходимое звено таких
транспорт электронов в цепи ды-хательных ферментов,
синтез Пг и лейкотриенов,
пролиферация и дифференци-ровка клеток,
фагоцитоз,
метаболизм катехоламинов и др.
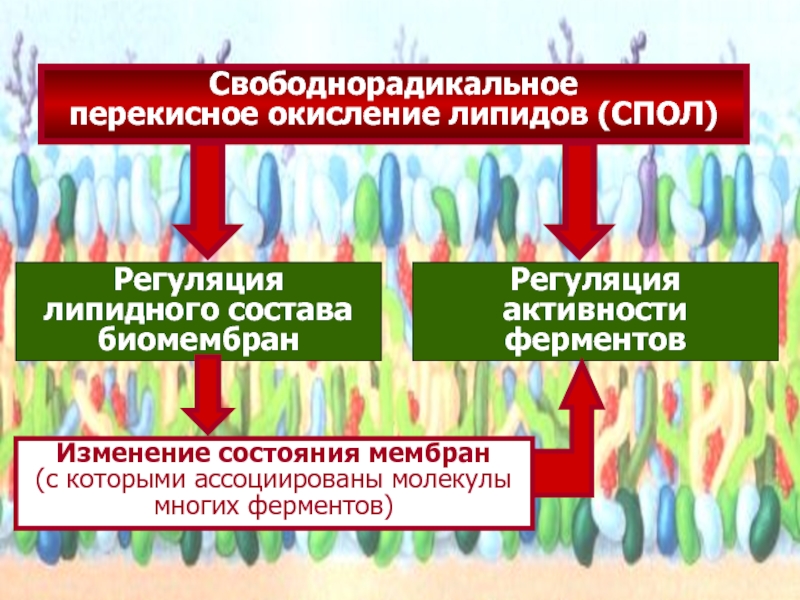
Слайд 46Свободнорадикальное
перекисное окисление липидов (СПОЛ)
Регуляция липидного состава биомембран
Регуляция активности ферментов
Изменение состояния
(с которыми ассоциированы молекулы многих ферментов)
Слайд 47
Чрезмерная активация
свободнорадикальных и перекисных реакций
Изменения физико-химических свойств липидов мембран
Изменения конформации липопротеиновых и белковых комплексов
Ингибирование активности ферментных систем
Образование структур-ных дефектов в мембра-не (т.н. называемых прос-тейших каналов – кластеров)
Нарушен. рецепции и передачи гуморальных воздействий, трансмембранного переноса ионов, генерации и проведения нервных импульсов, обмена в-в, межклеточных взаимодействий
Фрагментация мембран
Гибель клетки
Образование трансмемб-ранных каналов проница-емости (неконтролируемый ток катионов и др. молекул органич. и неорганических веществ в клетку и из неё)
Слайд 48
Чрезмерной активации сво-боднорадикальных и пере-кисных реакций препятству-ют факторы антиоксидант-ной
Одним из таких процессов явля-ется взаимодействие радикалов и гидроперекисей липидов между собой, что ведёт к образованию «нерадикальных» соединений.
Слайд 49
Значительная активация гидролаз
Состав и состояние мембран могут мо-дифицировать
Липазы
мембраносвязанные
лизосомальные
свободные (солюбилизированные)
Фосфолипазы
Протеазы
Слайд 50
Патогенный фактор
Активация гидролаз
↑ Активности и/или содержания в клетке гидролаз
Интенсивный гидролиз фосфолипидов
Значительное повышение проницаемости мембран и снижение кинетических свойств ферментов
Слайд 51
Внедрение амфифильных соединений в мембрану
Активация липопероксидных реакций и гидролаз (главным
Накопление в клетке амфифильных в-в
(гидроперекиси липидов, СЖК, фосфолипиды, в частности глицерофосфолипиды, фосфатидилхолины, фосфатидилэтаноламины, фосфатидилсерины)
Массированное внедрение амфифилов в мембраны
Формирование обширных кластеров и микроразрывов в них
Слайд 52
Расстройства реакций обновления мембран
Действие повреждающего фактора
Существенное подавление репаративного ресинтеза альтерированных или
Недостаточная эффективность восстановления мембран
Потенцирование степени и масштаба повреждения мембранного аппарата клеток
Слайд 53
Нарушения конформации макромолекул
Нарушение энергообеспечения клеток
Отклонения физико-химических парамет-ров клетки от нормы
Изменения
Искажения или потеря их функций, в том числе к подавление каталитической активности ферментов
Значительные изменения физико-химического состояния клеточных мембран
Слайд 54
Перерастяжение и разрыв клеточных мембран
Расстройства клеточного метаболизма
Избыток в клетках гидрофильных молекул
Значительное увеличение осмотического и онкотического давления в клетках
Гипергидратация клеток
Перерастяжение и разрыв мембран набухших клеток и мембранных органоидов
Слайд 55
Дисбаланс ионов и воды в клетке
Ионный дисбаланс характеризуется изменением
В наибольшей мере это относится к К+, Na+, Ca2+, Mg2+, Cl-, т.е. ионам, которые принимают участие в таких жизненно важ-ных процессах, как возбуждение, проведе-ние потенциалов действия (ПД), электроме-ханическое сопряжение и др.
Слайд 56
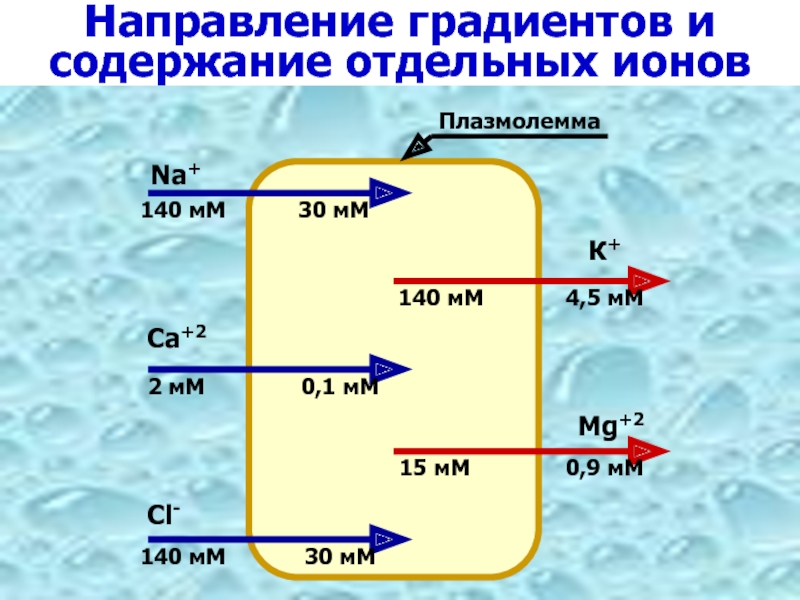
Направление градиентов и содержание отдельных ионов
Na+
140 мМ
30 мМ
Сa+2
2 мМ
0,1 мМ
Сl-
140 мМ
30
К+
Mg+2
140 мМ
4,5 мМ
15 мМ
0,9 мМ
Плазмолемма
Слайд 57
Дисбаланс ионов и воды в клетке
Нарушение работы
Na+-К+-АТФ-азы сарколеммы
Нарушение работы
Na+-Cа+-АТФ-азы сарколеммы
Нарушения работы
Накопление в ци-тозоле избытка Na+
Потеря клеткой К+
Накопление в цитозоле избытка Ca2+
Слайд 58
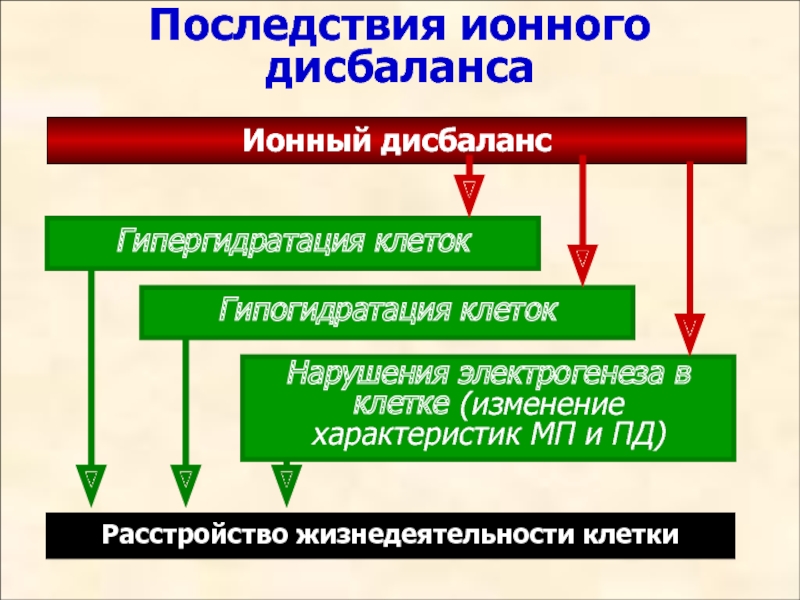
Последствия ионного дисбаланса
Ионный дисбаланс
Гипергидратация клеток
Гипогидратация клеток
Нарушения электрогенеза в клетке (изменение
Расстройство жизнедеятельности клетки
Слайд 59
Генетические
нарушения в клетке
Повреждения ядерного
генома и/или механизмов
экспрессии генов, репли-
кации и репарации ДНК,
клеточного цикла – суще-
ственные механизмы аль-
терации, имеющие далеко
идущие последствия.
Эти повреждения особенно важны для малигнизации клеток и процессов он-когенеза.
Слайд 60
Генетические нарушения в клетке
Повреждение клетки и её гибель могут
Наиболее значимые причины повреж-дений ДНК:
разрушение фрагментов ДНК при воздей-ствии на неё сверхсильных патогенных агентов;
расщепление ДНК при значительной ак-тивации нуклеаз (предсуществующих или синтезирующихся de novo);
деградация ДНК активированными транс-феразами, что сопровождается разрывами межнуклеотидных связей.
Слайд 61
Генетические нарушения в клетке
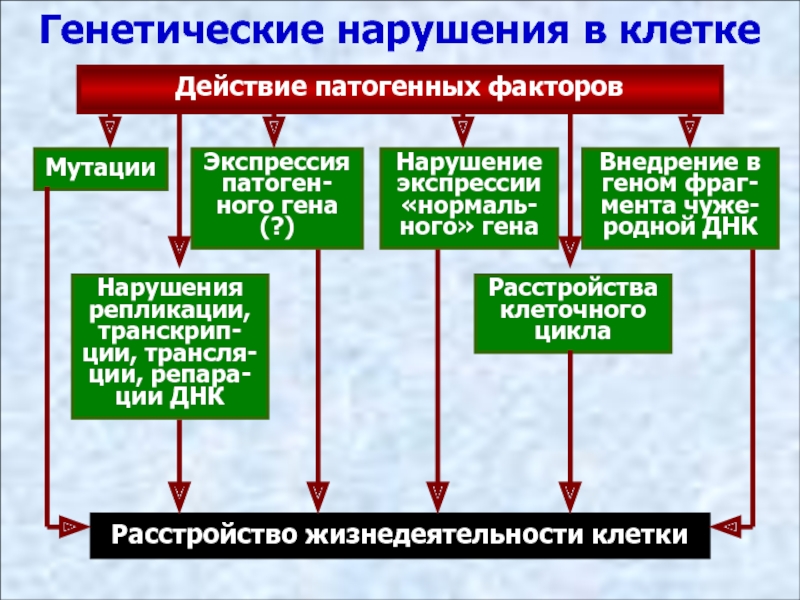
Действие патогенных факторов
Мутации
Экспрессия патоген-ного гена (?)
Нарушение экспрессии «нормаль-ного»
Внедрение в геном фраг-мента чуже-родной ДНК
Нарушения репликации, транскрип-ции, трансля-ции, репара-ции ДНК
Расстройства клеточного цикла
Расстройство жизнедеятельности клетки
Слайд 62
Расстройства регуляции функций клеток
Нарушения жизнедеятельности клетки могут быть результатом расстройств
Слайд 63
Расстройства регуляции функций клеток
Все виды информационных межклеточных взаимодей-ствий
Межклеточные информаци-онные взаимодействия ук-ладываются в следующую схему:
сигнал → рецептор → второй посредник → ответ
Пауль Эрлих
(1854-1915)
Слайд 64
Межклеточные информационные сигналы
Сигналы
Передачу сигналов от клетки к
Специфичность воздействия сигналь-ных молекул определяют рецепторы клетки-мишени, связывающие только собственные лиганды (сигнальные молекулы).
Слайд 65
Межклеточные информационные сигналы
Сигналы
Все лиганды (в зависимости от
Гидрофильные молекулы (нейромедиаторы, цитокины, пептидные гормоны, Аг) не проникают через плазматическую мембрану и связываются с рецепторами плазмолеммы (мембранные рецепто-ры).
Жирорастворимые молекулы (стероидные и тиреоидные гормоны) проникают через плазмо-лемму и связываются с рецепторами внутри клет-ки (ядерные рецепторы).
Слайд 66
Рецепторы
Схематическое представление клеточной мембраны: по липидному «морю» плавают молекулы белковых трансмембранных
Описаны три класса клеточных рецепторов: мембранные,
ядерные,
сиротские.
Слайд 67
Расстройства взаимодействия БАВ с рецепторами
Расстройства взаимодействия БАВ с
Пример: накопление токсичных продуктов СПОЛ при ишемии миокарда изменяет фи-зико-химические свойства мембран. Это сопровождается нарушением реакций сердца на НА и АХ, воспринимающихся ре-цепторами мембраны клеток.
Слайд 68
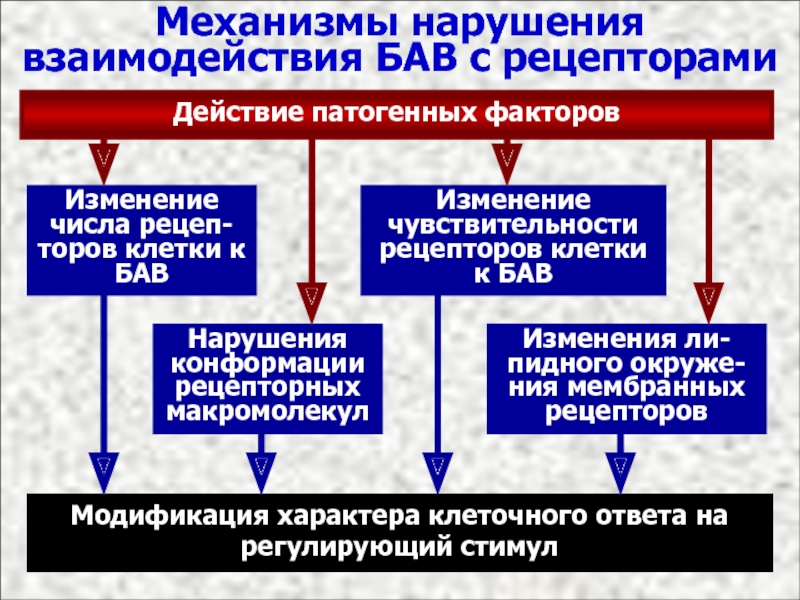
Механизмы нарушения взаимодействия БАВ с рецепторами
Действие патогенных факторов
Изменение числа рецеп-торов клетки
Изменение чувствительности рецепторов клетки к БАВ
Нарушения конформации рецепторных макромолекул
Модификация характера клеточного ответа на регулирующий стимул
Изменения ли-пидного окруже-ния мембранных рецепторов
Слайд 69
Вторые посредники
Внутриклеточные сигнальные мо-лекулы (вторые посредники) переда-ют информацию с
Вторые посредники представлены мно-гочисленным классом соединений:
циклические нуклеотиды (цАМФ и цГМФ),
инозитолтрифосфат,
диацилглицерол,
Са2+.
Слайд 70
Расстройства регуляции функции на уровне вторых посредников
На уровне внутриклеточных
Пример: нарушение формирования МП в кардиомиоцитах при накоплении в них избытка цАМФ (это является од-ной из возможных причин развития аритмий сердца).
Слайд 71
Ответы клеток-мишеней
Функции клеток являются следст-вием реализации генетической ин-формации (например,
изменения характера функциониро-вания,
стимуляция или подавление активно-сти,
перепрограммирование синтезов и т.д.
Слайд 72
Расстройства регуляции функции на уровне ответа на сигнал
На уровне
Пример: нарушение активации клеточ-ных ферментов (например, в связи с де-фицитом цАМФ или цГМФ), может сущест-венно изменить интенсивность метаболи-ческих реакций и как следствие – приве-сти к расстройству жизнедеятельности клетки.
Слайд 73
Типовые формы
патологии клетки
Дистрофии
Дисплазии
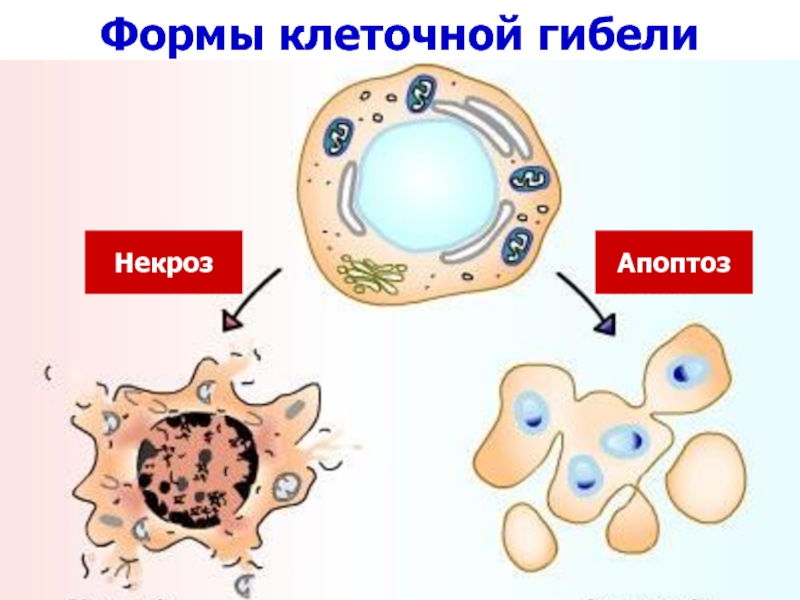
Некроз
Апоптоз
Нарушения отдельных субклеточных структур и компонентов
Слайд 74
Дистрофии клеток
Клеточные дистрофии – нарушения обмена веществ, сопровождающиеся расстройством
Слайд 75
Механизмы дистрофии клеток
Синтез аномальных, в норме не встреча-ющихся в клетке, веществ
Избыточное превращение одних соеди-нений в другие (например, жиров и углеводов в белки, углеводов в жиры).
Декомпозиция (фанероз): распад субкле-точных структур и/или веществ (например, белково-липидных комплексов мембран).
Инфильтрация клеток и межклеточного вещества органическими и неорганиче-скими соединениями (например, ЛПНП и Са2+ клеток интимы артерий при атеросклерозе).
Слайд 76
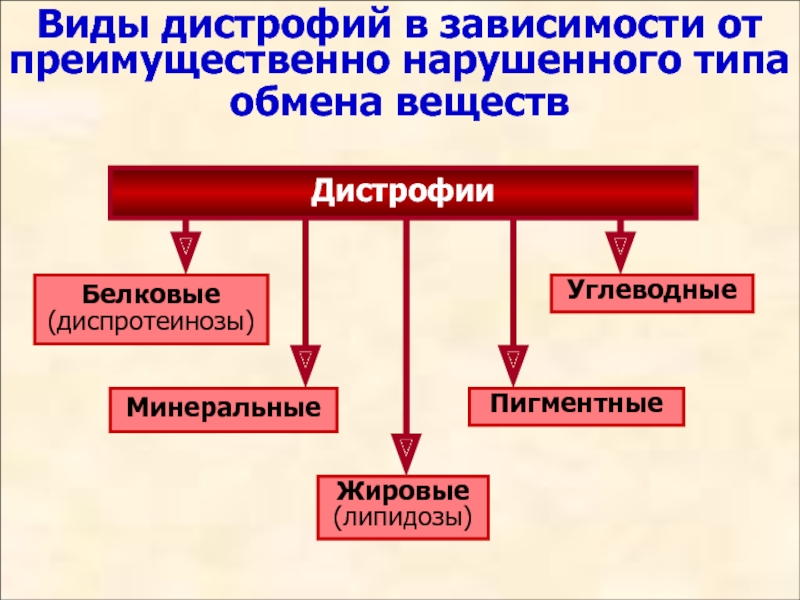
Виды дистрофий в зависимости от преимущественно нарушенного типа обмена веществ
Дистрофии
Белковые
(диспротеинозы)
Минеральные
Жировые
(липидозы)
Пигментные
Углеводные
Слайд 77
Дисплазии клеток
Дисплазии – нарушения дифферен-цировки клеток, сопровождающиеся стойкими изменениями
Среди дисплазии выделяют метапла-зии, характеризующиеся замещением в конкретном органе характерных для него клеток клетками другого типа.
Клеточные дисплазии лежат в основе опу-холевого роста и в клинической практике рассматриваются как предраковые состоя-ния.
Слайд 78
Дисплазии клеток
Дифференцировка клеток определя-ется генетической программой, но ре-ализация этой
При одном и том же отклонении в ге-номе различных клеток проявления дисплазии могут носить «разноликий» характер.
Слайд 79
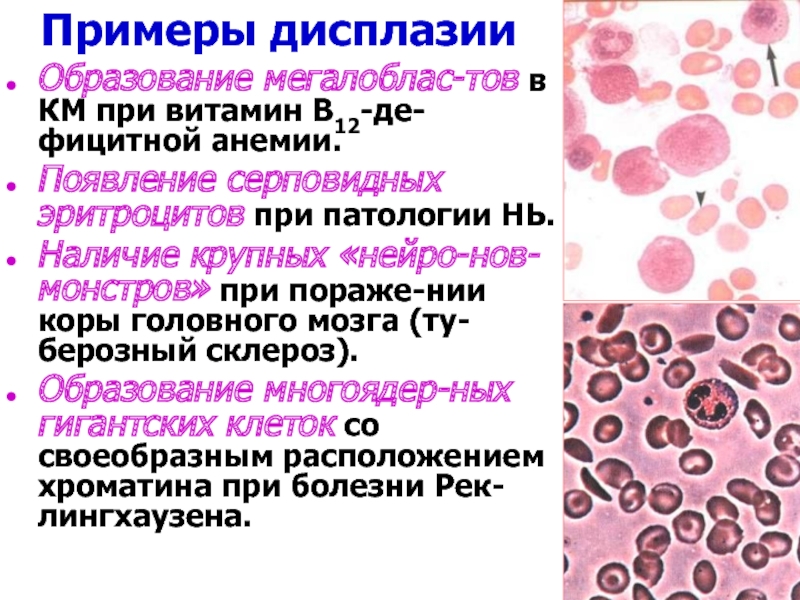
Примеры дисплазии
Образование мегалоблас-тов в КМ при витамин В12-де-фицитной анемии.
Появление серповидных эритроцитов при патологии НЬ.
Наличие крупных «нейро-нов-монстров» при пораже-нии коры головного мозга (ту-берозный склероз).
Образование многоядер-ных гигантских клеток со своеобразным расположением хроматина при болезни Рек-лингхаузена.
Слайд 80
Примеры метаплазии
Фиброзно-кистозная бо-лезнь молочной железы. Появление в грудной железе
Пищевод Баретта. Замещение многослойного плоского эпителия СО пищевода однослойным эпите-лием, характерным для тонкой кишки.
Оссифицирующий миозит. Скелетные мышечные волокна за-мещаются фиброзной тканью, со-держащей очаги костной ткани.
Слайд 81
Гибель клетки
Развитие организма, формирование тканей и их функционирование предпо-лагают
Массовую гибель клеток в раннем онтогенезе называют запрограммиро-ванной.
Клетки, выполнившие свои функ-ции, погибают в течение всей жизни организма.
Клетки гибнут при повреждении и некрозе ткани, при различных заболеваниях, избирательно пора-жающих отдельные типы клеток (дегенерация).
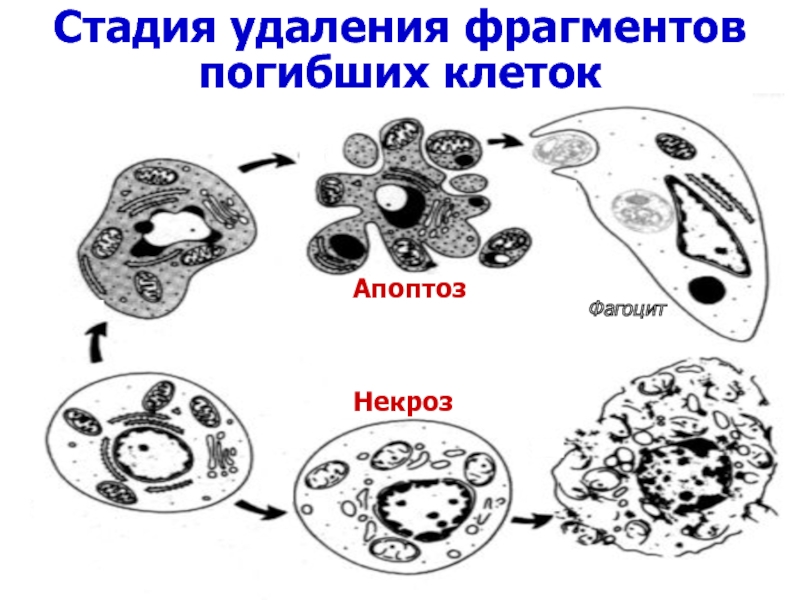
Слайд 83
Некроз
Некроз (от греч. nekros – мертвый) – омертвение, гибель
Некроз:
развивается при чрезмерной альте-рации клетки,
не требует затрат энергии,
генетически не контролируется («анархических путь гибели»),
представляет угрозу окружающим структурам (сопровождается разви-тием воспалительного процесса).
Слайд 85
Значение некроза
Значение некроза определяется его сущностью – «местной
Некроз жизненно важных органов, особен-но крупных участков их, нередко ведет к смерти (инфаркты миокарда, ишемические нек-розы головного мозга, некрозы коркового веще-ства почек, острый панкреатит, осложнившийся панкреонекрозом).
Некроз является причиной тяжёлых ослож-нений многих заболеваний (разрыв сердца при миомаляции, параличи при геморрагическом и ишемическом инсультах, инфекции при массив-ных пролежнях, интоксикации в связи с воздей-ствием на организм продуктов тканевого распада и т.д.).
Слайд 86
Значение некроза
Клинические проявления некроза могут быть самыми разнообразными:
Патологическая электрическая активность,
Нарушение перистальтики в некротизиро-ванной кишке может вызвать функциональ-ную (динамическую) кишечную непроходи-мость.
Часто наблюдаются кровоизлияния в некро-тизированную ткань, например, кровохар-кание (hаemoptysis) при некрозе лёгкого.
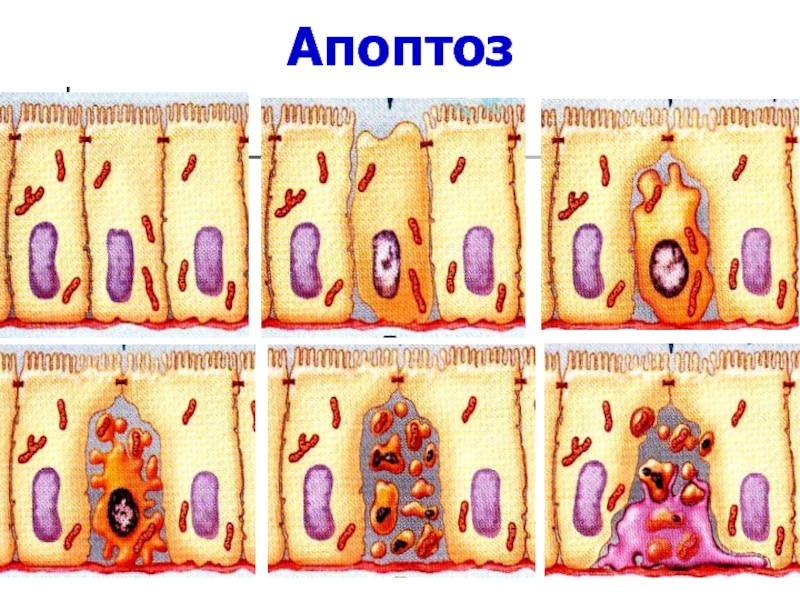
Слайд 87
Апоптоз
Апоптоз (от греч. apoptosis – «отпадаю-щий») – форма гибели
ток, возникающая под
действием вне- или
внутриклеточных фак-
торов, осуществляю-
щаяся путём активации
специализированных
внутриклеточных про-
цессов, регулируемых
определёнными гена-
ми.
Апоптоз — программированная гибель клетки.
Слайд 88
Апоптоз:
программу апоптоза запускает ин-формационный сигнал,
энергозависим и требует синтеза РНК и белков,
завершается
не сопровождается развитием воспа-лительного процесса,
наблюдается в ходе многих естест-венных процессов, а также при адап-тации клетки к повреждающим фак-торам.
Слайд 91
Значение апоптоза
Поддержание нормальных про-цессов морфогенеза. Запрограмми-рованная гибель клеток – естествен-ный процесс
Формирование частей тела в результате отмира-ния ненужных участков тканей (формирование ладоней путём разрушения клеток в межпальце-вых промежутках).
Запрограммированная гибель нейробластов (от 25 до 75%) на определённых этапах развития мозга.
Слайд 92
Значение апоптоза
Поддержание клеточного гомео-стаза. Клетки, выполнившие свою функцию, гибнут путём апоптоза.
Гибель клеток в активно пролиферирующих и самообновляющихся популяциях – эпителиоци-тов кишечника, лейкоцитов, эритроцитов.
Гибель клеток, выполнивших свою функцию, при удалении клонов иммунокомпетентных клеток при иммунном ответе.
Гибель эозинофилов после дегрануляции.
Отторжение эндометрия во время менструаль-ного цикла.
Регрессия молочной железы после прекращения лактации.
Слайд 93
Значение апоптоза
Дегенерация. При некоторых пато-логических состояниях наблюдают от-носительно избирательную гибель кле-ток
Слайд 94
Значение апоптоза
Селекция разновидностей клеток внутри популяции
Ликвидации аутоагрессивных Т-клеток в процес-се
Устранение клеток тканей, подвергшихся воз-действию цитотоксических Т-лимфоцитов или естественных киллеров.
Выбраковка ненужных и опасных для организма клонов лимфоцитов (аутоагрессивных): програм-мированная гибель клеток в защите «иммуноло-гически привилегированных» зон (внутренние среды глаза, щитовидная железа и семенники).
Слайд 95
Значение апоптоза
Старение
Гормонозависимая инволюция клеток эн-дометрия и атрезии фолликулов яичников у
Гормонозависимая инволюция клеток тка-ни простаты и яичек у пожилых мужчин.
Трансфекция. Внедрение в клетку нуклеиновой кислоты вируса (при вирус-ном гепатите, миокардите, энцефалите, СПИДе).
Слайд 96
Значение апоптоза
Повреждение клетки. Воздействие на клетку агентов, повреждающих её, но не
Опухолевый рост
(апоптоз выявляется как
при формировании опу-
холевого узла, так и при
его деструкции).
Слайд 97
Патология, связанная с нарушением апоптоза
Заболевания, связанные с ослабле-нием апоптоза:
Аутоиммунные процессы.
Злокачественные
Заболевания, связанные с усилени-ем апоптоза:
Врождённые аномалии (б-нь Дауна и др.).
Болезни крови (цитопении) – миелодис-плазии, тромбоцитопении, апластическая, В12- и фолиеводефицитные анемии, нейтропения.
Инфекционные (бактериальные) за-болевания
Слайд 98
Патология, связанная с нарушением апоптоза
Заболевания, связанные с усилени-ем апоптоза:
Вирусные инфекционные
Дистрофические заболевания НС (боко-вой амиотрофический склероз, болезнь Альцгей-мера, спинальная мышечная атрофия).
Инфаркт миокарда (преобладание апоптоза миоцитов в период «реперфузии» миокарда).
Токсический гепатит (апоптоз гепатоцитов под действием ядов, в том числе этанола).
Слайд 99
Механизмы адаптации клеток к повреждению
Внутриклеточные адаптивные механизмы:
компенсация нарушений энергетиче-ского обеспечения клетки;
защита мембран и ферментов клетки;
уменьшение выраженности (устране-ние) дисбаланса ионов и воды;
устранение дефектов генетической программы клетки и механизмов её реализации;
Слайд 100
Механизмы адаптации клеток к повреждению
Внутриклеточные адаптивные механизмы:
компенсация расстройств механизмов регуляции внутриклеточных
снижение функциональной активно-сти клеток;
регенерация;
гипертрофия;
гиперплазия.
Слайд 101
Механизмы адаптации клеток к повреждению
Межклеточные механизмы:
Для межклеточных (системных) меха-низмов адаптации к
Пути взаимодействия
Обмен метаболитами, местными БАВ – цитокинами, ионами.
Реализация реакций системы ИБН.
Изменения лимфо- и кровообращения.
Эндокринные влияния.
Нервные воздействия.