- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Онкоморфология. Определение и термины презентация
Содержание
- 1. Онкоморфология. Определение и термины
- 2. ОПРЕДЕЛЕНИЕ И ТЕРМИНЫ Опухоль - "патологический процесс,
- 3. ЭПИДЕМИОЛОГИЯ ОПУХОЛЕЙ Число случаев злокачественных опухолей, регистрируемых
- 4. Генетический дефект заключается в отсутствии или малой активности эндо-
- 5. ПРИЧИНЫ РАЗВИТИЯ И ПАТОГЕНЕЗ ОПУХОЛЕЙ Выделяют 3
- 6. Теория химических канцерогенов Описано более 1000 химических
- 7. Генотоксические канцерогены К генотоксическим канцерогенам относятся полициклические
- 8. Эпигенетические канцерогены ЭК представлены хлорорганическими соединениями, иммунодепрессантами
- 9. Химический канцерогенез Химический канцерогенез имеет многоступенчатый характер
- 10. Теория физических канцерогенов К физическим канцерогенам относятся
- 11. Вирусно-генетическая теория Ряд опухолей может развиться под
- 12. ДНК-содержащие онковирусы ДНК-содержащие онковирусы содержат 2 группы
- 13. РНК-содержащие онковирусы РНК-содержащие онковирусы относятся к ретровирусам
- 14. Полиэтиологическая теория канцерогенеза Эта теория объединяет все
- 15. КЛЕТОЧНЫЕ ОНКОГЕНЫ, АНТИОНКОГЕНЫ Клеточные онкогены кодируют синтез
- 16. По функциональной активности и структурному сходству с
- 17. Механизмы активации протоонкогенов Для того чтобы стимулировать
- 18. Механизмы активации протоонкогенов активация при транслокации участка
- 19. Антионкогены, или гены — супрессоры рака В
- 20. Генетические механизмы онкогенеза В норме при
- 21. Поддержание интенсивного деления новых поколений опухолевых клеток
- 22. 3.Путем синтеза аномальных сигнал-преобразующих протеинов, постоянно подающих
- 23. ПАТОГЕНЕЗ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ Патогенез злокачественных опухолей
- 24. 2. Активация клеточных онкогенов и супрессия антионкогенов.
- 25. ОСНОВНЫЕ СВОЙСТВА ОПУХОЛЕЙ В зависимости от степени
- 26. ОСНОВНЫЕ СВОЙСТВА ОПУХОЛЕЙ Злокачественные опухоли построены из
- 27. ОПУХОЛИ Гетерологичные анатомически идентична материнской ткани
- 28. Основные свойства опухолей Автономный
- 29. Атипизм опухоли Морфологический атипизм -
- 30. Биохимический атипизм Все перестройки метаболизма в опухоли
- 31. Антигенный атипизм В опухолях выделяют 5
- 32. Функциональный атипизм Характеризуется утратой опухолевыми клетками специализированных
- 33. МОРФОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА ОПУХОЛЕЙ Опухоли построены из
- 34. В зависимости от развитости стромы опухоли подразделяют
- 35. В гистиоидных опухолях доминирует паренхима, строма практически
- 36. Характер роста опухолей по отношению к окружающим
- 37. Стадии морфогенеза - стадия предопухоли —
- 38. Предопухолевая дисплазия Развитию большинства злокачественных опухолей предшествуют
- 39. Стадия неинвазивной опухоли Прогрессирование дисплазии связывают с
- 40. Стадия инвазивной опухоли Она характеризуется появлением инфильтрирующего
- 41. Фазы инвазии опухоли Во второй фазе опухолевая
- 42. Стадия метастазирования Это заключительная стадия морфогенеза опухоли,
- 43. Метастазирование Метастатический каскад условно может быть разделен
- 44. Метастазирование Патологоанатомические признаки метастазов: 1. Множественность опухолевых
- 45. МОРФОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ ОПУХОЛЕЙ На основании гистогенетического принципа
- 46. Разновидности анатомических форм опухоли 1.
- 47. Злокачественные опухоли Злокачественная опухоль, развивающаяся из
Слайд 2ОПРЕДЕЛЕНИЕ И ТЕРМИНЫ
Опухоль - "патологический процесс, характеризующийся безудержным (автономным или бесконтрольным)
Инициаторы опухолевого роста - факторы, после воздействия которых, появляются опухолевые клетки.
Канцерогены - факторы или агенты любой природы, вызывающие образование злокачественной опухоли.
Слайд 3ЭПИДЕМИОЛОГИЯ ОПУХОЛЕЙ
Число случаев злокачественных опухолей, регистрируемых каждый год, составляет около 5,9
Большая группа опухолей у детей имеет явное наследственное происхождение: ретинобластома, опухоль Вильмса и гепатобластома. В семьях больных данными опухолями обнаруживают специфические хромосомные аномалии.
Слайд 4Генетический дефект заключается в отсутствии или малой активности эндо- и экзонуклеаз-полимераз, устраняющих повреждения ДНК клеток
Наследственное заболевание
пигментная ксеродерма
связана с генетическим дефектом
репарации ДНК, при котором риск
развития рака кожи возрастает в
1000 раз.
Слайд 5ПРИЧИНЫ РАЗВИТИЯ И ПАТОГЕНЕЗ ОПУХОЛЕЙ
Выделяют 3 основные группы канцерогенных агентов: химические,
Слайд 6Теория химических канцерогенов
Описано более 1000 химических канцерогенных веществ, из которых только
Канцерогенные агенты подразделяются на две большие группы: генотоксические и эпигенетические в зависимости от их способности взаимодействовать с ДНК.
Слайд 7Генотоксические канцерогены
К генотоксическим канцерогенам относятся полициклические ароматические углеводороды, ароматические амины, нитрозосоединения
Часть генотоксических канцерогенов может напрямую взаимодействовать с ДНК, поэтому они называются прямыми. Другие должны претерпеть химические превращения в клетках, в результате которых они становятся активными – непрямые канцерогены. Активация непрямых генотоксических канцерогенов происходит с участием ряда ферментных систем клетки. Активированные метаболиты реагируют с различными участками ДНК.
Слайд 8Эпигенетические канцерогены
ЭК представлены хлорорганическими соединениями, иммунодепрессантами и др. Они не дают
Происхождение химических канцерогенов может быть экзо- и эндогенным.
Эндогенные канцерогены - холестерин, желчные кислоты, аминокислота, триптофан, некоторые стероидные гормоны, пероксиды липидов. Накоплению эндогенных канцерогенов в организме могут способствовать некоторые заболевания.
Слайд 9Химический канцерогенез
Химический канцерогенез имеет многоступенчатый характер и протекает в несколько стадий:
Стадия инициации - взаимодействие генотоксического канцерогена с геномом клетки и его перестройка. Клетка малигнизируется, начинает бесконтрольно делиться.
Вещество, определяющее начало стадии промоции, называется промотором. Эффект химических канцерогенов зависит от длительности введения и дозы. Эффект от действия различных химических канцерогенов может суммироваться.
Опухолевая прогрессия - безудержный рост опухоли.
Для реализации своего действия химические канцерогены должны воздействовать на ядерную ДНК и вызвать ее повреждения.
Слайд 10Теория физических канцерогенов
К физическим канцерогенам относятся три группы факторов: солнечная, космическая
1. Космическая, солнечная (в том числе ультрафиолетовая) радиация, является самым распространенным канцерогенным фактором.
2. Ионизирующая и неионизирующая радиация. Выявлено канцерогенное воздействие ионизирующей радиации в связи с использованием рентгеновских лучей в медицине, работой с радиоактивными источниками в промышленности, аварии на АЭС.
Слайд 11Вирусно-генетическая теория
Ряд опухолей может развиться под действием особых вирусов, которые называются
Слайд 12ДНК-содержащие онковирусы
ДНК-содержащие онковирусы содержат 2 группы генов: гены, необходимые для репликации
ДНК-содержащие онковирусы встраиваются либо полностью, либо частично в геном клетки-хозяина и в подавляющем большинстве случаев вызывают гибель этой клетки. При попадании ДНК-содержащего онковируса в чувствительные клетки только в одном из миллиона случаев возникает злокачественная трансформация клетки. К ДНК-содержащим онковирусам относятся аденовирус, вирусы группы герпеса, паповавирусы, вирус ветряной оспы и вирус гепатита В. Вирусы данной группы значительно чаще вызывают различные инфекционные болезни, чем опухолевый рост.
Слайд 13РНК-содержащие онковирусы
РНК-содержащие онковирусы относятся к ретровирусам и за исключением вирусов иммунодефицита
Слайд 14Полиэтиологическая теория канцерогенеза
Эта теория объединяет все другие, поскольку эффект всех известных
Слайд 15КЛЕТОЧНЫЕ ОНКОГЕНЫ, АНТИОНКОГЕНЫ
Клеточные онкогены кодируют синтез белков, которые называются онкобелками, или
Слайд 16По функциональной активности и структурному сходству с элементами сигнальной митогенетической цепочки
- онкобелки — гомологи факторов роста (c-sis, int-r, k-fgt и др.);
- онкобелки — голомоги рецепторов к факторам роста (с-еrbВ, c-erbA и др.);
- онкобелки, связанные с работой рецепторов, — аналоги G-белка (c-ras) и протеинкиназные белки (c-src, c-fps, c-fes, c-abl, c-met);
- онкобелки, передающие ростовые сигналы на ДНК (c-fos, c-jun, c-myc и др.).
Слайд 17Механизмы активации протоонкогенов
Для того чтобы стимулировать пролиферацию клеток, протоонкогены должны превратиться
- инсерционная активация — активация под действием встроенных в геном генов (вирусных);
Слайд 18Механизмы активации протоонкогенов
активация при транслокации участка хромосомы с встроенным в него
активация путем амплификации (умножении копий) протоонкогена;
активация при точечных мутациях протоонкогенов.
Слайд 19Антионкогены, или гены — супрессоры рака
В геноме клеток обнаруживаются гены, которые,
Слайд 20Генетические механизмы онкогенеза
В норме при появлении в делящейся клетке мутантной ДНК
(гена – активатора апоптоза или про-апоптотического гена или антионкогена). Оба гена активируют синтез белка р53, который
блокирует синтез копии дефектной ДНК и индуцирует синтез белка р21.
Белок р21 останавливает митоз в фазе G-2 и индуцирует апоптоз мутантной клетки.
Слайд 21Поддержание интенсивного деления новых поколений опухолевых клеток
Высокую пролиферативную активность новых поколений
1. Путем синтеза и выведения избытка ростовых факторов, которые стимулируют постоянное деление соседних опухолевых клеток из межклеточного матрикса.
2. Путем синтеза в опухолевой клетке избытка нормальных мембранных ростовых рецепторов или рецепторов с повышенной чувствительностью к ростовым факторам. Это стимулирует деление опухолевой клетки при нормальной концентрации митогенных факторов в межклеточном матриксе.
Слайд 223.Путем синтеза аномальных сигнал-преобразующих протеинов, постоянно подающих в ядро клетки сигнал
4. Путем усиления синтеза клеткой ДНК-связывающихся протеинов, через гены c-fos, c-jun, c-myc активирующих транскрипцию ДНК и стимулирующих деление клетки без повышения концентрации митогенных факторов в межклеточном матриксе.
Слайд 23ПАТОГЕНЕЗ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ
Патогенез злокачественных опухолей может быть представлен как стадийный процесс,
1. Изменения в геноме соматической клетки под действием различных канцерогенных агентов и в ряде случаев при наличии определенных наследственных изменений генома.
Слайд 24
2. Активация клеточных онкогенов и супрессия антионкогенов.
3. Экспрессия клеточных онкогенов, нарушения продукции регуляторных
4. Злокачественная трансформация клеток с приобретением способности к автономному росту.
Слайд 25ОСНОВНЫЕ СВОЙСТВА ОПУХОЛЕЙ
В зависимости от степени зрелости, темпов роста, характера роста,
Доброкачественные опухоли построены из зрелых дифференцированных клеток, обладают медленным экспансивным ростом с формированием капсулы из соединительной ткани на границе с окружающей нормальной тканью, не рецидивируют после удаления, не дают метастазов.
Слайд 26ОСНОВНЫЕ СВОЙСТВА ОПУХОЛЕЙ
Злокачественные опухоли построены из частично или вовсе недифференцированных клеток,
Злокачественные опухоли из эпителия называются раком, или карциномой, из производных мезенхимной ткани — саркомы.
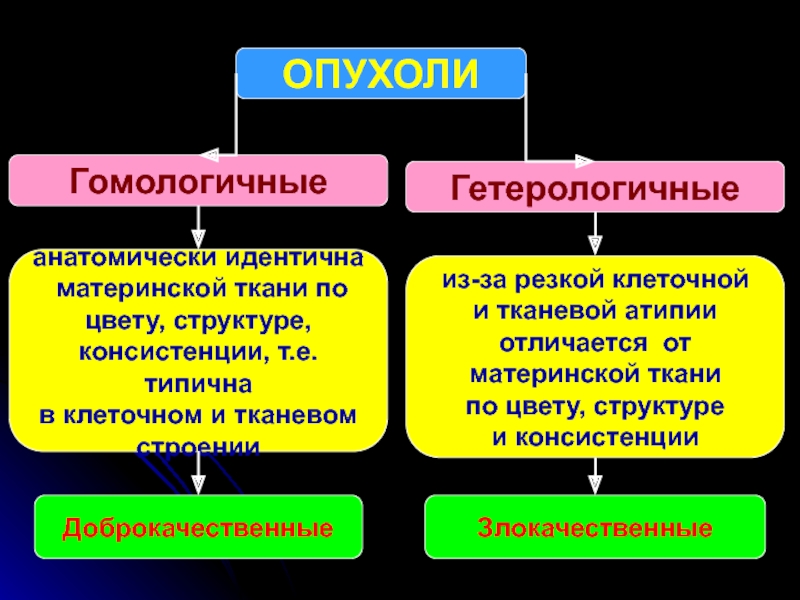
Слайд 27ОПУХОЛИ
Гетерологичные
анатомически идентична
материнской ткани по
цвету, структуре,
консистенции, т.е. типична
в клеточном и тканевом
строении
из-за
и тканевой атипии
отличается от
материнской ткани
по цвету, структуре
и консистенции
Гомологичные
Злокачественные
Доброкачественные
Слайд 28Основные свойства опухолей
Автономный рост опухоли характеризуется отсутствием контроля
При аутокринной стимуляции роста опухолевая клетка сама продуцирует факторы роста или онкобелки (мелкоклеточный рак легкого продуцирует ростовой гормон бомбезин и одновременно рецепторы к нему). При паракринной стимуляции фактор роста взаимодействует с рецепторами на раковых клетках и стимулирует их пролиферацию.
Слайд 29 Атипизм опухоли
Морфологический атипизм - ткань опухоли не повторяет строение
Морфологический атипизм представлен двумя вариантами: тканевым и клеточным.
Тканевой атипизм выражается в изменении соотношения между паренхимой и стромой опухоли, чаще с преобладанием паренхимы; изменением величины и формы тканевых структур с появлением уродливых тканевых образований различной величины.
Клеточный атипизм заключается в появлении полиморфизма клеток как по форме, так и по величине, укрупнении в клетках ядер, увеличении ядерно-цитоплазматического соотношения в пользу ядра, появлении крупных ядрышек. в опухолевых клетках обнаруживаются клетки с гиперхромными ядрами, гигантскими ядрами, многоядерные клетки и фигуры патологических митозов.
Слайд 30Биохимический атипизм
Все перестройки метаболизма в опухоли направлены на обеспечение ее роста
Слайд 31Антигенный атипизм
В опухолях выделяют 5 типов антигенов:
1. антигены вирусных опухолей,
2. антигены опухолей, вызванных канцерогенами;
3. изоантигены трансплантационного типа — опухолеспецифичные антигены;
4. онкофетальные антигены — эмбриональные антигены (а-фетопротеин, раковоэмбриональный антиген и др.);
5. гетероорганные антигены.
Слайд 32Функциональный атипизм
Характеризуется утратой опухолевыми клетками специализированных функций, присущих аналогичным зрелым клеткам,
Слайд 33МОРФОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА ОПУХОЛЕЙ
Опухоли построены из паренхимы и стромы. Паренхима опухоли —
Строма в опухоли, так же как и строма в нормальной ткани, в основном выполняет трофическую, модулирующую и опорную функции. Стромальные элементы опухоли представлены клетками и экстрацеллюлярным матриксом соединительной ткани, сосудами и нервными окончаниями.
Слайд 34В зависимости от развитости стромы опухоли подразделяют на органоидные и гистиоидные.
В
развитая строма. Степень развитости стромы может
варьировать от узких редких фиброзных прослоек и
сосудов капиллярного типа в медуллярном раке до
мощных полей фиброзной ткани, в которой
эпителиальные опухолевые цепочки едва бывают
различимыми, в фиброзном раке, или скирре.
Слайд 35В гистиоидных опухолях доминирует паренхима, строма практически отсутствует, так как представлена
Слайд 36Характер роста опухолей по отношению к окружающим тканям бывает экспансивным с
В полых органах выделяют также два типа роста в зависимости от отношения опухоли к их просвету: экзофитный при росте опухоли в просвет, и эндофитный — при росте опухоли в стенку органа.
Уни- и мультицентрический рост
Слайд 37Стадии морфогенеза
- стадия предопухоли — гиперплазии и предопухолевой дисплазии;
- стадия
- стадия инвазивного роста опухоли;
- стадия метастазирования.
Слайд 38Предопухолевая дисплазия
Развитию большинства злокачественных опухолей предшествуют предопухолевые процессы. К предопухолевым процессам
Слайд 39Стадия неинвазивной опухоли
Прогрессирование дисплазии связывают с дополнительными воздействиями, ведущими к последующим
Слайд 40Стадия инвазивной опухоли
Она характеризуется появлением инфильтрирующего роста. В опухоли появляются развитая
Инвазия опухоли протекает в три фазы и обеспечивается генетическими перестройками. Первая фаза инвазии характеризуется ослаблением контактов между клетками. На клеточной поверхности снижается концентрация ионов кальция, что приводит к повышению отрицательного заряда опухолевых клеток.
Слайд 41Фазы инвазии опухоли
Во второй фазе опухолевая клетка секретирует протеолитические ферменты и
Слайд 42Стадия метастазирования
Это заключительная стадия морфогенеза опухоли, сопровождающаяся определенными гено- и фенотипическими
Слайд 43Метастазирование
Метастатический каскад условно может быть разделен на четыре этапа:
1. формирование метастатического
2. инвазия в просвет сосуда;
3. циркуляция опухолевого эмбола в кровотоке (лимфотоке);
4. оседание на новом месте с формированием вторичной опухоли
Слайд 44Метастазирование
Патологоанатомические признаки метастазов:
1. Множественность опухолевых узлов в органе,
2. Чёткость их
3. Гетерологичность опухолевой ткани.
Слайд 45МОРФОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ ОПУХОЛЕЙ
На основании гистогенетического принципа с учетом морфологического строения, локализации,
1. Эпителиальные опухоли без специфической локализации (органонеспецифические).
2. Опухоли экзо- и эндокринных желез, а также эпителиальных покровов (органоспецифические).
3. Мезенхимальные опухоли.
4. Опухоли меланинобразующей ткани.
5. Опухоли нервной системы и оболочек мозга.
6. Опухоли системы крови.
7. Тератомы.
Слайд 46Разновидности анатомических форм опухоли
1. Анатомически опухоль может выглядеть как:
– опухолево-клеточный инфильтрат
в ткани,
– опухолевый узел,
– полип,
– язва,
– изъязвленная бляшка,
– опухолевая киста.
Слайд 47Злокачественные опухоли
Злокачественная опухоль, развивающаяся из клеток эпителия, — это рак. Различают
"Рак на месте" (carcinoma in situ). Форма рака без инфильтрирующего роста (в пределах эпителиального пласта), но с выраженным клеточным атипизмом..
Плоскоклеточный (эпидермальный) рак.
Аденокарцинома (железистый рак). Развивается из призматического эпителия, выстилающего слизистые оболочки, и эпителия желез.
Слизистый (коллоидный) рак.
Солидный рак.
Мелкоклеточный рак.
Фиброзный рак (скирр). Построен из атипичных клеток, замурованных в сильно развитой строме (грубоволокнистой соединительной ткани).
Медуллярный (аденогенный) рак. Форма низкодифференцированного рака, построенного из атипичных эпителиальных клеток. Характеризуется преобладанием паренхимы над стромой. В нем часто встречаются некрозы и кровоизлияния.