- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Кріогенна техніка і технологія презентация
Содержание
- 1. Кріогенна техніка і технологія
- 2. Основні кріогенні рідини Азот Кисень Аргон Неон Фтор Метан Водень Гелій-4 Гелій-3
- 3. Загальна інформація кріорідина під час кипіння при
- 4. Основні властивості кріорідин
- 5. Джерело кріорідин Дійсний склад може відрізнятися від
- 6. Склад сухого атмосферного повітря поблизу поверхні Землі
- 7. Заходи безпеки Кріорідини, потрапляючи на відкриті ділянки
- 8. Рідкий азот (N2) Прозора рідина з нормальною
- 9. Рідкий азот (N2) Найчастіше використовують у кріогенних
- 10. Рідкий азот (N2) Під час зберігання зрідженого
- 11. Рідкий кисень (O2) Кисень також має істотну
- 12. Рідкий кисень (O2) Рідкий кисень не горить,
- 13. Рідкий кисень (O2) У технологіях, хімії, мета-лургії,
- 14. Рідкий кисень (O2) При концентраціях понад 60
- 15. Рідкий аргон (Ar) Прозора рідина, яку добувають
- 16. Рідкий неон (Ne) Прозора рідина, яку добувають
- 17. Рідкий метан (СН4) Метан – основна складова
- 18. Рідкий фтор (F) Світло-жовта рідина. Високотоксичний. Дуже
- 19. Рідкий водень (H2) Прозора рідина, найчастіше добувають
- 20. Рідкий водень (H2) У звичайному стані у
- 21. Рідкий водень (H2) Теплота конверсії водню (706
- 22. Рідкий водень (H2) Вихід – прискорена конверсія
- 23. Рідкий водень (H2) 1 – резервуар рідкого
- 24. Рідкий гелій-4 (4He) Прозора рідина, яку
- 25. Рідкий гелій-4 (4He) Надплина компонента Не-ІІ практично
- 26. Рідкий гелій-4 (4He) Затоплений струмінь – надплинна
- 27. Рідкий гелій-4 (4He) «Товсті» плівки –рідкий Не-ІІ
- 28. Рідкий гелій-4 (4He) Фонтанування Нагріваючись, рідина втрачає
- 29. Рідкий гелій-4 (4He) Рідкий Не-ІІ за рахунок
- 30. Рідкий гелій-3 (3He) Прозора рідина. Є побічним
- 31. Дякую за увагу! Готуйтесь до тесту!
Слайд 3Загальна інформація
кріорідина під час кипіння при низькій температурі може швидко поглинути
кріорідини можна порівняно легко транспортувати та зберігати
кріорідини добре контактують з тілами складної форми.
Кріогенна рідина (кріорідина) – це речовина, що перебуває у рідкому стані за кріогенних температур
Кріорідини – основні робочі тіла, холодоносії, холодоагенти у кріогенних технологіях, бо:
Слайд 5Джерело кріорідин
Дійсний склад може відрізнятися від стандартного. Зокрема вміст кисню поблизу
Більшість кріорідин добувають з повітря, що є сумішшю багатьох газів. Стандартний склад повітря поблизу поверхні Землі наведено у таблиці.
Слайд 7Заходи безпеки
Кріорідини, потрапляючи на відкриті ділянки шкіри, спричинюють обморожування, а також
Слайд 8Рідкий азот (N2)
Прозора рідина з нормальною температурою кипіння 77 К.
Порівняно дешевий,
Добувають з повітря
(~78 об.%)
Слайд 9Рідкий азот (N2)
Найчастіше використовують у кріогенних системах заморожування (у тому числі
Слайд 10Рідкий азот (N2)
Під час зберігання зрідженого азоту не слід допускати його
Слайд 11Рідкий кисень (O2)
Кисень також має істотну частку в повітрі (~21 об.%),
Слайд 12Рідкий кисень (O2)
Рідкий кисень не горить, вибухобезпечний, але є сильним окисником,
Спроба прискорити смаження барбекю додавши рідкого кисню призвела до вибуху
Слайд 13Рідкий кисень (O2)
У технологіях, хімії, мета-лургії, машинобудуванні, будівництві, медицині та ін.)
Слайд 14Рідкий кисень (O2)
При концентраціях понад 60 % газоподібний кисень токсичний. Використовувати
Слайд 15Рідкий аргон (Ar)
Прозора рідина, яку добувають з повітря (0,93 об.%); інертний,
Слайд 16Рідкий неон (Ne)
Прозора рідина, яку добувають з повітря (18⋅10-4 об.%); інертний,
Суміш азоту з неоном при проходженні електричного розряду світиться помаранчевим кольором (її використовують у газорозрядних лампах)
Слайд 17Рідкий метан (СН4)
Метан – основна складова природного газу. Горючий. З повітрям
Слайд 18Рідкий фтор (F)
Світло-жовта рідина. Високотоксичний. Дуже активний, реагує з усіма органічними
При контакті з більшістю металів на поверхні утворює тонку плівку фториду, що захищає метал, проте при зберіганні у металевій тарі за певних умов можливе загоряння контейнера
Слайд 19Рідкий водень (H2)
Прозора рідина, найчастіше добувають з природного газу. Водень горючий
Слайд 20Рідкий водень (H2)
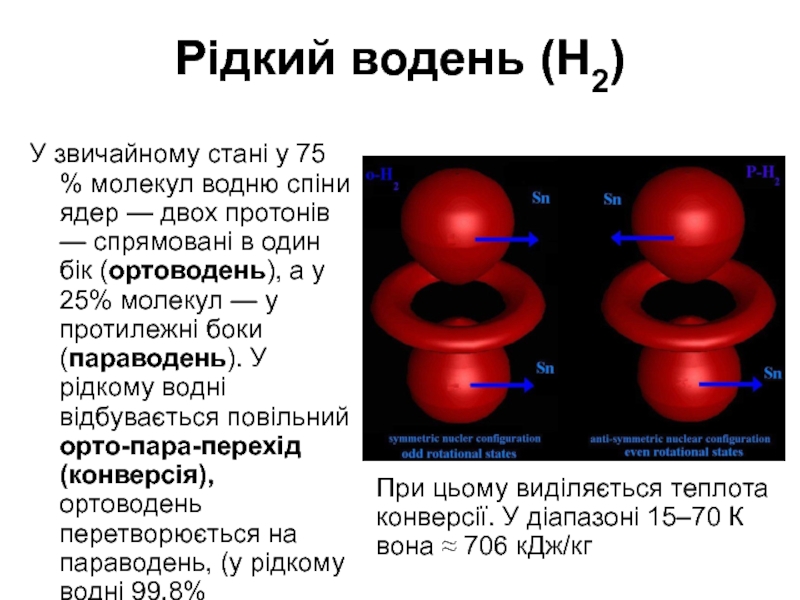
У звичайному стані у 75 % молекул водню спіни
При цьому виділяється теплота конверсії. У діапазоні 15–70 К вона ≈ 706 кДж/кг
Слайд 21Рідкий водень (H2)
Теплота конверсії водню (706 кДж/кг) вища за теплоту його
Слайд 22Рідкий водень (H2)
Вихід – прискорена конверсія у спеціальних реакторах за наявності
Слайд 23Рідкий водень (H2)
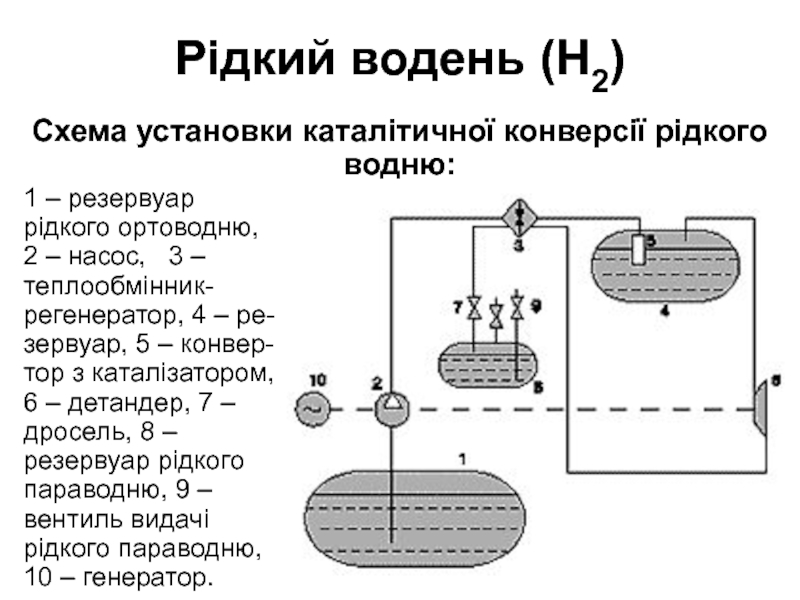
1 – резервуар рідкого ортоводню, 2 – насос,
Схема установки каталітичної конверсії рідкого водню:
Слайд 24Рідкий гелій-4 (4He)
Прозора рідина, яку добувають з природного газу (0,2–2
Надплинна компонента Не-ІІ складається з атомів гелію, що мають нульову енергію, її вміст зростає зі зменшенням температури.
Слайд 25Рідкий гелій-4 (4He)
Надплина компонента Не-ІІ практично не має в’язкості – вона
Теплопровідність надплинної компоненти дуже висока (до 105 кВт/(м⋅К). Насправді теплота у ній переноситься за рахунок дуже інтенсивної конвекції та хвиль. Тому кипіння після λ-переходу припиняється – йде лише випаровування з поверхні
Слайд 26Рідкий гелій-4 (4He)
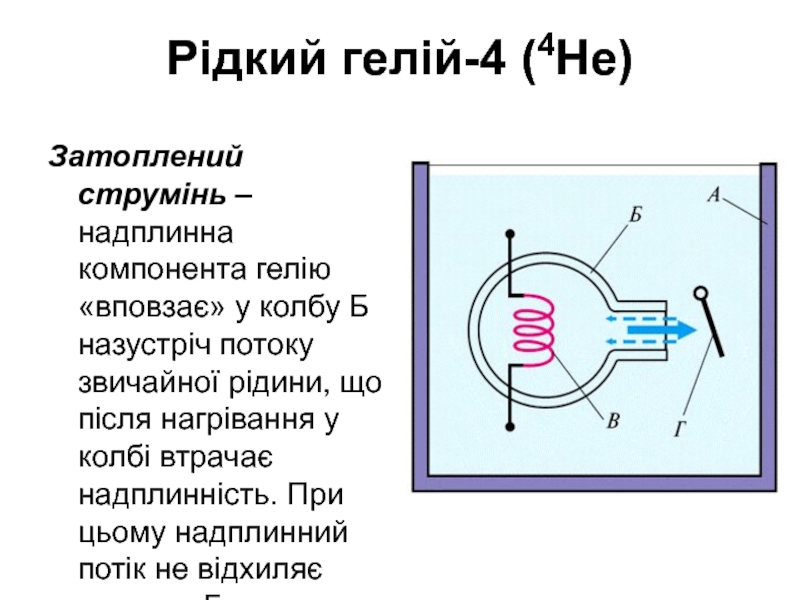
Затоплений струмінь – надплинна компонента гелію «вповзає» у колбу
Слайд 27Рідкий гелій-4 (4He)
«Товсті» плівки –рідкий Не-ІІ утворює плівку завтовшки близько 100
Слайд 28Рідкий гелій-4 (4He)
Фонтанування
Нагріваючись, рідина втрачає надплинність, надплинна компонента надходить крізь поруватий
Слайд 29Рідкий гелій-4 (4He)
Рідкий Не-ІІ за рахунок низької в’язкості перетікає з холодніших
Слайд 30Рідкий гелій-3 (3He)
Прозора рідина. Є побічним продуктом розпаду радіоактивного тритію.
Розглядається,
Суміш рідких 3Не і 4Не за T<0,827 К сама розділяється на дві фази — надплинну і нормальну — з поглинанням теплоти. Цей ефект використовують у рефрижераторах розчинення.