- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Комплемент. Межклеточные пространства, заполненные тканевой жидкостью презентация
Содержание
- 1. Комплемент. Межклеточные пространства, заполненные тканевой жидкостью
- 4. Межклеточные пространства, заполненные тканевой жидкостью Скелетная
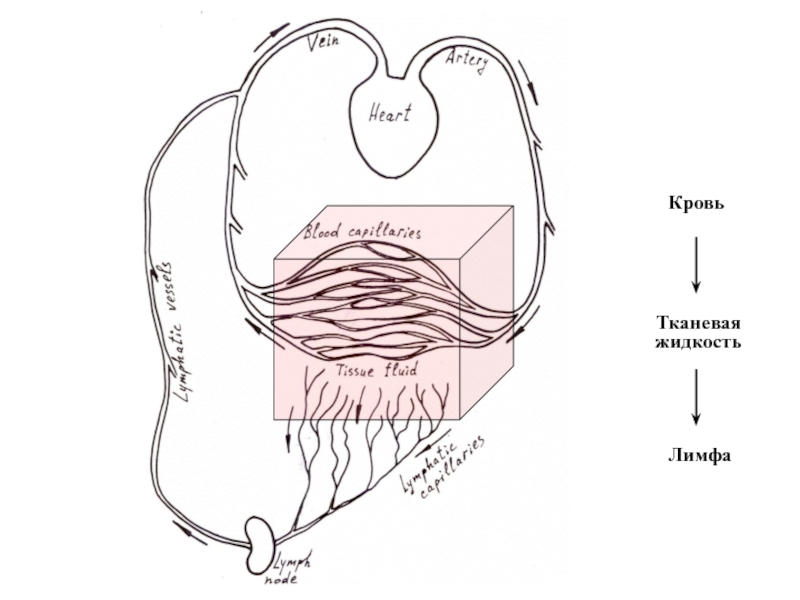
- 5. Talin Кровь Тканевая жидкость Лимфа
- 6. Вирусы
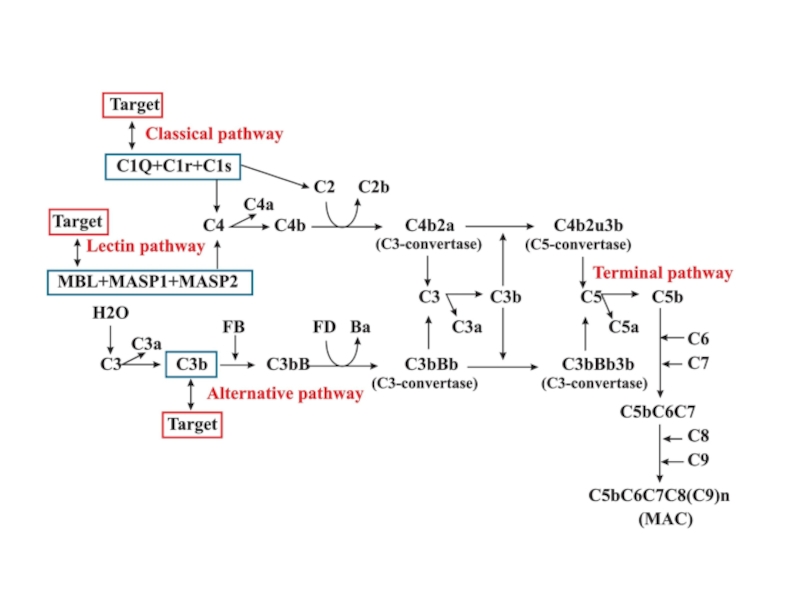
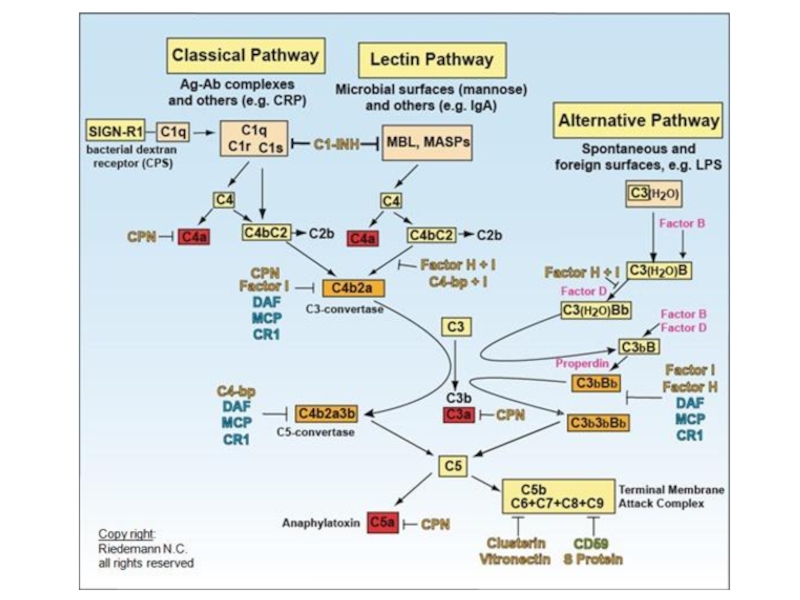
- 7. Типичное представление системы комплемента
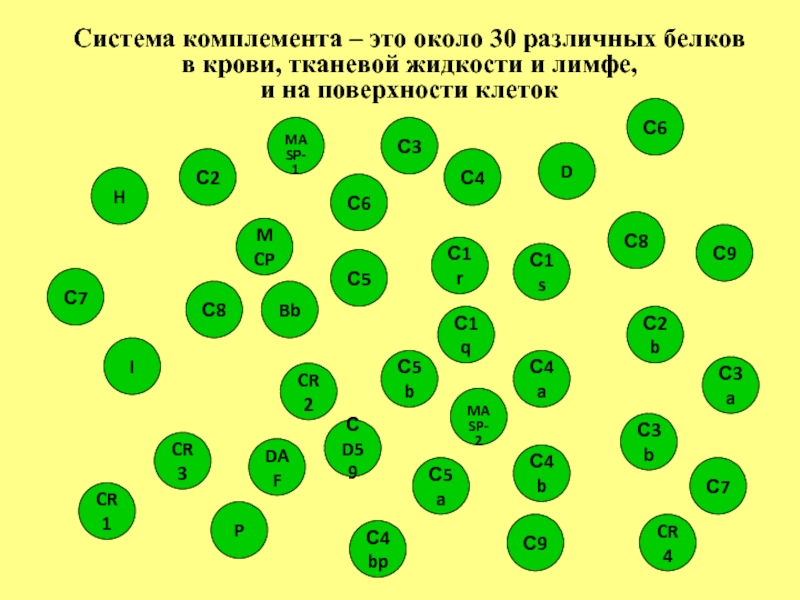
- 11. Неклассическое представление о системе комплемента: Динамическая структура
- 12. С3 С1q С8 С2 С1r С6
- 13. Где производятся факторы комплемента: Гепатоциты Лейкоциты Фибробласты Жировые клетки Эпителиальные клетки
- 16. Типичное протеолитическое преобразование белков комплемента: отщепление фрагмента
- 17. Типы превращений белков комплемента: Протеолитическое отщепление небольшого
- 18. Белок С3 – ключевой фактор системы комплемента.
- 19. При спонтанном гидролизе тиоэфирной группы домены TED
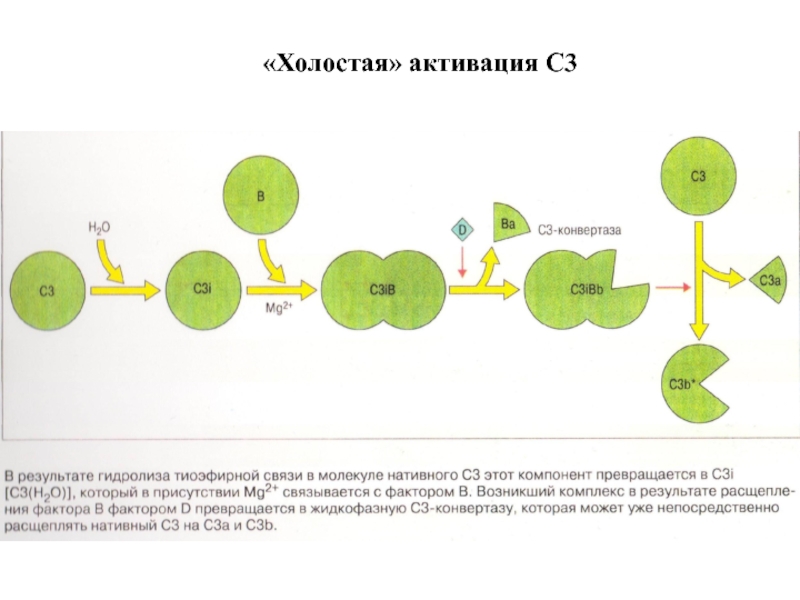
- 20. «Холостая» активация С3
- 21. Конвертаза С3
- 22. Тиоэфирная группа, образована Cys 1010 – Gln
- 23. Тиоэфирная группа белка С3 способна реагировать с
- 24. C3b Образовалась конвертаза C3
- 25. Комплекс C3b + Bb нестабилен. Его стабилизирует
- 26. Пропердин – небольшой белок (54 kDa) системы
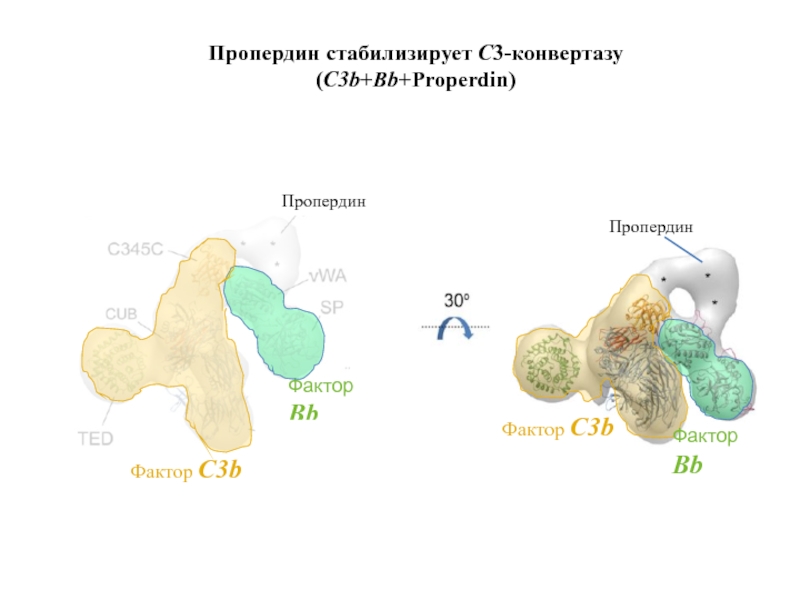
- 27. Пропердин Пропердин стабилизирует С3-конвертазу (C3b+Bb+Properdin) Фактор Bb Пропердин
- 28. Спонтанный гидролиз тиоэфирной группы – событие
- 29. Конвертаза С3
- 30. С3 С3b С3b-B D B С3b-Bb
- 31. Три важных следствия возникновения твердофазовой С3-конвертазы:
- 32. C3a C3b C3b Химическая ковалентная пришивка C3b к поверхности
- 33. Модификация поверхности микробной клетки множеством молекул
- 34. ФАГОЦИТОЗ ОПСОНИЗИРОВАННОЙ МИКРОБНОЙ ЧАСТИЦЫ Рецепторы
- 35. Complement Receptors
- 36. Малые пептиды, образующиеся при расщеплении факторов
- 37. C3b
- 38. Небольшие пептиды С3a (C4a, C5a) являются
- 39. Рецептор C3a (С4а или С5а) в клеточной
- 40. Индукторы
- 41. Цитокины из очага воспаления попадают в кровь.
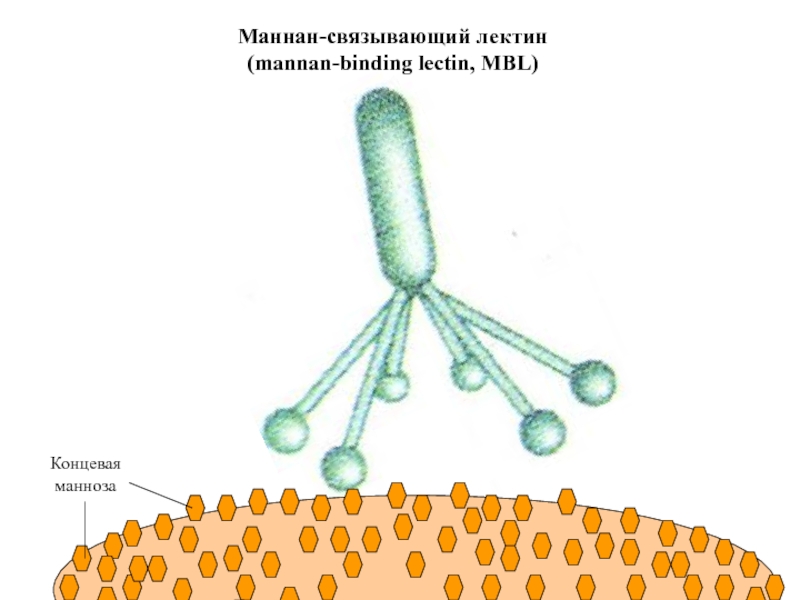
- 42. Маннан-связывающий лектин (mannan-binding lectin, MBL)
- 43. Структура олигосахаридов, которые связывает MBL
- 44. Маннан-связывающий лектин Каждая субъединица (голова-шея) складывается
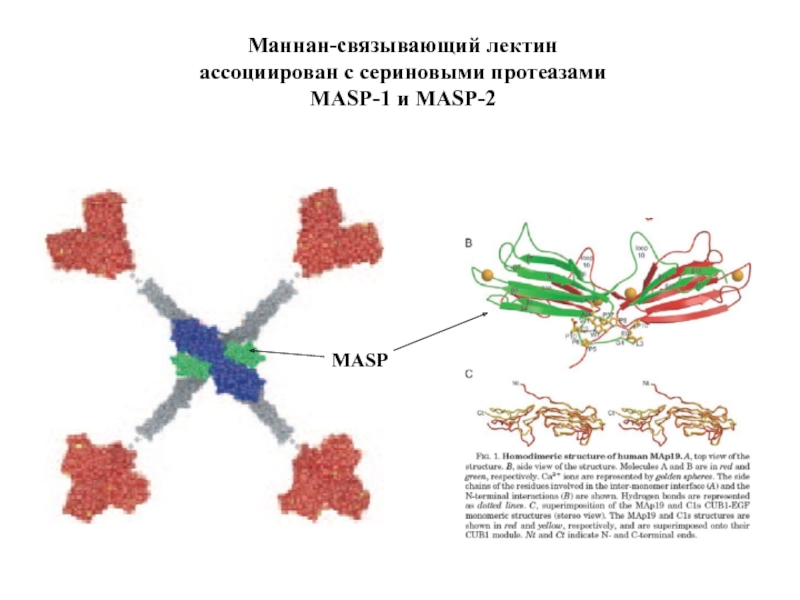
- 45. Маннан-связывающий лектин ассоциирован с сериновыми протеазами MASP-1 и MASP-2 MASP
- 46. Figure 6 Structural Basis of Complement Activation
- 47. C4 -> C4b + C4a C2
- 48. Подобно лектиновой активации комплемента , функционирует классический
- 49. Активация протеаз C1r происходит в результате конформационных движений коллагеноподобных тяжей C1q (стебли тюльпанов)
- 50. Маннан-связывающий лектин
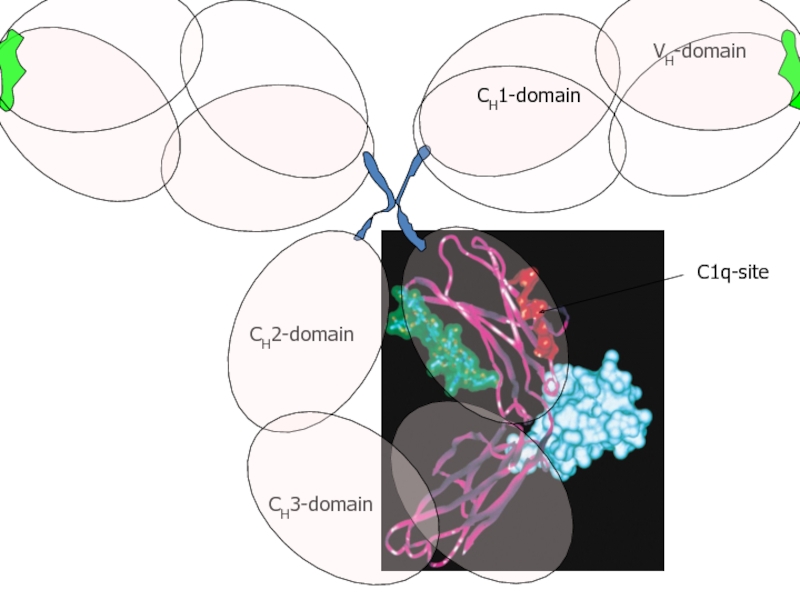
- 52. C1q-site CH3-domain CH2-domain
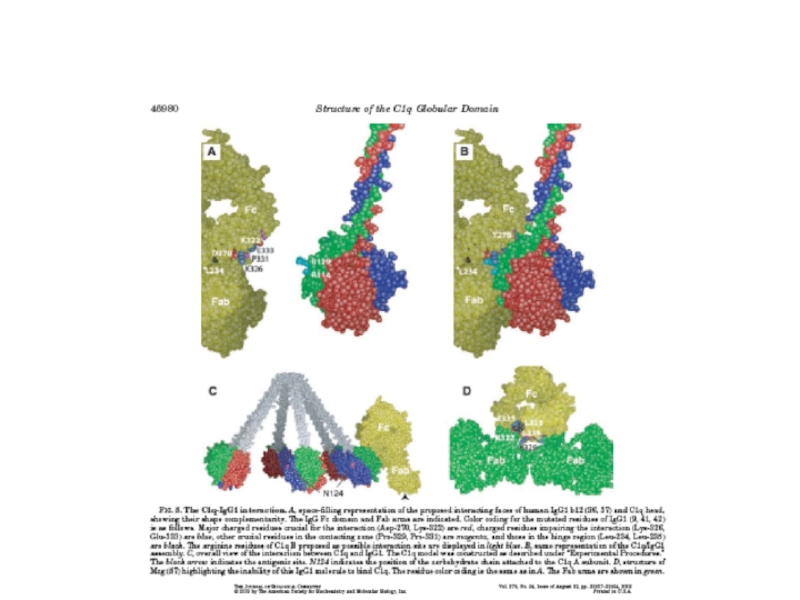
- 53. Модель взаимодействия C1q c Fc-фрагментом антитела (IgG)
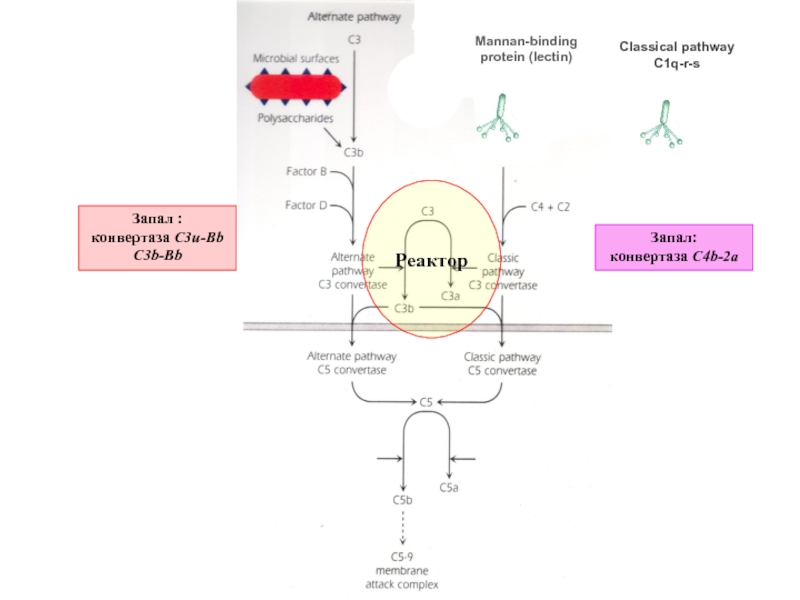
- 55. Реактор Запал : конвертаза C3u-Bb C3b-Bb Запал: конвертаза C4b-2a
- 56. Еще одно важное следствие работы твердофазовой конвертазы
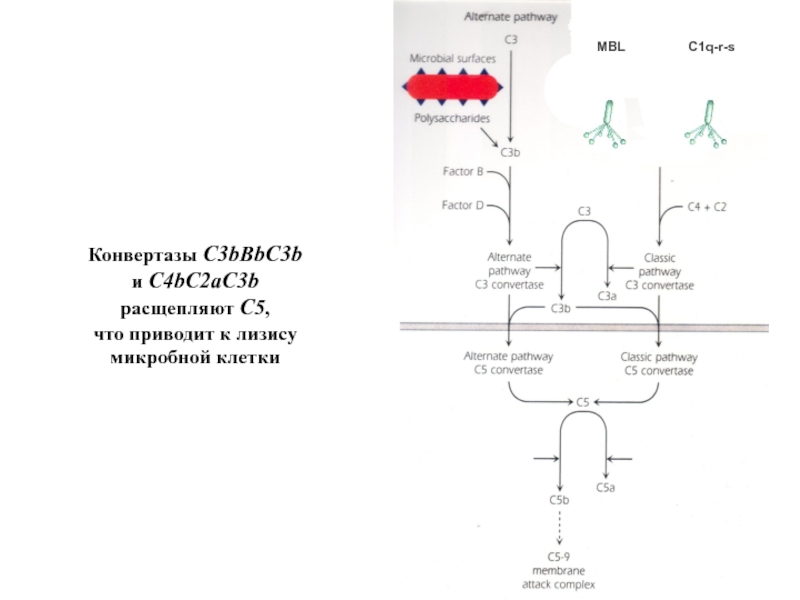
- 57. Конвертазы C3bBbС3b и С4bC2aС3b расщепляют С5, что приводит к лизису микробной клетки
- 58. С5 Конвертаза C5 отщепляет небольшой пептид C5a
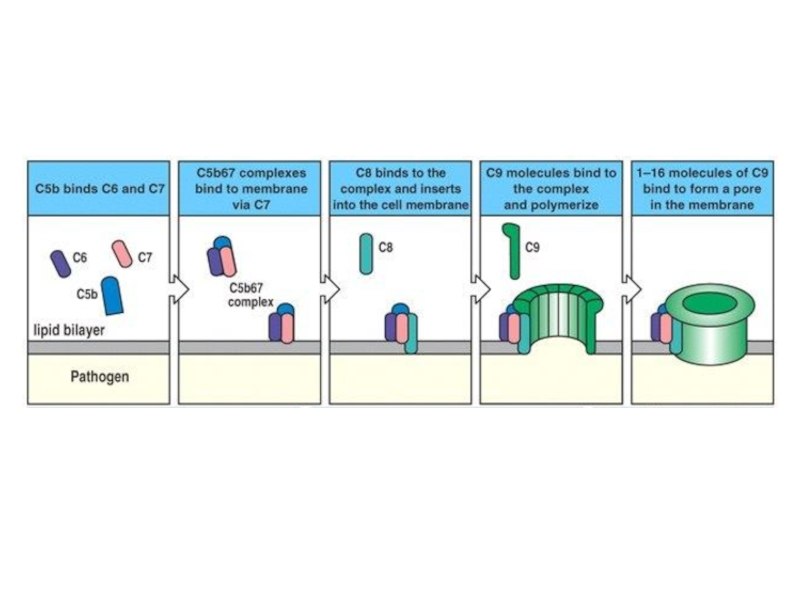
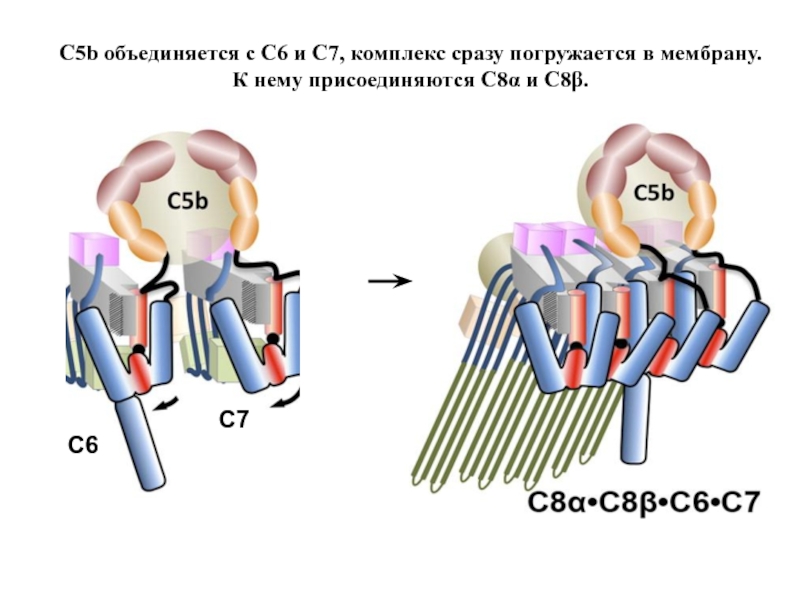
- 62. C5b объединяется с C6 и C7, комплекс
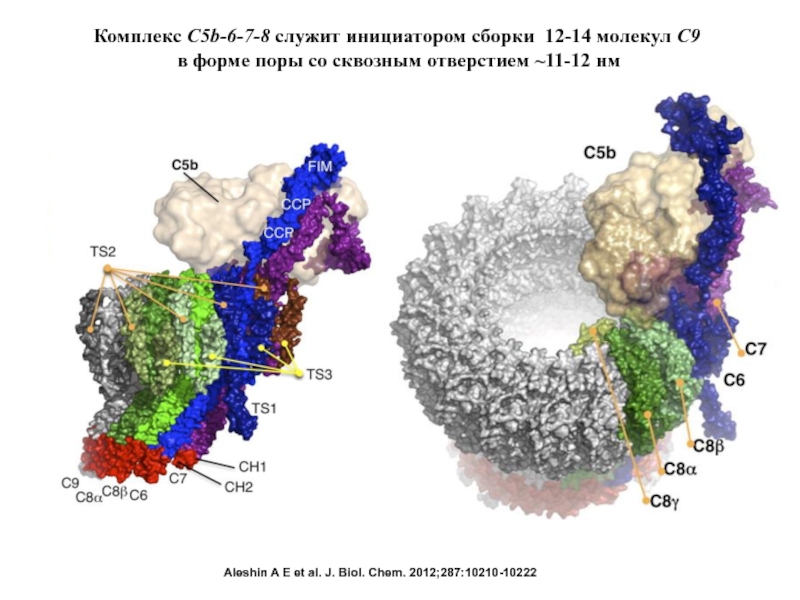
- 63. Комплекс C5b-6-7-8 служит инициатором сборки 12-14 молекул
- 64. Основные эффекторные функции комплемента Опсонизация частиц (облегчение
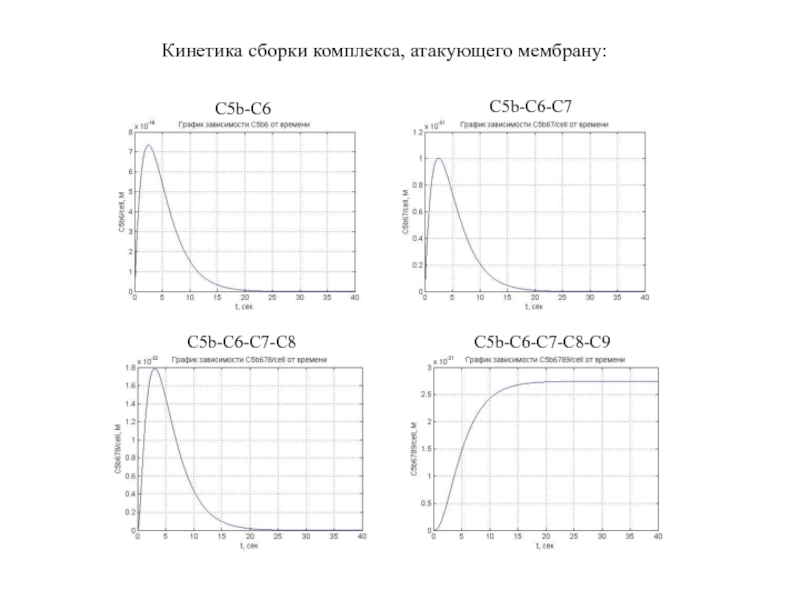
- 65. Немного кинетики
- 66. Кинетика сборки комплекса, атакующего мембрану: C5b-C6 C5b-C6-C7 C5b-C6-C7-C8 C5b-C6-C7-C8-C9
- 67. C1q per cell seconds
- 68. Математическая модель комплемента показывает, что распространение
- 69. Клетки нашего организма надежно защищены от агрессивного действия комплемента
- 70. Белки, которыми защищены наши клетки от агрессивного действия комплемента
- 71. Глюкозаминогликан/ сиаловая кислота Глюкозаминогликан/ сиаловая
- 72. Mapping FH and C3 mutants on complex
- 73. Фактор Н Поверхность наших клеток C3b
- 74. На поверхности наших клеток протеаза I разрезает
- 75. DAF – очень похож на N-концевой фрагмент
- 76. Поверхность наших клеток C3b Протеаза I Decay accelerating factor (DAF) Фактор, ускоряющий распад
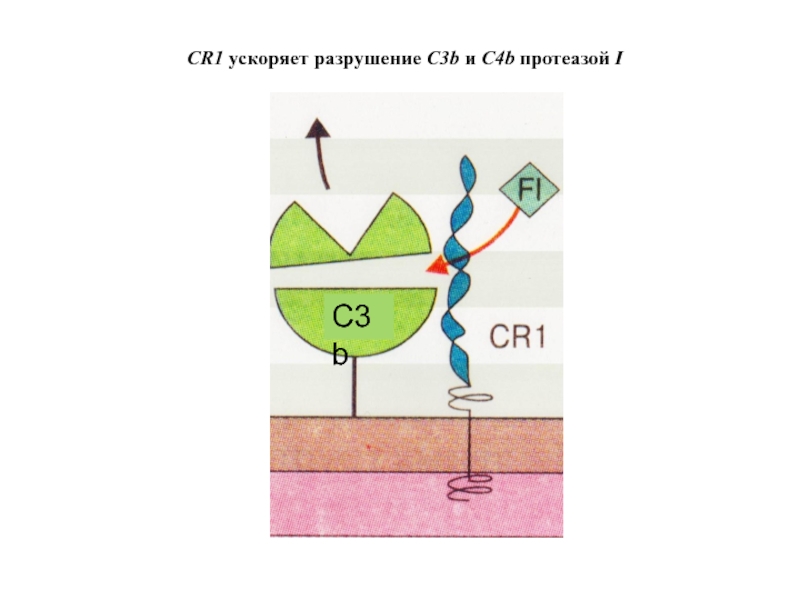
- 77. CR1 ускоряет разрушение C3b и C4b протеазой I
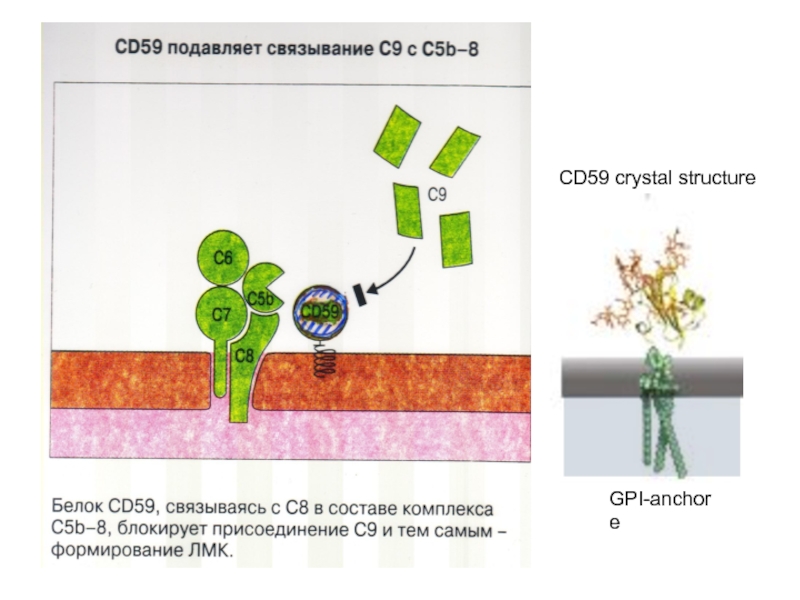
- 78. CD59 crystal structure GPI-anchore
- 79. Комплекс C5b-6-7-8 служит инициатором сборки 12-14 молекул
- 81. C3b Поверхность наших клеток Cobra venom
- 82. С3 С1q С8 С2 С1r С6
- 83. Может ли активация комплемента распространяться за пределы атакованной поверхности?
- 84. Клетки искусственно атаковали комплементом (розовые) и без промедления перемешали с интактными клетками (красные).
- 85. Перенос агрессивных факторов комплемента с одних клеток
- 87. Атака комплемента ограничена размерами незащищенной поверхности.
- 88. Система комплемента: Точность (+10 мкм)
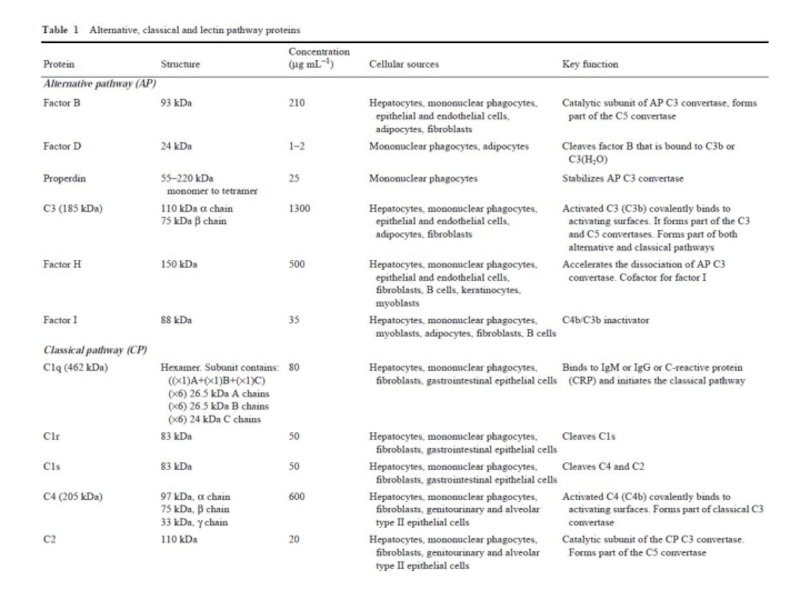
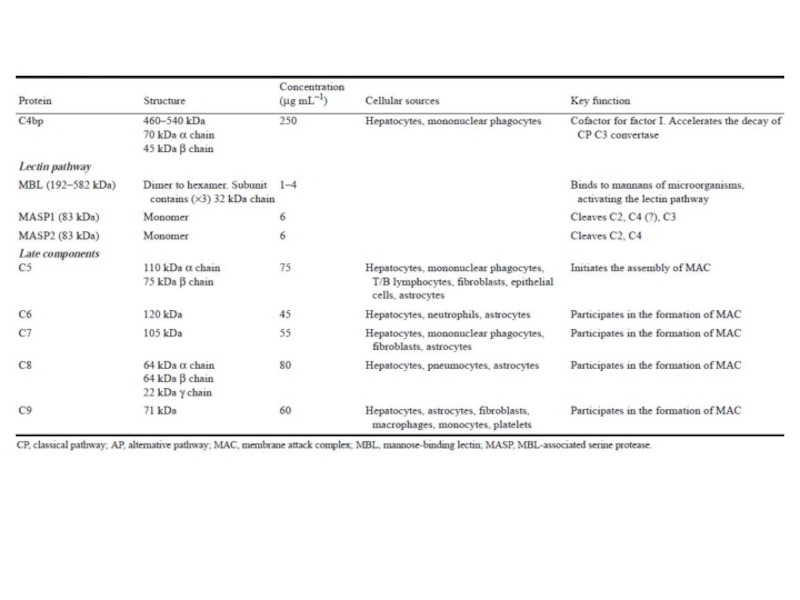
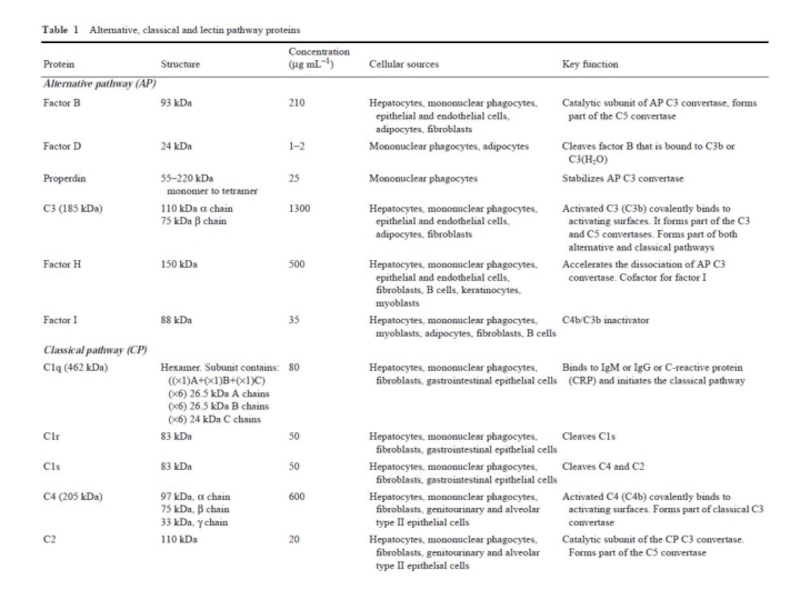
- 89. Большинство белков комплемента крупнее альбумина (см. следующую
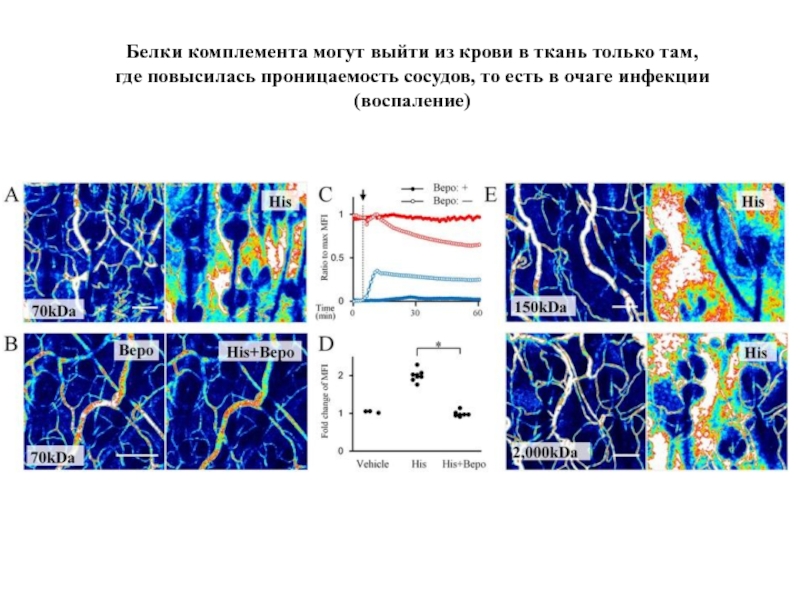
- 92. Белки комплемента могут выйти из крови в
- 93. вирусов и
Слайд 2
Эндотелий
венулы
IL-1α
IL-1β
IL-6
IL-8
GM-CSF
Фибробласт
Макрофаг
Дендритная
клетка
Тучная клетка
Жидкая фаза тканей ядовита для микроорганизмов
Цитокины
Слайд 3
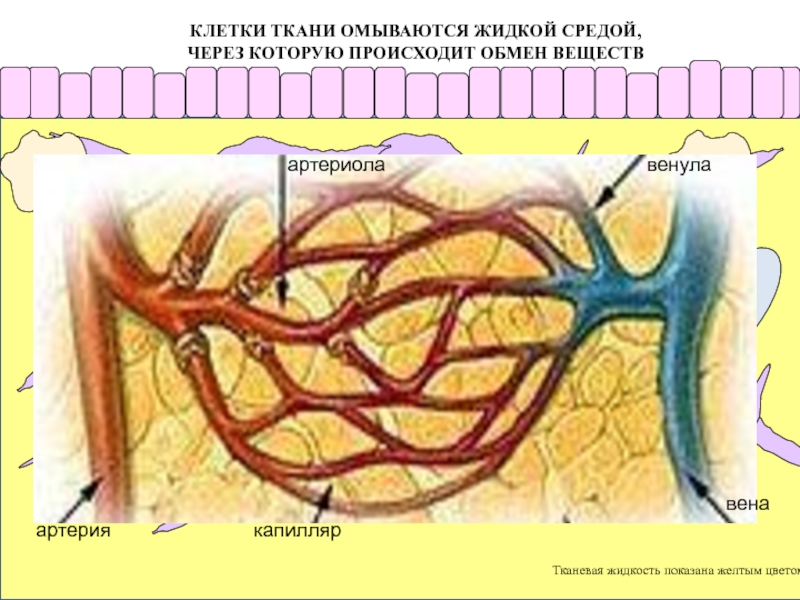
КЛЕТКИ ТКАНИ ОМЫВАЮТСЯ ЖИДКОЙ СРЕДОЙ,
ЧЕРЕЗ КОТОРУЮ ПРОИСХОДИТ ОБМЕН ВЕЩЕСТВ
Тканевая жидкость
Клетки, населяющие
ткань
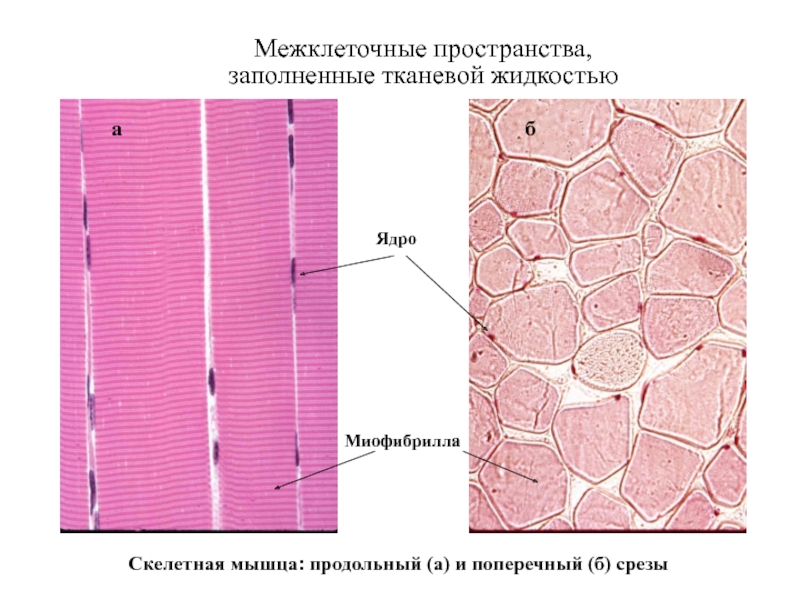
Слайд 4Межклеточные пространства,
заполненные тканевой жидкостью
Скелетная мышца: продольный (а) и поперечный (б)
а
б
Миофибрилла
Ядро
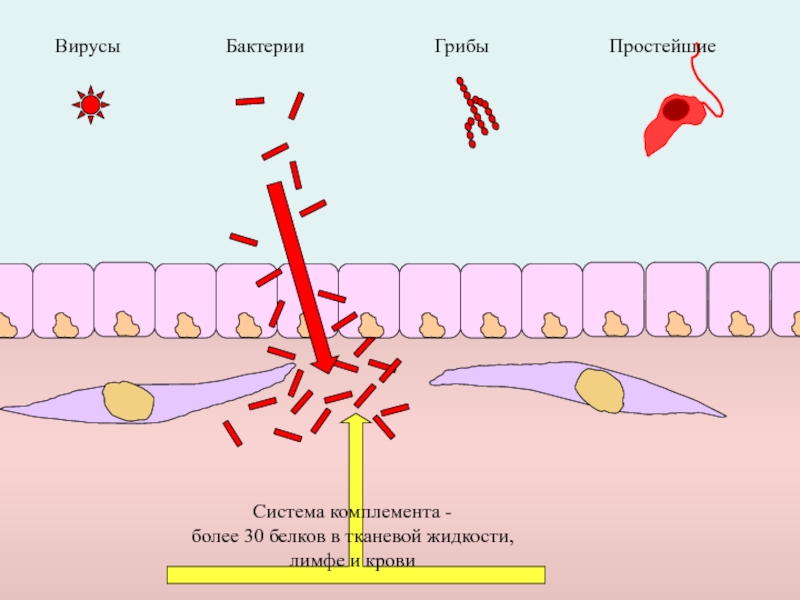
Слайд 6
Вирусы
Система комплемента -
более 30 белков в тканевой жидкости,
лимфе и крови
Слайд 11Неклассическое представление о системе комплемента:
Динамическая структура молекул
Развертывание во времени (Кинетика)
Функциональные
Развертывание в пространстве
Слайд 12
С3
С1q
С8
С2
С1r
С6
С9
С4
С3a
С7
С1s
С3b
С2b
С4b
С4a
С5
С5a
С5b
С9
С8
С6
С7
I
С4bp
H
P
DAF
D
Bb
MCP
СD59
MASP-
1
MASP-
2
CR1
CR2
H
CR4
H
H
CR3
Система комплемента – это около 30 различных белков
в
и на поверхности клеток
Слайд 13Где производятся факторы комплемента:
Гепатоциты
Лейкоциты
Фибробласты
Жировые клетки
Эпителиальные клетки
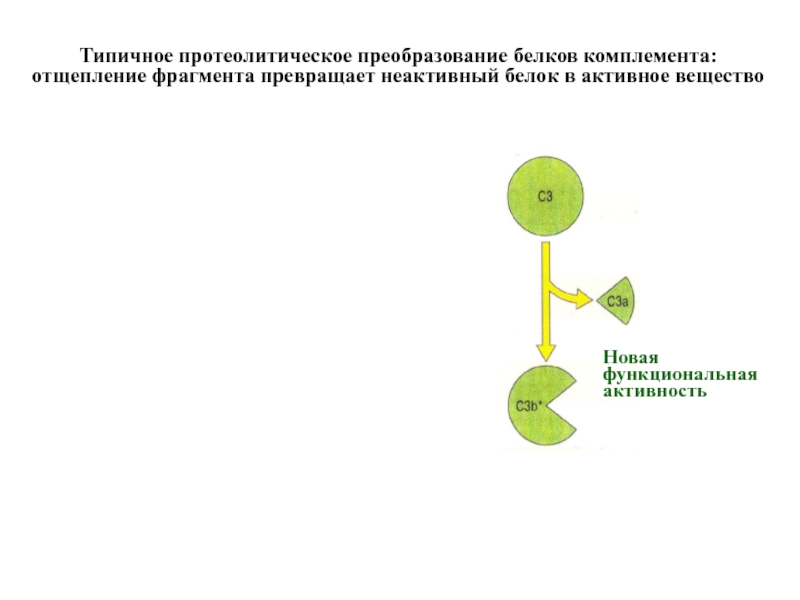
Слайд 16Типичное протеолитическое преобразование белков комплемента:
отщепление фрагмента превращает неактивный белок в активное
Новая
функциональная
активность
Откалывая фрагменты от обыкновенного булыжника,
древние люди превращали его в нож, скребок или
другой полезный инструмент
Слайд 17Типы превращений белков комплемента:
Протеолитическое отщепление небольшого пептида → оба фрагмента активны.
Конформационное изменение белка с последующим протеолитическим отщеплением пептида и изменением активности белка.
Отщепление пептида от одного из белков с последующей стыковкой (docking) двух белковых молекул → появление новой активности у тандема.
Протеолитическое отщепление пептида, приводящее к активации белка.
Протеолитическое отщепление пептида и последующее конформационное изменение белка → появление новой активности
Стыковка (docking) двух белковых молекул с последующим протеолитическим отщеплением пептида от одного из белков → появление новой активности у тандема.
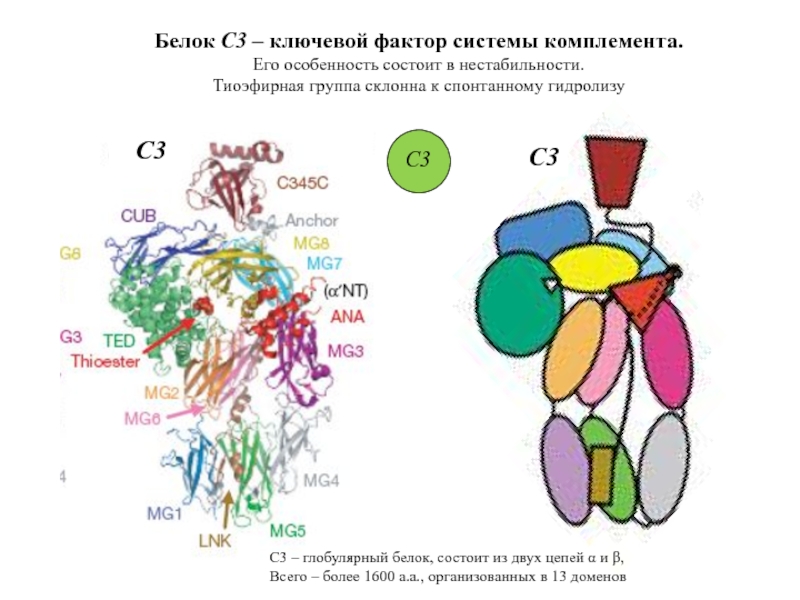
Слайд 18Белок С3 – ключевой фактор системы комплемента.
Его особенность состоит в нестабильности.
Тиоэфирная группа склонна к спонтанному гидролизу
С3 – глобулярный белок, состоит из двух цепей α и β,
Всего – более 1600 a.a., организованных в 13 доменов
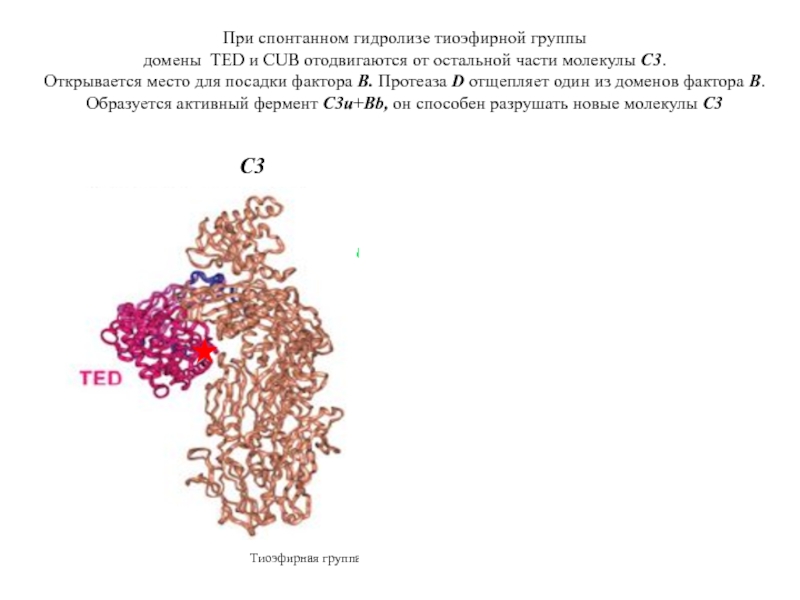
Слайд 19При спонтанном гидролизе тиоэфирной группы
домены TED и CUB отодвигаются от остальной
Открывается место для посадки фактора В. Протеаза D отщепляет один из доменов фактора B.
Образуется активный фермент C3u+Bb, он способен разрушать новые молекулы С3
фактор B
C3
C3u
(C3H20)
протеаза D
С3-конвертаза
(C3u+Bb)
Тиоэфирная группа не может пришиваться к поверхности, C3uBb остается в жидкой фазе, называется «жидкофазовая конвертаза С3»
Слайд 21
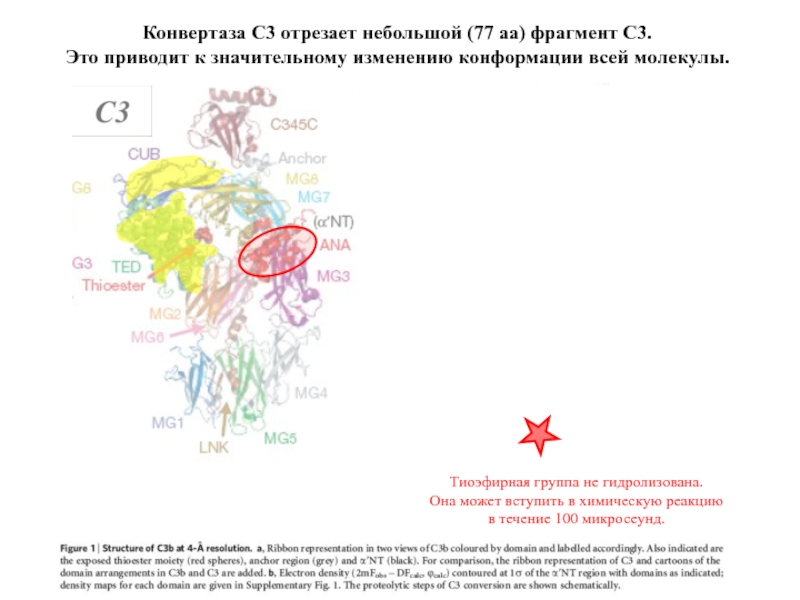
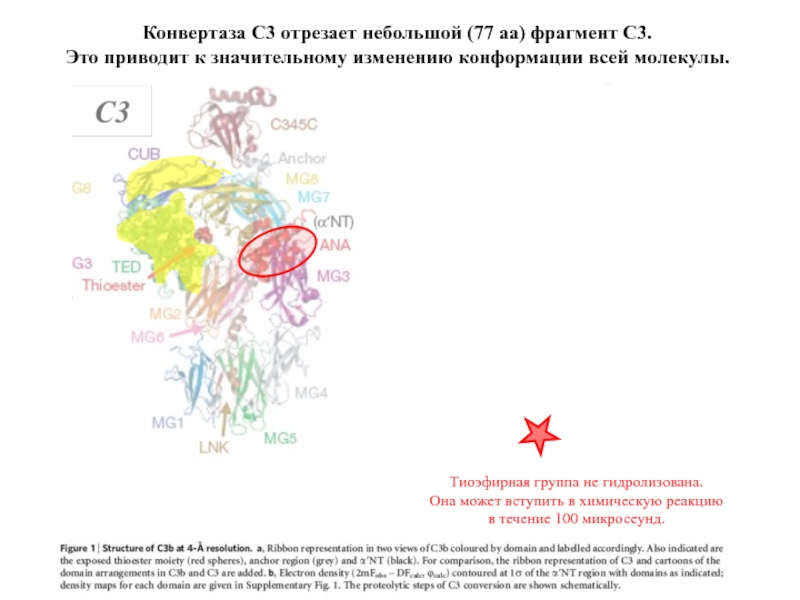
Конвертаза С3 отрезает небольшой (77 аа) фрагмент С3.
Это приводит к
Тиоэфирная группа не гидролизована.
Она может вступить в химическую реакцию
в течение 100 микросеунд.
Слайд 22Тиоэфирная группа, образована Cys 1010 – Gln 1013.
В нативном C3 она
В активированном C3b она перемещается на поверхность молекулы и становится реакционноактивной, то есть способной вступить в реакцию (в виде ацил-имидазолового промежуточного продукта, который существует около 100 микросекунд)
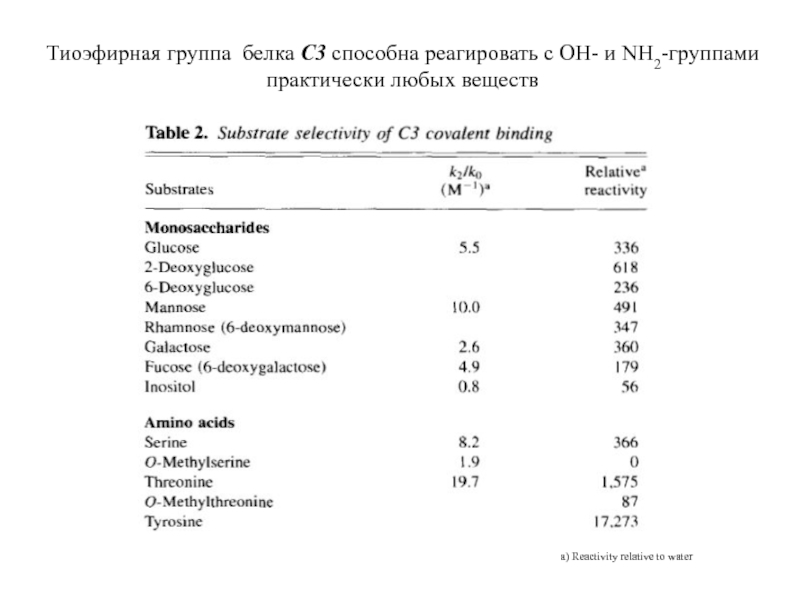
Слайд 23Тиоэфирная группа белка С3 способна реагировать с OH- и NH2-группами
практически
a) Reactivity relative to water
Слайд 24
C3b
Образовалась конвертаза C3
Ковалентная связь
с поверхностью
Протеаза
D
Образование твердофазовой С3-конвертазы (C3b+Bb)
Слайд 25Комплекс C3b + Bb нестабилен.
Его стабилизирует пропердин.
Фактор C3b
Фактор B
Фактор Bb
Фактор C3b
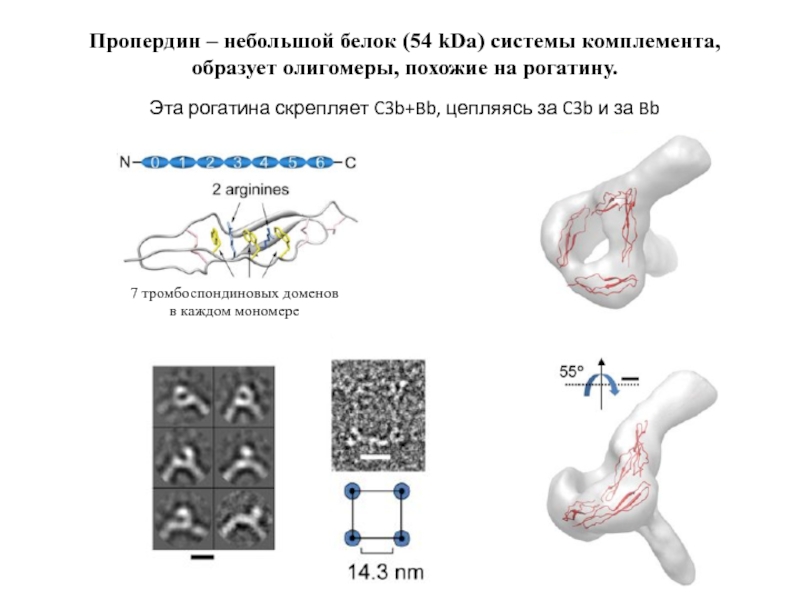
Слайд 26Пропердин – небольшой белок (54 kDa) системы комплемента, образует олигомеры, похожие
Эта рогатина скрепляет C3b+Bb, цепляясь за C3b и за Bb
7 тромбоспондиновых доменов
в каждом мономере
Слайд 28
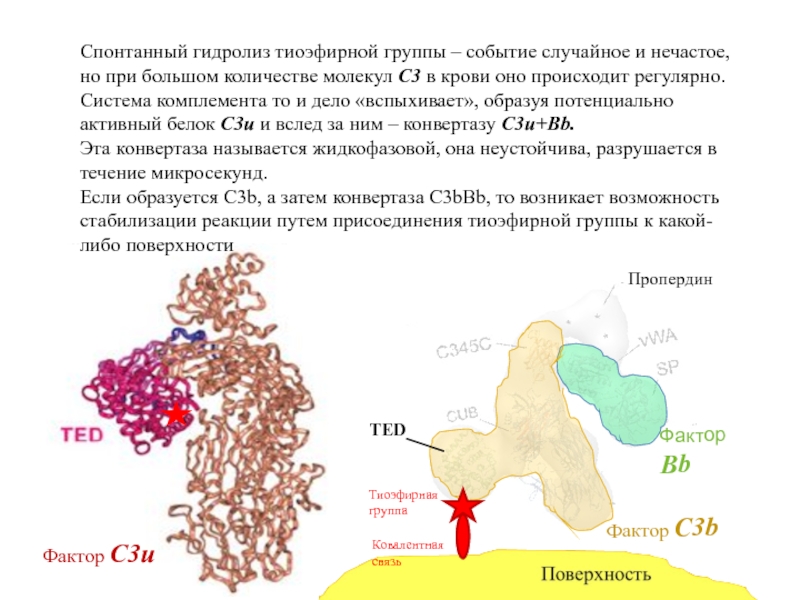
Спонтанный гидролиз тиоэфирной группы – событие случайное и нечастое, но при
Система комплемента то и дело «вспыхивает», образуя потенциально активный белок C3u и вслед за ним – конвертазу C3u+Bb.
Эта конвертаза называется жидкофазовой, она неустойчива, разрушается в течение микросекунд.
Если образуется C3b, а затем конвертаза C3bBb, то возникает возможность стабилизации реакции путем присоединения тиоэфирной группы к какой-либо поверхности
Фактор C3u
Тиоэфирная
группа
Ковалентная
связь
Слайд 29
Конвертаза С3 отрезает небольшой (77 аа) фрагмент С3.
Это приводит к
Тиоэфирная группа не гидролизована.
Она может вступить в химическую реакцию
в течение 100 микросеунд.
Слайд 30
С3
С3b
С3b-B
D
B
С3b-Bb
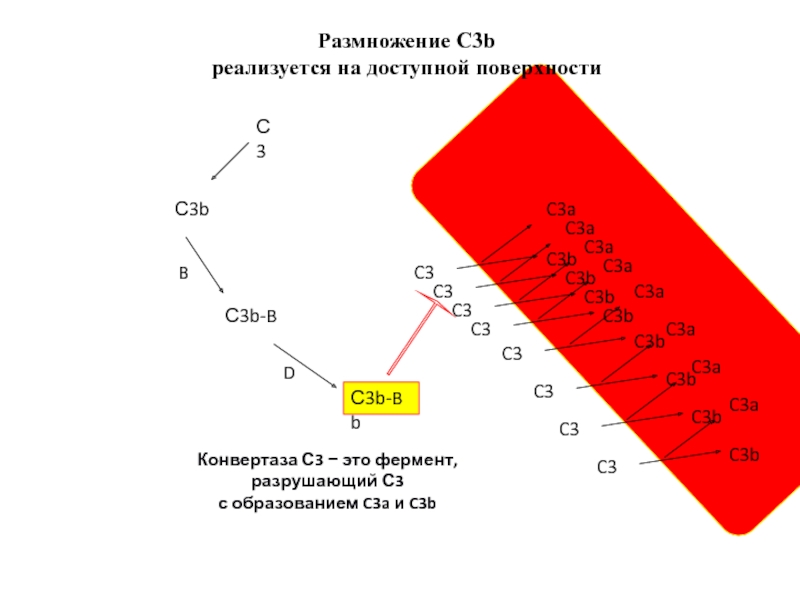
Размножение С3b
реализуется на доступной поверхности
Конвертаза С3 − это фермент, разрушающий С3
с образованием C3a и C3b
Слайд 31Три важных следствия возникновения твердофазовой С3-конвертазы:
1. Поверхность модифицируется химически (ковалентно
2. От этой поверхности исходит поток небольших фрагментов C3a
(создается градиентное поле химического вещества)
3. Каждая новая молекула продукта (C3b) может стать ферментом (C3bBb),
производящим этот же самый продукт (C3b). Процесс имеет свойства цепной реакции,
что приводит к химическому взрыву!
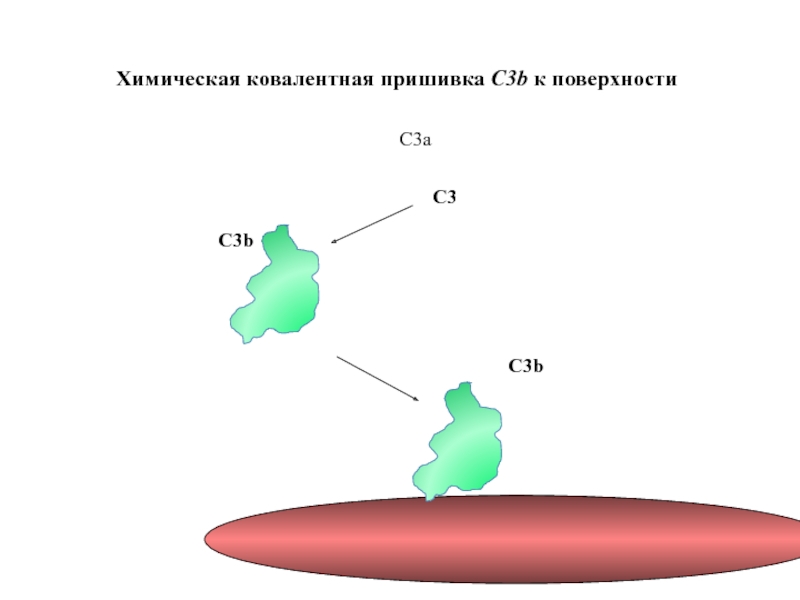
Слайд 33
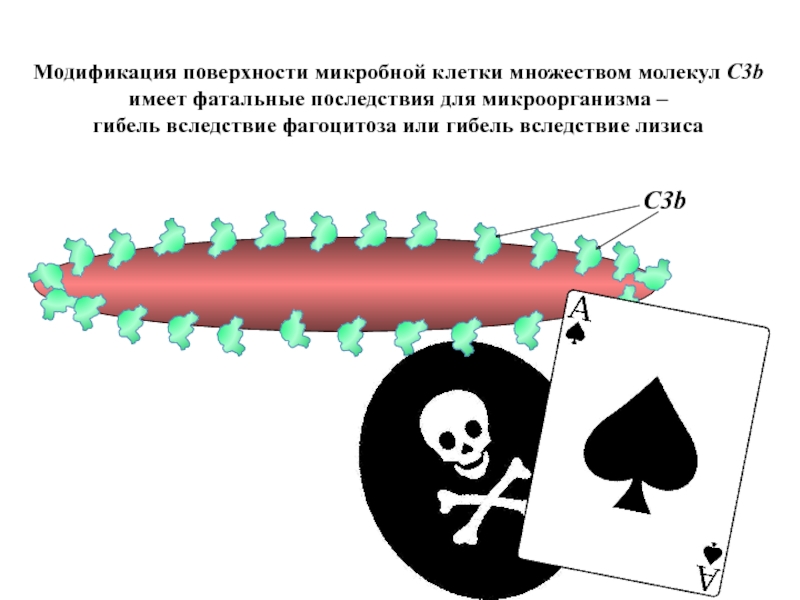
Модификация поверхности микробной клетки множеством молекул C3b
имеет фатальные последствия для
гибель вследствие фагоцитоза или гибель вследствие лизиса
C3b
Слайд 34
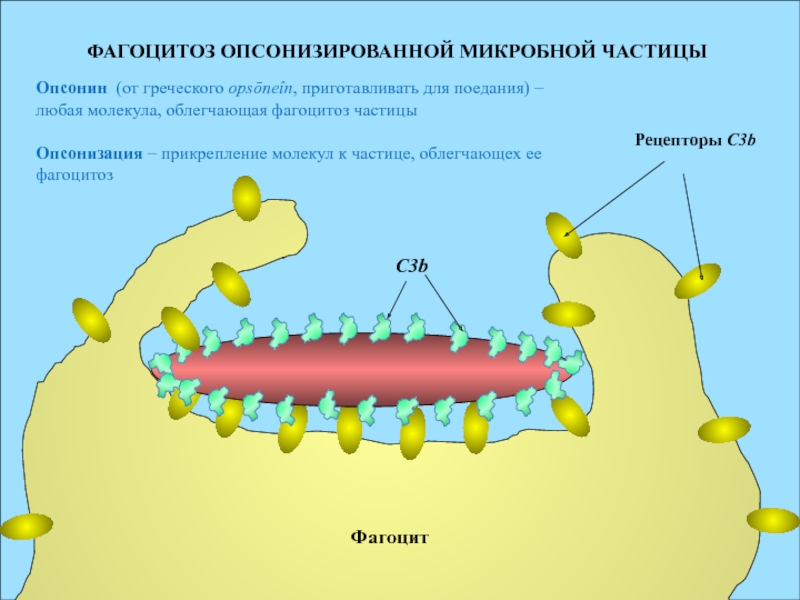
ФАГОЦИТОЗ ОПСОНИЗИРОВАННОЙ МИКРОБНОЙ ЧАСТИЦЫ
Рецепторы С3b
Фагоцит
Опсонин (от греческого opsōneîn, приготавливать для поедания)
любая молекула, облегчающая фагоцитоз частицы
Опсонизация – прикрепление молекул к частице, облегчающех ее фагоцитоз
Слайд 36
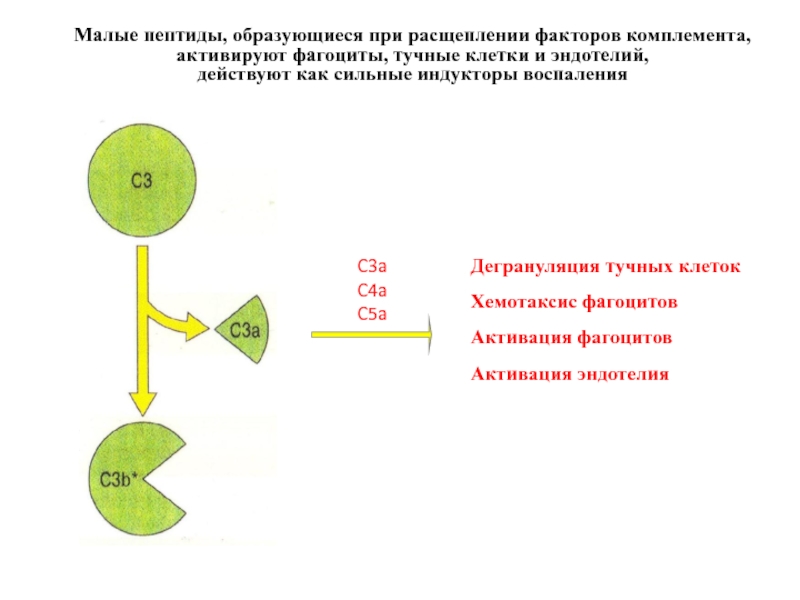
Малые пептиды, образующиеся при расщеплении факторов комплемента,
активируют фагоциты, тучные клетки
действуют как сильные индукторы воспаления
Дегрануляция тучных клеток
Хемотаксис фагоцитов
Активация фагоцитов
Активация эндотелия
C3a
C4a
C5a
Слайд 37
C3b
Лавинообразный процесс образования C3b и C3a.
Стабилизированные на поверхности молекулы C3b превращаются
Не стабилизированные молекулы C3b (в жидкой фазе) быстро разрушаются протеазами.
Молекулы C3a образуют диффузионный градиент с эпицентром на реакционной поверхности.
Слайд 38
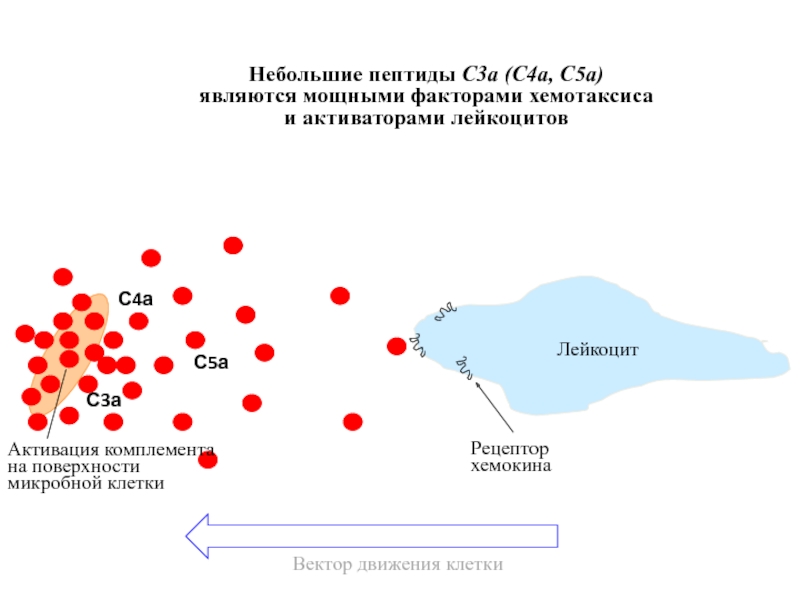
Небольшие пептиды С3a (C4a, C5a)
являются мощными факторами хемотаксиса
и активаторами лейкоцитов
Лейкоцит
Рецептор
хемокина
Активация комплемента
на поверхности
микробной клетки
Вектор движения клетки
С5а
С4а
С3а
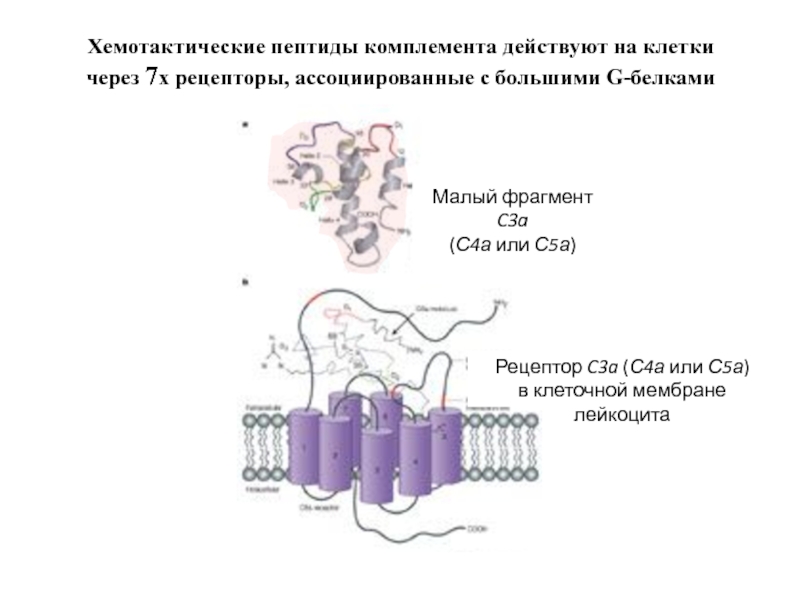
Слайд 39Рецептор C3a (С4а или С5а)
в клеточной мембране лейкоцита
Хемотактические пептиды комплемента действуют
через 7x рецепторы, ассоциированные с большими G-белками
Слайд 40
Индукторы хемотаксиса и воспаления:
Сигналы SOS, которые выделяют эпителиальные клетки, тучные клетки,
Вещества микробной природы (formyl-пептиды)
Малые пептиды комплемента C3a, C4a и C5a
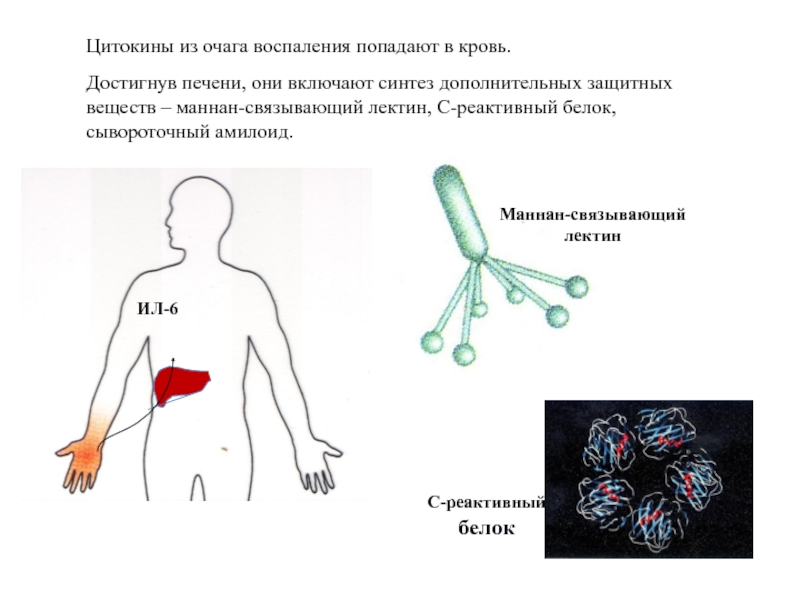
Слайд 41Цитокины из очага воспаления попадают в кровь.
Достигнув печени, они включают синтез
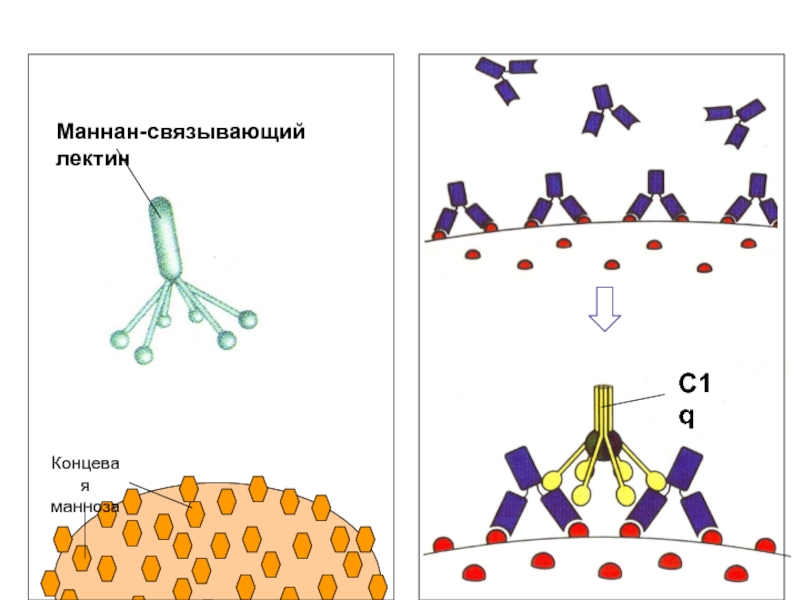
Маннан-связывающий
лектин
ИЛ-6
Слайд 44Маннан-связывающий лектин
Каждая субъединица (голова-шея) складывается
из трех небольших мономеров ~10kDa
Биологической активностью
тетрамеры, пентамеры или гексамеры,
то есть «чудовища» с 4, 5 или 6 головами
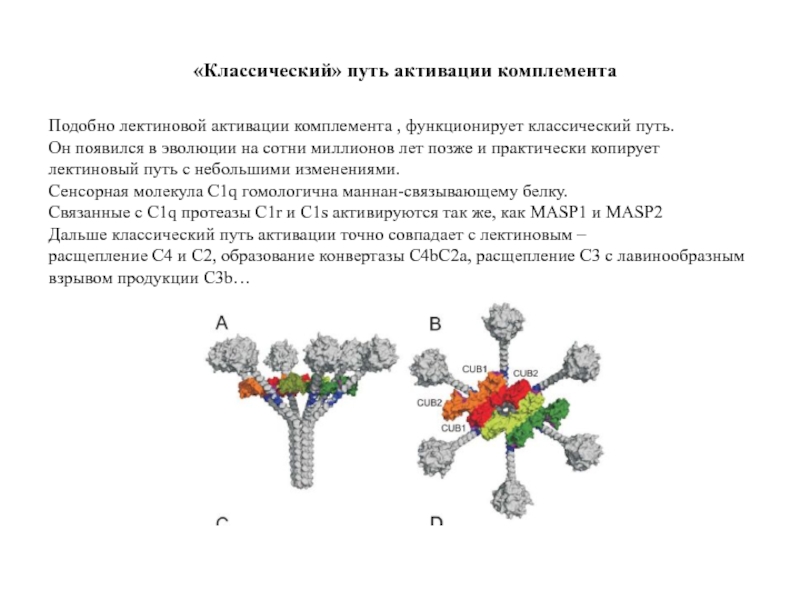
Слайд 46Figure 6 Structural Basis of Complement Activation in the Lectin Pathway
Alexandre R. Gingras , Umakhanth Venkatraman Girija , Anthony H. Keeble , Roshni Panchal , Daniel A. Mitchell , Pet...
Structural Basis of Mannan-Binding Lectin Recognition by Its Associated Serine Protease MASP-1: Implications for Complement Activation
Structure Volume 19, Issue 11 2011 1635 - 1643
http://dx.doi.org/10.1016/j.str.2011.08.014
Движение коллагеноподобных стержней молекулы маннан-связывающего лектина перемещает субъединицы MASP, что приводит к их суперпозиции и активации
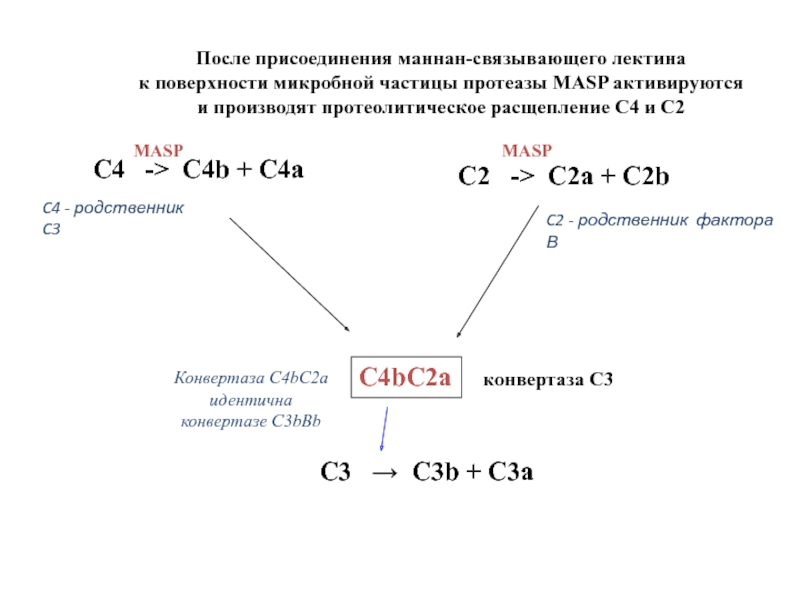
Слайд 47C4 -> C4b + C4a
C2 -> C2a + C2b
После
к поверхности микробной частицы протеазы MASP активируются
и производят протеолитическое расщепление C4 и C2
C4bC2a
конвертаза C3
MASP
MASP
C3 → C3b + C3a
C4 - родственник C3
C2 - родственник фактора В
Конвертаза C4bC2a
идентична
конвертазе C3bBb
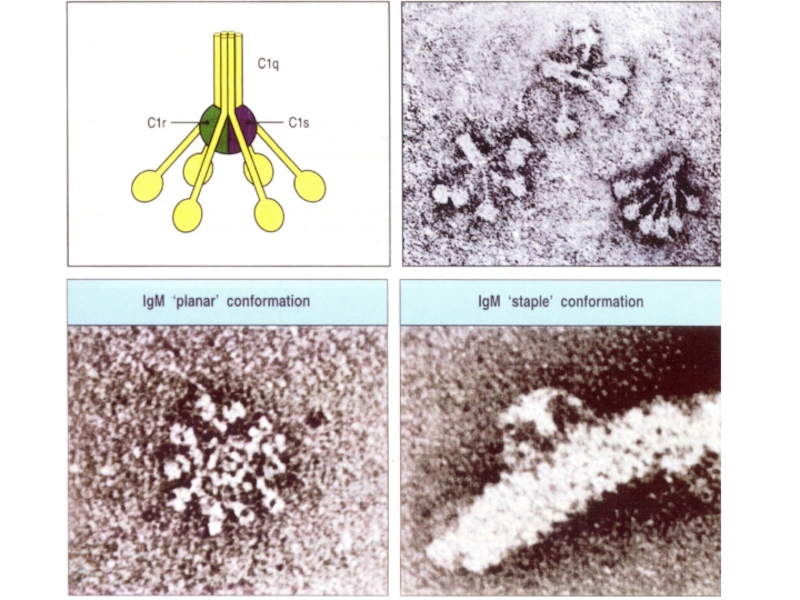
Слайд 48Подобно лектиновой активации комплемента , функционирует классический путь.
Он появился в эволюции
лектиновый путь с небольшими изменениями.
Сенсорная молекула С1q гомологична маннан-связывающему белку.
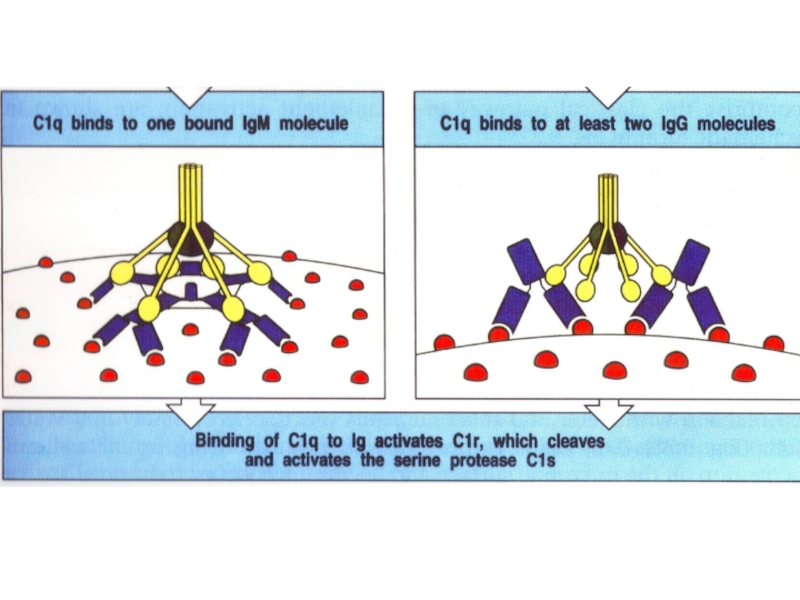
Связанные с C1q протеазы C1r и C1s активируются так же, как MASP1 и MASP2
Дальше классический путь активации точно совпадает с лектиновым –
расщепление C4 и C2, образование конвертазы C4bC2a, расщепление C3 с лавинообразным
взрывом продукции C3b…
«Классический» путь активации комплемента
Слайд 49Активация протеаз C1r происходит в результате
конформационных движений коллагеноподобных
тяжей C1q
Слайд 56Еще одно важное следствие работы твердофазовой конвертазы C3:
В результате нарастания концентрации
новых конвертаз C3b-Bb-C3b и C4b-2a-C3b.
Это – ферменты, расщепляющие C5 (конвертазы С5).
C3b-Bb
C4b-C2a
-C3b
-C3b
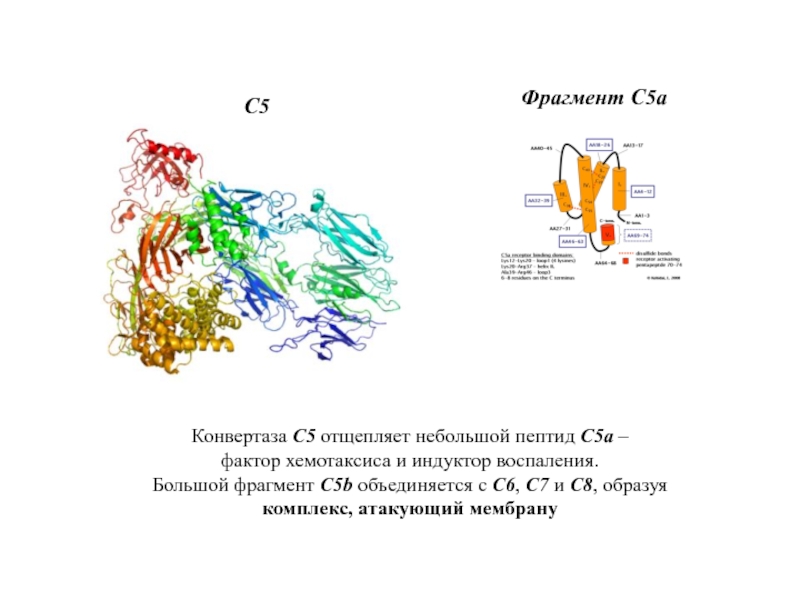
Слайд 58С5
Конвертаза C5 отщепляет небольшой пептид C5a –
фактор хемотаксиса и индуктор
Большой фрагмент C5b объединяется с C6, C7 и С8, образуя
комплекс, атакующий мембрану
Фрагмент С5а
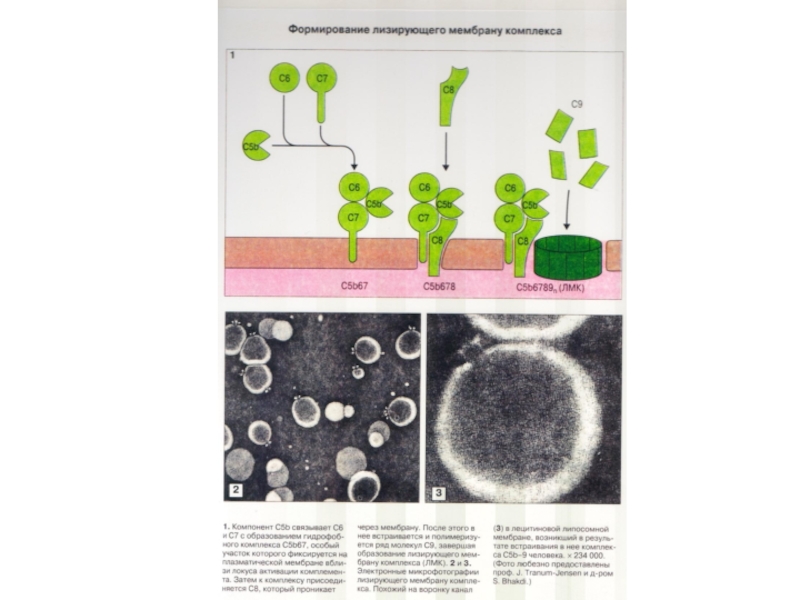
Слайд 62C5b объединяется с C6 и C7, комплекс сразу погружается в мембрану.
К
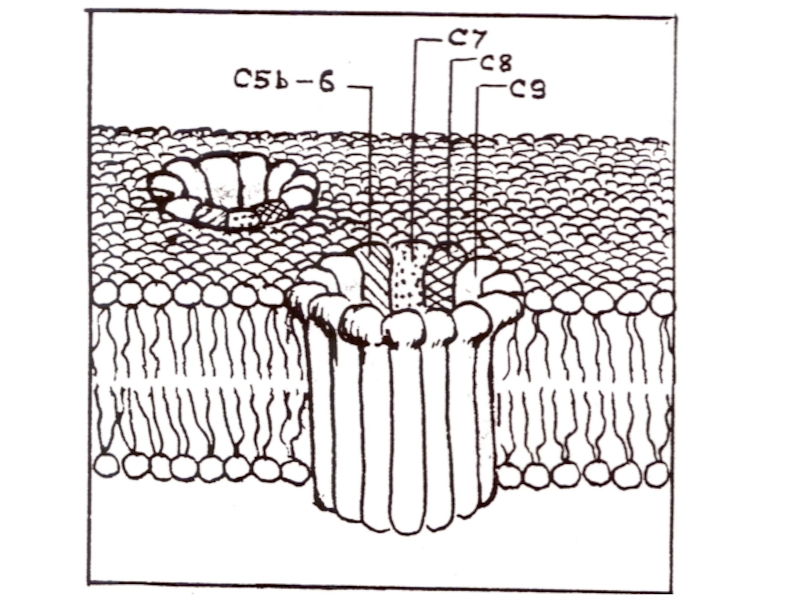
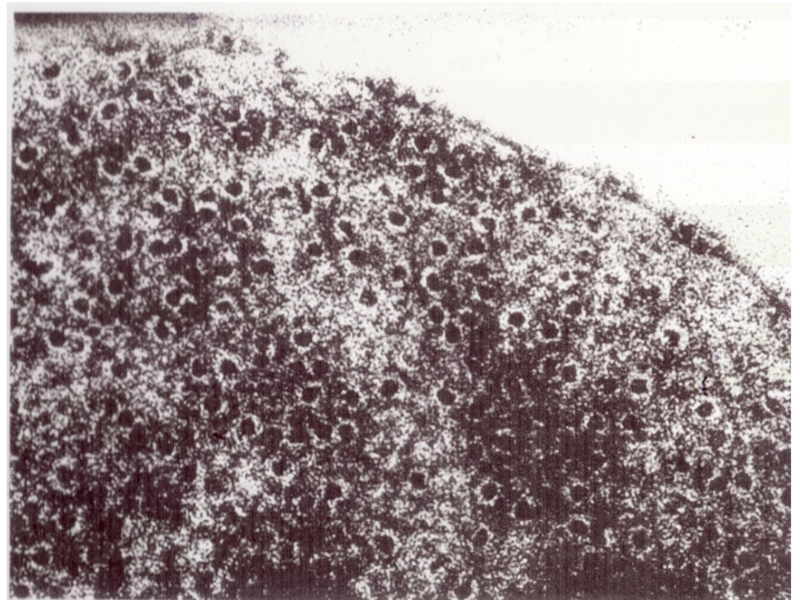
Слайд 63Комплекс C5b-6-7-8 служит инициатором сборки 12-14 молекул C9
в форме поры
Aleshin A E et al. J. Biol. Chem. 2012;287:10210-10222
Слайд 64Основные эффекторные функции комплемента
Опсонизация частиц (облегчение фагоцитоза).
Привлечение фагоцитов (хемотаксис).
Цитолиз незащищенных клеток
Индукция воспаления.
Слайд 68Математическая модель комплемента показывает, что распространение
лавинообразной активации (цепная реакция) останавливается
не в результате истощения каких-либо факторов комплемента, например,
С3 или B.
Главной причиной остановки взрыва является истощение поверхности,
на которой зародилась и распространяется цепная реакция.
Следовательно, реакция остановится только тогда, когда комплемент
«выжжет» всю доступную незащищенную поверхность.
Начавшись в одной точке поверхности (например, бактерия или вирус), комплемент химически модифицирует всю поверхность, без остатка (стратегия «выжженной земли»).
Слайд 71
Глюкозаминогликан/ сиаловая кислота
Глюкозаминогликан/ сиаловая кислота
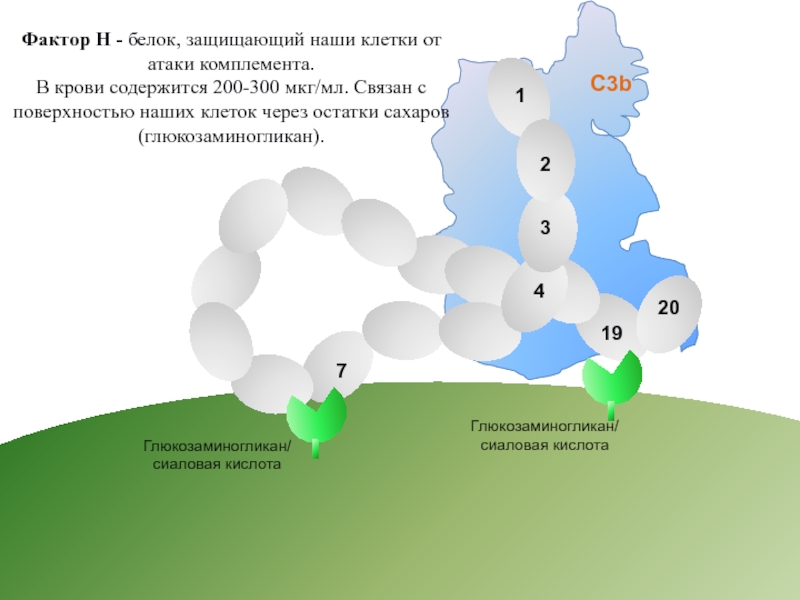
Фактор H - белок, защищающий наши клетки
В крови содержится 200-300 мкг/мл. Связан с поверхностью наших клеток через остатки сахаров (глюкозаминогликан).
C3b
Слайд 72Mapping FH and C3 mutants on complex structure. The molecules are
C3b
N-концевые домены фактора H прочно связываются с C3b
H
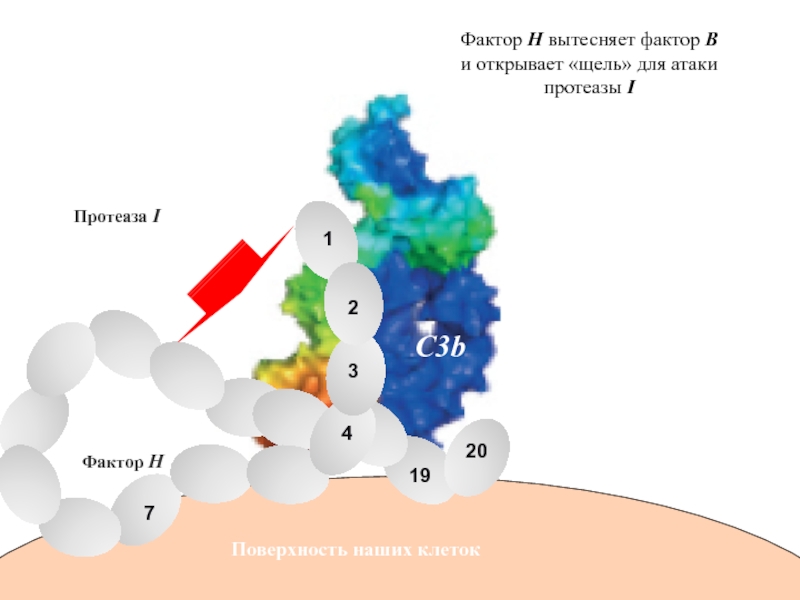
Слайд 73Фактор Н
Поверхность наших клеток
C3b
Фактор Н вытесняет фактор В
и открывает «щель»
протеазы I
Протеаза I
Слайд 74На поверхности наших клеток
протеаза I разрезает C3b на три части.
Этому
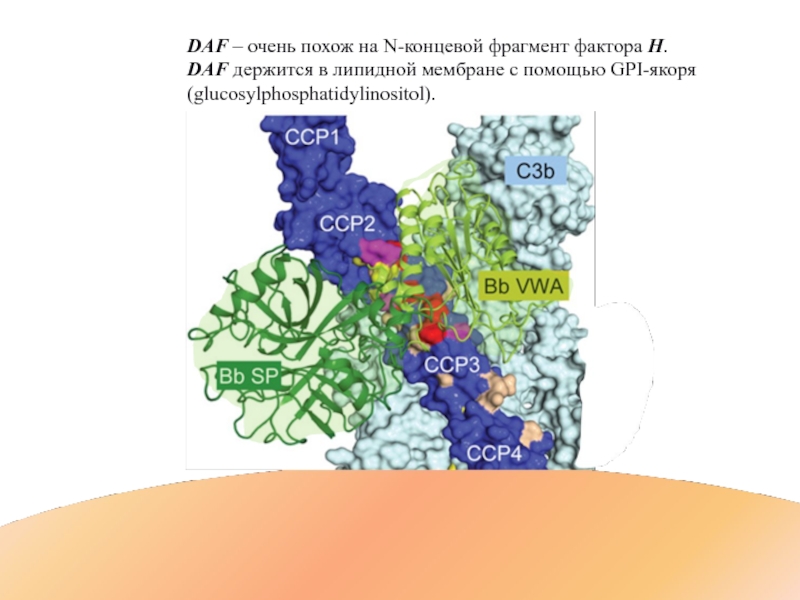
Слайд 75DAF – очень похож на N-концевой фрагмент фактора H.
DAF держится в
Слайд 76
Поверхность наших клеток
C3b
Протеаза I
Decay accelerating factor (DAF)
Фактор, ускоряющий распад
Слайд 79Комплекс C5b-6-7-8 служит инициатором сборки 12-14 молекул C9
в форме поры
Aleshin A E et al. J. Biol. Chem. 2012;287:10210-10222
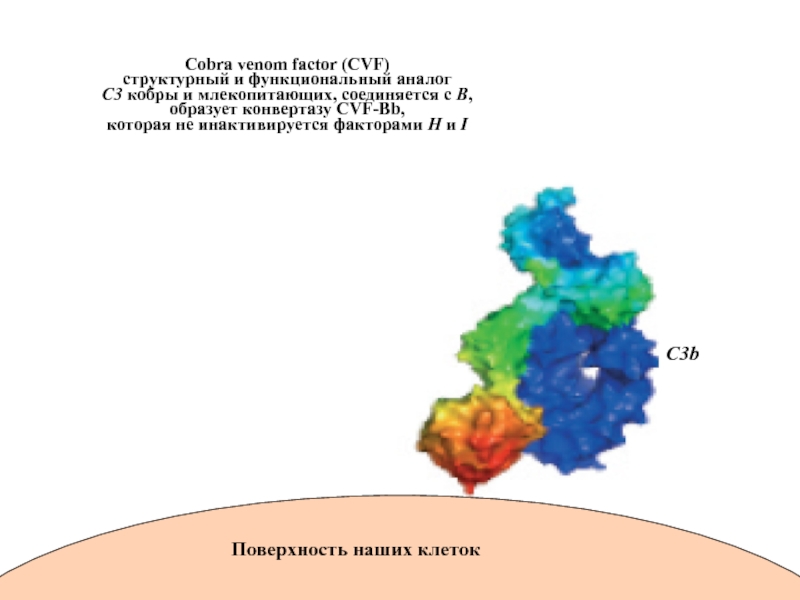
Слайд 81C3b
Поверхность наших клеток
Cobra venom factor (CVF)
структурный и функциональный аналог
С3 кобры
образует конвертазу CVF-Bb,
которая не инактивируется факторами H и I
Слайд 82
С3
С1q
С8
С2
С1r
С6
С4
С1s
С3b
С2b
С4b
С5
С5a
С5b
С9
С7
I
С4bp
H
P
DAF
D
Bb
MCP
СD59
MASP-
1
MASP-
2
CR1
CR2
H
CR4
H
H
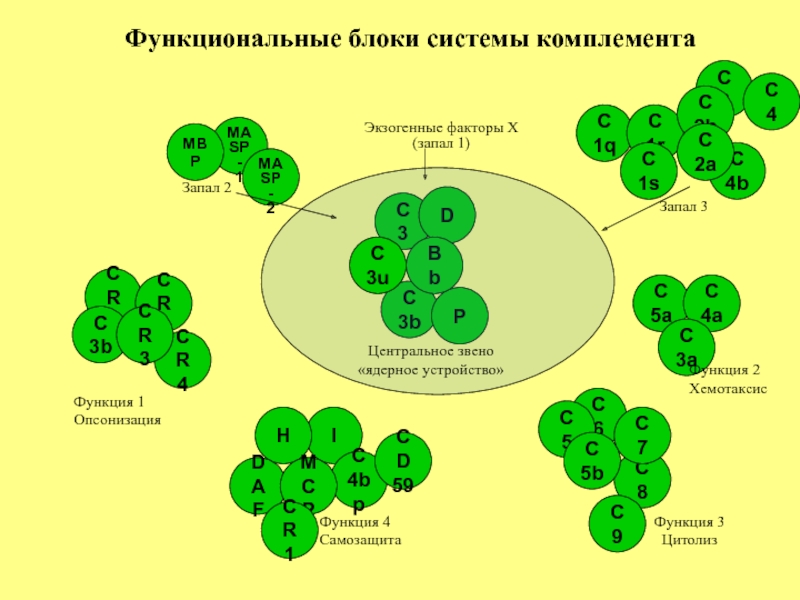
Функциональные блоки системы комплемента
С2a
MBP
CR1
С4a
С3a
С3u
Центральное звено
«ядерное устройство»
Функция 2
Хемотаксис
Запал 3
Функция 3
Цитолиз
Функция
Самозащита
Функция 1
Опсонизация
Экзогенные факторы X
(запал 1)
Запал 2
C3b
CR3
Слайд 84Клетки искусственно атаковали комплементом (розовые)
и без промедления перемешали с интактными
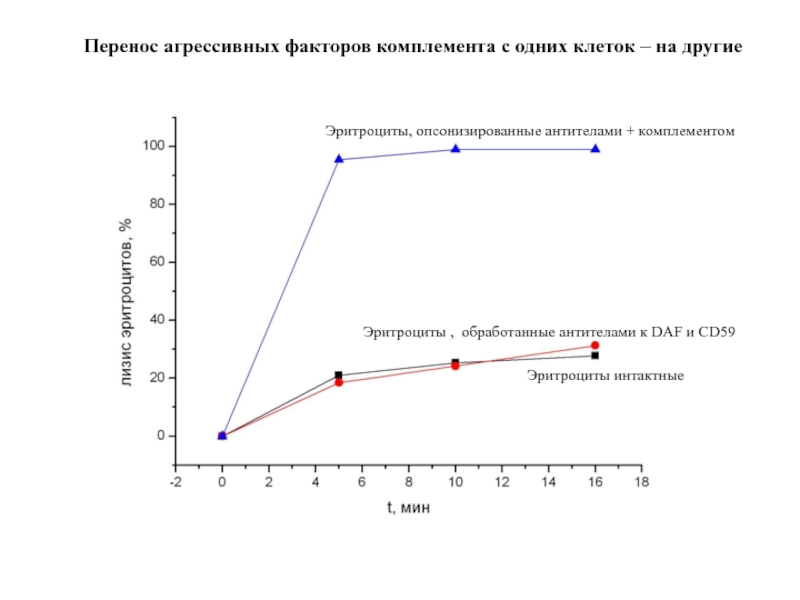
Слайд 85Перенос агрессивных факторов комплемента с одних клеток – на другие
Эритроциты интактные
Эритроциты
Эритроциты, опсонизированные антителами + комплементом
Слайд 86
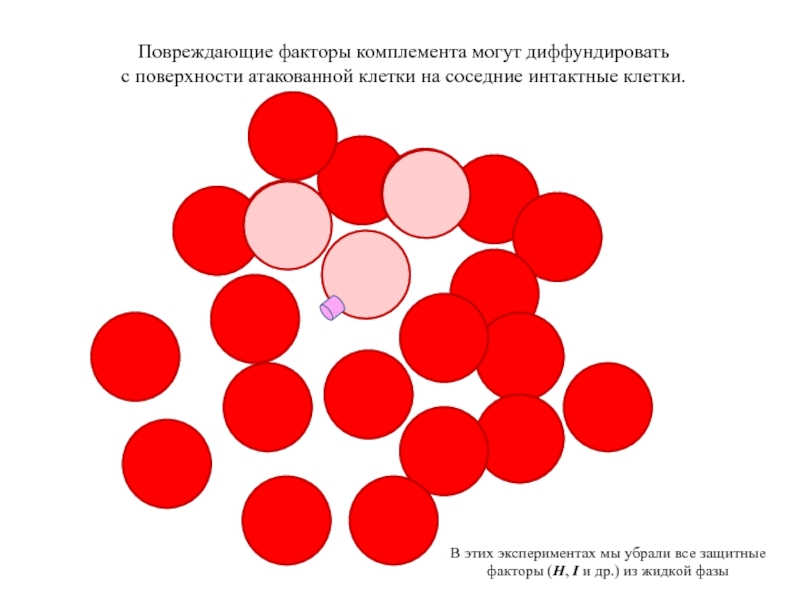
Повреждающие факторы комплемента могут диффундировать
с поверхности атакованной клетки на соседние
В этих экспериментах мы убрали все защитные факторы (H, I и др.) из жидкой фазы
Слайд 87
Атака комплемента ограничена размерами незащищенной поверхности.
Границы незначительно «размыты», но не
Распространение цепной реакции активированного комплемента в масштабах организма невозможно. Спасают два фактора – защитные вещества и короткое время жизни активных белков комплемента в жидкой фазе.
10 мкм
Слайд 88Система комплемента:
Точность (+10 мкм)
Быстрота (10-30 секунд)
Агрессивность (стратегия «выжженной земли»)
Удовлетворительная
Вездесущность (нет ни малейшего уголочка в организме, куда она не проникнет)
Локализация атаки в пространстве и во времени.
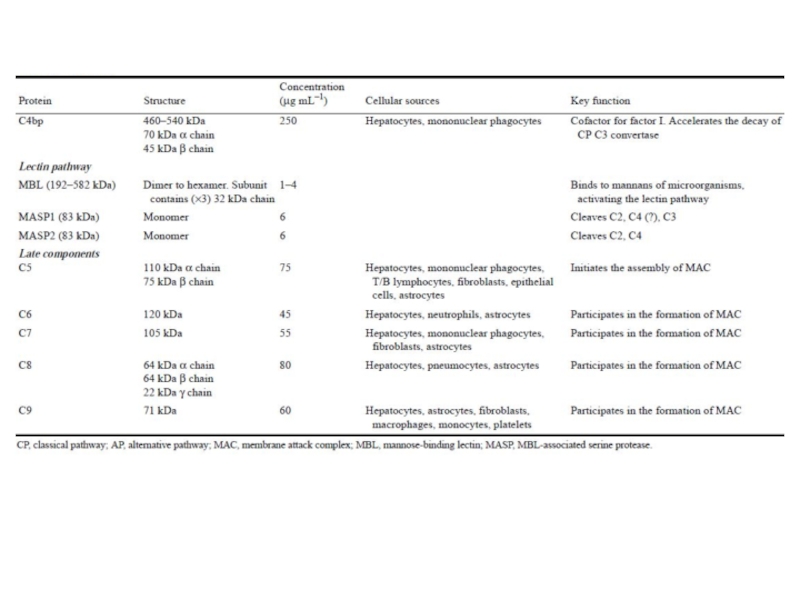
Слайд 89Большинство белков комплемента крупнее альбумина
(см. следующую таблицу), следовательно, через стенку
обычных
При изменении проницаемости кровеносных сосудов
вблизи очага инфекции или повреждения именно здесь
выходят белки комплемента и мгновенно запускают
смертельную для микробов атаку