- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Экологическая группа арбо- и робовирусов. Реовирусы. Рабдовирусы презентация
Содержание
- 1. Экологическая группа арбо- и робовирусов. Реовирусы. Рабдовирусы
- 2. Экологическая группа арбо- и робовирусов: общие признаки
- 3. Экологическая группа арбо- и робовирусов: состав Togaviridae (Alphavirus) Flaviviridae Bunyaviridae Arenaviridae Reoviridae Filoviridae
- 4. Флавивирусы сем. Flaviviridae (от
- 5. Флавивирусы: антигенные группы РТГА: клещевого энцефалита японского энцефалита лихорадки денге жёлтой лихорадки (типовой вид)
- 6. Строение Флавивирусы имеют сферическую форму. Вирион
- 7. Схема строения флавивируса
- 8. Флавивирусы: репродукция в цитоплазме свыше 20 часов
- 9. Флавивирусы: культивирование куриный эмбрион культура клеток (симпласты)
- 10. Флавивирусные инфекции умеренного пояса = группа клещевого
- 11. Клещевой энцефалит: возбудитель выделен в Восточной Сибири
- 12. Клещевой энцефалит: антигенные варианты вируса передаётся клещами
- 13. Клещевой энцефалит Прокормители клещей: Грызуны, Птицы, Дикие
- 14. Клещевой энцефалит: патогенез Трансмиссивно (укус клеща) Алиментарно
- 15. Клещевой энцефалит: клинические формы лихорадочная менингеальная очаговая (наиболее тяжёлая: – параличи шеи и верхних конечностей
- 16. Клещевой энцефалит: иммунитет напряжённый
- 17. Клещевой энцефалит: динамика появления антител через неделю
- 18. Клещевой энцефалит: вирусологическая диагностика Экспресс-диагностика Ag в
- 19. Клещевой энцефалит: иммунопрофилактика Вакцина: -
- 20. Вирус японского энцефалита РНК-содержащий вирус рода
- 21. Японский энцефалит полиморфное заболевание – от бессимптомного
- 22. Японский энцефалит Для профилактики: – культуральная
- 23. Вирус омской геморрагической лихорадки По антигенным свойствам
- 24. ОМСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА Природно-очаговое заболевание, Встречается на
- 25. ОМСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА Пути передачи: Укус клеща, Снятие шкурок, Через инфицированную вирусом воду.
- 26. ОМСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА Характерно: поражение эндотелия кровеносных
- 27. Жёлтая лихорадка = особо опасная карантинная инфекция,
- 28. Патогенез желтой лихорадки Размножается в регионарных лимфатических
- 29. Специфическая профилактика Людям, направляющимся в неблагополучные
- 30. Буньявирусы: классификация Bunyaviridae Bunyavirus – комариные энцефалиты
- 31. Буньявирусы: структура Вирион буньявирусов — сферический, окружен
- 32. Буньявирусы: свойства репродукция в цитоплазме (отпочковывание через
- 33. Микробиологическая диагностика Вирусы культивируют путем внутримозго-
- 34. Крымская (крым-конго) геморрагическая лихорадка: патогенез укус иксодового
- 35. Геморрагическая лихорадка с почечным синдромом (ГЛПС) резервуар
- 36. Аренавирусы: свойства электронно-плотные гранулы (рибосомальные агрегаты клетки-хозяина)
- 37. Аренавирусы: структура Вирион, имеет сферическую или
- 38. Строение вириона
- 39. Аренавирусы: репродукция — в цитоплазме;
- 40. Микробиологическая диагностика Вирусологический метод: вирус выделяют из
- 41. Специфическая профилактика Для специфической профилактики разрабатываются живые вакцины.
- 42. Вирус лимфоцитарного хориоменингита (ЛХМ) вызывает лимфоцитарный
- 43. Филовирусы (от пах. filum — нить)
- 44. Филовирусы: структура - Вирусы имеют вид
- 45. Электронограмма вирионов Эбола
- 46. Филовирусы: репродукция Репродукция и сборка —
- 47. Микробиологическая диагностика Проводится в специализированных лабораториях с
- 48. Вирус Эбола 2 серовара Суданский Заирский от
- 49. Реовирусы (семейство Reoviridae) Реовирусы (от первых букв
- 50. Структура реовирусов и ротавирусов Вирионы реовирусов имеют
- 51. Структура реовирусов и ротавирусов Внутренний капсид реовирусов
- 52. Структура реовирусов и ротавирусов Наружный капсид реовирусов
- 53. Структура реовирусов и ротавирусов
- 54. Ротавирусы
- 55. Ротавирусные гастроэнтериты: общая характеристика у взрослых –
- 56. Ротавирусные гастроэнтериты: патогенез больные и вирусоносители ⇓
- 57. Ротавирусные гастроэнтериты: вирусологическая диагностика Обнаружение вирусов в
- 58. Рабдовирусы: классификация Rhabdoviridae Vesiculovirus (вирус везикулярного стоматита – арбовирус) Lyssavirus (вирус бешенства)
- 59. Рабдовирусы: структура Вирусы имеют форму цилиндра с
- 60. Рабдовирусы: структура
- 61. Вирус бешенства Вызывает бешенство (rhabies, синонимы —
- 62. Вирус бешенства Различают два вируса бешенства:
- 63. Вирус-фикс (virus fixe) Пастер (+ Ру и
- 64. Свойства вируса бешенства мало устойчив во внешней среде репродуцируется в цитоплазме (включения Бабеша-Негри)
- 65. Вирус бешенства
- 66. Бешенство: патогенез укус или ослюнение ⇓ первичная
- 67. Бешенство: периоды болезни инкубационный (от 7 дней
- 68. Бешенство: вирусологическая диагностика Обнаружение включений Бабеша-Негри (не
- 69. Включения Бабеша-Негри
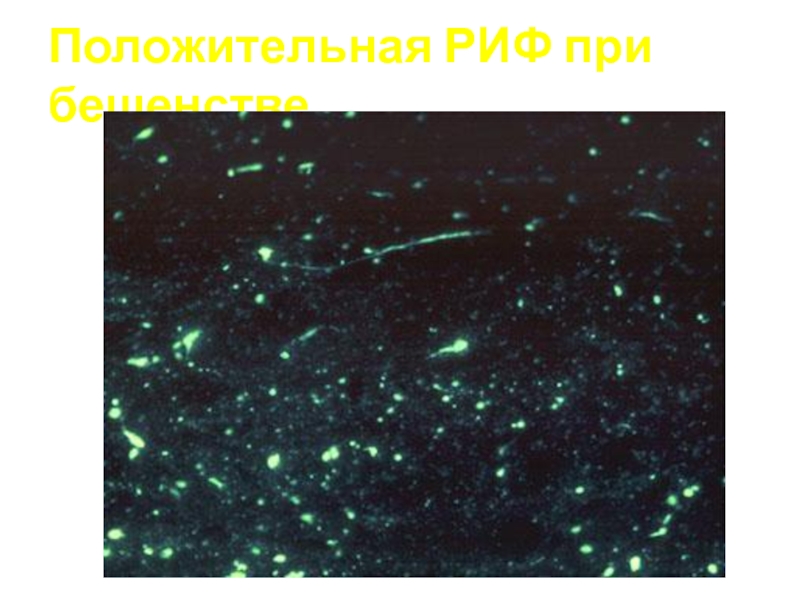
- 70. Положительная РИФ при бешенстве
- 71. Современные препараты для профилактики бешенства Антирабические вакцины
Слайд 3Экологическая группа арбо- и робовирусов: состав
Togaviridae (Alphavirus)
Flaviviridae
Bunyaviridae
Arenaviridae
Reoviridae
Filoviridae
Слайд 4
Флавивирусы
сем. Flaviviridae
(от лат. ftavus — желтый, по типовому вирусу желтой
лихорадки) — семейство РНК-содержащих оболочечных вирусов
Слайд 5Флавивирусы:
антигенные группы
РТГА:
клещевого энцефалита
японского энцефалита
лихорадки денге
жёлтой лихорадки (типовой вид)
Слайд 6Строение
Флавивирусы имеют сферическую форму.
Вирион состоит из оболочки, капсида и генома
— однонитевой линейной плюс-РНК.
Шипы оболочки состоят из двух белков, из них (Е1) является гемагглютинином.
Шипы оболочки состоят из двух белков, из них (Е1) является гемагглютинином.
Слайд 8Флавивирусы: репродукция
в цитоплазме
свыше 20 часов
отпочковывание от мембран эндоплазматического ретикулума (выход из
клетки – путём экзоцитоза) – клетка долго остаётся жизнеспособной
Слайд 10Флавивирусные инфекции умеренного пояса = группа клещевого энцефалита
клещевой энцефалит
японский (русский, осенний)
энцефалит
омская геморрагическая лихорадка
омская геморрагическая лихорадка
Слайд 11Клещевой энцефалит: возбудитель
выделен в Восточной Сибири (Л.А.Зильбер, 1937)
изменчив (антигенные и биологические
свойства)
нейротропность
устойчив в кислой среде
нейротропность
устойчив в кислой среде
Слайд 12Клещевой энцефалит: антигенные варианты вируса
передаётся клещами Ixodes perculcatus (таежный) → тяжёлая
форма инфекции на Дальнем Востоке
передаётся клещами Ixodes ricinus (лесной)→ более лёгкая форма инфекции
У клещей происходит трансовариальная и трансфазовая передача вируса
передаётся клещами Ixodes ricinus (лесной)→ более лёгкая форма инфекции
У клещей происходит трансовариальная и трансфазовая передача вируса
Слайд 13Клещевой энцефалит
Прокормители клещей:
Грызуны,
Птицы,
Дикие и домашние животные.
Человек – тупиковое звено.
Природно-очаговое заболевание.
Слайд 14Клещевой энцефалит: патогенез
Трансмиссивно (укус клеща)
Алиментарно (сырое коровье и козье молоко)
⇓
кровь
⇓
первичная репликация
лимфоциты
гепатоциты
клетки
селезёнки
эндотелий сосудов
⇓
генерализация
гематогенная
лимфогенная
⇓
вторичная репликация
двигательные нейроны передних рогов шейного сегмента спинного мозга
мозжечок
мягкая оболочка головного мозга
эндотелий сосудов
⇓
генерализация
гематогенная
лимфогенная
⇓
вторичная репликация
двигательные нейроны передних рогов шейного сегмента спинного мозга
мозжечок
мягкая оболочка головного мозга
Слайд 15Клещевой энцефалит: клинические формы
лихорадочная
менингеальная
очаговая (наиболее тяжёлая: – параличи шеи и верхних
конечностей
Слайд 17Клещевой энцефалит: динамика появления антител
через неделю после заражения – антигемагглютинины (РТГА)
через
2 недели после заражения – комплементсвязывающие (РСК)
через месяц после заражения – вирус нейтрализующие (РН)
через месяц после заражения – вирус нейтрализующие (РН)
Слайд 18Клещевой энцефалит: вирусологическая диагностика
Экспресс-диагностика
Ag в крови (РНГА, ИФА)
геном вируса в крови
(ПЦР)
Вирусологический метод
кровь, ликвор
⇓
интрацеребральное заражения мышей-сосунков
⇓
3 – 4 пассажа
⇓
Ag в мозговой ткани
РНГА
РСК
РН (наиболее специфичная реакция)
Серологический метод
парные сыворотки (в зависимости от динамики появления антител)
Вирусологический метод
кровь, ликвор
⇓
интрацеребральное заражения мышей-сосунков
⇓
3 – 4 пассажа
⇓
Ag в мозговой ткани
РНГА
РСК
РН (наиболее специфичная реакция)
Серологический метод
парные сыворотки (в зависимости от динамики появления антител)
Слайд 19Клещевой энцефалит: иммунопрофилактика
Вакцина:
- культуральная инактивированная формалином,
FISME immun-inject –
культуральная очищенная концентрированная, Австрия,
Энцепур-К - очищенная концентрированная инактивированная, ФРГ
2. Специфический иммуноглобулин
Донорский (из плазм доноров, проживающих на территории природных очагов),
Гетерологичный лошадиный
Энцепур-К - очищенная концентрированная инактивированная, ФРГ
2. Специфический иммуноглобулин
Донорский (из плазм доноров, проживающих на территории природных очагов),
Гетерологичный лошадиный
Слайд 20Вирус японского энцефалита
РНК-содержащий вирус рода Flavivirus семейства Flaviviridae,
Обладает нейротропностью, размножается
в нейронах ЦНС (вызывая их гибель)
Слайд 21Японский энцефалит
полиморфное заболевание – от бессимптомного до тяжелейшего: лихорадки, интоксикации, менинго-энцефалита
передаётся
комарами (от человека – лишь при массовых эпидемиях)
Природный резервуар и источник = комары, птицы, дикие млекопитающие, свиньи
Природный резервуар и источник = комары, птицы, дикие млекопитающие, свиньи
Слайд 22Японский энцефалит
Для профилактики:
– культуральная инактивированная сорбированная вакцина из штамма Пекин-1,
-
Живая аттенуированная вакцина из дикого штамма SA14
Лечение – в первые дни сыворотка переболевших или гетерологичный иммуноглобулин
Лечение – в первые дни сыворотка переболевших или гетерологичный иммуноглобулин
Слайд 23Вирус омской геморрагической лихорадки
По антигенным свойствам близок вирусу клещевого энцефалита,
Отличие –
не проявляет нейротропных свойств,
Размножается в культуре клеток без ЦПД, исключение клетки эмбриона свиньи (разрушение монослоя)
Размножается в культуре клеток без ЦПД, исключение клетки эмбриона свиньи (разрушение монослоя)
Слайд 24ОМСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА
Природно-очаговое заболевание,
Встречается на территории Западной Сибири,
Характерна сезонность:
- весенне-осенняя
лихорадка связана с движением клещей,
- осенне-зимний период – отлов ондатр,
Природный хозяин и переносчик –клещ (норовый болотный и пастбищный),
Естественный резервуар птицы, грызуны, особенно ондатра,
Человек – тупиковое звено.
- осенне-зимний период – отлов ондатр,
Природный хозяин и переносчик –клещ (норовый болотный и пастбищный),
Естественный резервуар птицы, грызуны, особенно ондатра,
Человек – тупиковое звено.
Слайд 25ОМСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА
Пути передачи:
Укус клеща,
Снятие шкурок,
Через инфицированную вирусом воду.
Слайд 26ОМСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА
Характерно: поражение эндотелия кровеносных капилляров, нервной системы и надпочечников.
Клинические проявления: лихорадка, интоксикация, геморрагический синдром, менингоэнцефалит
Слайд 27Жёлтая лихорадка
= особо опасная карантинная инфекция,
один серотип вируса,
поражается:
печень (основное место репродукции)
⇨ желтуха
почки ⇨ жировое перерождение
миокард ⇨ дегенеративные изменения
Механизм заражения – трансмиссивный,
типы:
джунглевая (лесная) – комарами от обезьян
городская (классическая) – комарами от людей
почки ⇨ жировое перерождение
миокард ⇨ дегенеративные изменения
Механизм заражения – трансмиссивный,
типы:
джунглевая (лесная) – комарами от обезьян
городская (классическая) – комарами от людей
Слайд 28Патогенез желтой лихорадки
Размножается в регионарных лимфатических узлах → кровь → вирусемия
→ печень, почки, селезенка, головной мозг → дистрофия и некроз гепатоцитов,
Поражается клубочковый и канальцевый аппараты почек
Поражается клубочковый и канальцевый аппараты почек
Слайд 29Специфическая профилактика
Людям, направляющимся в неблагополучные по желтой лихорадке регионы, прививают
живую вакцину (штамм 17 D), которая создает длительный иммунитет (более 10 лет); ревакцинацию проводят раз в 20 лет.
Менее распространена живая вакцина из штамма «Дакар».
Менее распространена живая вакцина из штамма «Дакар».
Слайд 30Буньявирусы: классификация
Bunyaviridae
Bunyavirus – комариные энцефалиты
Phlebovirus – москитные лихорадки
Nairovirus (Nairobivirus) – вирус
крымской геморрагической лихорадки (иксодовые клещи)
Hantavirus – вирус ГЛПС (робовирус)
Hantavirus – вирус ГЛПС (робовирус)
Слайд 31Буньявирусы: структура
Вирион буньявирусов — сферический,
окружен оболочкой с двумя гликопротеинами (G1, G2);
включает
три уникальные кольцевые минус однонитевые РНК, связанные с N-белком (нуклеокапсиды).
Симметрия капсида спиральная.
Нуклеокапсиды включают большую (L), среднюю (М) и малую (S) нити РНК, связанные с РНК-зависимой РНК-пол имеразой (L-белок), и два неструктурных белка (NSs, NSm).
В отличии от других однонитевых минус-РНК-вых вирусов, буньявирусы не имеют матриксного белка.
Симметрия капсида спиральная.
Нуклеокапсиды включают большую (L), среднюю (М) и малую (S) нити РНК, связанные с РНК-зависимой РНК-пол имеразой (L-белок), и два неструктурных белка (NSs, NSm).
В отличии от других однонитевых минус-РНК-вых вирусов, буньявирусы не имеют матриксного белка.
Слайд 32Буньявирусы: свойства
репродукция в цитоплазме (отпочковывание через аппарат Гольджи, выход путём экзоцитоза
или при лизисе клетки-хозяина)
Слайд 33Микробиологическая диагностика
Вирусы культивируют путем внутримозго-
вого заражения новорожденных белых мышей, крыс
и хомячков.
Для определения антигенов вирусов или антител в крови применяют РСК, РТГА, РН, ИФА, РИА. Маркерные гены определяют в ПЦР.
Для определения антигенов вирусов или антител в крови применяют РСК, РТГА, РН, ИФА, РИА. Маркерные гены определяют в ПЦР.
Слайд 34Крымская (крым-конго) геморрагическая лихорадка: патогенез
укус иксодового клеща
контактный путь
⇓
кровь
⇓
тяжёлые множественные кровоизлияния
полость желудка
полость
кишечника
лёгкие
кожа (сыпь)
⇓
[инфекционно-токсический шок с диссеминированным внутрисосудистым свёртыванием крови]
Смертность 8 – 12 % (может – до 40 %)
лёгкие
кожа (сыпь)
⇓
[инфекционно-токсический шок с диссеминированным внутрисосудистым свёртыванием крови]
Смертность 8 – 12 % (может – до 40 %)
Слайд 35Геморрагическая лихорадка с почечным синдромом (ГЛПС)
резервуар инфекции – мышевидные грызуны
инфицирование: контакт
(кожи и слизистых) с их экскрементами
основное место репродукции вируса – эндотелий сосудов (преимущественно – мозгового слоя почек)
большинство больных выздоравливает, но при геморрагическом нефрозонефрите смертность (в среднем 5-10%) может достигать 44%
основное место репродукции вируса – эндотелий сосудов (преимущественно – мозгового слоя почек)
большинство больных выздоравливает, но при геморрагическом нефрозонефрите смертность (в среднем 5-10%) может достигать 44%
Слайд 36Аренавирусы: свойства
электронно-плотные гранулы (рибосомальные агрегаты клетки-хозяина)
5 фрагментов РНК (2 – вирусоспецифические)
2
антигенные группы (РСК, внутри – РН)
Старого Света
вирус лимфоцитарного хориоменингита
вирус Ласса
Нового Света
вирус Хунин
вирус Мачупо
робовирусы
вызывают (кроме ВЛХ) тяжелейшие заболевания со смертностью до 70%
Старого Света
вирус лимфоцитарного хориоменингита
вирус Ласса
Нового Света
вирус Хунин
вирус Мачупо
робовирусы
вызывают (кроме ВЛХ) тяжелейшие заболевания со смертностью до 70%
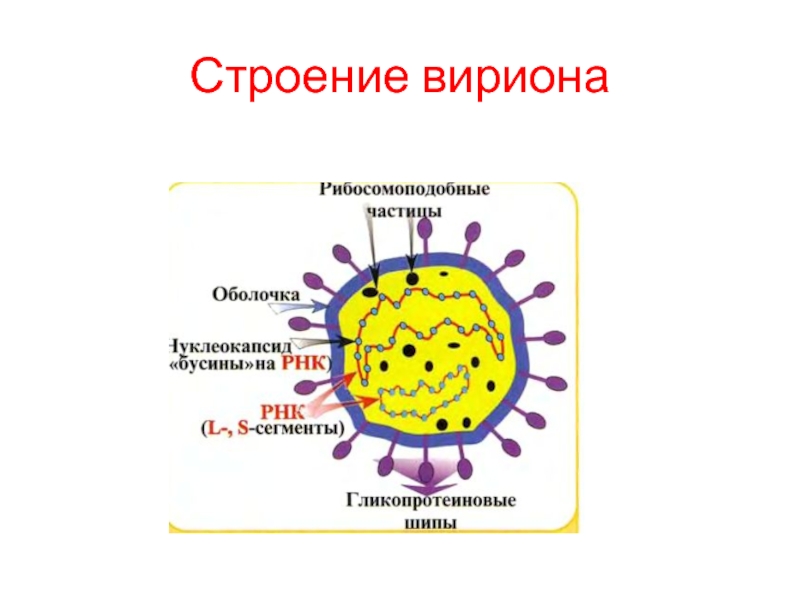
Слайд 37Аренавирусы: структура
Вирион, имеет сферическую или овальную форму.
Снаружи окружен оболочкой
с булавовидными гликопротеиновыми шипами 6Р1 и GP2.
Под оболочкой расположены 12-15 клеточных рибосом, похожих на песчинки, что отражено в названии семейства.
Капсид — спиральный.
Геном представлен 2 сегментами (L, S) однонитевой минус-РНК;
кодирует 5 белков, в частности, L-, Z-, N-, G-белки.
Вирион содержит транскриптазу (L-белок, РНК-полимераза).
Под оболочкой расположены 12-15 клеточных рибосом, похожих на песчинки, что отражено в названии семейства.
Капсид — спиральный.
Геном представлен 2 сегментами (L, S) однонитевой минус-РНК;
кодирует 5 белков, в частности, L-, Z-, N-, G-белки.
Вирион содержит транскриптазу (L-белок, РНК-полимераза).
Слайд 39Аренавирусы: репродукция
— в цитоплазме;
после сборки и включения в вирион
рибосомоподобных частиц происходит его почкование через плазматическую мембрану клетки.
Слайд 40Микробиологическая диагностика
Вирусологический метод: вирус выделяют из крови, отделяемого глотки, из плевральной,
цереброспинальной жидкости, мочи при заражении культуры клеток или мышей-сосунков, хомячков. Вирусы идентифицируют в РСК, РН, РИФ, ИФА; применяют ПЦР.
Серологический метод: антитела в сыворотке крови выявляют в РСК, РИФ, ИФА.
Серологический метод: антитела в сыворотке крови выявляют в РСК, РИФ, ИФА.
Слайд 42Вирус лимфоцитарного хориоменингита (ЛХМ)
вызывает лимфоцитарный хориоменингит, протекающий в виде гриппоподобного
заболевания или тяжелых форм в виде серозного менингита или менингоэнцефалита с лейко- и тром- боцитоленией.
ЛХМ распространяется с выделениями домашних мышей, загрязняющих продукты питания, воду и воздух.
ЛХМ распространяется с выделениями домашних мышей, загрязняющих продукты питания, воду и воздух.
Слайд 43Филовирусы
(от пах. filum — нить) — семейство нитевидных РНК-содержащих оболочечных
вирусов.
Содержит:
род «Марбург-подобных вирусов»
род «Эбола-подобных вирусов»,
эндемичны для Африки (от обезьян)
Вызывают крайне тяжёлые геморрагические лихорадки.
Вирус Марбург передается при контакте с тканями больной африканской зеленой макаки или сывороткой крови больного человека. Выделен в 1967 г. в г. Марбурге.
Вирус Эбола впервые выделен в 1976 г. при эпидемии в Заире и Судане. Летальность 90 %. Передается при контакте с больными. Возможны воздушно-капельный и половой пути передачи.
Содержит:
род «Марбург-подобных вирусов»
род «Эбола-подобных вирусов»,
эндемичны для Африки (от обезьян)
Вызывают крайне тяжёлые геморрагические лихорадки.
Вирус Марбург передается при контакте с тканями больной африканской зеленой макаки или сывороткой крови больного человека. Выделен в 1967 г. в г. Марбурге.
Вирус Эбола впервые выделен в 1976 г. при эпидемии в Заире и Судане. Летальность 90 %. Передается при контакте с больными. Возможны воздушно-капельный и половой пути передачи.
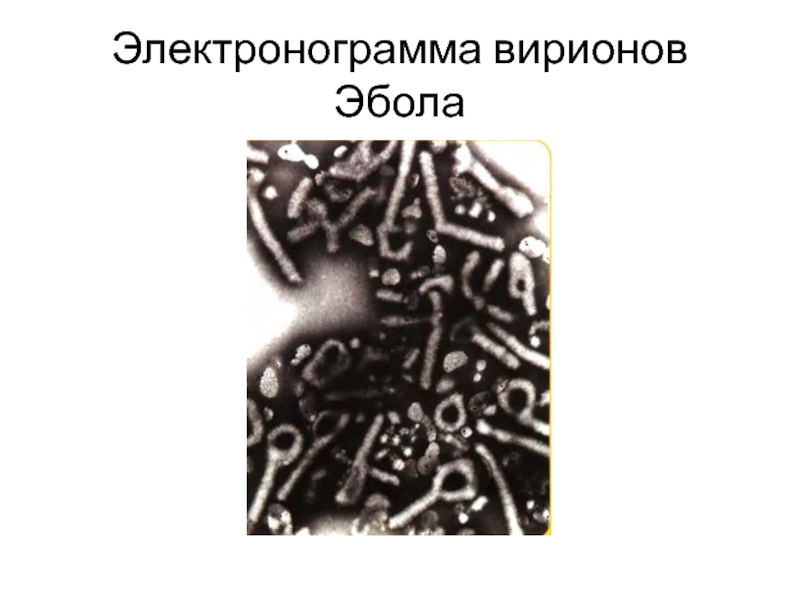
Слайд 44Филовирусы: структура
- Вирусы имеют вид длинных филаментов с оболочкой и
однонитевой минус- РНК, заключенной в капсид.
- Симметрия капсида спиральная.
- На оболочке имеются гликопротеиновые шипы (спикулы).
- При электронной микроскопии негативно контрастированных препаратов вируса Эбола видны нитевидные, иногда ветвящиеся вирионы, имеющие форму цифры или кольца. Они состоят из липопротеиновой оболочки (с поверхностными выступами — шипами), окружающей спиральный нуклеокапсид.
- Симметрия капсида спиральная.
- На оболочке имеются гликопротеиновые шипы (спикулы).
- При электронной микроскопии негативно контрастированных препаратов вируса Эбола видны нитевидные, иногда ветвящиеся вирионы, имеющие форму цифры или кольца. Они состоят из липопротеиновой оболочки (с поверхностными выступами — шипами), окружающей спиральный нуклеокапсид.
Слайд 46Филовирусы: репродукция
Репродукция и сборка — в цитоплазме.
Выход из клетки
— почкованием через клеточную мембрану.
Слайд 47Микробиологическая диагностика
Проводится в специализированных лабораториях с допуском к работе с вирусами
1 группы патогенности.
Для определения компонентов вирусов и антител применяют ПЦР, РИФ, ИФА, РН, РСК.
Вирусы выделяют на культуре клеток VeroEb и на морских свинках.
Для определения компонентов вирусов и антител применяют ПЦР, РИФ, ИФА, РН, РСК.
Вирусы выделяют на культуре клеток VeroEb и на морских свинках.
Слайд 48Вирус Эбола
2 серовара
Суданский
Заирский
от обезьян и людей
контактный и аэрозольные пути (в т.ч.
через медицинский инструментарий)
нарушение функции тромбоцитов вплоть до развития геморрагического шока (смертность от 30 до 90%)
нарушение функции тромбоцитов вплоть до развития геморрагического шока (смертность от 30 до 90%)
Слайд 49Реовирусы (семейство Reoviridae)
Реовирусы (от первых букв англ. respiratory, enteric, orphan viruses)
— семейство безоболочечных вирусов, содержащих двунитевую фрагментированную РНК; включает респираторные и кишечные вирусы, а также некоторые арбовирусы. Семейство содержит 4 рода: Orthoreovirus, Orbivirus, Coltivirus, Rotavirus.
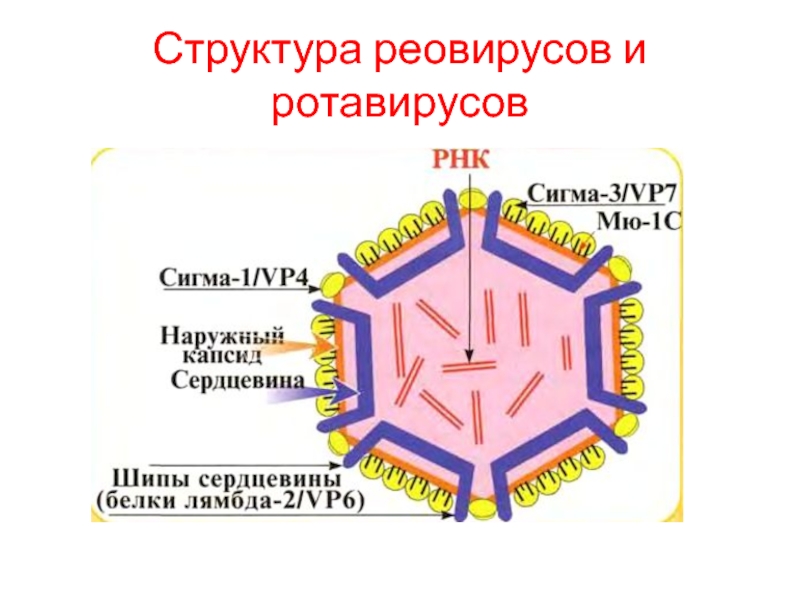
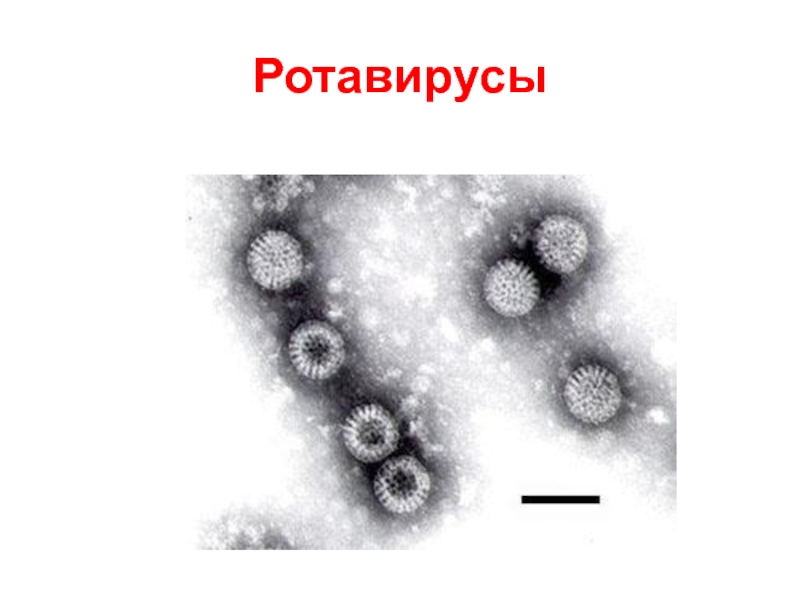
Слайд 50Структура реовирусов и ротавирусов
Вирионы реовирусов имеют сферическую форму, двухслойный капсид икосаэдрического
типа; оболочки нет.
Геном представлен двунитевой фрагментированной линейной РНК (10-11).
Вирион содержит транскриптазу (РНК- зависимую РНК-полимеразу).
Внутренний капсид и геномная РНК составляют сердцевину вириона.
Геном представлен двунитевой фрагментированной линейной РНК (10-11).
Вирион содержит транскриптазу (РНК- зависимую РНК-полимеразу).
Внутренний капсид и геномная РНК составляют сердцевину вириона.
Слайд 51Структура реовирусов и ротавирусов
Внутренний капсид реовирусов содержит систему транскрипции; белки лямбда-
1, лямбда-3, мю-2.
От сердцевины отходят шипы, представленные белком лямбда-2.
У ротавирусов внутренний капсид включает белки VP1, VP2, VP3, VP6.
От сердцевины отходят шипы, представленные белком лямбда-2.
У ротавирусов внутренний капсид включает белки VP1, VP2, VP3, VP6.
Слайд 52Структура реовирусов и ротавирусов
Наружный капсид реовирусов состоит из белков сигма-1, сигма-3,
мю-1С, а также белков лямбда-2, отходящих от сердцевины и выступающих в виде шипов.
Белок сигма-1 является гемагглютинином и прикрепительным белком.
Белок мю-1С определяет способность реовирусов заражать клетки кишечника и впоследствии поражать ЦНС.
У ротавирусов наружный капсид включает белки VP4 (шипы, выступающие на поверхности вириона, являющиеся гемагглютинином и прикрепительным белком) и VP7 — основной компонент наружного капсида, являющийся типоспецифическим антигеном.
Белок сигма-1 является гемагглютинином и прикрепительным белком.
Белок мю-1С определяет способность реовирусов заражать клетки кишечника и впоследствии поражать ЦНС.
У ротавирусов наружный капсид включает белки VP4 (шипы, выступающие на поверхности вириона, являющиеся гемагглютинином и прикрепительным белком) и VP7 — основной компонент наружного капсида, являющийся типоспецифическим антигеном.
Слайд 55Ротавирусные гастроэнтериты: общая характеристика
у взрослых – легко
у детей – значительно тяжелей
25%
всех гастроэнтеритов детей до года
60 % всех гастроэнтеритов детей 1 – 3 лет
40 % всех гастроэнтеритов детей 4 – 6 лет
ежегодно погибает от 1 до 3 млн. детей
60 % всех гастроэнтеритов детей 1 – 3 лет
40 % всех гастроэнтеритов детей 4 – 6 лет
ежегодно погибает от 1 до 3 млн. детей
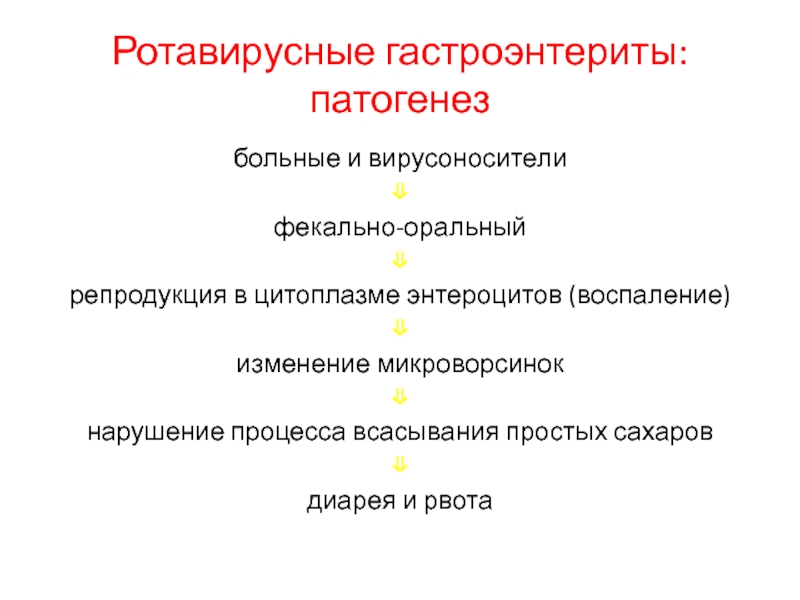
Слайд 56Ротавирусные гастроэнтериты: патогенез
больные и вирусоносители
⇓
фекально-оральный
⇓
репродукция в цитоплазме энтероцитов (воспаление)
⇓
изменение микроворсинок
⇓
нарушение процесса
всасывания простых сахаров
⇓
диарея и рвота
⇓
диарея и рвота
Слайд 57Ротавирусные гастроэнтериты: вирусологическая диагностика
Обнаружение вирусов в фекалиях (ИЭМ)
Выявление Ag в фекалиях
(ИФА и др.)
Нарастание титра Ig (РСК, РН, ИФА и др.) – диагностикум = ротавирусы животных
Нарастание титра Ig (РСК, РН, ИФА и др.) – диагностикум = ротавирусы животных
Слайд 58Рабдовирусы: классификация
Rhabdoviridae
Vesiculovirus (вирус везикулярного стоматита – арбовирус)
Lyssavirus (вирус бешенства)
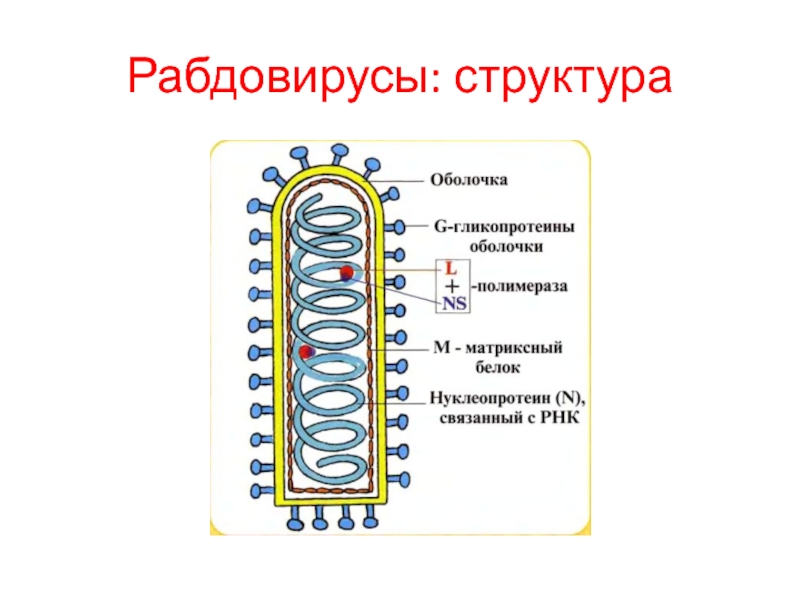
Слайд 59Рабдовирусы: структура
Вирусы имеют форму цилиндра с полукруглым и плоским концами, отсюда
и их название — Rhabdoviridae (греч. rhabdos — прут, палка).
Пулевидная форма характерна для вирусов, поражающих позвоночных, а бациллярная, с округленными концами — для вирусов везикулярного стоматита.
Вирион рабдовирусов состоит из оболочки и рибонуклеопротеина (нуклеокапсида) спиральной симметрии, содержит транскриптазу.
Геном — однонитевая нефрагментированная линейная минус-РНК.
Пулевидная форма характерна для вирусов, поражающих позвоночных, а бациллярная, с округленными концами — для вирусов везикулярного стоматита.
Вирион рабдовирусов состоит из оболочки и рибонуклеопротеина (нуклеокапсида) спиральной симметрии, содержит транскриптазу.
Геном — однонитевая нефрагментированная линейная минус-РНК.
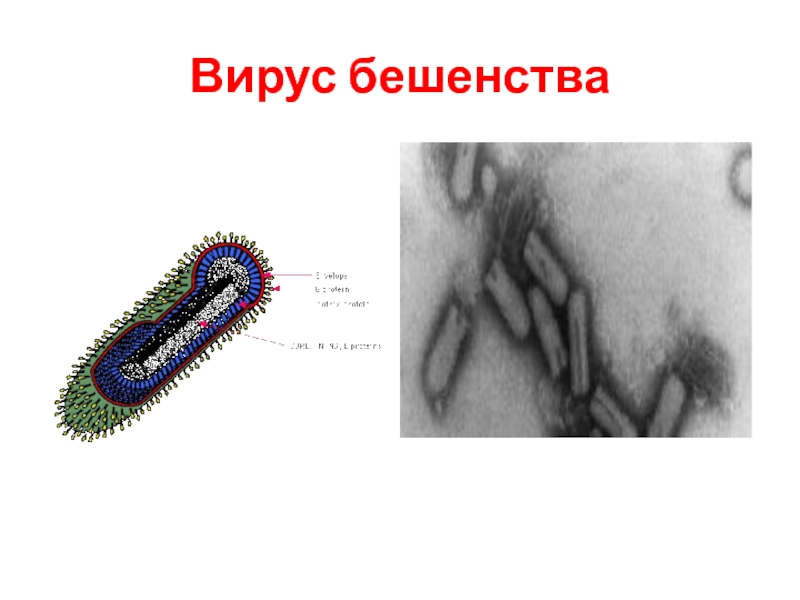
Слайд 61Вирус бешенства
Вызывает бешенство (rhabies, синонимы — водобоязнь, гидрофобия), развивающееся после укуса
или ослюнения раны инфицированным животным.
Поражается ЦНС с развитием симптомов возбуждения, параличом дыхательной и глотательной мускулатуры; заканчивается летально.
Поражается ЦНС с развитием симптомов возбуждения, параличом дыхательной и глотательной мускулатуры; заканчивается летально.
Слайд 62Вирус бешенства
Различают два вируса бешенства:
дикий (уличный) вирус, циркулирующий среди животных,
патогенный для человека;
фиксированный (virus fixe), полученный Л. Пастером в качестве антирабической вакцины многократным пассированием дикого вируса через мозг кроликов, утративший патогенность для человека, не образующий включений, не выделяющийся со слюной.
Оба вируса идентичны по антигенам.
фиксированный (virus fixe), полученный Л. Пастером в качестве антирабической вакцины многократным пассированием дикого вируса через мозг кроликов, утративший патогенность для человека, не образующий включений, не выделяющийся со слюной.
Оба вируса идентичны по антигенам.
Слайд 63Вирус-фикс (virus fixe)
Пастер (+ Ру и Шамберлан)
пассирование в мозге кролика до
одинакового («фиксированного») инкубационного периода
мозг кролика, высушенный в парах КОН = вакцина Пастера (первое применение – 1885 г.)
идентичен по антигенному составу «уличному вирусу»
мозг кролика, высушенный в парах КОН = вакцина Пастера (первое применение – 1885 г.)
идентичен по антигенному составу «уличному вирусу»
Слайд 64Свойства вируса бешенства
мало устойчив во внешней среде
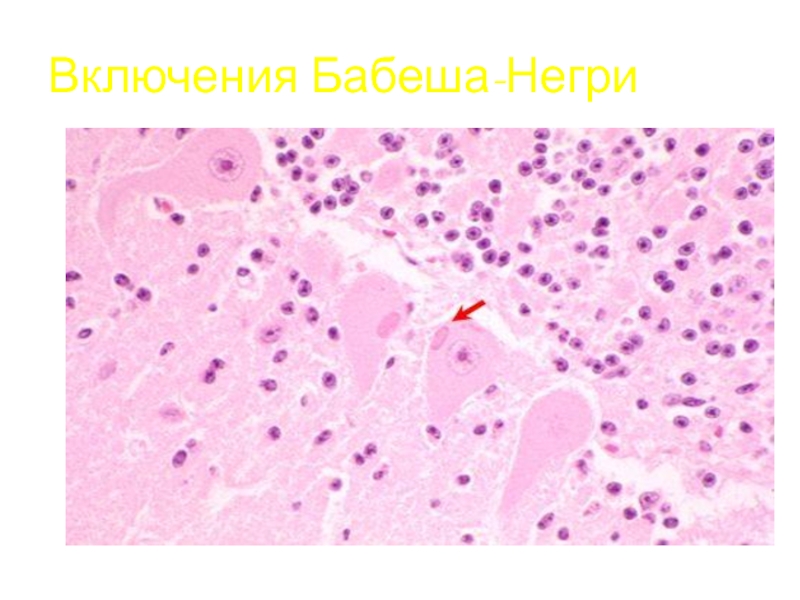
репродуцируется в цитоплазме (включения Бабеша-Негри)
Слайд 66Бешенство: патогенез
укус или ослюнение
⇓
первичная репликация
мышечная ткань
соединительная ткань
⇓
миграция по аксонам периферических нервов
⇓
базальные
ганглии и ЦНС
⇓
репликация в сером веществе с дегенеративным поражением нейронов
⇓
миграция по центробежным нейронам в различные ткани (в т.ч. слюнные железы)
⇓
репликация в сером веществе с дегенеративным поражением нейронов
⇓
миграция по центробежным нейронам в различные ткани (в т.ч. слюнные железы)
Слайд 67Бешенство: периоды болезни
инкубационный (от 7 дней до года)
продромальный (1 – 3
дня)
период возбуждения (2 – 3 дня, редко – до 6 дней)
паралитический период
Общая продолжительность болезни 5 - 14 дней
период возбуждения (2 – 3 дня, редко – до 6 дней)
паралитический период
Общая продолжительность болезни 5 - 14 дней
Слайд 68Бешенство: вирусологическая диагностика
Обнаружение включений Бабеша-Негри (не все биовары вируса)
кора больших полушарий
кора
мозжечка
амонов рог
продолговатый мозг
Выявление Ag в тех же препаратах (РИФ)
Выделение вируса
слюна, секционный материал
⇓
интрацеребрально б. мыши или кролики
внутримышечно хомячки
⇓
мозг погибшего животного
⇓
включения, Ag
амонов рог
продолговатый мозг
Выявление Ag в тех же препаратах (РИФ)
Выделение вируса
слюна, секционный материал
⇓
интрацеребрально б. мыши или кролики
внутримышечно хомячки
⇓
мозг погибшего животного
⇓
включения, Ag
Слайд 71Современные препараты для профилактики бешенства
Антирабические вакцины
вирус выращен в мозговой ткани животных
аттенуированные
Ферми
Хемпта
инактивированные
Семпла
Хемпта-Николича
вирус
выращен на культурах клеток
Внуково-32
на линии клеток W1-38
Антирабический гаммаглобулин
удлиняет инкубационный период (повышает эффективность вакцинации)
снижает вероятность развития поствакцинальных осложнений
Внуково-32
на линии клеток W1-38
Антирабический гаммаглобулин
удлиняет инкубационный период (повышает эффективность вакцинации)
снижает вероятность развития поствакцинальных осложнений