- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Безопасность при гемотрансфузии презентация
Содержание
- 1. Безопасность при гемотрансфузии
- 2. Определение ОМК Кровопотерю следует
- 3. Определение ОМК Кровопотеря: не <
- 4. Массивная кровопотеря Одномоментная или внегоспитальная >30%
- 5. Попытки лечения кровью предпринимались с древности
- 6. О чем говорит группа крови? Лучшие черты
- 7. Пионер В 1667 году французский ученый
- 8. Первые переливания 1615 (1628)
- 9. Трансфузии XX век Karl Landsteiner родился в
- 10. Современный период Показания Плазмозаменители Компоненты Альтернативы
- 11. Гравиметрическое определение кровопотери по сравнению с визуальной
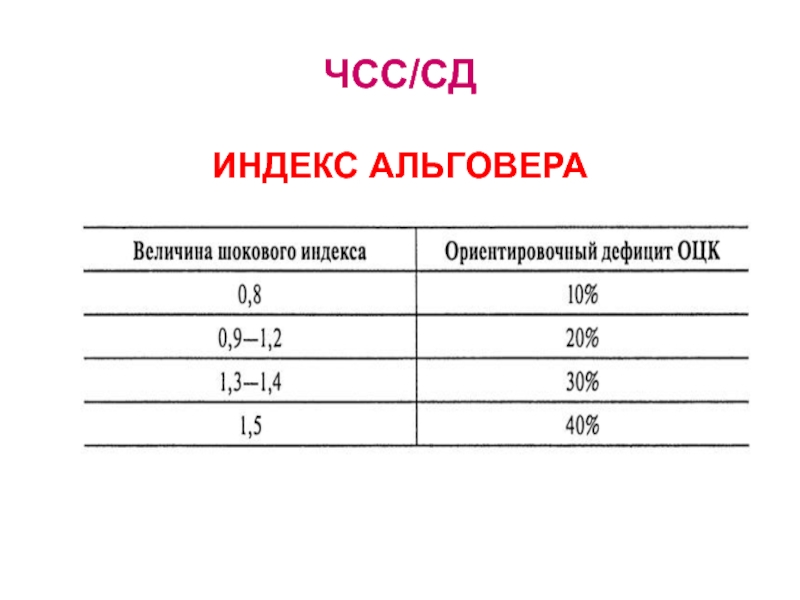
- 12. ЧСС/СД ИНДЕКС АЛЬГОВЕРА
- 13. Контроль ЦВД Ориентировочно можно определить дефицит ОЦК
- 14. Гравиметрическое определение кровопотери по сравнению с визуальной
- 16. РАСЧЕТ ОБЪЕМА КРОВОПОТЕРИ
- 17. ИТ пpи остpой кpовопотеpе
- 18. Первые 3
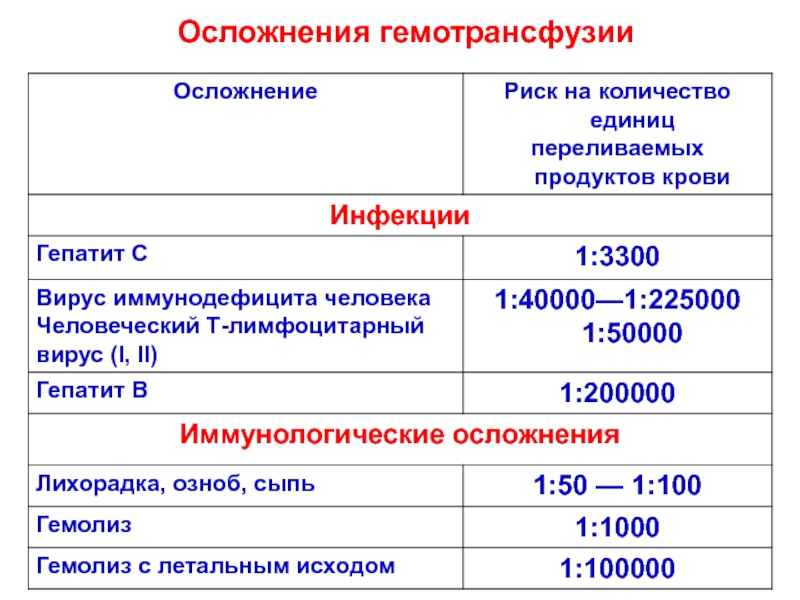
- 19. Осложнения гемотрансфузии
- 20. Гемотрансфузия - (transfusio) –
- 21. Компоненты крови
- 22. 1832 г. Россия. Используя изобретенные Бланделлом инструменты,
- 23. 1900 г. австрийский врач Карл
- 24. К. Ландштейнер (1901 г.) и польский врач
- 25. В организме человека
- 26. А В α β + = +
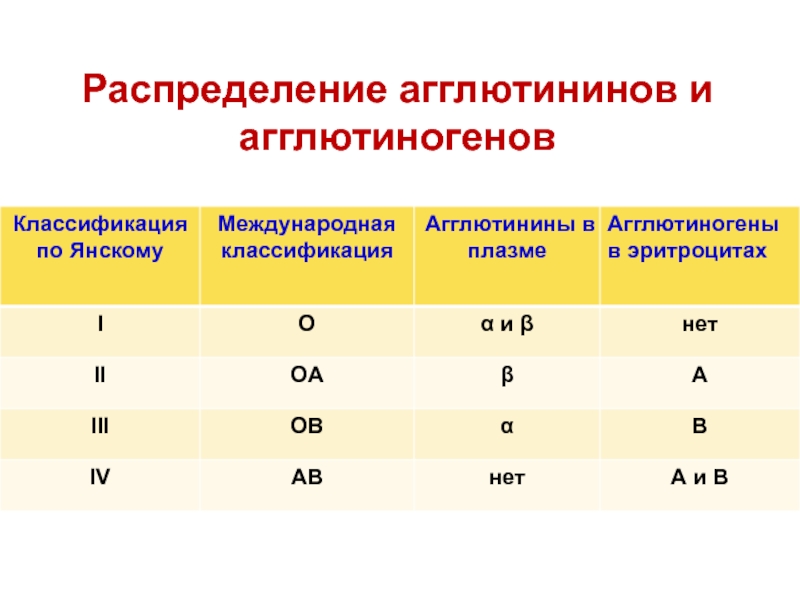
- 27. Распределение агглютининов и агглютиногенов
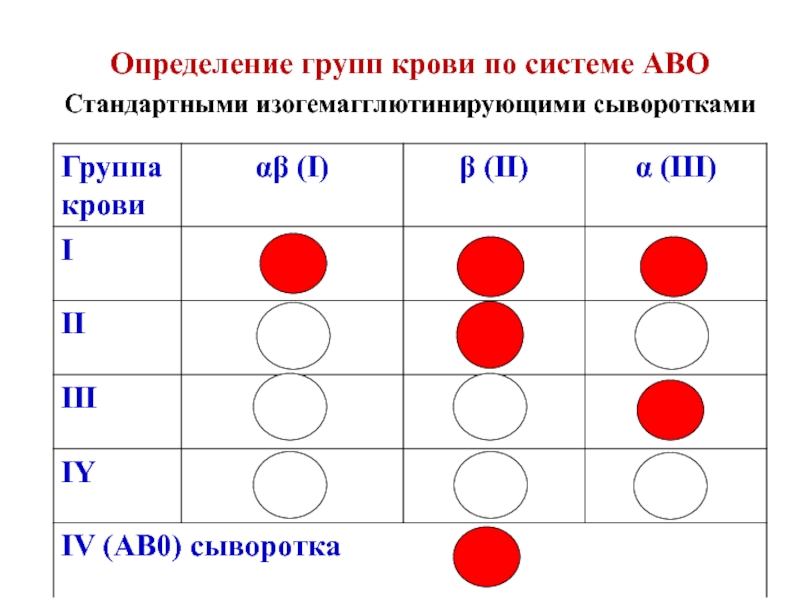
- 28. Определение групп крови по системе АВО
- 29. Анти - В
- 30. В 1940 г. Карл Ландштейнер открыл у
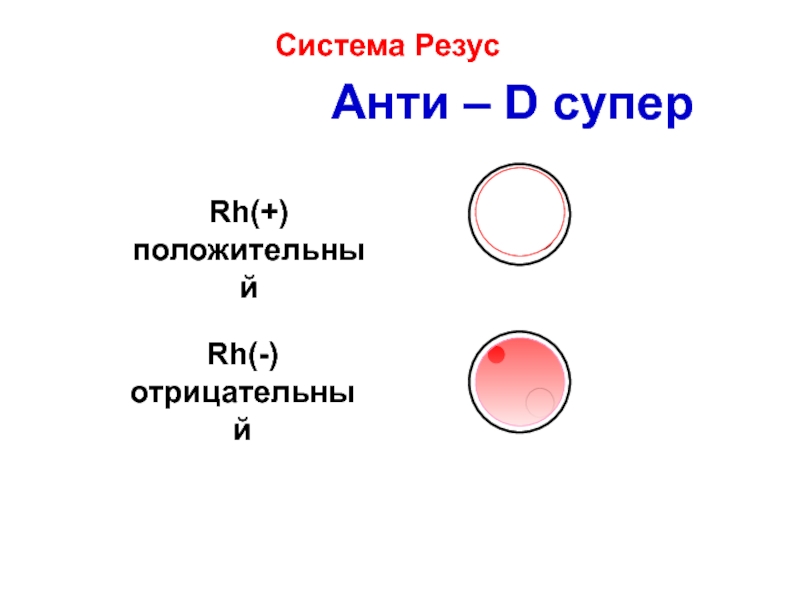
- 31. Анти – D супер Rh(+) положительный
- 32. Резус-конфликт. Возникает, если у матери Rh-отрицательная
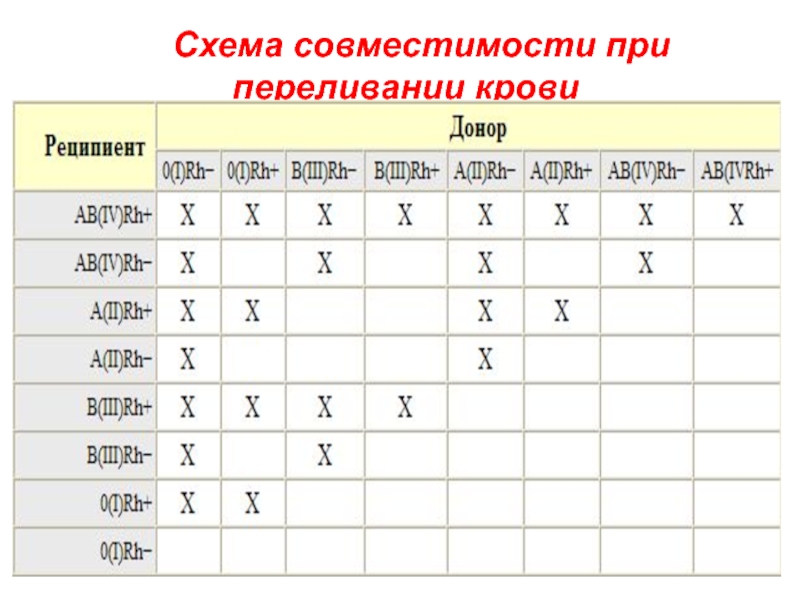
- 33. Схема совместимости при переливании крови
- 34. ИСТОЧНИКИ КРОВИ Фибринолизная (трупная) кровь Плацентарную кровь
- 35. Способы гемотрансфузии: Аутогемотрансфузия (переливание заранее заготовленной крови,
- 36. МЕТОДЫ ПЕРЕЛИВАНИЯ КРОВИ Внутривенное. Внутриартериальное Внутрикостное Внутриаортальное
- 37. Показания к гемотрансфузии: Абсолютные
- 38. Показания к гемотрансфузии: Относительные: Анемия Воспалительные
- 39. Порядок действий врача при гемотрансфузии:
- 40. Проба на индивидуальную совместимость 2-3 капли плазмы
- 41. Проба на биологическую совместимость 3-х кратное переливание
- 42. Осложнения при переливании крови: Осложнения механического характера:
- 43. Осложнения инфекционного характера: передача инфекционных заболеваний (грипп,
- 44. Кровезамещающие растворы – лечебные растворы, предназначенные для
- 45. Дезинтоксикационные растворы (гемодез, полидез)
- 46. Регуляторы КЩС Кристаллоидные р-ры
- 47. Альтернативой аллогенным гемотрансфузиям стали современные методы кровосбережения:
- 48. Трансфузия аутоплазмы в качестве гемостатического
- 49. Если пациент категорически отказывается от гемотрансфузии, рекомендуем
- 50. МЕТОДЫ ИНТРАОПЕРАЦИОННОГО СБЕРЕЖЕНИЯ
- 51. ПОСЛЕОПЕРАЦИОННЫЕ МЕРОПРИЯТИЯ 1. Продолжить назначение гемостатиков.
- 52. Исторические вехи: В 1818 г. J. Blundell
- 53. 1795 г. американский врач Филипп Синг Физик
- 54. Немного истории: William Highmore (1874), предложил собирать
- 55. Современная эра реинфузии Американский
- 56. Принцип аппаратной реинфузии Промышленные стерильные системы сбора
- 57. Рабочие моменты Сепарационная камера позволяет проводить
- 58. РАБОЧИЕ МОМЕНТЫ
- 59. Преимущества C.A.T.S. Непрерывно-поточный метод отмывки
- 60. Режимы обработки: "Высококачественный" (High Quality Wash)
- 61. Режимы обработки: "Ускоренный" (High Flow Wash) -
- 62. Режимы обработки: Срочный" (Emergency Wash) - максимальная
- 63. Абсолютные и относительные противопоказания к ИАРЭ.
- 64. Осложнения: Коагулопатии.
- 65. НЕДОСТАТКИ: Плазма крови, вместе с промывными водами
- 66. Клиническое наблюдение Пациентка М., 32л. поступила в
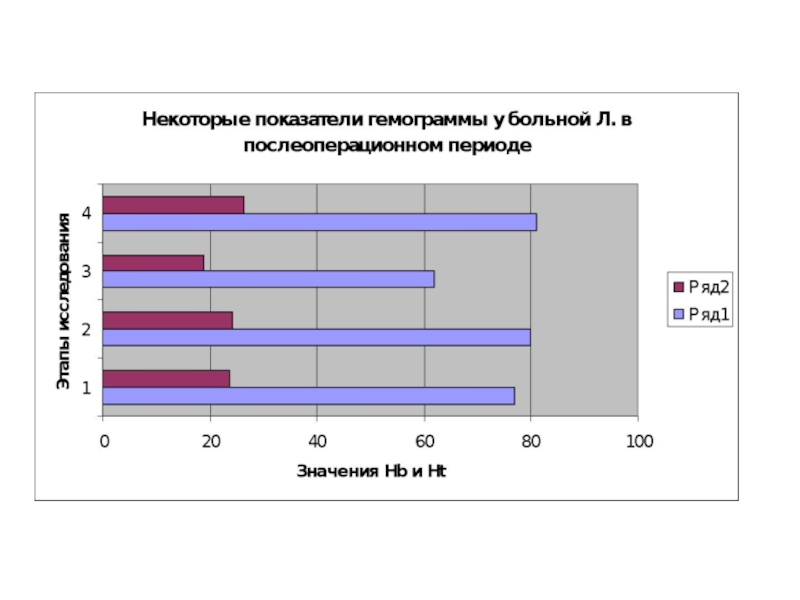
- 67. Анестезиологическое пособие у больной Л., 41 г.
- 68. Параметры коагулограммы на
- 69. Пациентка Л., 41 г. поступила в ОПБ
- 70. Анестезиологическое пособие у больной Л., 41 г.
- 71. Через 2 часа по окончанию операции при
- 72. Интраоператорно проводилась коррекция гемокоагуляции (транексам 750 мг),
- 73. Параметры коагулограммы на
- 75. Какой раствор? Сколько?
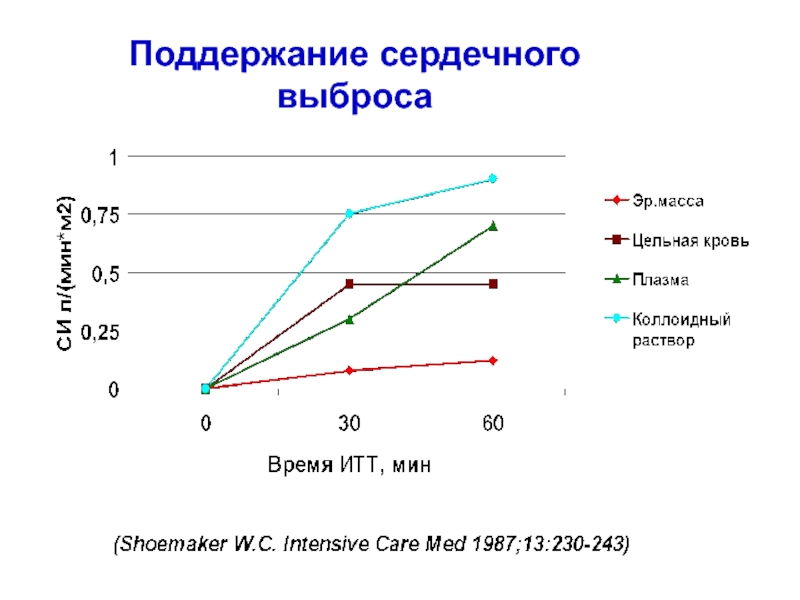
- 76. Поддержание сердечного выброса
- 77. Сравнительные объемы различных растворов, необходимых для увеличения
- 78. Классификация ГЭК
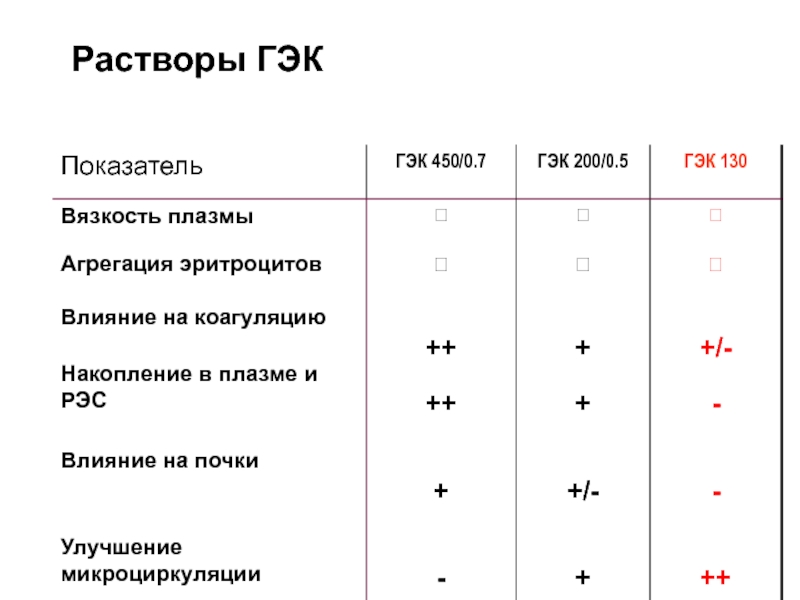
- 79. Растворы ГЭК
- 80. Волемический эффект 6% ГЭК 130 Результат:
- 81. Венофундин Фармакологические свойства Средний молекулярный вес:
- 82. Коллоиды и риск повреждения почек. Декстраны- острое
- 83. Критерии "RIFLE" (Risk, Injury, Failure, Loss and
- 84. Примечание * – p
- 85. Существенный положительный эффект на острое повреждение почки
- 86. Желатины Преимущества: Минимальное влияние на систему гемостаза
- 87. Больная С., 28 лет поступила на лечение
- 89. Показатели гемограммы. Исходная 110 г/л
- 90. АЛЬБУМИН: PRO ET CONTRA
- 91. Инфузионная терапия Martin GS et al.
- 92. 20% альбумин человеческий компании Бакстер. Основные преимущества:
- 93. Извечный спор – коллоиды и/или кристаллоиды?
- 94. Использование кристаллоидов для плазмозамещения - объем
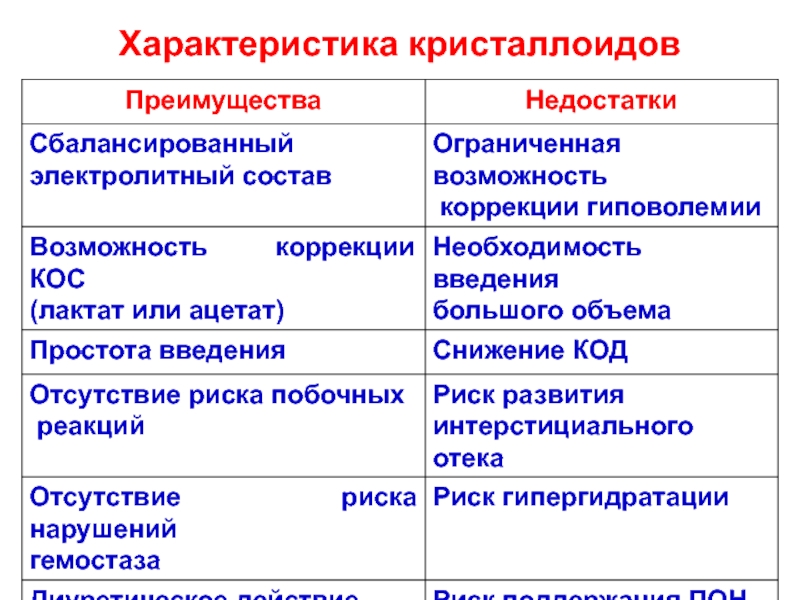
- 95. Характеристика кристаллоидов
- 96. Является ли «физиологический» раствор физиологическим?
- 97. В эксперименте: Усиление
- 98. Является полиионным, изоосмолярным
- 99. Рекомендация 1 Учитывая риск развития гиперхлоремического ацидоза
- 100. Что же из кристаллоидов предпочесть?
- 101. ОПЛ: отек легких на фоне инфузии кристаллоидов
- 102. При кровопотере до 25% ОЦК суточный объем
- 103. 1. Общий объём вводимой жидкости на
- 104. По-прежнему дискутабелен вопрос должных значений Ht, Hb
- 105. Переливание СЗП показано только для восполнения плазменных
- 106. Принципы применения СЗП Трансфузия аутоплазмы
- 107. Пеpеливание больших количеств плазмы может пpивести к
- 108. Изменения гемостаза при физиологической беременности Рост ряда
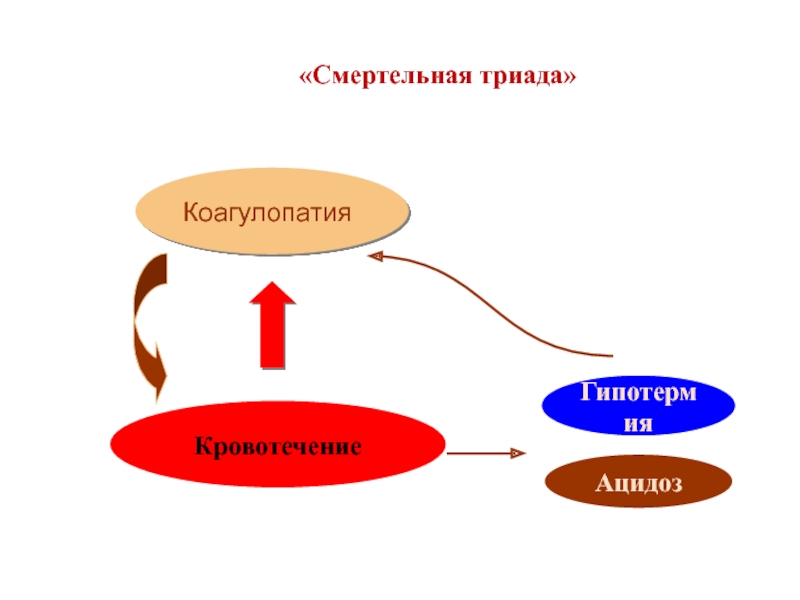
- 109. Кровотечение Гипотермия Ацидоз Коагулопатия «Смертельная триада»
- 110. Стадии ДВС-синдрома: Гиперкоагуляция. Коагулопатия потребления. Коагулопатия
- 111. Лабораторные проявления острого ДВС-синдрома включают (А.В.
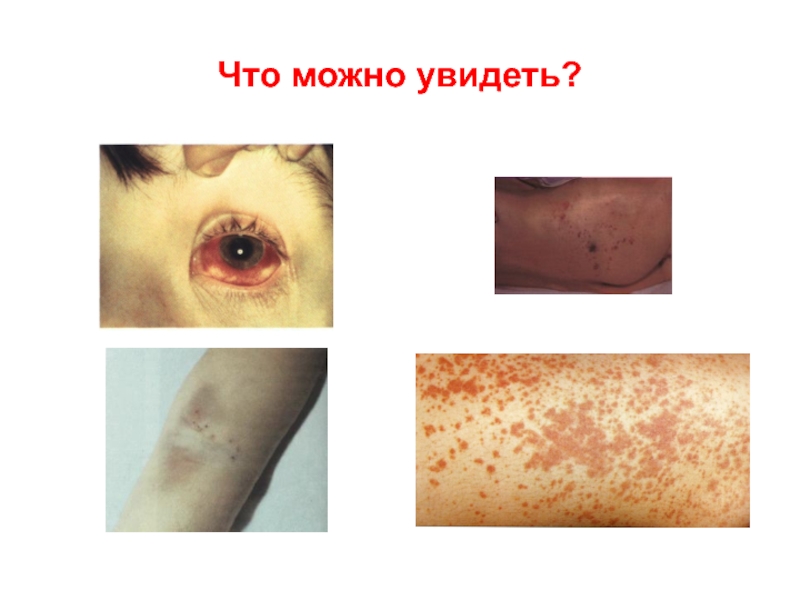
- 112. Что можно увидеть?
- 113. Nota bene !
- 114. Анестезиологическая тактика -1 Искусственные коллоидных растворы: при
- 115. АHЕСТЕЗИОЛОГИЧЕСКОЕ ПОСОБИЕ Премедикация: 0,1% метацин
- 116. Анестезиологическое пособие Интубация трахеи должна быть
- 117. ПАТОЛОГИЧЕСКИЙ ФИБРИНОЛИЗ (ГИПЕРФИБРИНОЛИЗ) Массивная кровопотеря (обычная доза
- 118. Противопоказания к применению Транексама Повышенная чувствительность к
- 119. Применение апротинина повышает риск
- 120. D. Karalapillai, P. Popham. Recombinant factor VIIa
- 121. Boehlen F., Morales M.A., Fontane P., Ricon
- 122. КОАГИЛ-VII Первый отечественный рекомбинантный фактор свертывания
- 123. Aledot L.M. Comparative trombotic event incidence after
- 124. Критический обзор применения рекомбинантного VIIa
- 125. Анестезиологическая тактика -3 Ингибиторы протеаз (контрикал в/в
- 126. Нарушение функции коагуляции – коагулопатия
- 127. ПОДДЕРЖАНИЕ ТЕМПЕРАТУРНОГО ГОМЕОСТАЗА
- 128. Фактор II свёртывания
Слайд 2Определение ОМК
Кровопотерю следует считать массивной если в течение
(по А.И. Горбашко, 1982; Е.А. Вагнер, В.М. Тавровский, 1977)
Слайд 3Определение ОМК
Кровопотеря:
не < 30% ОЦК в течение 1-2 часов
50% ОЦК за 6 часов
100% ОЦК за сутки
Слайд 4Массивная кровопотеря
Одномоментная или внегоспитальная >30% ОЦК
Постепенная, в условиях
операционной
Слайд 5Попытки лечения кровью предпринимались с древности
Гиппократ рекомендовал лечить душевнобольных с применением
Кровь употребляли с лечебной целью и во время войн. Например, за египетскими войсками всегда следовали стада баранов, кровью которых лечили раненых – все потому, что долгие столетия выпитая кровь считалась заменой потерянной.
Слайд 6О чем говорит группа крови?
Лучшие черты
I группа – честолюбие, широкий
II группа – стремление к совершенству, надежность, пунктуальность
III группа – любовь к животным, высокий творческий потенциал
IV группа – здравомыслие, сочувствие
Худшие черты
I группа – жадность, инфантильность
II группа – сконцентрированность на себе, конформизм
III группа – забывчивость, лень, безответственность IV группа – нерешительность, переменчивость, злопамятность
Слайд 7Пионер
В 1667 году французский ученый
Жан Батист Дени произвел первое переливание
В качестве иглы использовали птичье перо, а в качестве шприца- рыбий пузырь. Дени перелил один стакан крови от ягнёнка больному юноше, страдающему лихорадкой. Больной пережил тяжёлую аллергическую реакцию, но поправился.
Слайд 8Первые переливания
1615 (1628)
1665-’66
1667
William Harvey
Открытие кровообращения
Wilkins & Lower
Переливание собака/собака
Jean-Baptiste Denis
Первая
Слайд 9Трансфузии XX век
Karl Landsteiner родился в Вене
14 июня 1868 г.
Нобелевская
1901
Слайд 11Гравиметрическое определение кровопотери по сравнению с визуальной оценкой на модели послеродового
Al Kadri H., Al Anazi B., Tamim H. Visual estimation versus gravimetric measurement of postpartum blood loss:
a prospective cohort study. Arch. Gynecol. Obstet. 2011;283:1207–1213.
Yoong W., Karavolos S., Damodaram M. et al. Observer accuracy and reproductubility of blood loss in obstetrics:
how accurate are health professionals? Arch. Gynecol. Obstet. 2010; 281:207–213.
Средняя погрешность гравиметрического метода в исследовании составила 4%, а метода визуальной оценки 34,7% с тенденцией к преувеличению объема кровопотери. Корреляция Пирсона между актуальной и измеренной кровопотерей составило
0,995 для гравиметрического метода и 0,629
для метода визуальной оценки.
Необходимо проводить регулярные тренинги
акушерской бригады по освоению и рутинному
применению гравиметрического метода.
Karl Pearson
1857–1936
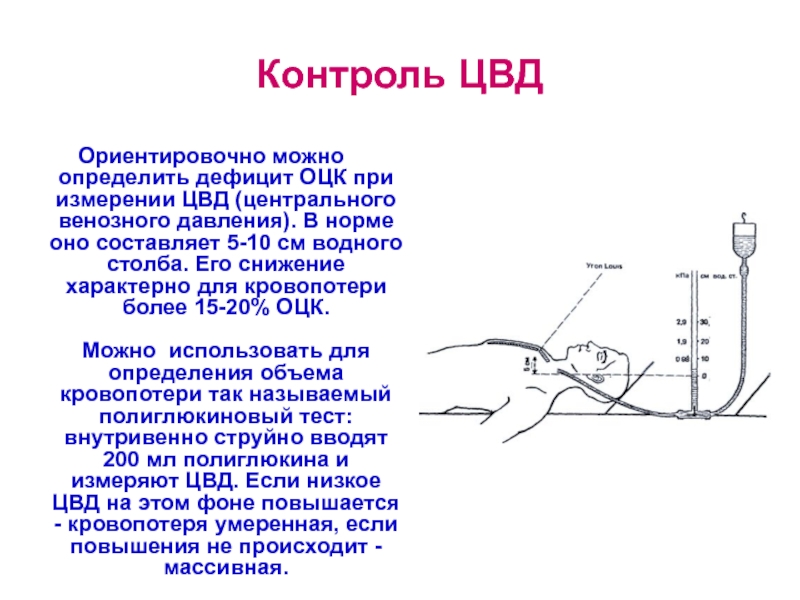
Слайд 13Контроль ЦВД
Ориентировочно можно определить дефицит ОЦК при измерении ЦВД (центрального венозного
Слайд 14Гравиметрическое определение кровопотери по сравнению с визуальной оценкой на модели послеродового
Lilley G.J., Collis R.E. Gravimetric measurement of blood loss versus visual estimation in simulated postpartum haemmorage.
Int. J. Obstet. Anesth. 2013; V.22(51):10.
Самым частым методом определения кровопотери остается визуальная оценка. В литературе неоднократно указано на неточность метода визуальной оценки, причем одни авторы считают, что метод недооценивает объем кровопотери, а другие, что преувеличивает этот объем.
Слайд 17
ИТ пpи остpой кpовопотеpе
напpавлена на:
восполнение ОЦК,
поддеpжание адекватной тканевой пеpфузии
ноpмализацию
улучшение метаболизма клетки.
Гемотpансфузия - один из основных методов лечения остpой массивной кровопотери.
1 доза донорских эритроцитов увеличивает у пациента Hb на 10г/л и Ht на 3-4%
Цель терапии – сохранить адекватный уровень потребления О2 тканями для поддержания метаболизма в них.
Слайд 20
Гемотрансфузия - (transfusio) – переливание, смешивание - метод управления
Слайд 221832 г. Россия. Используя изобретенные Бланделлом инструменты, и его методику, акушер
1840 г. под руководством Бланделла английский врач Сэмюэль Армстронг Лэйн впервые использовал переливание крови для лечения гемофилии.
Слайд 23 1900 г. австрийский врач Карл Ландштейнер открыл и описал
Слайд 24К. Ландштейнер (1901 г.) и польский врач Я.Янский (1907 г.) открыли
Все эти открытия дали мощный толчок исследованиям в области перекрестной совместимости крови.
1907 году в Нью-Йорке было произведено первое переливание крови больному от здорового человека, с предварительной проверкой крови донора и реципиента на совместимость (Рубен Оттенберг). Он же обратил внимание на универсальную пригодность первой группы крови.
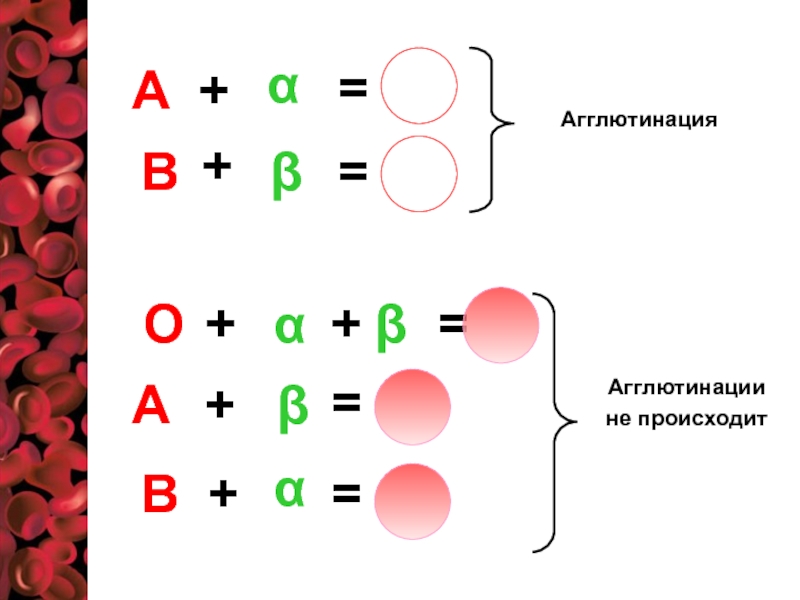
Слайд 25
В организме человека антиген группы крови (агглютиноген) и антитела к
ЗОЛОТОЕ ПРАВИЛО
ЛАНДШТЕЙНЕРА
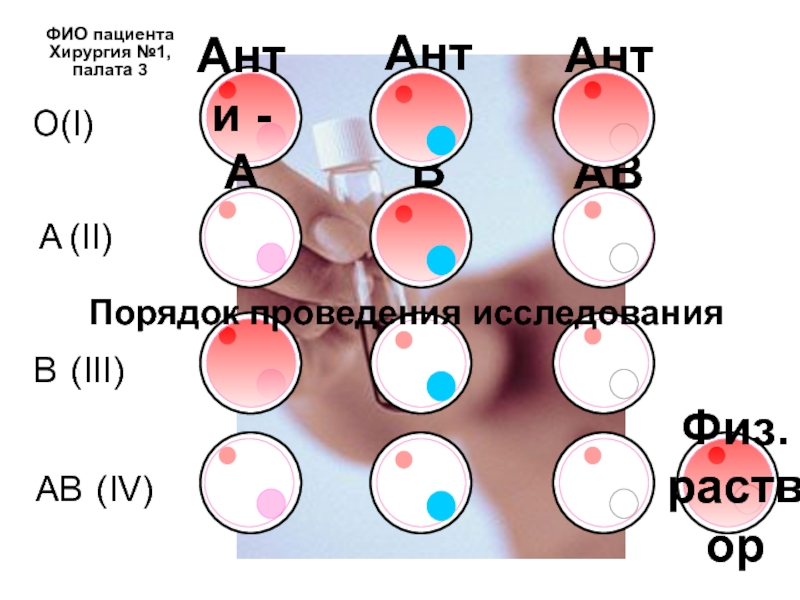
Слайд 29
Анти - В
Анти - А
Анти – АВ
O(I)
A (II)
B (III)
AB (IV)
Физ. раствор
ФИО
Хирургия №1, палата 3
Порядок проведения исследования
Слайд 30В 1940 г. Карл Ландштейнер открыл у макак типа «резус» в
Известно, что у 85-86% людей земного шара резус присутствует (Rh+)- резус-положительная кровь.
У 14-15% -резус отсутствует (Rh-)-резус отрицательная кровь.
Слайд 32Резус-конфликт. Возникает, если у матери Rh-отрицательная кровь, а у плода Rh-
Слайд 34ИСТОЧНИКИ КРОВИ
Фибринолизная (трупная) кровь
Плацентарную кровь
Кровь, излившейся в серозные полости
Группы доноров:
Безвоздмезное донорство
Кадровые
Доноры резерва
Иммунные доноры
Слайд 35Способы гемотрансфузии:
Аутогемотрансфузия (переливание заранее заготовленной крови, реинфузия)
Переливание донорской крови
Прямое переливание
Непрямое переливание:
Обменное
Слайд 37Показания к гемотрансфузии:
Абсолютные
Острая кровопотеря
Травматический шок II-III степени.
Слайд 38Показания к гемотрансфузии:
Относительные:
Анемия
Воспалительные заболевания с тяжелой интоксикацией
Продолжающееся кровотечение
Нарушение свертывающей системы
Снижение иммунного
Длительные хронические процессы
Некоторые виды отравлений
Слайд 39
Порядок действий врача при гемотрансфузии:
Определить показания к гемотрансфузии
Определить группу крови и
Выбрать соответствующую кровь и макроскопически определить ее годность
Перепроверить группу крови донора по системе АВО.
Провести пробу на индивидуальную совместимость по системе АВО
Провести пробу на индивидуальную совместимость по резус фактору
Провести биологическую пробу
Произвести гемотрансфузию
Заполнить документацию
Осуществить наблюдение за пациентом после гемотрансфузии
Слайд 40Проба на индивидуальную совместимость
2-3 капли плазмы больного + капля донора (масштаб
Наблюдение в течение 5 минут
Присутствие агглютинации – кровь несовместима
Совместимость по Rh-фактору
1)(на водяной бане (2-3 капли сыворотки больного+ капля донора),
2)с помощью желатина-1 капля крови донора+ 2 капли подогретого желатина+ 2-3 капли сыворотки больного),
Слайд 41Проба на биологическую совместимость
3-х кратное переливание с интервалом 3 минуты крови
Дозы:
Дети до 2-х лет- 2 мл.
Дети от 2 до 5 лет- 5 мл.
Дети от 5 до 10 лет- 10 мл.
Старше 10 лет-15 мл.
При операции под наркозом:
После переливания 100 мл крови -5 мл. крови+ несколько капель гепарина= центрифугируют= оценивают результат
Слайд 42Осложнения при переливании крови:
Осложнения механического характера:
острое расширение сердца
воздушная эмболия
тромбозы и эмболии
нарушение
Осложнения реактивного характера
А) Гемотрансфузионные реакции (пирогенные, антигенные, аллергические)
Б) Гемотрансфузионные осложнения:
Гемотрансфузионный шок
Синдром массивных гемотрансфузий
Цитратная интоксикация
Калиевая интоксикация
Слайд 43Осложнения инфекционного характера:
передача инфекционных заболеваний (грипп, корь, бруцеллез, токсоплазмоз и др.)
передача
развитие банальной хирургической инфекции (флебит, флегмона, сепсис)
Слайд 44Кровезамещающие растворы – лечебные растворы, предназначенные для замещения утраченных или нормализация
Классификация:
Кровезаменители гемодинамического действия- нормализуют показатели центральной и периферической гемодинамики.
производные декстрана (полиглюкин, полифер, рондекс, макродекс)
препараты желатина (желатиноль, гелофузин, геможель)
производные гидроксиэтилкрахмала (рефортан, стабизол)
производные полиэтиленгликоля (полиоксидин)
Слайд 45
Дезинтоксикационные растворы
(гемодез, полидез)
Для парентерального питания
белковые препараты
жировые эмульсии (липофундин, интралипид, фатген)
углеводы (сорбит, маннит, ксилит)
Слайд 46Регуляторы КЩС
Кристаллоидные р-ры (Рингера-Локка, лактасол, ацесоль, хлосоль, дисоль,
Осмодиуретики (маннитол, сорбитол)
Переносчики кислорода (геленпол,перфторан, перфукол, флюсол-да)
Инфузионные антигипоксанты (мафусол, полиоксифумарин, реамберин)
Слайд 47Альтернативой аллогенным гемотрансфузиям стали современные методы кровосбережения:
предоперационная заготовка аутокрови и аутоплазмы
предоперационная
интраоперационная аппаратная реинфузия крови
Слайд 48
Трансфузия аутоплазмы в качестве гемостатического копонента при проведении нормоволемической
Аутоплазматрансфузия расширяет возможности проведения острой нормоволемической гемодилюции при интраоперационной кровопотере объемом до 25% ОЦК и способствует снижению риска развития геморрагических и посттрансфузионных осложнений в послеопреционном периоде.
Шейкина Т.В., Рогачевский О.В., Пучко Т.К., Шифман Е.М. Влияние острой нормоволемической гемодилюции с аутплазмотрансуфузией на показатели гемостаза при абдоминальном родоразрешении//Общая реаниматология. 2011. VII. 2. С.35–38.
Слайд 49Если пациент категорически отказывается от гемотрансфузии, рекомендуем следующую тактику ведения
ПЛАНОВЫЕ
1. Расширенная коагулограмма.
2. За 2 недели до плановой операции прекращается приём салицилатов, дипиридамола, НПВС.
3. Коррекция анемии: эритропоэтин 2500 ЕД 2-3 раза в неделю п/к; препараты железа - 100 мг х 3 раза в сутки внутрь, витамин В12.
4. Искусственное повышение с помощью эритропоэтина исходной концентрации Hb до 130-140 г/л, Ht до 35%, эритроцитов до 3,5 млн.
Противопоказания к применению эритропоэтина: неуправляемая артериальная гипертензия, эпилепсия, эклампсия, тромбоцитоз.
Слайд 50 МЕТОДЫ ИНТРАОПЕРАЦИОННОГО СБЕРЕЖЕНИЯ
1. Гемодилюция.
2.Хирургические методы (электрокоагуляция,
3. Весь комплекс гемостатиков.
4. Реинфузия в настоящее время
приказу допустима лишь с помощью
«селл-сэйвера».
Слайд 51ПОСЛЕОПЕРАЦИОННЫЕ МЕРОПРИЯТИЯ
1. Продолжить назначение гемостатиков.
2. Эритропоэтин (10000 ЕД в сутки
3. Препараты железа (1,5 мг/кг в сутки в/м). Альтернативой является внутривенное введение сахарата железа (Venofer), обладающего большей биодоступностью. (100 - 200 мг в сутки в течении недели).
При использовании Spongostan, Surgicel пользоваться
селл-сэйверами нельзя!
4. Продолжить инфузию перфторана
Слайд 52Исторические вехи:
В 1818 г. J. Blundell оказался беспомощным свидетелем маточного кровотечения,
«Рассуждая позже на эту мрачную тему, я отметил обстоятельства, которые придавали ей особый интерес. Я не мог противостоять нахлынувшим размышлениям о том, что эта больная, вероятно, могла быть спасена переливанием крови; и, несмотря на то, что здесь была небольшая благоприятная возможность для операции в обычном режиме, сосуды могли быть пополнены кровью посредством шприца с легкостью и быстротой».
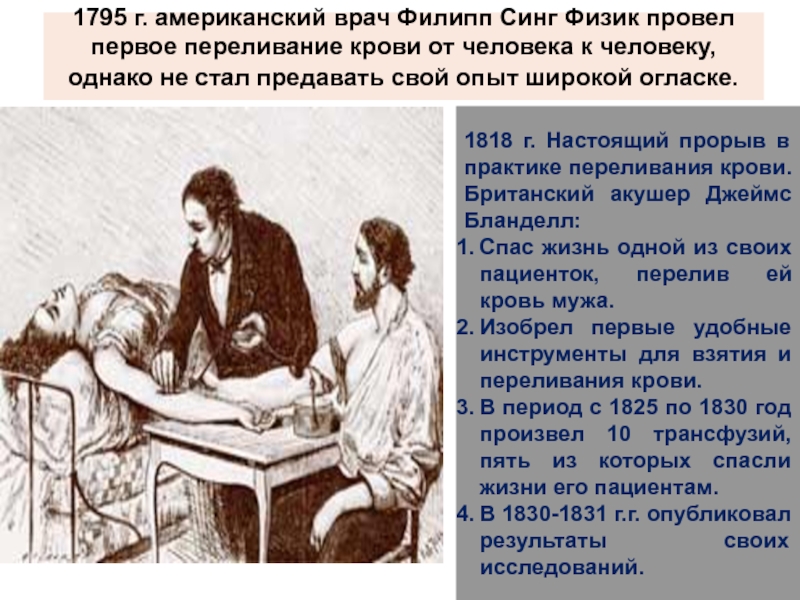
Слайд 531795 г. американский врач Филипп Синг Физик провел первое переливание крови
1818 г. Настоящий прорыв в практике переливания крови. Британский акушер Джеймс Бланделл:
Спас жизнь одной из своих пациенток, перелив ей кровь мужа.
Изобрел первые удобные инструменты для взятия и переливания крови.
В период с 1825 по 1830 год произвел 10 трансфузий, пять из которых спасли жизни его пациентам.
В 1830-1831 г.г. опубликовал результаты своих исследований.
Слайд 54Немного истории:
William Highmore (1874), предложил собирать кровь, излившуюся после родов, согревать
В 1914-15 г.г. три исследователя из разных стран (A. Hustin, Belgium; R. Lewisohn, USA; L. Agote, Argentina), работающих независимо друг от друга, пришли к выводу, что цитрат натрия может быть использован при гемотрансфузиях в качестве антикоагулянта.
В 1886 г. John Duncan (Edinburg) первым перелил около 100 мл излившейся крови во время ампутации нижней конечности. Антикоагулянтом служил
цитрат натрия.
Слайд 55Современная эра реинфузии
Американский военный хирург Gerald Klebanoff (1968)
Klebanoff работал в сотрудничестве с лабораториями Bentley, поэтому первым промышленно выпущенным в 1971 году аппаратом для реинфузии крови стал Bentley ATS 100.
Упрощённая обработка крови (только фильтрация) сопровождалась: лизисом эритроцитов, повышением уровня свободного Hb, расстройством гемокоагуляции, почечной недостаточностью, воздушной эмболией.
Слайд 56Принцип аппаратной реинфузии
Промышленные стерильные системы сбора и фильтрации раневой крови, как
Слайд 57Рабочие моменты
Сепарационная камера
позволяет проводить
непрерывно – поточную
отмывку крови
независимо от объема
скорости обработки.
Слайд 59 Преимущества C.A.T.S.
Непрерывно-поточный метод отмывки крови, независимый от объема
Постоянно высокий уровень гематокрита. Система обеспечивает постоянный и высокий уровень Ht (65%) независимо от используемой программы, идентичный уровню Ht, получаемому на станции переливания крови;
Высокая скорость обработки. Программа экстренной отмывки крови позволяет получать до 100 мл эритроцитарной массы в минуту.
Слайд 60Режимы обработки:
"Высококачественный"
(High Quality Wash) – тщательная
обработка загрязнённой крови.
7 циклов
"Качественный" (Quality Wash) –
стандартная программа интра- и
послеоперационной обработки как
раневой, так и дренажной крови.
5 циклов отмывания.
Реинфузия только через лейкоцитарные фильтры:(PALL RCXL-1 (США),
ПК 23-01 « ИНТЕРОКО» (Россия)!
«Аспекты онкологической безопасности аппаратной реинфузии отмытых эритроцитов при онкоурологических операциях»
Болихова Н.А., Петрова М.В., Чазова Н.Л., Мельникова Н.В., ФГУ «РНЦРР Росмедтехнологий» , г.Москва. http://vestnik.rncrr.ru/vestnik/v9/papers/bolihova_v9.htm
Слайд 61Режимы обработки:
"Ускоренный" (High Flow Wash) - для обработки чистой крови при
"Быстрый" (Ultra Flow Wash) - для обработки чистой крови при массивной одномоментной кровопотере. 1 цикл отмывания. Поток эритромассы - 50-100 мл/мин.
Слайд 62Режимы обработки:
Срочный" (Emergency Wash) - максимальная скорость обработки. 1 цикл отмывания.
"Экстренный 190" (Blood Transfer 190) - работает как система сбора и фильтрации в ургентных случаях. Кровь только фильтруется и перегоняется из кардиотомного резервуара в мешок для реинфузии со скоростью 100-190 мл/мин. Кровь не отмыта и не концентрирована.
"Экстренный 350" (Blood Transfer 350) - то же самое, только скорость перегонки повышается до 200-350 мл/мин.
Слайд 63 Абсолютные и относительные противопоказания к ИАРЭ.
По
гноем; содержимым кишечника; веществами, противопоказанными к введению в сосудистое русло (антибиотики, не разрешённые к парентеральному применению, бетадин, перекись водорода, спирт, гемостатические препараты на основе коллагена)
*25th Congress of the International Society of Blood Transfusion: Plenary and State-of-the-art Lectures by T. Kristensen(Editor) Special Order. Karger Paperback
Слайд 64Осложнения:
Коагулопатии.
Удлинение АЧТВ или тромбинового времени должно быть
2. Гемолиз.
Механическая обработка крови, пропускание ее через роликовый насос и длинные магистрали всегда чреваты развитием гемолиза, а следовательно, острой почечной недостаточностью.
Профилактика гемолиза состоит в тщательном отмывании крови. Следует обратить особое внимание на ограничение степени разрежения в вакуум-аспираторе.
При заметном гемолизе используют осмодиуретики, ощелачивают плазму.
Слайд 65НЕДОСТАТКИ:
Плазма крови, вместе с промывными водами безвозвратно утрачивается.
Восстановление КОД и
Нестабильность и резкое укорочение срока хранения, а также хрупкость эритроцитов и примесь частично разрушенных клеток.
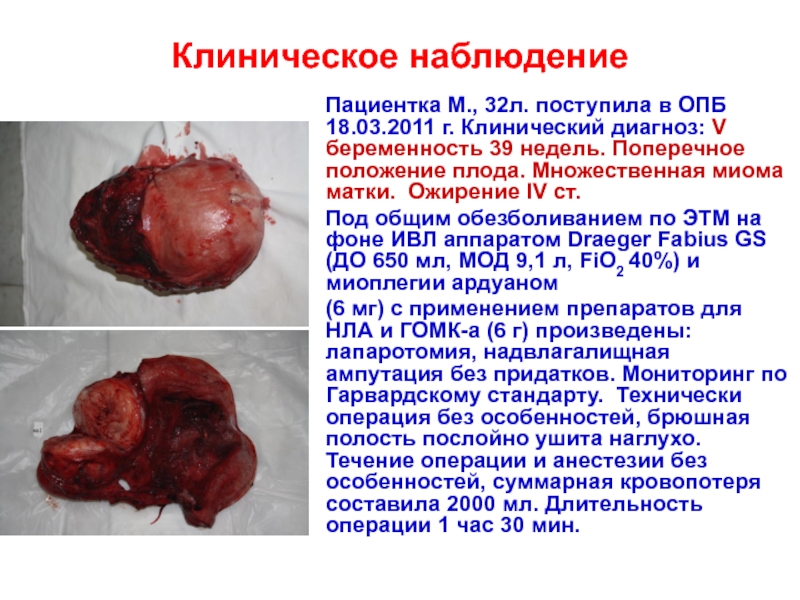
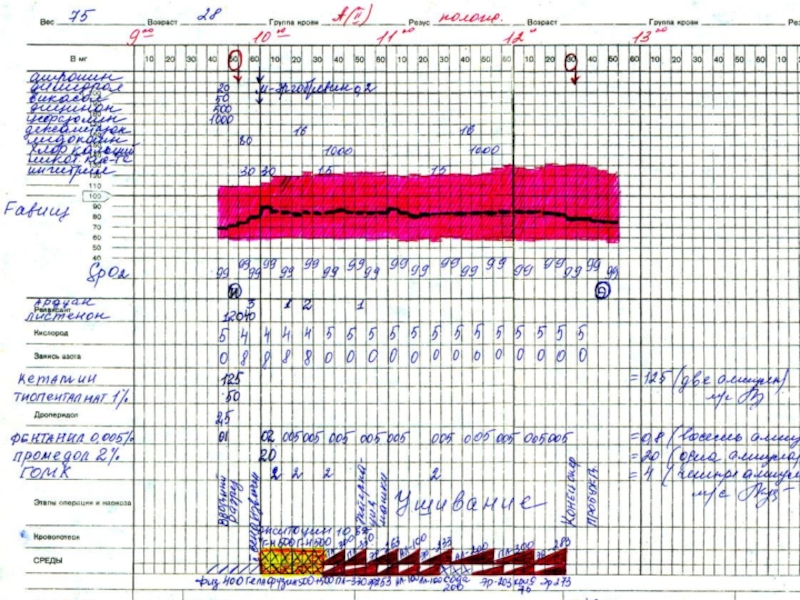
Слайд 66Клиническое наблюдение
Пациентка М., 32л. поступила в ОПБ 18.03.2011 г. Клинический диагноз:
Под общим обезболиванием по ЭТМ на фоне ИВЛ аппаратом Draeger Fabius GS (ДО 650 мл, МОД 9,1 л, FiO2 40%) и миоплегии ардуаном
(6 мг) с применением препаратов для НЛА и ГОМК-а (6 г) произведены: лапаротомия, надвлагалищная ампутация без придатков. Мониторинг по Гарвардскому стандарту. Технически операция без особенностей, брюшная полость послойно ушита наглухо. Течение операции и анестезии без особенностей, суммарная кровопотеря составила 2000 мл. Длительность операции 1 час 30 мин.
Слайд 68
Параметры коагулограммы на момент перевода:
Этаноловый тест – слабо +
Фибриноген «В» –
Толерантность плазмы к гепарину – 6 мин
Антитромбин III - 75,5%
Тромбиновое время 15,3 сек
Фибринолитическая активность 260 мин
Тромботест - V ст.
Фибриноген - 5,3 г/л
ПО - 0,82
Протромбиновое время – 14,65 сек
Ретракция сгустка – 46%
АДФ-агрегация тромбоцитов -13 сек
АЧТВ - 23,4 сек
Активность системы протеина С - 0,7
Каолиновое время - 63 сек
Слайд 69Пациентка Л., 41 г. поступила в ОПБ 6.08.08 г. Клинический диагноз:
Больная по религиозным мотивам (свидетельница Иеговы) категорически отказалась от применения крови и её препаратов. Со дня поступления эпокрин (2000 ЕД/сутки), фолиевая кислота и витамин В12 (500 мкг/сутки).
Hb вырос со 103 до 133 г/л, Ht с 32,1% до 36%, эритроциты с 3280000 до 3900000.
15.08.08 под спинно-мозговой анестезией (маркаин-спинал 13 мг) произведено ретровезикальное кесарево сечение. Течение операции и анестезии без особенностей, интраоператорная кровопотеря составила 800 мл. Длительность операции 48 минут.
Слайд 71Через 2 часа по окончанию операции при очередном массаже матки из
Слайд 72Интраоператорно проводилась коррекция гемокоагуляции (транексам 750 мг), Биологический гемостаз адекватен (ВСК
Слайд 73
Параметры коагулограммы на момент перевода:
Этаноловый тест – слабо +
Фибриноген «В» –
Толерантность плазмы к гепарину – 6 мин
Антитромбин III - 75,5%
Тромбиновое время 15,3 сек
Фибринолитическая активность 260 мин
Тромботест - V ст.
Фибриноген - 5,3 г/л
ПО - 0,82
Протромбиновое время – 14,65 сек
Ретракция сгустка – 46%
АДФ-агрегация тромбоцитов -13 сек
АЧТВ - 23,4 сек
Активность системы протеина С - 0,7
Каолиновое время - 52 сек
Слайд 77Сравнительные объемы различных растворов, необходимых для увеличения объема плазмы на 1000
Взято с изменениями из Zornow и Prough5
Слайд 78Классификация ГЭК
Высокий:
450.000 Da - Стабизол
Средний
200.000 Da - Хаес-стерил, Рефортан, Инфукол, Гемохес
130.000 Da - ВОЛЮВЕН, ВОЛЮЛАЙТ
Низкий:
70.000 Da
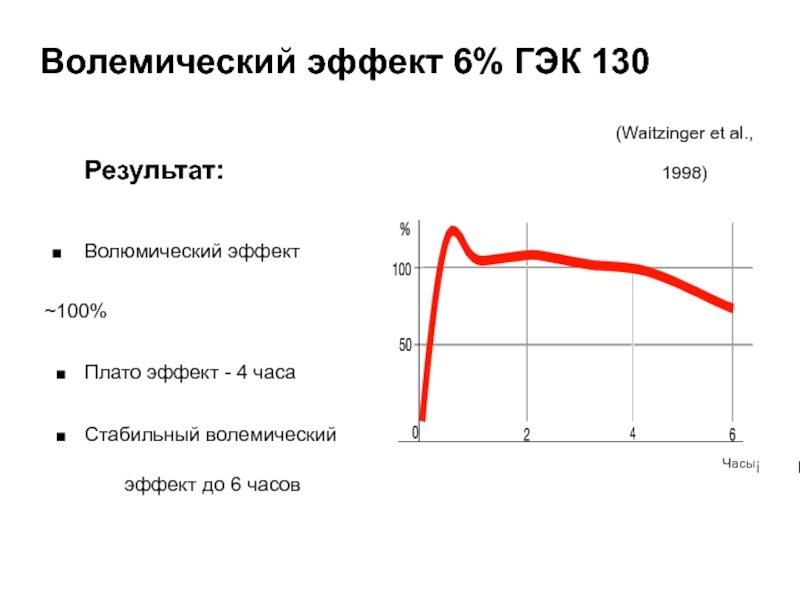
Слайд 80Волемический эффект 6% ГЭК 130
Результат:
■ Волюмический эффект ~100%
■ Плато эффект -
■ Стабильный волемический эффект до 6 часов
(Waitzinger et al., 1998)
Слайд 81Венофундин
Фармакологические свойства
Средний молекулярный вес:
Молярное замещение:
C2:C6:
Крахмал:
HES-concentration: 6 % (60 g/l)
Осмолярность: 309 mOsm/l
Кристаллоид: 0.9 % натрия хлорид
120000 – 140000 Da
0.42
6:1
Слайд 82Коллоиды и риск повреждения почек.
Декстраны- острое повреждение почек (Matheson NA,. 1970;
ГЭК 450
ГЭК 200*
ГЭК 130/0,42
Альбумин - минимальное влияние на почки
;
ГЭК 130/0,4 – минимальное влияние на почки
Желатины – не оказывает отрицательного влияния, однако требуются дополнительные исследования**
Чем выше концентрация, молекулярная масса и степень замещения, тем выше риск ОПН
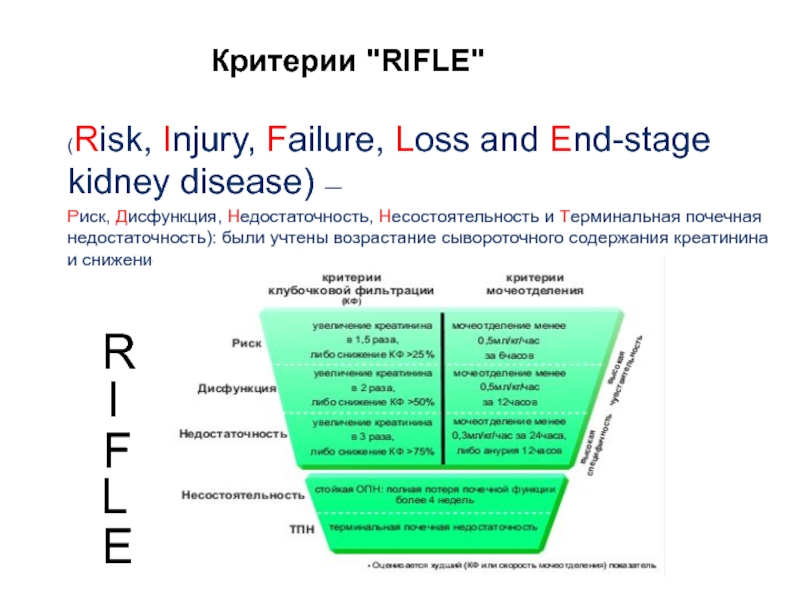
Слайд 83Критерии "RIFLE"
(Risk, Injury, Failure, Loss and End-stage kidney disease) ―
Риск,
R
I
F
L
E
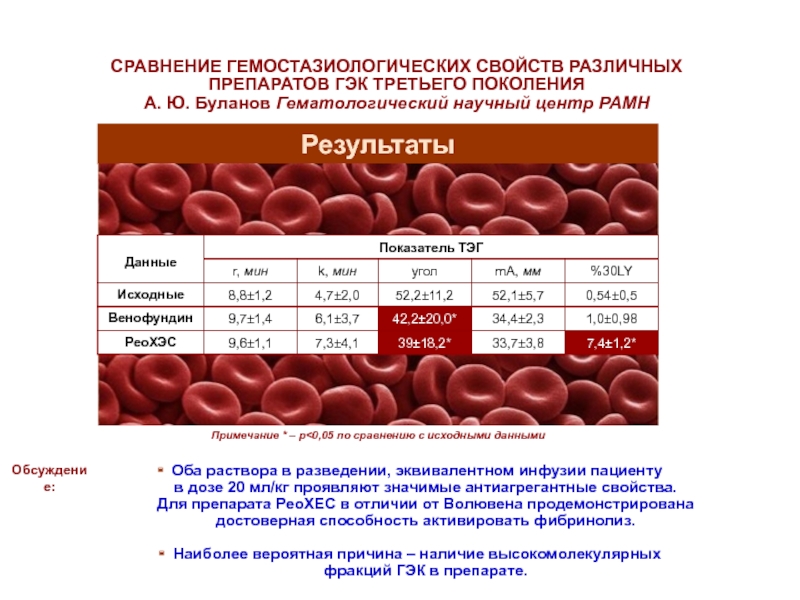
Слайд 84Примечание * – p
Наиболее вероятная причина – наличие высокомолекулярных фракций ГЭК в препарате.
Обсуждение:
СРАВНЕНИЕ ГЕМОСТАЗИОЛОГИЧЕСКИХ СВОЙСТВ РАЗЛИЧНЫХ ПРЕПАРАТОВ ГЭК ТРЕТЬЕГО ПОКОЛЕНИЯ
А. Ю. Буланов Гематологический научный центр РАМН
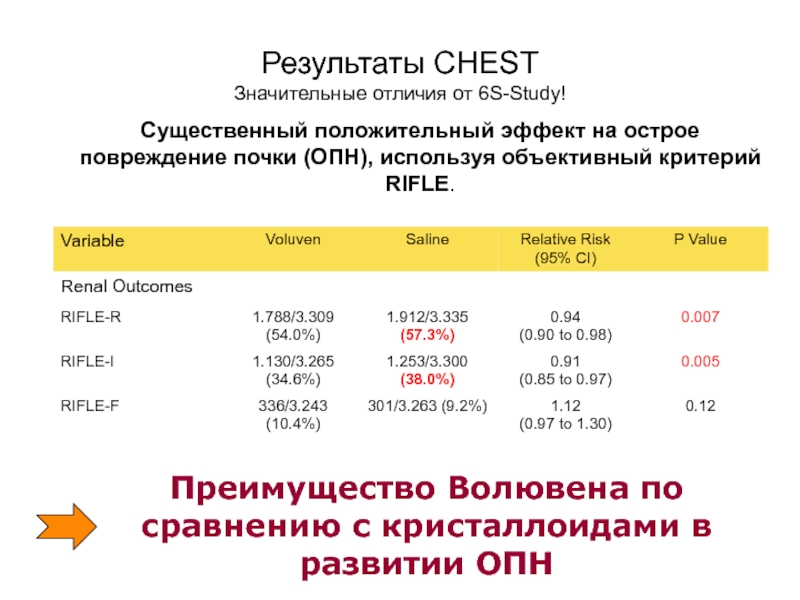
Слайд 85Существенный положительный эффект на острое повреждение почки (ОПН), используя объективный критерий
Результаты CHEST
Значительные отличия от 6S-Study!
Преимущество Волювена по сравнению с кристаллоидами в развитии ОПН
Слайд 86Желатины
Преимущества:
Минимальное влияние на систему гемостаза
Нет ограничения дозы введения
Препараты последнего поколения (Гелофузин)
Слайд 87Больная С., 28 лет поступила на лечение в отделение патологии беременности
Слайд 89 Показатели гемограммы. Исходная 110 г/л гемоглобин, эритроциты 3250000, гематокрит 33
В 10.15. 27.2.: эритроциты 2340000, гемоглобин 75 г/л, гематокрит 23,1 л/л, ВСК 3 мин 45 сек – 4 мин 25 сек, тромбоциты 234000;
в 11.25 гемоглобин 64 г/л, гематокрит 20,5 л/л, тромбоциты 94000, ВСК 4.50-5.35, эритроциты 2090000;
в 12.18 гемоглобин 82 г/л, гематокрит 25,5 л/л, эритроциты 26000000, тромбоциты 92000 ВСК 4.25-4.40.
Объём инфузии: эритроцитарная масса 3430 мл, физиологический раствор 2000 мл, альбумин 800 мл, СЗП 1200 мл, бикарбонат натрия 200 мл. Общий объём инфузии составил 9 л 630 мл, диурез 1000 мл, соотношение коллоидов и кристаллоидов 3:1.
Слайд 90АЛЬБУМИН: PRO ET CONTRA
Возможные осложнения:
Отек легких.
Нарушение газообмена в легких.
Нарушение
Теоретическая возможность заражение вирусным гепатитом.
Анафилактоидные реакции.
Стоимость альбумина в 3 раза больше, чем ГЭК.
ЗА:
Поддержание КОД.
Обеспечение про- и антикоагулянтной активности.
Антиоксидантная функция, что особенно важно при сепсисе, массивной кровопотере.
Транспортная функция (Переносит лекарства, гормоны, минералы, нутриенты (жиры, аминокислоты) и др.).
Гемодинамическая. 1 грамм альбумина удерживает 19 мл воды. Поддерживает артериальное давление.
Детоксикационная. Связывает и переносит к органам выделения билирубин, желчные кислоты, свободные радикалы и различные токсины.
Буферная. Участвует в поддержании кислотно- щелочного равновесия (КЩР).
Слайд 91Инфузионная терапия Martin GS et al. Crit Care Med 2002;30:2175-2182 Сrit Care
Альбумин
Более эффективен при гипопротеинемии (<50 г/л) по сравнению с кристаллоидами
Улучшает оксигенацию
Возможны детоксицирующие и абсорбирующие свойства
Онкотическое давление крови <15 мм.рт.ст.
Но:
Высокая стоимость
Может усилить интерстициальный отек на фоне повышенной проницаемости сосудов
Слайд 9220% альбумин человеческий компании Бакстер. Основные преимущества:
1. Комфорт для пациента, спокойствие
частота любых нежелательных побочных действий не превышает 0,003%;
отсутствие консервантов;
2. Надежный терапевтический эффект.
свойства белка максимально сохранены: T1/2=19 дней;
альбумина не менее 95% от растворенного вещества (в среднем 97%);
3.Трансфузионное инфицирование исключено.
ни одного случая передачи инфекции за всю историю применения.
4. Быстрый старт.
полностью готов к применению;
не требует хранения в холодильнике;
концентрации электролитов не влияют на показатели гомеостаза;
универсальная концентрация 20%.
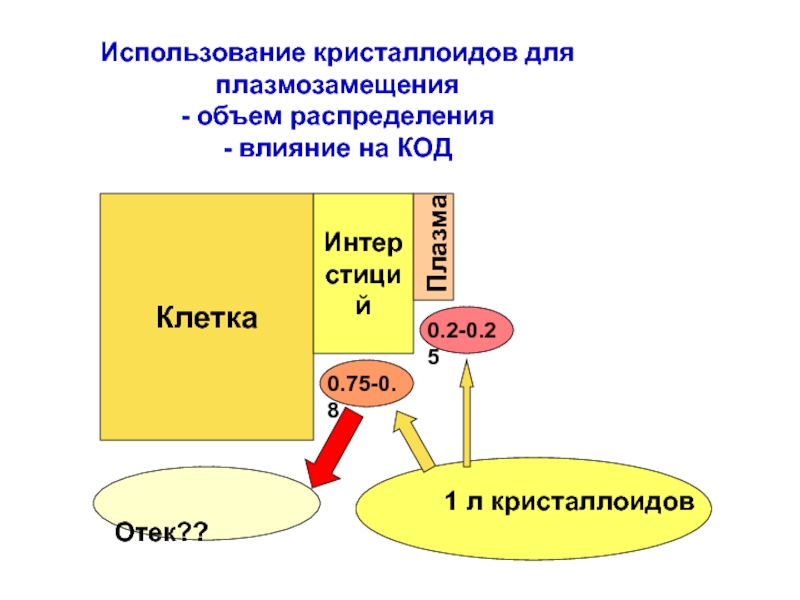
Слайд 94Использование кристаллоидов для плазмозамещения
- объем распределения
- влияние на КОД
Клетка
Интер
стиций
Плазма
Слайд 97 В эксперименте:
Усиление
воспалительной реакции
Вазодилатация
Почечная вазоконстрикция
В
Задержка мочи
Абдоминальный дискомфорт
Послеоперационная тошнота и рвота
Ментальные нарушения
Grocott 2005, Boldt 2002, Williams 1999, Morgan 2005,
Kellum 2004,2007, Wilcox 1983, Wilkes 2001
Последствия гиперхлоремического метаболического ацидоза (ГХМА)
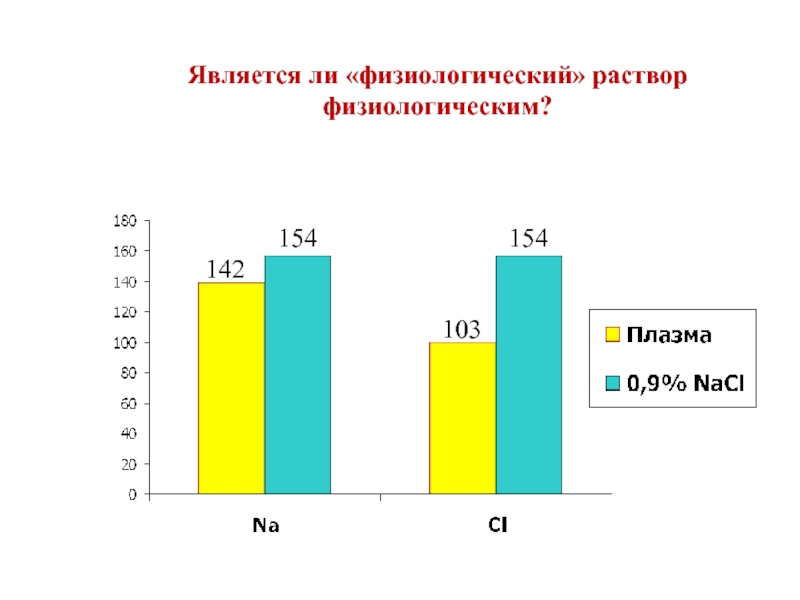
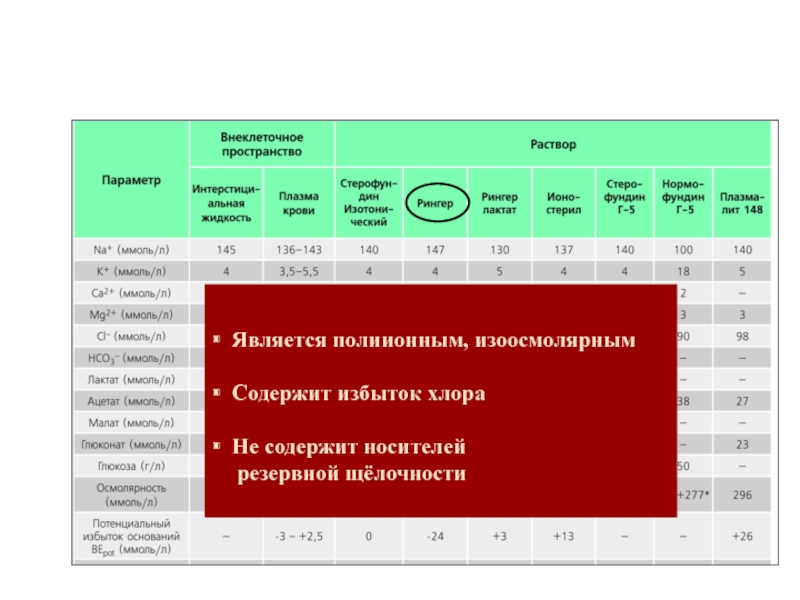
Слайд 98
Является полиионным, изоосмолярным
Содержит избыток хлора
Не содержит носителей
Слайд 99Рекомендация 1
Учитывая риск развития гиперхлоремического ацидоза в обычной практике, в случае,
Уровень доказательности 1b
Сбалансированные электролитные растворы:
время рекомендаций?
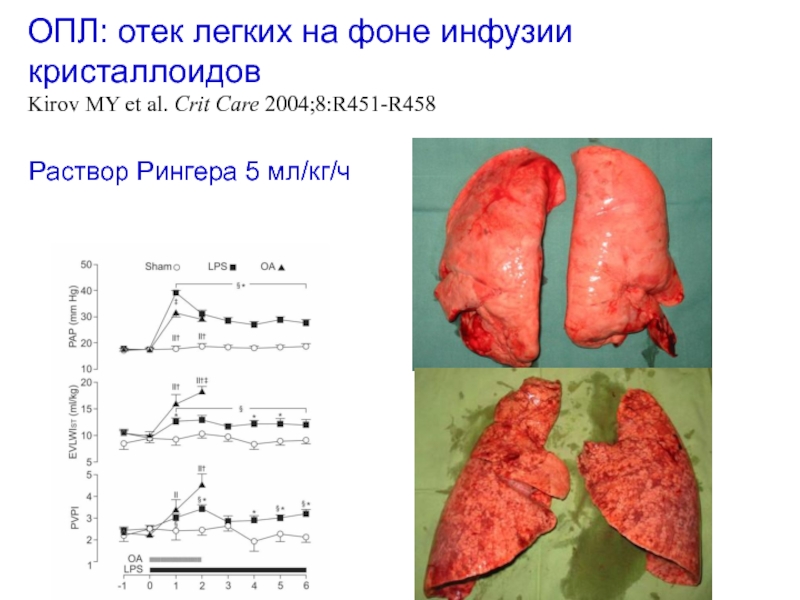
Слайд 101ОПЛ: отек легких на фоне инфузии кристаллоидов Kirov MY et al.
Раствор Рингера 5 мл/кг/ч
Слайд 102При кровопотере до 25% ОЦК суточный объем трансфузии составляет 200-250% кровопотери,
Слайд 103 1. Общий объём вводимой жидкости на 300% превышает кровопотерю. 2. Возмещение кровью
При кровопотере более 50% ОЦК:
Слайд 104По-прежнему дискутабелен вопрос должных значений Ht, Hb и эритроцитов при восполнение
Адекватное кол-во эритроцитов необходимо для «масс-эффекта» - обеспечение должного ламинарного потока, прижимающего тромбоциты к стенкам сосудов и эндотелию, где они и должны работать. Показано, что система свёртывания работает лучше при гематокрите > 35% .
(Семинар по острым кровотечениям и свёртывающей системе Ассоциации Британских Анестезиологов , 2008).
Слайд 105Переливание СЗП показано только для восполнения плазменных факторов свёртывания!
Кровопотеря свыше 25-30% ОЦК
Снижение концентрации фибриногена до 0,8 г/л
Снижение протромбинового индекса менее 60%
Удлинение ТВ или АЧТВ более чем в 1,8 раза от контроля
Разовая доза СЗП – 10-20 мл/кг массы (при 70 кг – 700-1400 мл)
(В.М.Городецкий и соавт., 2004)
Принципы применения СЗП
Слайд 106Принципы применения СЗП
Трансфузия аутоплазмы в качестве гемостатического копонента
при
Аутоплазматрансфузия расширяет возможности проведения острой нормоволемической гемодилюции при интраоперационной кровопотере объемом до 25% ОЦК и способствует снижению риска развития геморрагических и посттрансфузионных осложнений в послеопреционном периоде.
Шейкина Т. В., Рогачевский О. В., Пучко Т. К., Шифман Е. М. Влияние острой нормоволемической гемодилюции с аутплазмотрансуфузией на показатели гемостаза
при абдоминальном родоразрешении//Общая реаниматология. 2011. VII. 2. С. 35–38.
Слайд 107Пеpеливание больших количеств плазмы может пpивести к опасным осложнениям (З.С. Баркаган,
До лечения
После лечения
Слайд 108Изменения гемостаза при физиологической беременности
Рост ряда факторов свертывания (фибриноген, факторы VII,
Снижается уровень протеинов С и S
Снижение активности фибринолиза – увеличение уровня активированного тромбином ингибитора фибринолиза -TAFI (thrombin activatable fibrinolysis inhibitor) до 7,60-13,50 мкг/мл к 35-36 нед, увеличивается уровень ингибиторов активатора плазминогена (PAI-1 и PAI-2).
В родах активируется как система гемостаза, так и фибринолиз
Система гемостаза возвращается к норме через 4-6 недель после родов
Слайд 110Стадии ДВС-синдрома:
Гиперкоагуляция.
Коагулопатия потребления.
Коагулопатия потребления с геморрагическим синдромом.
Исход.
По течению:
Острый
Подострый
Хронический
Слайд 111Лабораторные проявления острого ДВС-синдрома включают
(А.В. Куликов, 2006):
Тромбоциты ‹ 150 000
Фибриноген
Продукты деградации фибриногена › 1/40.
D-димер › 2.
ПТИ ‹ 70.
Снижение антитромбина III, плазминогена.
Увеличение тромбинового времени, АПТВ, ВСК, активация протеолиза.
Слайд 113Nota bene !
Если имеет
Уходить из брюшной полости только после нормализации гемодинамики и гемостаза; при неудовлетворительном гемостазе завершить операцию наложением лапаростомы.
Слайд 114Анестезиологическая тактика -1
Искусственные коллоидных растворы: при нарушении гемокоагуляции предпочтительнее Гелоплазма баланс!
При нарушенной сосудистой проницаемости предпочтительнее ГЭК-130 (ВОЛЮВЕН или ВОЛЮЛАЙТ)!
При кровопотере более 1200 мл приступить к гемотрансфузии.
Гепарин при остром ДВС-синдроме запрещен!
Слайд 115АHЕСТЕЗИОЛОГИЧЕСКОЕ ПОСОБИЕ
Премедикация: 0,1% метацин или атропин. Антигистаминные препараты, малые транквилизаторы
наркотические анальгетики 1/2-1/3 от обычной дозировки
Основная опасность индукции - возможность pазвития глубокой гипотензии и декомпенсации кpовообpащения.
Для вводного наpкоза обычно используется кетамин
Слайд 116Анестезиологическое пособие
Интубация трахеи должна быть выполнена быстро и атравматично.
Анестезиологическое пособие пpоводят на фоне базис-наркоза ГОМК-ом с пpименением наркотических анальгетиков. N2O следует исключить?
Профилактика и лечение гипотермии.
Пролонгированная ИВЛ до стабилизации состояния пациента.
Слайд 117ПАТОЛОГИЧЕСКИЙ ФИБРИНОЛИЗ
(ГИПЕРФИБРИНОЛИЗ)
Массивная кровопотеря (обычная доза 10-15 мг/кг массы тела).
Сопутствующие тромбофилии (гемофилия,
HELLP-синдром
Заболевания печени
Слайд 118Противопоказания
к применению Транексама
Повышенная чувствительность к препарату;
Применение концентратов активированного протромбинового комплекса (КАПК),
При сочетанном применении с ингибиторами протеолиза (контрикал) имеет место риск тромботических осложнений. Применять при этом препараты ТК можно лишь в самых крайних случаях и с очень большой осторожностью.
Слайд 119
Применение апротинина повышает риск инфаркта миокарда
и сердечной недостаточности, инсульта и
Mangano D. T., Tudor I. C., Dietzel C. The risk associated
with aprotinin in cardiac surgery. New Eng. J. Med. 2006;354(4):353–365
Слайд 120D. Karalapillai, P. Popham. Recombinant factor VIIa in a massive postpartum
Протоколы по применению rFVIIa
при акушерских кровотечениях
находятся в начальной стадии разработки
Слайд 121Boehlen F., Morales M.A., Fontane P., Ricon B., ron O., Moerloose
Bouwmeester F.W., Jonkhoff A.R., Vorheijen R., van Geijn H. Seccesful treatment of life Threatening postpartum hemorrhage with recombinant activated factor VII. Obstet. Gynecol. 2003: 101; 1174–1176.
Segal S., Shemesh I.Y., Blumenthal R., et al. Treatment of obstetric hemorrhage with recombinant activated factor VII (rRVIIa). Acta Haematol. 2002; 108: 162–163.
Фактор VIIа в дозе 90–100 мкг/кг при акушерском
кровотечении, не поддающемуся стандартной терапии,
выполняет гемостатическую функцию даже при
развившемся диссеминированном внутрисосудистом
свертывании
Слайд 122КОАГИЛ-VII
Первый отечественный рекомбинантный фактор свертывания крови
МНН: Эптаког альфа (активированный)
Фармакотерапевтическая группа: гемостатическое
Лекарственная форма: лиофилизат для приготовления раствора для внутривенного введения
Биоаналог
У
1мл раствора содержит 0,6 мг Эптакога альфа активированного
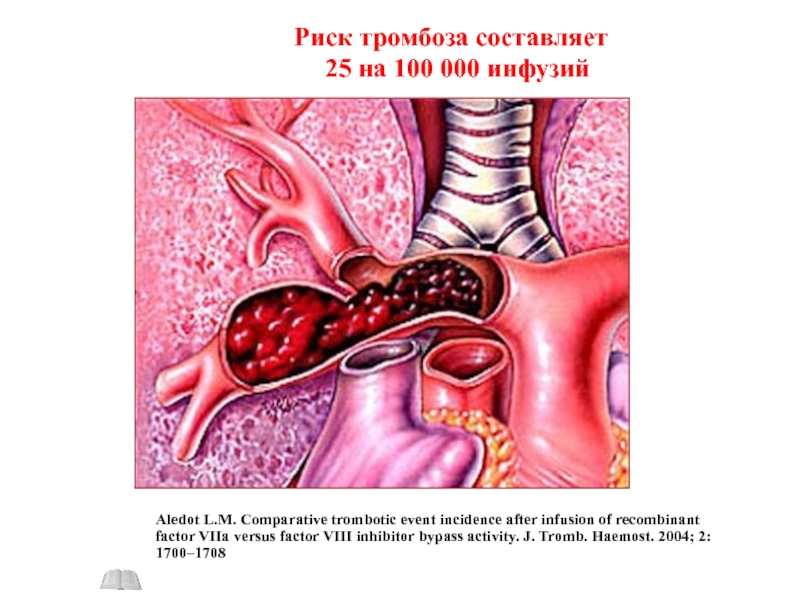
Слайд 123Aledot L.M. Comparative trombotic event incidence after infusion of recombinant factor
Риск тромбоза составляет
25 на 100 000 инфузий
Слайд 124
Критический обзор применения рекомбинантного VIIa фактора
при жизнеугрожающих послеродовых кровотечениях
Massimo Franchini,
rFVIIa при беременности: выводы
Слайд 125Анестезиологическая тактика -3
Ингибиторы протеаз (контрикал в/в болюсно 200 тыс. ЕД, затем
Заместительная терапия предусматривает также назначение криопреципитата (VIII фактор) 7-8 доз
Ранняя пpофилактическая стеpилизация кишечника.
Профилактика и лечение гипотермии, способствующей гипокоагуляции (подогрев инфузионных сред, согревание пациентки).
Слайд 126Нарушение функции коагуляции – коагулопатия
Причины:
Мокрая одежда/отсутствие одежды
Геморрагический шок нарушает перфузию
и метаболическую активность
Растворы и препараты крови
комнатной температуры
Решения:
Подогретые растворы
Сухая одежда
Гипотермия
Слайд 128 Фактор II свёртывания
Фактор VII свёртывания
Фактор X свёртывания
а так же каждый флакон содержит
Протеин С (~400 МЕ)
Гепарин (~0,5 МЕ/МЕ фактора IX)
Антитромбин III (0,75 – 1,5 МЕ/мл)
Хранение
от 2 до 8°С
Internal use statement goes here.
Введение ВВ струйно, эффект наступает в течении нескольких минут после введения одной дозы
МНН: Факторы свертывания крови II, VII, IX и X
в комбинации Гемостатическое средство