- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Жидкостная хроматография презентация
Содержание
- 1. Жидкостная хроматография
- 2. Аналитическая химия - 1 Жидкостная хроматография В
- 3. Аналитическая химия - 1 НЭЖХ диаметр колонки
- 4. Аналитическая химия - 1 ВЭЖХ Изократическая Градиентная
- 5. Аналитическая химия - 1 Отличие ВЭЖХ от
- 6. Аналитическая химия - 1 Особенности ВЭЖХ Параметры
- 7. Аналитическая химия - 1 Общая схема прибора
- 8. Аналитическая химия - 1 Колонки Предохранительная колонка
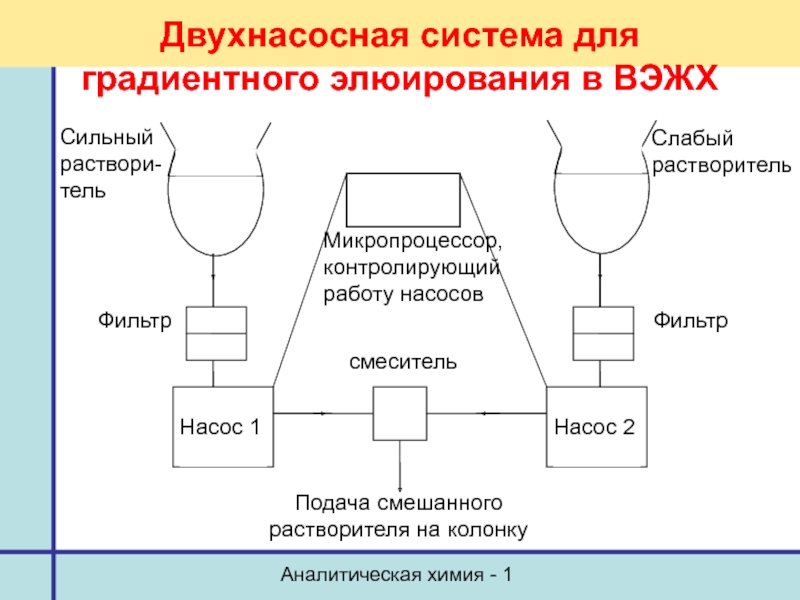
- 9. Аналитическая химия - 1 Двухнасосная система для градиентного элюирования в ВЭЖХ
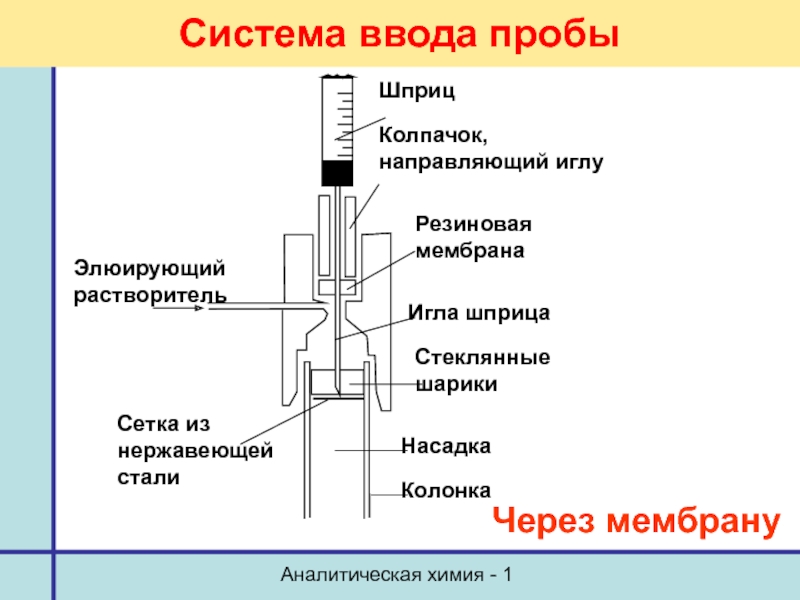
- 10. Аналитическая химия - 1 Система ввода пробы Через мембрану
- 11. Аналитическая химия - 1 Система ввода пробы
- 12. Аналитическая химия - 1 Детекторы УФ (254
- 13. Аналитическая химия - 1 Детекторы Дифференциальный рефрактометр
- 14. Аналитическая химия - 1 Детекторы СФМ (190-650
- 15. Аналитическая химия - 1 Качественный анализ Построение
- 16. Аналитическая химия - 1 Адсорбционная - ЖТХ
- 17. Аналитическая химия - 1 Сорбенты (НФ) Сорбенты
- 18. Аналитическая химия - 1 Требования к ПФ
- 19. Аналитическая химия - 1 Элюенты (ПФ) Элюотропный
- 20. Аналитическая химия - 1 Элюенты (ПФ) В
- 21. Аналитическая химия - 1 Элюенты (ПФ) Элюотропный
- 22. Аналитическая химия - 1 Распределительная - ЖЖХ
- 23. Аналитическая химия - 1 Ионообменная хроматография Динамический
- 24. Аналитическая химия - 1 Ионообменная хроматография Ионообменники
- 25. Аналитическая химия - 1 Ионообменная хроматография Катионообменники
- 26. Аналитическая химия - 1 Ионообменная хроматография Катионообменная
- 27. Аналитическая химия - 1 Ионообменная хроматография Набухание
- 28. Аналитическая химия - 1 Ионы удерживаются тем
- 29. Аналитическая химия - 1 Детекторы Кондуктометрический детектор
- 30. Аналитическая химия - 1 Детекторы Спектрофотометрический Люминесцентный Полярографический
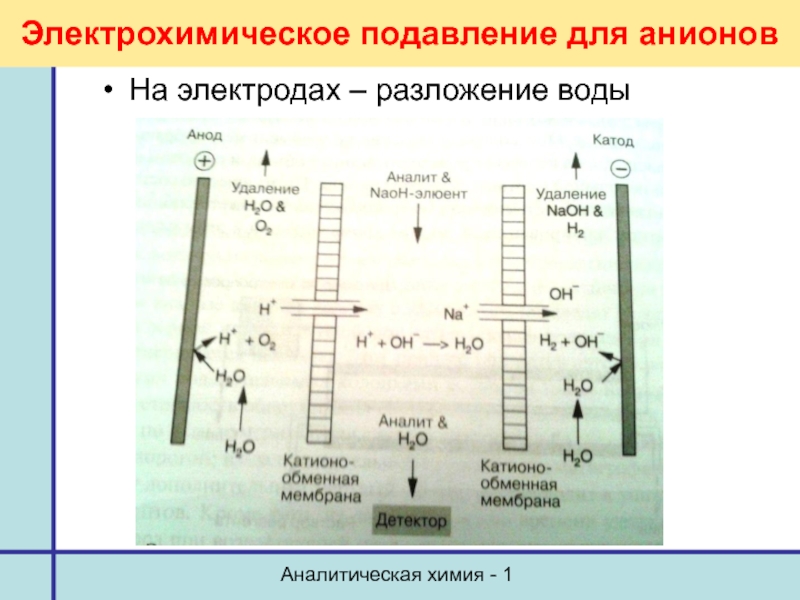
- 31. Аналитическая химия - 1 Электрохимическое подавление для анионов На электродах – разложение воды
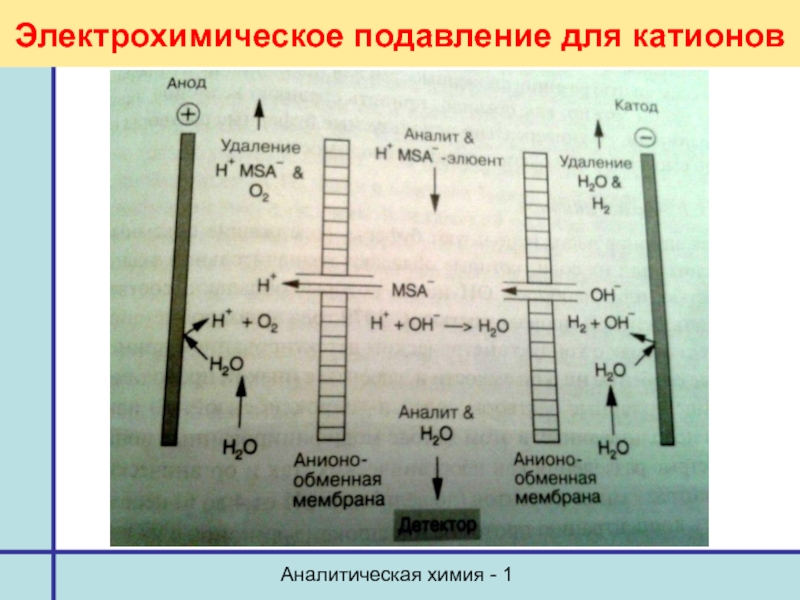
- 32. Аналитическая химия - 1 Электрохимическое подавление для катионов
Слайд 2Аналитическая химия - 1
Жидкостная хроматография
В зависимости от:
диаметра и длины колонки
размера
частиц сорбента
способа упаковки сорбента в колонке
способа упаковки сорбента в колонке
Низкоэффективная
Высокоэффективная
Слайд 3Аналитическая химия - 1
НЭЖХ
диаметр колонки ≈ n мм ÷ n см
длина колонки ≈ n×10 см
размер частиц сорбента > 10 мкм
заполнение колонки сорбентом - вручную
В ПРЕПАРАТИВНЫХ ЦЕЛЯХ
Жидкостная хроматография
Слайд 4Аналитическая химия - 1
ВЭЖХ
Изократическая
Градиентная
Мультиколоночная
Многоколоночная
Микроколоночная
Капиллярная
В АНАЛИТИЧЕСКИХ ЦЕЛЯХ
Слайд 5Аналитическая химия - 1
Отличие ВЭЖХ от ГХ
В ГХ газ-носитель не
сорбируется неподвижной фазой, а в ЖХ молекулы ПФ могут сорбироваться НФ
Молекулы ЖПФ сорбируются на поверхности НФ, молекулы определяемого соединения вытесняют молекулы элюента с поверхности сорбента ═>
↓энергия взаимодействия молекул вещества с поверхностью сорбента ═>
VR (ЖХ) < VR (ГХ), диапазон линейности изотермы сорбции ЖХ > диапазона линейности изотермы сорбции ГХ.
Молекулы ЖПФ сорбируются на поверхности НФ, молекулы определяемого соединения вытесняют молекулы элюента с поверхности сорбента ═>
↓энергия взаимодействия молекул вещества с поверхностью сорбента ═>
VR (ЖХ) < VR (ГХ), диапазон линейности изотермы сорбции ЖХ > диапазона линейности изотермы сорбции ГХ.
Слайд 6Аналитическая химия - 1
Особенности ВЭЖХ
Параметры удерживания и селективность в ГХ зависят
только от НФ, а в ЖХ – и от НФ, и от ПФ
Варьируя элюент, можно менять параметры удерживания и селективность. Возможно градиентное элюирование.
В ЖХ разделение обычно – при комнатной температуре
Для ЖХ – более сложное оборудование: система дегазации, устройство создания градиента, насосы, измерители давления, смеситель…
Варьируя элюент, можно менять параметры удерживания и селективность. Возможно градиентное элюирование.
В ЖХ разделение обычно – при комнатной температуре
Для ЖХ – более сложное оборудование: система дегазации, устройство создания градиента, насосы, измерители давления, смеситель…
Слайд 7Аналитическая химия - 1
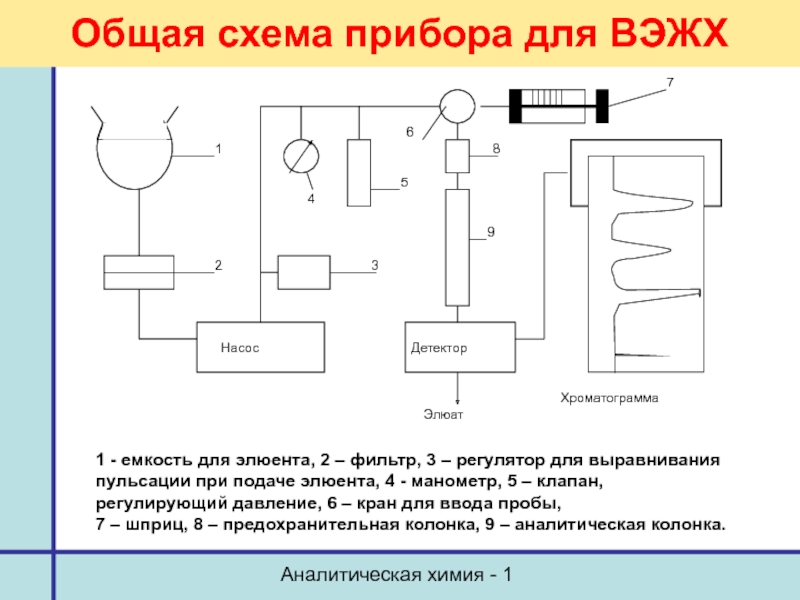
Общая схема прибора для ВЭЖХ
1 - емкость
для элюента, 2 – фильтр, 3 – регулятор для выравнивания
пульсации при подаче элюента, 4 - манометр, 5 – клапан,
регулирующий давление, 6 – кран для ввода пробы,
7 – шприц, 8 – предохранительная колонка, 9 – аналитическая колонка.
пульсации при подаче элюента, 4 - манометр, 5 – клапан,
регулирующий давление, 6 – кран для ввода пробы,
7 – шприц, 8 – предохранительная колонка, 9 – аналитическая колонка.
Слайд 8Аналитическая химия - 1
Колонки
Предохранительная колонка - короткая, защищает аналитическую колонку от
пыли, смол и других примесей. Используется для предварительного разделения или сорбции мешающих анализу компонентов.
Дегазация ПФ - удаление воздушных пузырьков
Фильтрование – внутри колонки фильтры для очистки ПФ от механических примесей, для удаления пыли.
Дегазация ПФ - удаление воздушных пузырьков
Фильтрование – внутри колонки фильтры для очистки ПФ от механических примесей, для удаления пыли.
Слайд 11Аналитическая химия - 1
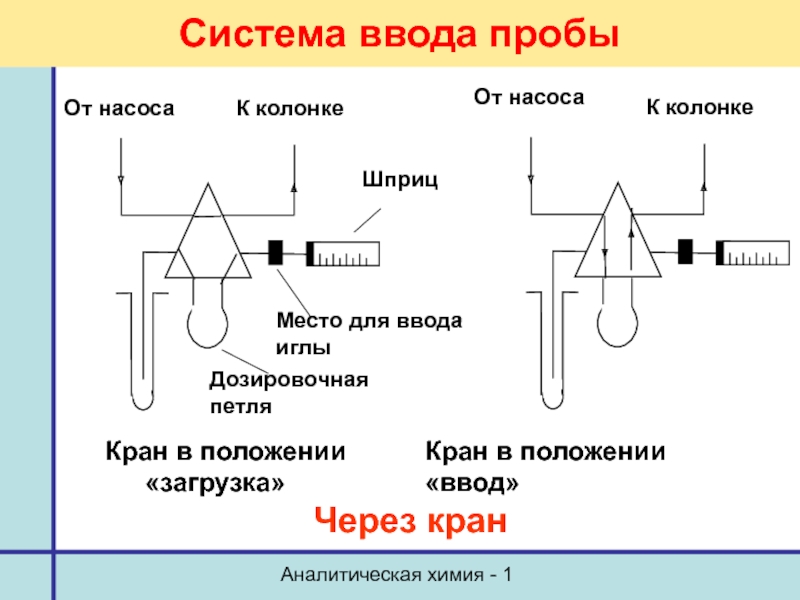
Система ввода пробы
Через кран
Кран в положении Кран в
положении
«загрузка» «ввод»
«загрузка» «ввод»
Слайд 12Аналитическая химия - 1
Детекторы
УФ (254 нм)
Альдегиды, кетоны, ароматические соединения.
Требования к
элюенту: прозрачность для УФ-излучения.
Флуоресцентный (280 нм)
ПО 10-9 - 10-10 г, диапазон линейности ~5 порядков концентрации
Флуоресцентный (280 нм)
ПО 10-9 - 10-10 г, диапазон линейности ~5 порядков концентрации
Слайд 13Аналитическая химия - 1
Детекторы
Дифференциальный рефрактометр
ПО 10-6 г, диапазон линейности ~4 порядка
концентрации. Предельные соединения
Кондуктометр
ПО 10-3 мкг/мл, диапазон линейности ~4 порядка концентрации. Ионная хр-фия.
Нефелометр проточный лазерный
В эксклюзионной хроматографии полимеров
Кондуктометр
ПО 10-3 мкг/мл, диапазон линейности ~4 порядка концентрации. Ионная хр-фия.
Нефелометр проточный лазерный
В эксклюзионной хроматографии полимеров
Слайд 14Аналитическая химия - 1
Детекторы
СФМ (190-650 нм)
Поглощение при постоянной длине волны
во времени или спектр в диапазоне длин волн в остановленном потоке
Вольтамперометрические детекторы
С плёночной ячейкой – стеклоуглеродный дисковый электрод, объем 0.06-0.3 мкл.
С трубчатой ячейкой – графитовое волокно.
ПО – пг, диапазон линейности 3 порядка
Вольтамперометрические детекторы
С плёночной ячейкой – стеклоуглеродный дисковый электрод, объем 0.06-0.3 мкл.
С трубчатой ячейкой – графитовое волокно.
ПО – пг, диапазон линейности 3 порядка
Слайд 15Аналитическая химия - 1
Качественный анализ
Построение зависимости
tR1 – tR2 или lgtR1
– lgtR2,
где tR1 и tR2 - времена появления
на хроматограмме пиков
искомых веществ на колонках с
НЖФ различной полярности
где tR1 и tR2 - времена появления
на хроматограмме пиков
искомых веществ на колонках с
НЖФ различной полярности
Слайд 16Аналитическая химия - 1
Адсорбционная - ЖТХ
Для разделения
неионных соединений – от
умеренно неполярных до умеренно полярных.
Нельзя - совсем неполярные (УВ) и сильнополярные (амины, спирты, кислоты).
Нельзя - совсем неполярные (УВ) и сильнополярные (амины, спирты, кислоты).
Слайд 17Аналитическая химия - 1
Сорбенты (НФ)
Сорбенты правильной сферической формы с узким распределением
по размерам (3±0.5, 5±1, 10±1 мкм) с поверхностью 200-600 м2/г.
Силикагель ≡Si-OH
Al2O3
Модифицированные сорбенты:
≡Si-O-Si-R, где R =
- полярные: -(СH2)4-CN, -(СH2)4-NH2, -(СH2)4-OH
- неполярные: -СH2-СH3, -(СH2)7-СH3,
-(СH2)17-СH3, -СH2-С6H6, -C(СH3)3
Силикагель ≡Si-OH
Al2O3
Модифицированные сорбенты:
≡Si-O-Si-R, где R =
- полярные: -(СH2)4-CN, -(СH2)4-NH2, -(СH2)4-OH
- неполярные: -СH2-СH3, -(СH2)7-СH3,
-(СH2)17-СH3, -СH2-С6H6, -C(СH3)3
Слайд 18Аналитическая химия - 1
Требования к ПФ
Чистота
Химическая инертность
Совместимость с детектором
Оптимальная вязкость
Безопасность
Доступность
Достаточная растворяющая
способность по отношению к анализируемым веществам
Смешиваемость друг с другом
Температура кипения
Возможность извлечения веществ из элюата
Смешиваемость друг с другом
Температура кипения
Возможность извлечения веществ из элюата
Слайд 19Аналитическая химия - 1
Элюенты (ПФ)
Элюотропный ряд – расположение растворителей в соответствии
с возрастанием их элюирующей силы.
Элюирующая сила растворителя – безразмерный параметр, который зависит от физических (поверхностное натяжение, вязкость) и химических (полярность) свойств ПФ
ЭСР показывает, во сколько раз энергия сорбции данного элюента больше, чем энергия сорбции элюента, выбранного в качестве стандарта.
Элюирующая сила растворителя – безразмерный параметр, который зависит от физических (поверхностное натяжение, вязкость) и химических (полярность) свойств ПФ
ЭСР показывает, во сколько раз энергия сорбции данного элюента больше, чем энергия сорбции элюента, выбранного в качестве стандарта.
Слайд 20Аналитическая химия - 1
Элюенты (ПФ)
В нормально-фазовой хроматографии стандарт – пентан, для
него ɛо = 0.
По элюирующей силе растворители делятся на слабые и сильные.
Слабые – слабо сорбируются НФ, коэффициенты распределения сорбируемых веществ между ПФ и НФ высокие.
Сильные – сорбируются сильно.
Растворитель тем сильнее, чем выше растворимость в нем пробы и чем сильнее взаимодействие растворитель-сорбат.
По элюирующей силе растворители делятся на слабые и сильные.
Слабые – слабо сорбируются НФ, коэффициенты распределения сорбируемых веществ между ПФ и НФ высокие.
Сильные – сорбируются сильно.
Растворитель тем сильнее, чем выше растворимость в нем пробы и чем сильнее взаимодействие растворитель-сорбат.
Слайд 21Аналитическая химия - 1
Элюенты (ПФ)
Элюотропный ряд зависит от полярности сорбента, т.е.
вида хроматографии
В нормально-фазовой при увеличении полярности растворителя ЭСР растет
В обращенно-фазовой при увеличении полярности растворителя ЭСР снижается
Элюотропный ряд Снайдера:
C5H12 < ц-C6H12 < CCl4 < бензол < СHCl3 < CH2Cl2 < CH3CN < ацетон < C2H5ОН < диоксан < CH3ОН < вода (для силикагеля)
В нормально-фазовой при увеличении полярности растворителя ЭСР растет
В обращенно-фазовой при увеличении полярности растворителя ЭСР снижается
Элюотропный ряд Снайдера:
C5H12 < ц-C6H12 < CCl4 < бензол < СHCl3 < CH2Cl2 < CH3CN < ацетон < C2H5ОН < диоксан < CH3ОН < вода (для силикагеля)
Слайд 22Аналитическая химия - 1
Распределительная - ЖЖХ
Распределение вещества между двумя несмешивающимися жидкостями,
разделение - за счет различной растворимости в жидкой НФ.
ЖЖХ - для разделения почти всех типов соединений, особенно полярных.
ЖЖХ - для разделения почти всех типов соединений, особенно полярных.
Слайд 23Аналитическая химия - 1
Ионообменная хроматография
Динамический процесс замещения ионов, связанных с НФ,
ионами элюента.
Соотношение концентраций обменивающихся ионов в растворе и в фазе сорбента определяется ионообменным равновесием.
Соотношение концентраций обменивающихся ионов в растворе и в фазе сорбента определяется ионообменным равновесием.
Слайд 24Аналитическая химия - 1
Ионообменная хроматография
Ионообменники при погружении в раствор электролита поглощают
из него
катионы (катионообменник) или
анионы (анионообменник), выделяя в раствор эквивалентное количество других ионов с тем же зарядом.
Природные ионообменники:
глины и цеолиты.
Синтетические:
высокомолекулярные материалы, напр., с матрицей из сшитого полистирола.
Сшивающий реагент - дивинилбензол.
катионы (катионообменник) или
анионы (анионообменник), выделяя в раствор эквивалентное количество других ионов с тем же зарядом.
Природные ионообменники:
глины и цеолиты.
Синтетические:
высокомолекулярные материалы, напр., с матрицей из сшитого полистирола.
Сшивающий реагент - дивинилбензол.
Слайд 25Аналитическая химия - 1
Ионообменная хроматография
Катионообменники содержат кислотные группы:
-SO3H, -COOH, -OH,
-PO3H2, -AsO3H2.
Анионообменники содержат оснòвные группы: –N(CH3)3+, =NH2+, ≡NH+.
Свойства ионообменника зависят от:
- природы ионогенных групп
- степени сшивания
- числа фиксированных ионов на 1 г
ионообменника.
Анионообменники содержат оснòвные группы: –N(CH3)3+, =NH2+, ≡NH+.
Свойства ионообменника зависят от:
- природы ионогенных групп
- степени сшивания
- числа фиксированных ионов на 1 г
ионообменника.
Слайд 26Аналитическая химия - 1
Ионообменная хроматография
Катионообменная реакция:
R-H + Na+ ↔ R-Na +
H+
Анионообменная реакция:
R-OH + Cl- ↔ R-Cl + OH-
Монофункциональные и полифункциональные ионообменники.
Характер ионогенных групп – потенциометрическим титрованием.
Емкость ионообменника – число ионогенных групп (ммоль на г или мл)
Анионообменная реакция:
R-OH + Cl- ↔ R-Cl + OH-
Монофункциональные и полифункциональные ионообменники.
Характер ионогенных групп – потенциометрическим титрованием.
Емкость ионообменника – число ионогенных групп (ммоль на г или мл)
Слайд 27Аналитическая химия - 1
Ионообменная хроматография
Набухание ионообменника в воде
Набухание зависит от:
-
количества гидрофильных ионогенных групп (чем их ↑, тем ↑емкость и ↑набухание),
- природы ионогенных групп,
- степени ионизации,
- заряда противоиона,
- концентрации внешнего раствора (чем ↓концентрация, тем ↑набухание),
- плотности матрицы, т.е содержания ДВБ (чем она ↑, тем ↓набухание).
- природы ионогенных групп,
- степени ионизации,
- заряда противоиона,
- концентрации внешнего раствора (чем ↓концентрация, тем ↑набухание),
- плотности матрицы, т.е содержания ДВБ (чем она ↑, тем ↓набухание).
Слайд 28Аналитическая химия - 1
Ионы удерживаются тем сильнее, чем больше их заряд
и размер.
Элюирующая способность ПФ возрастает с увеличением:
- концентрации ионов,
содержащихся в ней
- их сродства к ионообменнику.
Элюирующая способность ПФ возрастает с увеличением:
- концентрации ионов,
содержащихся в ней
- их сродства к ионообменнику.
Ионообменная хроматография
Слайд 29Аналитическая химия - 1
Детекторы
Кондуктометрический детектор - измерение электропроводности элюата.
Для снижения
фоновой электропроводности после разделяющей колонки – подавляющая (компенсационная), где элюент преобразуется в воду или раствор с очень низкой электропроводностью, а разделяемые ионы – в сильные электролиты.
Достоинство двухколоночной ИХ - ↓ПО и широкий диапазон линейности.
Одноколоночная ИХ - элюенты с низкой электропроводностью (ароматические кислоты и их соли, рН = 3-8).
Достоинство двухколоночной ИХ - ↓ПО и широкий диапазон линейности.
Одноколоночная ИХ - элюенты с низкой электропроводностью (ароматические кислоты и их соли, рН = 3-8).