- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Вольфрам және молибден презентация
Содержание
- 1. Вольфрам және молибден
- 2. Молибденнің ашылу тарихы «молибден» атауы грек тіліндегі «молибдос»сөзінен шығады, аудармасы қорғасын дегенді білдіреді..
- 3. Вольфрамның ашылу тарихы
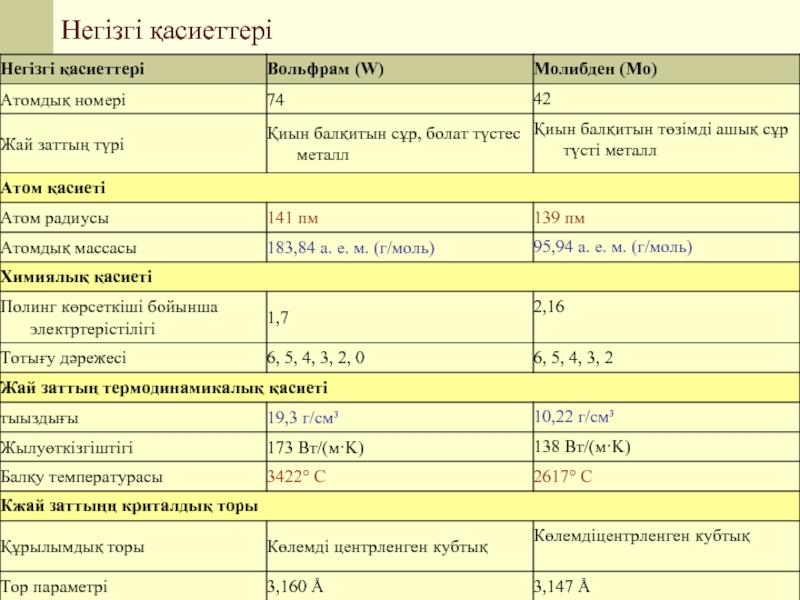
- 4. Негізгі қасиеттері
- 5. Молибденнің негізгі қасиеттері Ауада қалыпты температура кезінде
- 6. Вольфрамның негізгі қасиеттері Қалыпты кезде вольфрам химиялық
- 7. Вольфрам химиялық қасиеті 2 және 6
- 8. Сутекпен әрекеттесуі Балқу температурасына дейін әрекеттеспейді Азотпен
- 9. Оттекпен және оттекті қосылыстармен әрекеттесуі t =1000 -1200 оС әрекеттеседі WC және W2C түзеді
- 10. Галогенидтермен Фтормен бөлме температурасында Хлормен t
- 11. Қышқылдармен әрекеттесуі НF мен HNO3
- 12. Сілтілермен Сілті ерітіндісінде ерімейді Балқытылған сілтілерде әрекеттеседі
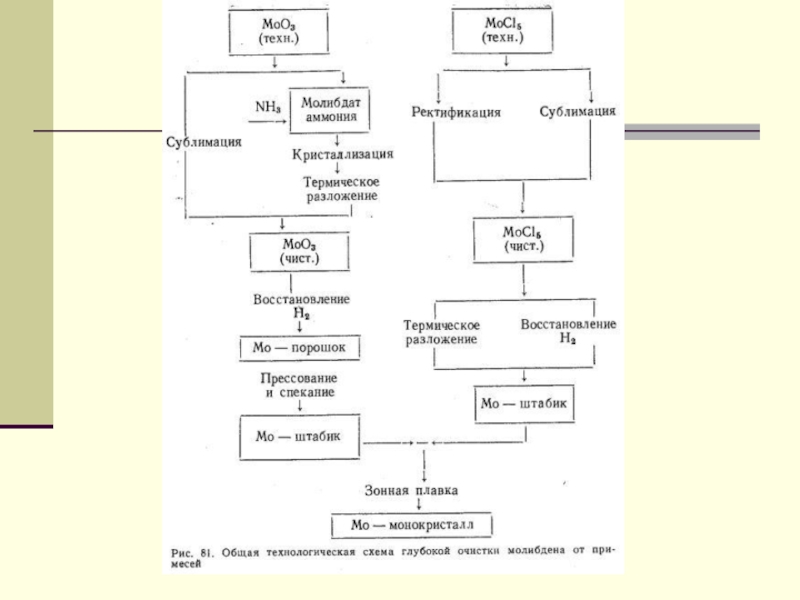
- 13. Молибденді бөліп алу әдістері 1. Экстракция 2. храмотография 3. сорбция 4. тұндыру
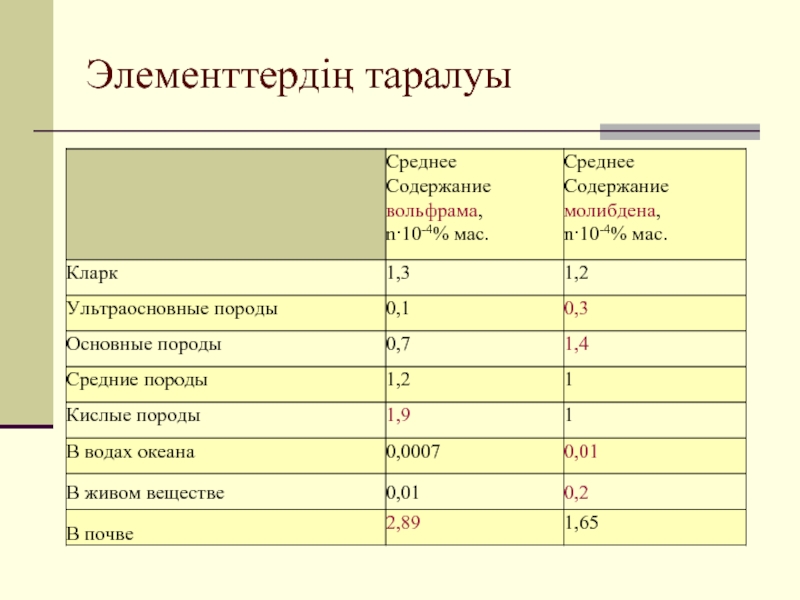
- 15. Элементтердің таралуы
- 16. Молибденнің минералдары Молибденнің 20-дан астам минералы белгілі
- 17. Вульфенит PbМо04 Молибденит МоS2 Повеллит СаМо04 1 2 3
- 18. Вольфрама минералдары 20 түрлы минералы бар. Ең
- 19. Вольфрамит MnWO4 – FeWO4 Шеелит CaWO4 1 2
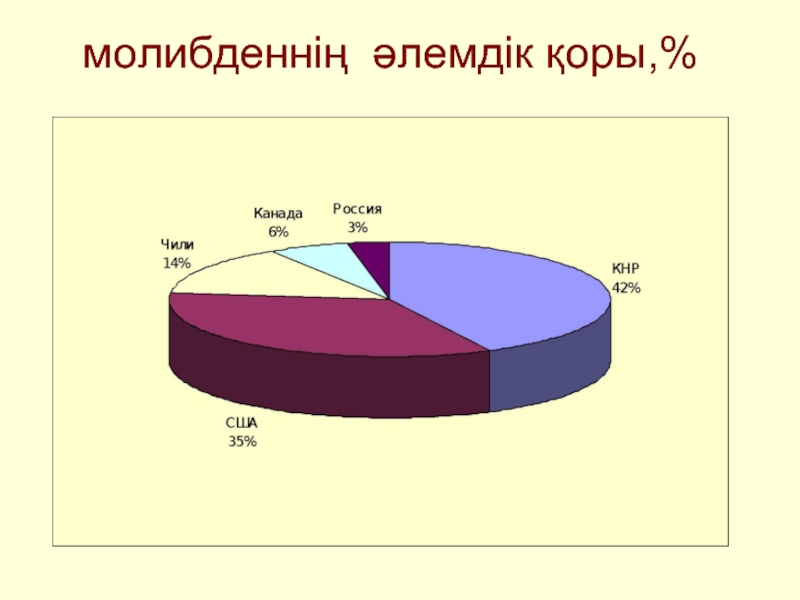
- 20. молибденнің әлемдік қоры,%
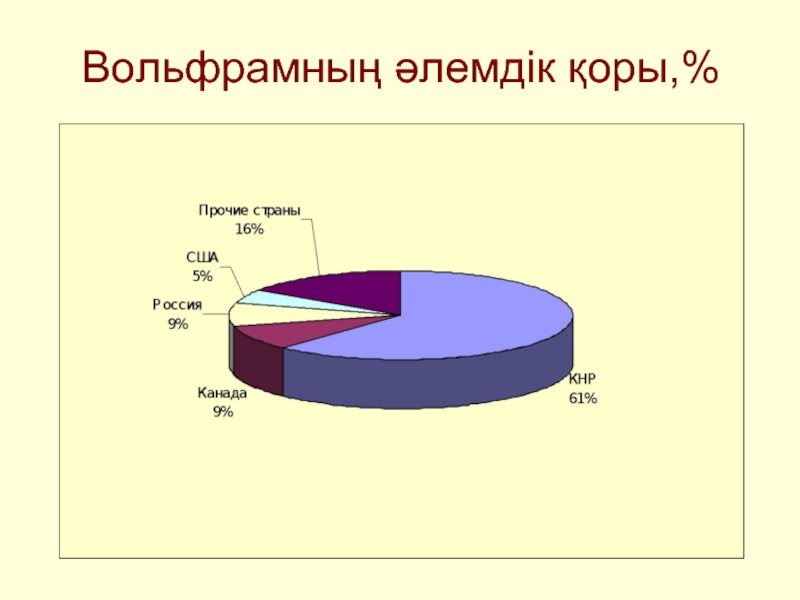
- 21. Вольфрамның әлемдік қоры,%
- 22. Молибденнің қолдану аясы Автомобиль Авиация Инструменттер және
- 23. Вольфрамның қолдану аясы Металдық вольфрам электролампаларда қолданылатын
- 24. Қоланылан әдебиеттер тізімі Иванов В.В. Экологическая геохимия
Слайд 2Молибденнің ашылу тарихы
«молибден» атауы грек тіліндегі «молибдос»сөзінен шығады, аудармасы қорғасын
Слайд 5Молибденнің негізгі қасиеттері
Ауада қалыпты температура кезінде молибден тұрақты. 400 °С температурада
700 °С сулы буы MoO2 дейін тотығады.
Температура жоарылатқан кезде молибден селенмен, күкіртпен, азотпен, оттекпен, сынаппен, сондай-ақ металл емес элементтермен әрекеттеседі.
80—100 °С молибден тұз және күкірт қышқылында ериді. Азот қышқылында, патша сұйығында және сутектің асқын тотыында қыздыран кезде ериді. Ең жақсы еріткіш ретінде азот пен күкірт қышқылының қоспасы болып табылады.
Слайд 6Вольфрамның негізгі қасиеттері
Қалыпты кезде вольфрам химиялық тұрақты.
400—500°С WO3-ке дейін тотығады..
600°С су буы WO2 дейін тотығады..
Галогендер, күкірт, оттек, кремний, бор жоғары температурада әрекеттеседі.
Қалыпты жадайда вольфрам тұз, күкірт, азот және ерітһген (HF) қышқылдарынды, және патша сұйығында ериді.
Азот қышқылында тез ериді.
Вольфрам қосылыстары 2 және 6 валенттіліті көрсетеді, жоғары валенттілік көрсететін қосылыстары тұрақты.
Слайд 7Вольфрам химиялық қасиеті
2 және 6 валентті болады.Соның ішіндегі ең тұрақтысы 6
Сұйылтылған азот қышқылында оңай ериді.
Ең қатты маңыздылары: үшоксидті вольфрам және вольфрам ангидриді, вольфраматтар.
Вольфраматтар оңай әрі тез полимерлі анион түзеді.
Слайд 8Сутекпен әрекеттесуі
Балқу температурасына дейін әрекеттеспейді
Азотпен әрекеттесуі
t > 2000 0С вольфрама
Слайд 9Оттекпен және оттекті қосылыстармен әрекеттесуі
t =1000 -1200 оС әрекеттеседі
WC және W2C
Слайд 10Галогенидтермен
Фтормен бөлме температурасында
Хлормен t = 800 0С
Күкіртпен t >
Химические свойства вольфрама
Слайд 11Қышқылдармен әрекеттесуі
НF мен HNO3 қоспасында жақсы ериді
азот қышқылы мен
Слайд 16Молибденнің минералдары
Молибденнің 20-дан астам минералы белгілі . Ең көп кездесетіндері:
-
- повеллит СаМоO4;
- молибдит (ферримолибдит) Fе2(МоO4)3· nН2O;
- вульфенит PbМо04;
- молибдо-шеелит Са(W,Мо)O4;
- чиллагит Рb(Мо,W)04;
- кёхлинит Вi2(Мо04)02;
- линдгренит Сu3(МоO4)2(ОН)2;
- ильземанит МоO3·SO3·5Н2O;
- ураномолибдат UO2·UO3·2МоO3 и др.
Бастапқы төрт минерал өндірісте орасан зор рөл алады.
Слайд 18Вольфрама минералдары
20 түрлы минералы бар. Ең көп кездесетін минералы вольфрамитті топтары
Көп кездесетін вольфрам сульфиді - тунгстенит WS2, және қышқылды қосылысының бірі- тунгстит, ферро- және купротунгстит, гидротунгстит..
Экзогенді ортада вульфенит топтары : штольцит - βРbWO4 түзсе, изоструктуралық шеелитпен және оның моноклинді түрі - распит - αРbWO4.
Слайд 22Молибденнің қолдану аясы
Автомобиль
Авиация
Инструменттер және бөлшектер
Өндірісте
Металлдық молибден
электрлік лампа
Радиоламп
Рентгендік түтікше
Электрлік пеште қолданылатын проволка.
Молибден қосылыстары — сульфидтер, оксидтер, молибдаттар — катализатор ретінде , бояғышар пигменттері ретінде.
Тез еритін молибден қосылыстары жер өңдеуге қолданылады.
Слайд 23Вольфрамның қолдану аясы
Металдық вольфрам электролампаларда қолданылатын электрлік жіпше, сваркада электрод ретінде,
Бояғыш ретінде, электротхникада.
Слайд 24Қоланылан әдебиеттер тізімі
Иванов В.В. Экологическая геохимия элементов: Справочник: В 6 кн./
Зеликман А.Н. Молибден – М.: Металлургия, 1970,440с.
Чернов Б.С., Белов С.В., Бронницкая Л.С. и др. Минеральное сырье. Вольфрам// Справочник. – М.: ЗАО "Геоинформмарк", 1998. - 37 с.
Перельман А.И. Геохимия – М.: Высш. шк.,1989. - 528 с.:илл.
Покалов В.Т. Минеральное сырье. Молибден// Справочник. – М.: ЗАО Теоинформмарк", 1997. - 44 с.
Douglas G. Brookins Eh-pH Diagrams for Geochemistry – Springer-Verlag, 1998.
http://www.mineral.ru